 高考化学之《考前抓大题》06 有机制备类实验二解析版.docx
高考化学之《考前抓大题》06 有机制备类实验二解析版.docx
- 文档编号:29175428
- 上传时间:2023-07-21
- 格式:DOCX
- 页数:26
- 大小:403.28KB
高考化学之《考前抓大题》06 有机制备类实验二解析版.docx
《高考化学之《考前抓大题》06 有机制备类实验二解析版.docx》由会员分享,可在线阅读,更多相关《高考化学之《考前抓大题》06 有机制备类实验二解析版.docx(26页珍藏版)》请在冰豆网上搜索。
高考化学之《考前抓大题》06有机制备类实验二解析版
大题06有机制备类实验
(二)
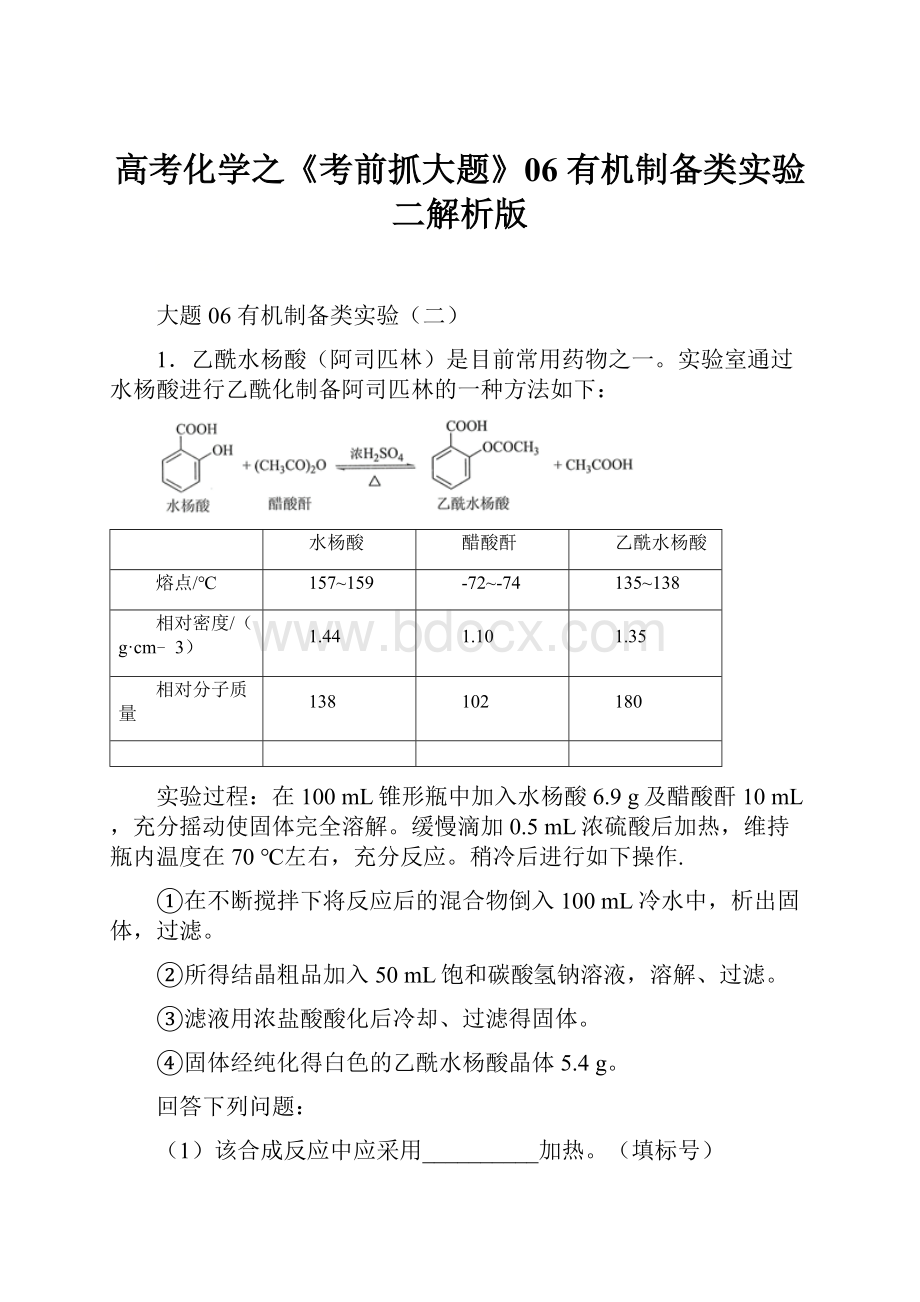
1.乙酰水杨酸(阿司匹林)是目前常用药物之一。
实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
水杨酸
醋酸酐
乙酰水杨酸
熔点/℃
157~159
-72~-74
135~138
相对密度/(g·cm﹣3)
1.44
1.10
1.35
相对分子质量
138
102
180
实验过程:
在100mL锥形瓶中加入水杨酸6.9g及醋酸酐10mL,充分摇动使固体完全溶解。
缓慢滴加0.5mL浓硫酸后加热,维持瓶内温度在70℃左右,充分反应。
稍冷后进行如下操作.
①在不断搅拌下将反应后的混合物倒入100mL冷水中,析出固体,过滤。
②所得结晶粗品加入50mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4g。
回答下列问题:
(1)该合成反应中应采用__________加热。
(填标号)
A.热水浴B.酒精灯C.煤气灯D.电炉
(2)下列玻璃仪器中,①中需使用的有________(填标号),不需使用的_______________________(填名称)。
(3)①中需使用冷水,目的是______________________________________。
(4)②中饱和碳酸氢钠的作用是_________________________________,以便过滤除去难溶杂质。
(5)④采用的纯化方法为____________。
(6)本实验的产率是_________%。
【答案】
(1)A
(2)BD分液漏斗、容量瓶
(3)充分析出乙酰水杨酸固体(结晶)
(4)生成可溶的乙酰水杨酸钠
(5)重结晶(6)60
【解析】
(1)因为反应温度在70℃,低于水的沸点,且需维温度不变,故采用热水浴的方法加热;
(2)操作①需将反应物倒入冷水,需要用烧杯量取和存放冷水,过滤的操作中还需要漏斗,则答案为:
B、D;分液漏斗主要用于分离互不相容的液体混合物,容量瓶用于配制一定浓度的溶液,这两个仪器用不到。
(3)反应时温度较高,所以用冷水的目的是使得乙酰水杨酸晶体充分析出;
(4)乙酰水杨酸难溶于水,为了除去其中的杂质,可将生成的乙酰水杨酸与碳酸氢钠反应生成可溶性的乙酰水杨酸钠,以便过滤除去杂质;
(5)每次结晶过程中会有少量杂质一起析出,可以通过多次结晶的方法进行纯化,也就是重结晶;
(6)水杨酸分子式为C7H6O3,乙酰水杨酸分子式为C9H8O4,根据关系式法计算得:
C7H6O3~C9H8O4
138180
6.9gm
m(C9H8O4)=(6.9g×180)/138=9g,则产率为
。
2.正丁醛是一种化工原料。
某实验小组利用如下装置合成正丁醛。
发生的反应如下:
CH3CH2CH2CH2OH
CH3CH2CH2CHO
反应物和产物的相关数据列表如下:
沸点/℃
密度/(g·cm-3)
水中溶解性
正丁醇
117.2
0.8109
微溶
正丁醛
75.7
0.8017
微溶
实验步骤如下:
将6.0gNa2Cr2O7放入100mL烧杯中,加30mL水溶解,再缓慢加入5mL浓硫酸,将所得溶液小心转移至B中。
在A中加入4.0g正丁醇和几粒沸石,加热。
当有蒸汽出现时,开始滴加B中溶液。
滴加过程中保持反应温度为90—95℃,在E中收集90℃以下的馏分。
将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75—77℃馏分,产量2.0g。
回答下列问题:
(1)实验中,能否将Na2Cr2O7溶液加到浓硫酸中,说明理由_____。
(2)加入沸石的作用是_____。
若加热后发现未加沸石,应采取的正确方法是______。
(3)上述装置图中,B仪器的名称是_____,D仪器的名称是_____。
(4)分液漏斗使用前必须进行的操作是_____(填正确答案标号)。
a.润湿b.干燥c.检漏d.标定
(5)将正丁醛粗产品置于分液漏斗中分水时,水在_____层(填“上”或“下”)
(6)反应温度应保持在90—95℃,其原因是_____。
(7)本实验中,正丁醛的产率为_____%。
【答案】
(1)不能,易迸溅
(2)防止暴沸冷却后补加
(3)分液漏斗直形冷凝管
(4)c
(5)下
(6)既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化
(7)51
【解析】
(1)不能将Na2Cr2O7溶液加到浓硫酸中,因为浓硫酸的密度大,容易发生迸溅。
(2)加入沸石的作用是防止暴沸,若加热后发现未加沸石,应该冷却后补加。
(3)B仪器的名称是分液漏斗,D仪器的名称直形冷凝管。
(4)分液漏斗使用前必须进行的第一项操作是检漏
(5)正丁醛密度为0.8017g·cm-3,小于水的密度
(6)根据题目所给反应物和产物的沸点数据可知,反应温度保持在90—95℃,既可保证正丁醛及时蒸出,又可尽量避免其被进一步氧化。
(7)设正丁醛的产率为x%,根据关系式
C4H10O——C4H8O
7472
4x2
解得:
x=51
【考点定位】有机化学实验、反应原理、基本操作、化学计算
3.环己烯是重要的化工原料。
其实验室制备流程如下:
回答下列问题:
Ⅰ.环己烯的制备与提纯
(1)原料环己醇中若含苯酚杂质,检验试剂为____________,现象为__________________。
(2)操作1的装置如图所示(加热和夹持装置已略去)。
①烧瓶A中进行的可逆反应化学方程式为________________________,浓硫酸也可作该反应的催化剂,选择
而不用浓硫酸的原因为________________________(填序号)。
a.浓硫酸易使原料碳化并产生
b.
污染小、可循环使用,符合绿色化学理念
c.同等条件下,用
比浓硫酸的平衡转化率高
②仪器B的作用为____________。
(3)操作2用到的玻璃仪器是____________。
(4)将操作3(蒸馏)的步骤补齐:
安装蒸馏装置,加入待蒸馏的物质和沸石,____________,弃去前馏分,收集83℃的馏分。
Ⅱ.环己烯含量的测定
在一定条件下,向
环己烯样品中加入定量制得的
,与环己烯充分反应后,剩余的
与足量
作用生成
,用
的
标准溶液滴定,终点时消耗
标准溶液
(以上数据均已扣除干扰因素)。
测定过程中,发生的反应如下:
①
②
③
(5)滴定所用指示剂为____________。
样品中环己烯的质量分数为____________(用字母表示)。
(6)下列情况会导致测定结果偏低的是____________(填序号)。
a.样品中含有苯酚杂质
b.在测定过程中部分环己烯挥发
c.
标准溶液部分被氧化
【答案】
(1)
溶液溶液显紫色
(2)
a、b减少环己醇蒸出
(3)分液漏斗、烧杯
(4)通冷凝水,加热
(5)淀粉溶液
(6)b、c
【解析】
【分析】
I.
(1)检验物质时通常是利用该物质的特殊性质,或利用不同物质间的性质差异。
苯酚能与氯化铁溶液发生显色反应而醇不能,可依此设计用氯化铁溶液检验苯酚的存在;
(2)书写陌生情境的化学方程式时,一定要将题给的所有信息挖掘出来,比如题给的反应条件,如催化剂、加热的温度、此反应已明确指出的“可逆”;
(3)催化剂选择FeCl3·6H2O而不用浓硫酸的理由分析,显然要突出浓硫酸的缺点,突出FeCl3·6H2O的优点;
(4)在发生装置中加装冷凝管,显然是为了冷凝回流,提高原料的利用率。
(5)计算此问时尽可能采用关系式法,找到已知和未知之间的直接关系。
(6)误差分析时,利用相关反应式将量尽可能明确化。
【详解】
I.
(1)检验苯酚的首选试剂是FeCl3溶液,原料环己醇中若含有苯酚,加入FeCl3溶液后,溶液将显示紫色;
(2)①从题给的制备流程可以看出,环己醇在FeCl3·6H2O的作用下,反应生成了环己烯,对比环己醇和环己烯的结构,可知发生了消去反应,反应方程式为:
,注意生成的小分子水勿漏写,题目已明确提示该反应可逆,要标出可逆符号,FeCl3·6H2O是反应条件(催化剂)别漏标;此处用FeCl3·6H2O而不用浓硫酸的原因分析中:
a项合理,因浓硫酸具有强脱水性,往往能使有机物脱水至炭化,该过程中放出大量的热,又可以使生成的炭与浓硫酸发生反应:
C+2H2SO4(浓)
CO2↑+SO2↑+2H2O;b项合理,与浓硫酸相比,FeCl3·6H2O对环境相对友好,污染小,绝大部分都可以回收并循环使用,更符合绿色化学理念;c项不合理,催化剂并不能影响平衡转化率;
②仪器B为球形冷凝管,该仪器的作用除了导气外,主要作用是冷凝回流,尽可能减少加热时反应物环己醇的蒸出,提高原料环己醇的利用率;
(3)操作2实现了互不相溶的两种液体的分离,应是分液操作,分液操作时需要用到的玻璃仪器主要有分液漏斗和烧杯;
(4)题目中已明确提示了操作3是蒸馏操作。
蒸馏操作在加入药品后,要先通冷凝水,再加热;如先加热再通冷凝水,必有一部分馏分没有及时冷凝,造成浪费和污染;
II.(5)因滴定的是碘单质的溶液,所以选取淀粉溶液比较合适;根据所给的②式和③式,可知剩余的Br2与反应消耗的Na2S2O3的物质的量之比为1:
2,所以剩余Br2的物质的量为:
n(Br2)余=
×cmol·L-1×vmL×10-3L·mL-1=
mol,反应消耗的Br2的物质的量为(b-
)mol,据反应①式中环己烯与溴单质1:
1反应,可知环己烯的物质的量也为(b-
)mol,其质量为(b-
)×82g,所以ag样品中环己烯的质量分数为:
。
(6)a项错误,样品中含有苯酚,会发生反应:
,每反应1molBr2,消耗苯酚的质量为31.3g;而每反应1molBr2,消耗环己烯的质量为82g;所以苯酚的混入,将使耗Br2增大,从而使环己烯测得结果偏大;b项正确,测量过程中如果环己烯挥发,必然导致测定环己烯的结果偏低;c项正确,Na2S2O3标准溶液被氧化,必然滴定时消耗其体积增大,即计算出剩余的溴单质偏多,所以计算得出与环己烯反应的溴单质的量就偏低,导致最终环己烯的质量分数偏低。
【点睛】
①向规范、严谨要分数。
要注意题设所给的引导限定词语,如“可逆”、“玻璃”等,这些是得分点,也是易扣分点。
②要计算样品中环己烯的质量分数,只需要算出环己烯的物质的量即可顺利求解。
从所给的3个反应方程式可以得出:
2Na2S2O3~I2~Br2~
,将相关已知数据代入计算即可。
③对于a项的分析,要粗略计算出因苯酚的混入,导致单位质量样品消耗溴单质的量增加,最终使测得环己烯的结果偏高。
4.实验室制备苯乙酮的化学方程式为:
制备过程中还有
等副反应。
主要实验装置和步骤如下:
(I)合成:
在三颈瓶中加入20g无水AlCl3和30mL无水苯。
为避免反应液升温过快,边搅拌边慢慢滴加6mL乙酸酐和10mL无水苯的混合液,控制滴加速率,使反应液缓缓回流。
滴加完毕后加热回流1小时。
(Ⅱ)分离与提纯:
①边搅拌边慢慢滴加一定量浓盐酸与冰水混合液,分离得到有机层
②水层用苯萃取,分液
③将①②所得有机层合并,洗涤、干燥、蒸去苯,得到苯乙酮粗产品
④蒸馏粗产品得到苯乙酮。
回答下列问题:
(1)仪器a的名称:
____________;装置b的作用:
________________________。
(2)合成过程中要求无水操作,理由是___________________________。
(3)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能导致_________________。
A.反应太剧烈
B.液体太多搅不动
C.反应变缓慢
D.副产物增多
(4)分离和提纯操作②的目的是__________________。
该操作中是否可改用乙醇萃取?
_____(填“是”或“否”),原因是___________________________________。
(5)分液漏斗使用前须___________________并洗净备用。
萃取时,先后加入待萃取液和萃取剂,经振摇并________________后,将分液漏斗置于铁架台的铁圈上静置片刻,分层。
分离上下层液体时,应先________________,然后打开活塞放出下层液体,上层液体从上口倒出。
(6)粗产品蒸馏提纯时,下面装置中温度计位置正确的是________________,可能会导致收集到的产品中混有低沸点杂质的装置是________________。
【答案】
(1)干燥管吸收HCl气体,并防止倒吸
(2)防止三氯化铝与乙酸酐水解
(3)AD
(4)把溶解在水中的苯乙酮提取出来以减少损失否乙醇与水混溶
(5)检查分液漏斗是否漏水放气打开上口玻璃塞(或使塞上的凹槽对准漏斗口上的小孔)
(6)CAB
【解析】
(1)仪器a为干燥管,装置b的作用是吸收反应过程中所产生的HCl气体,用倒扣于水面的漏斗可以防止倒吸。
故答案为吸收产生的氯化氢并防止倒吸;
(2)由于三氯化铝与乙酸酐均极易水解,所以要求合成过程中应该无水操作,故答案为防止三氯化铝与乙酸酐水解;
(3)若将乙酸酐和苯的混合液一次性倒入三颈瓶,可能会导致反应太剧烈及产生更多的副产物,故选AD;
(4)水层用苯萃取并分液的目的是把溶解在水中的苯乙酮提取出来以减少损失,由于乙醇能与水混溶,所以不能用酒精代替苯进行萃取操作,故答案为把溶解在水中的苯乙酮提取出来以减少损失,否,乙醇与水互溶;
(5)分液漏斗使用前须进行检漏,振摇后由于有机溶剂的挥发,分液漏斗内压强增大,所以要打开活塞进行放气操作。
放下层液体时,为了使液体能顺序滴下,应该先打开上口玻璃塞(或使塞上的凹槽对准漏斗口上的小孔),然后再打开下面的活塞,故答案为检查分液漏斗是否漏水,放气,打开上口的玻璃塞(或使塞上的凹槽对准漏斗上的小孔);
(6)蒸馏的目的是利用互溶的液体混合物中的不同组分的沸点不同提纯物质,装置中温度计是测蒸气温度的,所以温度计的水银球应该位于蒸馏烧瓶支管口处,位置正确的是C项,A、B项温度计的水银球在蒸馏烧瓶的支管口下甚至是液面下,测得的温度低于苯乙酮的沸点,使得苯乙酮中容易混入低沸点杂质,故答案为C,AB。
5.咖啡因是一种生物碱(易溶于水及乙醇,熔点234,5℃,100℃以上开始升华),有兴奋大脑神经和利尿等作用。
茶叶中含咖啡因1%~5%、单宁酸(Ka约为10−6,易溶于水及乙醇)约3%~10%,还含有色素、纤维素等。
实验室从茶叶中提取咖啡因的流程如下图所示。
索氏提取装置如图所示。
实验时烧瓶中溶剂受热蒸发,蒸汽沿蒸汽导管2上升至球形冷凝管,冷凝后滴入滤纸套筒1中,与茶叶末接触,进行萃取。
萃取液液面达到虹吸管3顶端时,经虹吸管3返回烧瓶,从而实现对茶叶末的连续萃取。
回答下列问题:
(1)实验时需将茶叶研细,放入滤纸套筒1中,研细的目的是______________,圆底烧瓶中加入95%乙醇为溶剂,加热前还要加几粒______________。
(2)提取过程不可选用明火直接加热,原因是______________,与常规的萃取相比,采用索氏提取器的优点是______________。
(3)提取液需经“蒸馏浓缩”除去大部分溶剂。
与水相比,乙醇作为萃取剂的优点是______________。
“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有______________(填标号)。
A.直形冷凝管B.球形冷凝管C.接收瓶D.烧杯
(4)浓缩液加生石灰的作用是中和_______和吸收_______。
(5)可采用如图所示的简易装置分离提纯咖啡因。
将粉状物放入蒸发皿中并小火加热,咖啡因在扎有小孔的滤纸上凝结,该分离提纯方法的名称是______________。
【答案】
(1)增加固液接触面积,提取充分沸石
(2)乙醇易挥发,易燃使用溶剂量少,可连续萃取(萃取效率高)
(3)乙醇沸点低,易浓缩AC
(4)单宁酸水
(5)升华
【解析】
【分析】
实验室从茶叶中提取咖啡因的流程为:
将茶叶末先进行索氏提取得到茶叶残渣和提取液,对提取液蒸馏浓缩得到浓溶液,然后向浓溶液中加入生石灰除去单宁酸和水,得到粉状物;由于咖啡因100℃以上开始升华,可通过加热升华的方法分离出咖啡因,据此解答。
【详解】
(1)将茶叶研细可增大接触面积,即可反应速率,使提取充分;蒸馏操作中,为了避免混合液体爆沸,需要加入沸石;
(2)该实验中的萃取剂为乙醇,乙醇易挥发,易燃,为了避免暴沸,提取过程不可选用明火直接加热;根据图示装置及题干描述可知,与常规的萃取相比,索氏提取器使用溶剂少,可连续萃取;
(3)提取液需经“蒸馏浓缩”除去大部分溶剂。
乙醇易挥发,则与水相比,乙醇作为萃取剂的优点是乙醇沸点低,易浓缩;结合蒸馏操作方法可知,“蒸馏浓缩”需选用的仪器除了圆底烧瓶、蒸馏头、温度计、接收管之外,还有冷凝管和接收器,其中蒸馏操作用直形冷凝管,回流时用球形冷凝管,所以应选用直形冷凝管,即选AC;
(4)生石灰为CaO,CaO为碱性氧化物,提取液中混有单宁酸,CaO能够中和单宁酸,还能够吸收水分;
(5)根据咖啡因“100℃以上开始升华”可知,该分离提纯方法为升华。
6.4,7—二甲基香豆素(熔点:
132.6℃)是一种重要的香料,广泛分布于植物界中,由间—甲苯酚为原料的合成反应如下:
实验装置图如下:
主要实验步骤:
步骤1:
向装置a中加入60mL浓硫酸,并冷却至0℃以下,搅拌下滴入间—甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL(0.21mol)的混合物。
步骤2:
保持在10℃下,搅拌12h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品
步骤3:
粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0g。
(1)简述装置b中将活塞上下部分连通的目的。
(2)浓H2SO4需要冷却至0℃以下的原因是。
(3)反应需要搅拌12h,其原因是。
(4)本次实验产率为(百分数保留一位小数)
(5)用(填药品名称)收集粗产品,用(填操作名称)的方法把粗产品分离。
【答案】
(1)平衡上下气压,使漏斗中液体顺利流下
(2)防止浓H2SO4将有机物氧化或炭化
(3)使反应物充分接触反应,提高反应产率
(4)90.3%
(5)CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O;饱和的碳酸钠溶液;分液
【解析】
(1)装置b中将活塞上下部分连通的目是平衡上下气压,使漏斗中液体顺利流下。
故填:
平衡上下气压,使漏斗中液体顺利流下;
(2)浓硫酸具有强氧化性和脱水性,因此浓H2SO4需要冷却至0℃以下的原因是防止浓H2SO4将有机物氧化或炭化。
故填:
防止浓H2SO4将有机物氧化或炭化;
(3)搅拌可以使反应物充分接触反应,提高反应产率。
故填:
使反应物充分接触反应,提高反应产率;
(4)反应中间—甲苯酚是0.29mol,乙酰乙酸乙酯是0.21mol,所以根据方程式可知理论上应该生成0.21mol4,7—二甲基香豆素,质量是0.21mol×174g/mol=36.54g。
实际生产中得到4,7—二甲基香豆素的质量是33.0g,所以本次实验产率为
。
故填:
90.3%;
(5)实验室制备乙酸乙酯的化学反应方程式CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O,用饱和的碳酸钠溶液收集粗产品,由于乙酸乙酯难溶于水,所以用分液的方法把粗产品分离。
故填:
CH3CH2OH+CH3COOH
CH3COOCH2CH3+H2O;饱和的碳酸钠溶液;分液。
7.苯甲酸是一种重要的化工原料。
实验室合成苯甲酸的原理、有关数据及装置示意图如下:
某学习小组在实验室制备、分离、提纯苯甲酸,并测定所得样品的纯度,步骤如下:
一、制备苯甲酸
在三颈瓶中加人2.7mL甲苯、100mL水和2~3片碎瓷片,开动电动搅拌器,a中通入流动水,在石棉网上加热至沸腾,然后分批加人8.5g高锰酸钾,继续搅拌约4~5h,直到甲苯层几乎近于消失、回流液不再出现油珠,停止加热和搅拌,静置。
[来
二、分离提纯
在反应混合物中加人一定量草酸(H2C204)充分反应,过滤、洗涤,将滤液放在冰水浴中冷却,然后用浓盐酸酸化,苯甲酸全部析出后减压过滤,将沉淀物用少量冷水洗涤,挤压去水分后放在沸水浴上干燥,得到粗产品。
三、测定纯度
称取mg产品,配成100mL乙醇溶液,移取25.00mL溶液于锥形瓶,滴加2~3滴酚酞,然后用标准浓度KOH溶液滴定。
请回答下列问题:
(1)装置a的名称是____,其作用为_________
(2)甲苯被高锰酸钾氧化的原理为:
请完成并配平该化学方程式。
(3)分离提纯过程中加人的草酸是一种二元弱酸,反应过程中有酸式盐和无色气体生成。
加人草酸的作用是,请用离子方程式表示反应原理
(4)产品减压过滤时用冷水洗涤的原因是
(5)选用下列操作,可以将粗产品进一步提纯。
(选填字母)
A、溶于水后过滤B、溶于乙醇后蒸馏
C、用甲苯萃取后分液D、升华
(6)测定纯度步骤中,滴定终点溶液的颜色变化是____。
若m=1.200g,滴定时用去0.1200mol·L-1标准KOH溶液20.00mL,则所得产品中苯甲酸的质量分数为
【答案】
(1)球形冷凝管冷凝回流,防止甲苯的挥发而降低产品产率
(2)1,2;1,2,1,1KOH
(3)将过量的高锰酸钾转化为二氧化锰,以便过滤除去。
2MnO4-+3H2C2O4=2MnO2↓+2HCO3-+4CO2↑+2H2O
(4)苯甲酸在冷水中的溶解度较小,用冷水洗涤可以减少产品的损失
(5)D
(6)溶液由无色变浅红色,且半分钟不退色97.6%
【解析】
(1)根据仪器的特征,装置a的名称是球形冷凝管,其作用为冷凝回流,防止甲苯的挥发而降低产品产率。
(2)根据题给信息,甲苯被高锰酸钾氧化为苯甲酸钾,高锰酸钾被还原成MnO2,根据化合价升降相等,可得甲苯、苯甲酸钾前的系数为1,高锰酸钾、MnO2前的系数为2,再根据电荷守恒可知有KOH生成,最后根据原子守恒配平。
即得化学方程式为
+2KMnO4
+2MnO2↓+H2O+KOH;
(3)草酸是一种二元弱酸,能被高锰酸钾氧化,生成CO2和水,高锰酸钾被还原生成MnO2,所以加人草酸的作用是将过量的高锰酸钾转化为二氧化锰,以便过滤除去,用离子方程式表示的反应原理为2MnO4-+3H2C2O4=2MnO2↓+2HCO3-+4CO2↑+2H2O;
(4)根据表格所给信息,苯甲酸在冷水中的溶解度较小,用冷水洗涤可以减少产品的损失,所以产品减压过滤时用冷水洗涤;
(5)根据题给信息,苯甲酸在100℃左右升华,所以将粗产品进一步提纯的最佳操作是升华,选D。
(6)酚酞作指示剂,在乙醇溶液中无色,用KOH溶液滴定,过量时溶液呈红色,所以滴定终点溶液的颜色变化是溶液由无色变浅红色,且半分钟不退色;
设滴定过程中消耗苯甲酸xg,
122g1mol
x0.12×0.02解得x=0.2976g
则所得产品中苯甲酸的质量分数为0.2976×4÷1.200×100%=97.
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 考前抓大题 高考化学之考前抓大题06 有机制备类实验二解析版 高考 化学 考前 抓大题 06 有机 制备 实验 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
