 全国高考化学考前复习大串讲专题61 化学实验基础知识.docx
全国高考化学考前复习大串讲专题61 化学实验基础知识.docx
- 文档编号:29042895
- 上传时间:2023-07-20
- 格式:DOCX
- 页数:13
- 大小:266.57KB
全国高考化学考前复习大串讲专题61 化学实验基础知识.docx
《全国高考化学考前复习大串讲专题61 化学实验基础知识.docx》由会员分享,可在线阅读,更多相关《全国高考化学考前复习大串讲专题61 化学实验基础知识.docx(13页珍藏版)》请在冰豆网上搜索。
全国高考化学考前复习大串讲专题61化学实验基础知识
知识归纳
一、重要仪器使用
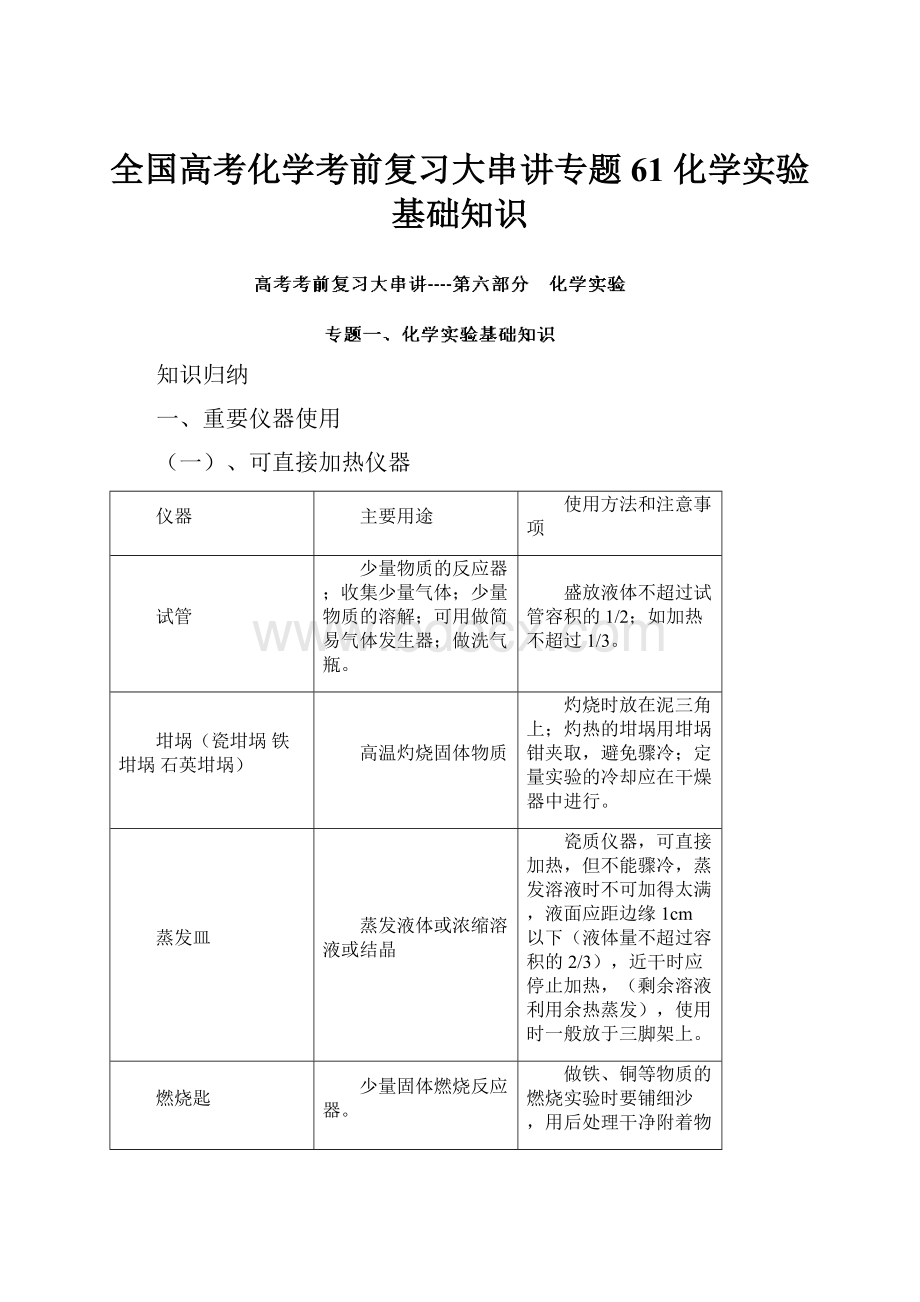
(一)、可直接加热仪器
仪器
主要用途
使用方法和注意事项
试管
少量物质的反应器;收集少量气体;少量物质的溶解;可用做简易气体发生器;做洗气瓶。
盛放液体不超过试管容积的1/2;如加热不超过1/3。
坩埚(瓷坩埚铁坩埚石英坩埚)
高温灼烧固体物质
灼烧时放在泥三角上;灼热的坩埚用坩埚钳夹取,避免骤冷;定量实验的冷却应在干燥器中进行。
蒸发皿
蒸发液体或浓缩溶液或结晶
瓷质仪器,可直接加热,但不能骤冷,蒸发溶液时不可加得太满,液面应距边缘1cm以下(液体量不超过容积的2/3),近干时应停止加热,(剩余溶液利用余热蒸发),使用时一般放于三脚架上。
燃烧匙
少量固体燃烧反应器。
做铁、铜等物质的燃烧实验时要铺细沙,用后处理干净附着物
硬质玻璃管
少量物质的反应器
耐热玻璃仪器,可直接用酒精喷灯加热,但不能骤冷。
(二)、必须加石棉网加热仪器
烧杯、烧瓶、蒸馏烧瓶、锥形瓶
(三)、计量仪器
主要用途:
用于精确配制一定体积和一定物质的量浓度的溶液(精确度0.O1mL)
使用方法和注意事项
①不做反应器,不加热,瓶塞不互换②用前检漏,不贮存试剂③不直接溶解
④使用时选合适的规格,⑤容积为20度标定
物质的量溶液配制
使用方法和注意事项
①不允许超过他的最高量程②不能当搅拌棒使用③注意水银球位置
天平的使用
主要用途:
粗略量取液体的体积(精确度0.1mL)
使用方法和注意事项①刻度由下而上,无“0”刻度②使用时选合适的规格
③不可用做反应器,不加热,不用直接配溶液④读数平视
滴定管
滴定管的使用
(四)、其它仪器
主要用途:
用于装配反应器,便于注入反应液体
使用方法和注意事项:
长颈漏斗在组装气体发生装置时,应使长管末端插入反应器的液体里,借助液封防止气体通过漏斗逸出。
主要用途:
①分离密度不同的且互不相溶的液体②用在反应器的随时加液装置
③用于萃取分离
使用方法和注意事项
①检验是否漏夜②分离液体时,下层液体由下口放出,上层液体由上口倒出③不宜装碱性溶液
④使用时盖塞上的凹槽和漏斗口上的小孔对齐(连通大气)。
萃取操作
使用方法和注意事项冷却水的进口应在组装仪器的低处,出水口在高处,这样才能使整套中充满水(低进高出)
使用方法和注意事项①控制气流速度,以便有效地吸收杂质
②注意气流方向③注意进气管和出气管的长度。
二、试剂的存放
(一)在空气中易变质的试剂:
这类试剂应隔绝空气或密封保存,有些试剂的保存还要采取特殊的措施。
1、易被氧化的试剂:
亚铁盐、活泼金属单质、白磷、氢硫酸、苯酚、Na2SO3、H2SO3等。
2、易吸收CO2的试剂:
CaO、NaOH、Ca(OH)2、Na2O2、漂白粉等。
3、易吸湿的试剂:
P2O5、CaC2、CaO、NaOH、无水CaCl2、浓H2SO4、无水CuSO4、FeCl3·6H2O、MgCl2·6H2O等。
4、易风化的试剂:
Na2CO3·10H2O。
5、见光或受热易分解的试剂:
这类试剂应用棕色瓶盛放且置于冷暗处。
如HNO3、硝酸银、双氧水、碘化钾、溴化钾、亚硝酸盐、漂白粉、氯水、溴水等。
保管与使用的注意事项:
用棕色、黄棕色、黑色等有色玻璃瓶盛装,若用无色玻璃瓶盛装时瓶外要套黑纸套,保存于阴凉处。
(二)易挥发的试剂:
浓氨水,浓盐酸,液溴,乙酸乙酯,二硫化碳,四氯化碳,汽油等。
保管与取用的注意事项:
要严密盖紧瓶盖,保存在阴凉通风处,取用后要立即盖紧瓶盖。
(三)危险品:
这类试剂应分类存放并远离火源。
易燃试剂:
遇明火即可燃烧的有汽油,苯,乙醇,酯类物质等有机溶剂和红磷,硫,镁,硝酸纤维等。
能自燃的有白磷。
本身不可燃但与可燃物接触后有危险的试剂有:
高锰酸钾,氯酸钾,硝酸钾,过氧化钠等。
易爆试剂:
有硝酸纤维,硝酸铵等。
剧毒试剂:
氰化物,汞盐,白磷,氯化钡,硝基苯等。
强腐蚀性试剂:
强酸,强碱,液溴,甲醇,苯酚,氢氟酸,醋酸等。
有些试剂不宜长久放置,应随用随配。
如硫酸亚铁溶液,氯水,氢硫酸,银氨溶液等。
三、常用的几种指示剂试纸的用途
①红色石蕊试纸遇到碱性溶液变蓝,蓝色石蕊试纸遇到酸性溶液时变红,它们可以定性地判断气体或溶液的酸、碱性。
②淀粉碘化钾试纸中的碘离子,当遇到氧化性物质时被氧化为碘,碘遇淀粉显示蓝色,它可以定性地检验氧化性物质的存在,如氯气、溴蒸气(和它们的溶液)、NO2等。
③pH试纸遇到酸碱性强弱不同的溶液时,显示不同的颜色,可与标准比色卡对照确定溶液的pH,
它可以粗略地检验溶液酸碱性的强弱。
试纸的使用方法:
①先把一小块试纸放在表面皿或玻璃片上,用沾有待测液的玻璃棒点试纸的中部,观察颜色的改变,判断溶液的性质。
②检验气体时,先用蒸馏水把试纸润湿,粘在玻璃棒的一端,用玻璃棒把试纸放到盛有待测气体的试管口,观察。
③PH试纸:
玻璃棒不仅要洁净,而且不能有蒸馏水,同时还要特别注意在用前,切不可用蒸馏水湿润。
三、典型实验操作
1、一定物质的量浓度溶液的配制:
(1)配制步骤
(2)溶液配制过程注意事项
_1)用量筒取液体试剂时,洗量筒的液体不能再倒入烧杯中___
2)烧杯及玻璃棒的洗涤液要倒入容量瓶
_3)在液面接近容量瓶的刻度线2—3cm时,应改用胶头滴管___
4)读数时,视线应与溶液的凹液面恰好相切
_5)容量瓶是配制溶液的容器,不是装试剂用的___
6)若用浓硫酸配制稀硫酸时,一定要注意将浓硫酸慢慢用玻璃棒引流到水中。
切不可相反操作!
(3)配置一定物质的量浓度的溶液误差分析
2、酸碱中和滴定
(1)酸碱中和滴定原理:
中学化学只要求掌握强酸与强碱的中和滴定,因此计算依据是:
H++OH-=H2O
(2)酸碱中和滴定注意事项:
1强碱滴定强酸时,一般用酚酞作指示剂;强酸滴定强碱时,常用甲基橙作指示剂
2在滴定过程中,如标准液滴在靠瓶口的内壁上,可用蒸馏水把它冲入瓶内。
③如标准液滴在锥形瓶外或其他损失时,都应重做。
(3)酸碱中和滴定误差分析
3、中和热的测定
测定原理:
ΔH=-(CmΔt)/n(H2O);
测定仪器:
量热计(温度计、烧杯、环形玻璃搅拌棒、量筒)
试剂:
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH(稍过量,为什么?
)
测定步骤:
可能误差:
50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图装置中进行中和反应。
通过测定反应过程中所放出的热量可计算中和热。
回答下列问题:
(1)从装置上看,图中尚缺少的一种玻璃用品是图中还有一明显问题是
(2)烧杯间填满碎纸条的作用是。
(3)实验中若用40mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量(填“相等”、“不相等”),所求中和热(填“相等”、“不相等”),简述理由
(4)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会(均填“偏大”、“偏小”、“无影响”);若用铜质搅拌棒进行上述实验,测得的中和热的数值会(均填“偏大”、“偏小”、“无影响”),试列举提高实验准确性,减少实验误差的做法
【典例剖析】
典例一、
【考点定位】本题主要是考查化学实验基础知识,元素化合物的性质等判断
【2016江苏省】根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的的是
【答案】C
典例二、
【考点定位】化学反应仪器的使用及物质性质的考查
(2017·淄博模拟)已知硫酸铜加热分解生成CuO、O2、SO2和SO3(g)。
通过测定产生的三种气体的量可确定该反应的方程式。
实验用到的仪器如下图所示。
有关操作和结果如下(已知:
H++HSO
===SO2↑+H2O)。
①准确称取一定质量的无水CuSO4固体充分加热到完全分解。
②实验后测得装置F总质量比实验前减少了0.96g(忽略水蒸气的损失和SO2的溶解)。
③干燥管C在实验后质量增加3.84g。
④由量筒中水的体积,折算出标准状况下相应气体的体积为224mL。
试回答下列问题:
(1)装置C的作用是__________________,装置F的作用是______________。
(2)使用上图所给仪器装置(可重复使用),按从左到右的方向连接各仪器,接口顺序为①→⑨⑩→⑥⑤→________→________→________→②。
(填序号)
(3)装置F中发生反应的化学方程式为_________________________。
(4)请通过计算,推断出该条件下反应的化学方程式为____________。
【答案】
(1)吸收SO2 吸收SO3
(2)③④ ⑥⑤(或③④) ⑧⑦
(3)SO3(g)+2NaHSO3===Na2SO4+2SO2+H2O(或SO3+H2O===H2SO4、H2SO4+2NaHSO3===Na2SO4+2SO2↑+2H2O)
(4)4CuSO4
4CuO+2SO3↑+2SO2↑+O2↑
【考前强训】
1.【黑龙江省哈尔滨师范大学附属中学2017年高三第三次模拟考试】下列实验装置(固定装置略去)能完成相应实验目的的是()
A.分离CCl4和水B.酸碱中和滴定C.吸收HCl尾气D.中和热的测定
【答案】A
【解析】A.分离CCl4和水选择分液操作,故A正确;B.NaOH溶液应盛放在碱式滴定管中,故B错误;C.HCl气体易溶解于水,用水吸收HCl时,三角漏斗只能略低于液面,防倒吸,故C错误;D.中和热测定实验时温度计是测混合溶液的温度,应插入混合溶液中,故D错误;答案为A。
2.【安徽省舒城中学2017届高三仿真
(一)理综】利用实验器材(规格和数量不限),能完成相应实验的一项是( )
选项
实验器材(省略夹持装置)
相应实验
A
烧杯、玻璃棒、蒸发皿
硫酸铜溶液的浓缩结晶
B
烧杯、玻璃棒、胶头滴管、滤纸
用盐酸除去硫酸钡中的少量碳酸钡
C
烧杯、玻璃棒、胶头滴管、容量瓶
用固体氯化钠配制0.5mol·L-1的溶液
D
烧杯、玻璃棒、胶头滴管、分液漏斗
用溴水和CCl4除去NaBr溶液中的少量NaI
【答案】D
3.(2017·朝阳区模拟)用灼烧法证明海带中含有碘元素,各步骤选用的实验用品不必都用到的是( )
选项
实验步骤
实验用品
A
步骤1:
将海带灼烧灰化
B
步骤2:
将海带灰溶解、过滤
C
步骤3:
氧化滤液中的I-
D
步骤4:
检验碘元素
【答案】C
【解析】氧化滤液中的I-不用容量瓶。
4.(2017·天津模拟)下列关于各实验装置的叙述中,不正确的是( )
A.图①可用于实验室制取NH3或O2
B.可用从a处加水的方法检验图②装置的气密性
C.实验室可用图③的方法收集Cl2或NH3
D.利用图④装置制硫酸和氢氧化钠,其中b为阴离子交换膜,c为阳离子交换膜
【答案】C
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 全国高考化学考前复习大串讲专题61 化学实验基础知识 全国 高考 化学 考前 复习 串讲 专题 61 实验 基础知识
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
