 完整word版届九年级中考复习浙教版科学讲义设计九年级上册4金属.docx
完整word版届九年级中考复习浙教版科学讲义设计九年级上册4金属.docx
- 文档编号:2887068
- 上传时间:2022-11-16
- 格式:DOCX
- 页数:9
- 大小:131.52KB
完整word版届九年级中考复习浙教版科学讲义设计九年级上册4金属.docx
《完整word版届九年级中考复习浙教版科学讲义设计九年级上册4金属.docx》由会员分享,可在线阅读,更多相关《完整word版届九年级中考复习浙教版科学讲义设计九年级上册4金属.docx(9页珍藏版)》请在冰豆网上搜索。
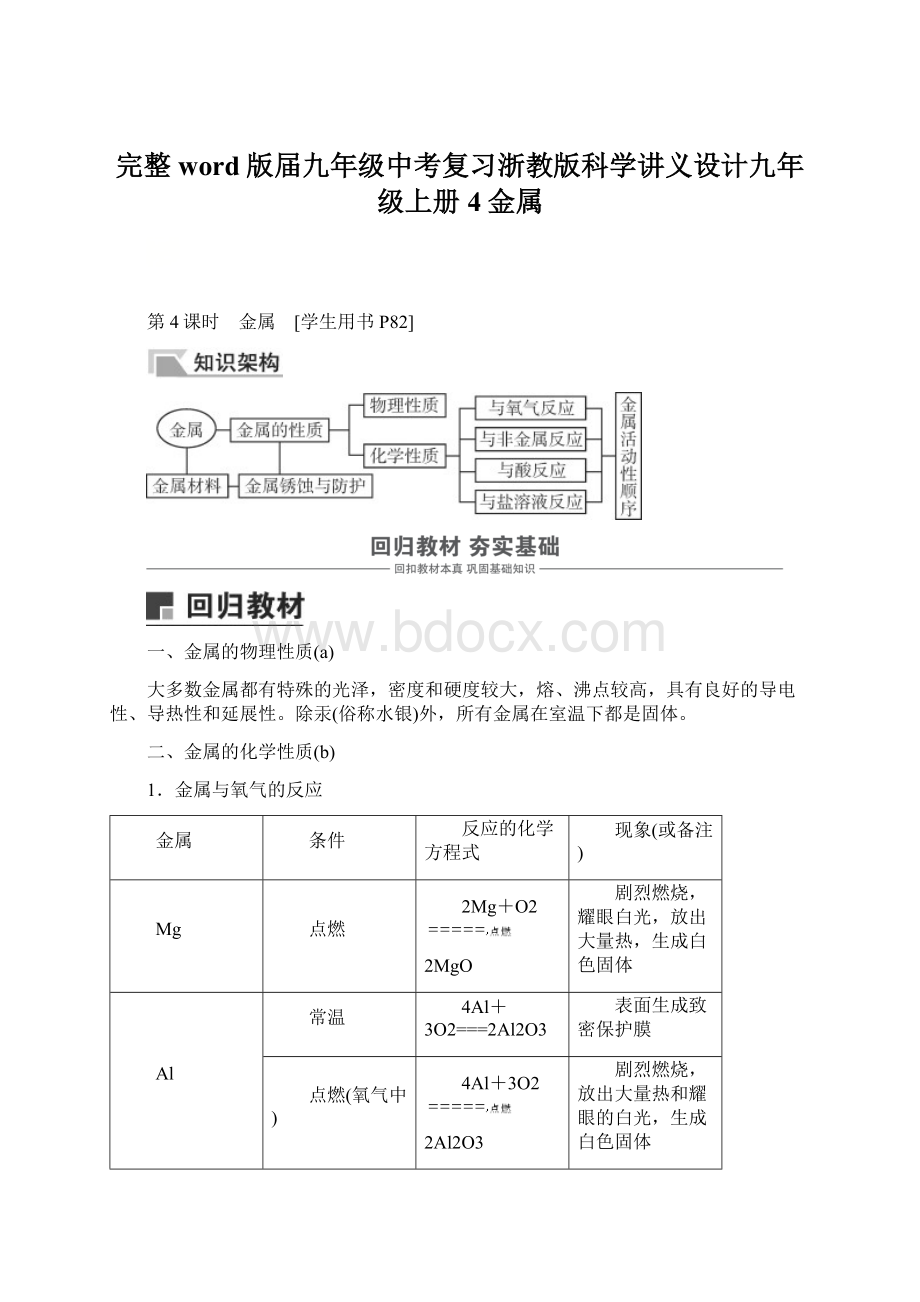
完整word版届九年级中考复习浙教版科学讲义设计九年级上册4金属
第4课时 金属 [学生用书P82]
一、金属的物理性质(a)
大多数金属都有特殊的光泽,密度和硬度较大,熔、沸点较高,具有良好的导电性、导热性和延展性。
除汞(俗称水银)外,所有金属在室温下都是固体。
二、金属的化学性质(b)
1.金属与氧气的反应
金属
条件
反应的化学方程式
现象(或备注)
Mg
点燃
2Mg+O2
2MgO
剧烈燃烧,耀眼白光,放出大量热,生成白色固体
Al
常温
4Al+3O2===2Al2O3
表面生成致密保护膜
点燃(氧气中)
4Al+3O2
2Al2O3
剧烈燃烧,放出大量热和耀眼的白光,生成白色固体
Fe
常温、潮湿空气
4Fe+3O2+nH2O===2Fe2O3·nH2O
在氧气和水共同作用下,会生成暗红色疏松的铁锈
氧气中点燃
3Fe+2O2
Fe3O4
剧烈燃烧,火星四射,放出大量热,生成黑色固体
Cu
加热
2Cu+O2
2CuO
铜丝表面逐渐变为黑色
潮湿空气
2Cu+O2+CO2+H2O===Cu2(OH)2CO3
铜表面生成一层绿色物质
Au、Ag
高温下也不与氧气反应,“真金不怕火炼”
大多数金属都能与氧气反应,但难易和剧烈程度不同。
Mg、Al等在常温下就能与氧气反应;Fe、Cu等在常温下几乎不能单独与氧气反应,点燃或加热情况下可以发生反应;Au、Ag等在高温时也不与氧气反应。
2.金属与酸的反应
金属
现象
反应的化学方程式
镁
剧烈反应,大量气泡,溶液仍为无色,放热
Mg+2HCl===MgCl2+H2↑
Mg+H2SO4===MgSO4+H2↑
铝
剧烈反应(比镁稍缓),大量气泡,溶液仍为无色,放热
2Al+6HCl===2AlCl3+3H2↑
2Al+3H2SO4===Al2(SO4)3+3H2↑
锌
反应较剧烈,大量气泡,溶液仍为无色,放热
Zn+2HCl===ZnCl2+H2↑
Zn+H2SO4===ZnSO4+H2↑
铁
反应缓慢,有气泡产生,溶液由无色逐渐变为浅绿色
Fe+2HCl===FeCl2+H2↑
Fe+H2SO4===FeSO4+H2↑
铜
不反应
Mg、Al、Zn、Fe的金属活动性比氢强,能置换出稀硫酸或稀盐酸中的氢。
等质量的Mg、Al、Zn、Fe四种金属与足量稀硫酸或稀盐酸反应时产生氢气的量:
__Al>Mg>Fe>Zn__。
3.金属与盐的反应
实验操作
现象
反应的化学方程式
铁丝浸入硫酸铜溶液
铁丝表面出现红色物质,溶液由蓝色逐渐变为浅绿色
Fe+CuSO4===Cu+FeSO4
铜丝浸入硝酸银溶液
铜丝表面出现银白色物质,溶液由无色逐渐变为蓝色
Cu+2AgNO3===Cu(NO3)2+2Ag
表中三种金属的活动性由强到弱的顺序:
Fe>Cu>Ag。
活动性强的金属能把活动性弱的金属从它的盐的水溶液中置换出来。
【知识拓展】
1.此类反应一定在溶液中进行,不溶于水的化合物一般不与金属反应,如Cu与AgCl不能进行置换反应。
2.K、Ca、Na活动性非常强,但不能用它们置换盐溶液中的金属,因为它们能同溶液中的水剧烈反应。
三、寻找金属变化的规律(b)
1.金属活动性顺序:
__K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au__。
2.金属的活动性顺序中,位置越靠前的金属活动性越强,位于氢前面的金属能置换出酸中的氢,位于前面的金属能把位于后面的金属从它的盐的水溶液中置换出来,K、Ca、Na三种活泼金属能直接置换出水中的氢。
四、金属的锈蚀和防护(a)
1.铁锈蚀的条件:
水、氧气。
铜锈蚀的条件:
水、氧气、二氧化碳。
2.防锈蚀的方法:
改变金属内部结构,如制成不锈钢等;在金属表面形成各种保护层,如涂防锈油、油漆;形成氧化物保护膜等。
3.保护金属资源的有效途径:
防止金属的腐蚀,金属的回收利用,有计划合理地开采矿物,寻找金属的替用品等。
五、金属材料——合金(a)
1.合金是把一种金属跟其他一种或几种金属(或非金属)一起熔合而成的具有金属特性的物质。
2.合金的形成条件:
其中任一金属的熔点不能高于另一金属的沸点(当由两种金属形成合金时)。
3.常见的铁合金有碳素钢和合金钢(锰钢、硅钢、钨钢、不锈钢等)。
常见的铜合金有青铜、黄铜、白铜等。
【知识拓展】
合金是金属与金属或金属与非金属的混合物。
合金的很多性能与组成它们的纯金属不同。
日常使用的大多数金属材料都是合金。
类型一 金属与酸反应
典例1[2019·绍兴]将质量均为10g的Mg、Fe、Zn三种金属分别放入质量和溶质质量分数均相同的三份稀硫酸中,反应完成后,生成氢气的质量关系不可能的是( D )
【解析】Mg、Fe、Zn三种金属与硫酸反应时均按1∶1的比例反应,Mg、Fe、Zn的相对原子质量分别为24、56、65,当Zn、Fe不足时,Mg、Fe、Zn反应生成氢气的质量Mg>Fe>Zn,图像可能是B选项;当Fe恰好完全反应或过量、Zn不足时,反应生成的氢气的质量Mg=Fe>Zn,图像可能是C选项;当Zn恰好完全反应或过量时,三份硫酸生成氢气的质量相等,图像可能是A选项。
(或借助数轴分析,以稀硫酸的质量为变量,
,设所加稀硫酸的质量为m。
10gZn恰好完全反应时,消耗稀硫酸的质量为mZn,10gFe恰好完全反应时,消耗稀硫酸的质量为mFe,10gMg恰好完全反应时,消耗稀硫酸的质量为mMg。
根据稀硫酸是否完全反应及相同质量的金属完全反应生成氢气质量的大小,由数轴可以知:
当m≤mZn时,A项符合;当m>mFe时,B项符合;当mZn<m≤mFe时,C项符合。
)
跟踪训练1[2019·杭州一模联考]小乐将一片未经打磨的铝片放入一盛有稀盐酸的容器后,将容器密封。
容器内的气压变化如图所示。
则下列分析错误的是( B )
图4-1
A.ab段气压变化不明显的原因是铝表面的氧化铝先与稀盐酸反应
B.bc段气压显著增大的唯一原因是铝与稀盐酸反应产生大量氢气
C.bc段铝与稀盐酸反应速率先变快后变慢,导致变慢的主要原因是稀盐酸的浓度降低
D.cd段气压逐渐下降的主要原因是反应结束后温度降低
类型二 金属与盐溶液反应
典例2[2019·宁波]将一定量的铜锌混合粉末放入盛有硝酸银溶液的烧杯中,不断搅拌,充分反应后过滤。
向得到的滤渣和滤液中分别加入足量的稀盐酸,均无现象。
则滤渣中( B )
A.一定有银,可能有铜和锌
B.一定有银,可能有铜,一定没有锌
C.一定有银和铜,可能有锌
D.一定有银和铜,一定没有锌
【解析】铜锌混合粉末与硝酸银溶液反应,根据金属活动性顺序,硝酸银先与锌反应,如果过量再与铜反应。
向滤渣中加入足量稀盐酸无明显现象,说明不含锌;向滤液中加入足量稀盐酸无明显现象,说明不含Ag+。
故锌、硝酸银均反应完全。
因此滤渣中一定有银,可能有铜,一定没有锌。
跟踪训练2[2019·临海三门温岭模拟]向一定质量的AgNO3溶液中加入铜、锌的混合粉末,充分反应后过滤,得到溶液甲和固体乙,下列判断不正确的是( D )
图4-2
A.若向溶液甲中滴加氯化钠溶液产生白色沉淀,则固体乙是Ag
B.若溶液甲呈蓝色,则固体乙中一定含Ag,可能含有Cu
C.若固体乙中含有锌、铜、银三种金属,则溶液甲中的溶质是Zn(NO3)2
D.若向固体乙中滴加稀盐酸没有气泡,则溶液甲中的溶质是Zn(NO3)2和Cu(NO3)2
类型三 探究金属活动性顺序
典例3[2019·杭州萧山区模拟]某化学小组的同学在探究银、铜、铁三种金属的有关性质时,进行了如图所示的实验,其中溶液过量:
图4-3
(1)①号试管中发生的反应方程式为__Fe+CuSO4===Cu+FeSO4__。
(2)试管内物质反应结束后,将①②试管内的物质倒入烧杯中,一段时间后,溶液中一定有的阳离子是__Fe2+、Cu2+__。
当看到__红色固体表面出现银白色(黑色)物质(答红色固体物质减少或消失均可)__现象时,能证明银、铜、铁三种金属的活动性顺序。
(3)请设计另一种能证明银、铜、铁三种金属活动性顺序的实验方案:
__将铜片分别放入盛有适量硫酸亚铁溶液和硝酸银溶液的烧杯中,观察铜片表面是否析出金属__。
跟踪训练3[2019·金华六校模拟]为了验证Fe、Cu、Ag三种金属的金属活动性强弱,小明设计了如图所示的实验,其中可以达到实验目的的组合是( C )
图4-4
A.①②B.①③
C.②④D.③④
类型四 金属的锈蚀与防护
典例4[2019·杭州校级模拟]小金发现家里的铜质水龙头表面出现了一层绿色的锈渍,他依照钢铁锈蚀的探究方法进行如下实验探究铜生成“铜绿”的条件:
【査阅资料】了解到这层锈渍的化学成分是碱式碳酸铜[Cu2(OH)2CO3],俗称“铜绿”。
它受热会分解生成三种氧化物。
请完成“铜绿”分解的化学方程式:
__1__Cu2(OH)2CO3===__2__CuO+__1__CO2↑+__H2O__。
【猜想与假设】经仔细了解了水龙头的使用环境后,据“铜绿”的组成和査阅的资料判断,铜绿可能是铜与__O2、CO2、H2O__作用而形成的。
【设计与实验】借鉴课本“铁钉锈蚀条件的探究”实验。
小金设计了“铜片锈蚀条件的探究”实验。
实验如图所示(所用铜片洁净、光亮,试管内的“
”为铜片):
实验较长时间后。
发现__D__试管中铜片最先生锈(填试管字母编号)。
图4-5
【评价与改进】小金设计的实验还不够完善,要得出正确的结论,还要补充一个实验。
你认为要补充的一个实验是(用图表示亦可)__把铜片放在一个盛有干燥空气的试管中,形成对照实验__。
跟踪训练4[2019·湖州南浔区一模]世界每年因锈蚀而损失的金属数量巨大,防止金属锈蚀已成为科学研究中的重大问题。
下列有关金属锈蚀与保护措施中不正确的是( C )
A.在铁表面刷油漆可以防止铁锈蚀
B.及时擦干被雨水淋湿的自行车可防止自行车生锈
C.铝的抗锈蚀性能比铁强,生活中可用钢丝球洗刷铝锅
D.铁锈蚀的实质是铁与空气中的氧气、水蒸气等发生了化学变化
1.[2019·嘉兴舟山]科学兴趣小组对金属R的活动性探究时发现:
将R放入稀硫酸中,有气泡产生,同时生成正二价的盐;将R放入ZnSO4溶液中无任何变化。
根据以上信息,下列化学方程式正确的是( C )
A.R+MgCl2===RCl2+Mg
B.R+2AgCl===RCl2+2Ag
C.R+2HCl===RCl2+H2↑
D.Al+RSO4===AlSO4+R
【解析】由题可知,金属R的活动性Zn>R>H。
R的活动性小于Mg,不能与MgCl2进行置换反应。
AgCl不溶于水,不与R反应。
Al与RSO4反应生成的应是Al2(SO4)3。
2.[2019·嘉兴秀洲区校级一模]根据金属活动性顺序判断,下列容器与所盛溶液不会发生化学反应的是( B )
A.用铁制容器盛盐酸
B.用铜制容器盛盐酸
C.用铁制容器盛硝酸银溶液
D.用铜制容器盛硝酸银溶液
3.[2019·杭州校级模拟]将一定量的铝粉和氧化铜粉末混合加热,化学方程式为:
2Al+3CuO
3Cu+Al2O3。
反应结束后,为了检验氧化铜是否完全反应,
取少量反应后的固体,加入足量的稀硫酸充分反应后,将铁片插入溶液中。
下列叙述的现象中,能够说明氧化铜没有完全反应的是( C )
①加入稀硫酸后,有气泡生成
②加入稀硫酸后,没有气泡生成
③插入溶液中的铁片表面有红色物质析出
④加入稀硫酸后,溶液中有红色不溶物质
A.①③④ B.②③
C.只有③D.③④
4.[2019·杭州
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 完整 word 九年级 中考 复习 浙教版 科学 讲义 设计 上册 金属
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
