 专题08 第26题 实验大综合强化训练高考化学二三轮复习题型大突破系列原卷版.docx
专题08 第26题 实验大综合强化训练高考化学二三轮复习题型大突破系列原卷版.docx
- 文档编号:2870884
- 上传时间:2022-11-16
- 格式:DOCX
- 页数:17
- 大小:468.27KB
专题08 第26题 实验大综合强化训练高考化学二三轮复习题型大突破系列原卷版.docx
《专题08 第26题 实验大综合强化训练高考化学二三轮复习题型大突破系列原卷版.docx》由会员分享,可在线阅读,更多相关《专题08 第26题 实验大综合强化训练高考化学二三轮复习题型大突破系列原卷版.docx(17页珍藏版)》请在冰豆网上搜索。
专题08第26题实验大综合强化训练高考化学二三轮复习题型大突破系列原卷版
专题08第26题实验大综合强化训练
1.在梨、香蕉等水果中存在着乙酸正丁酯。
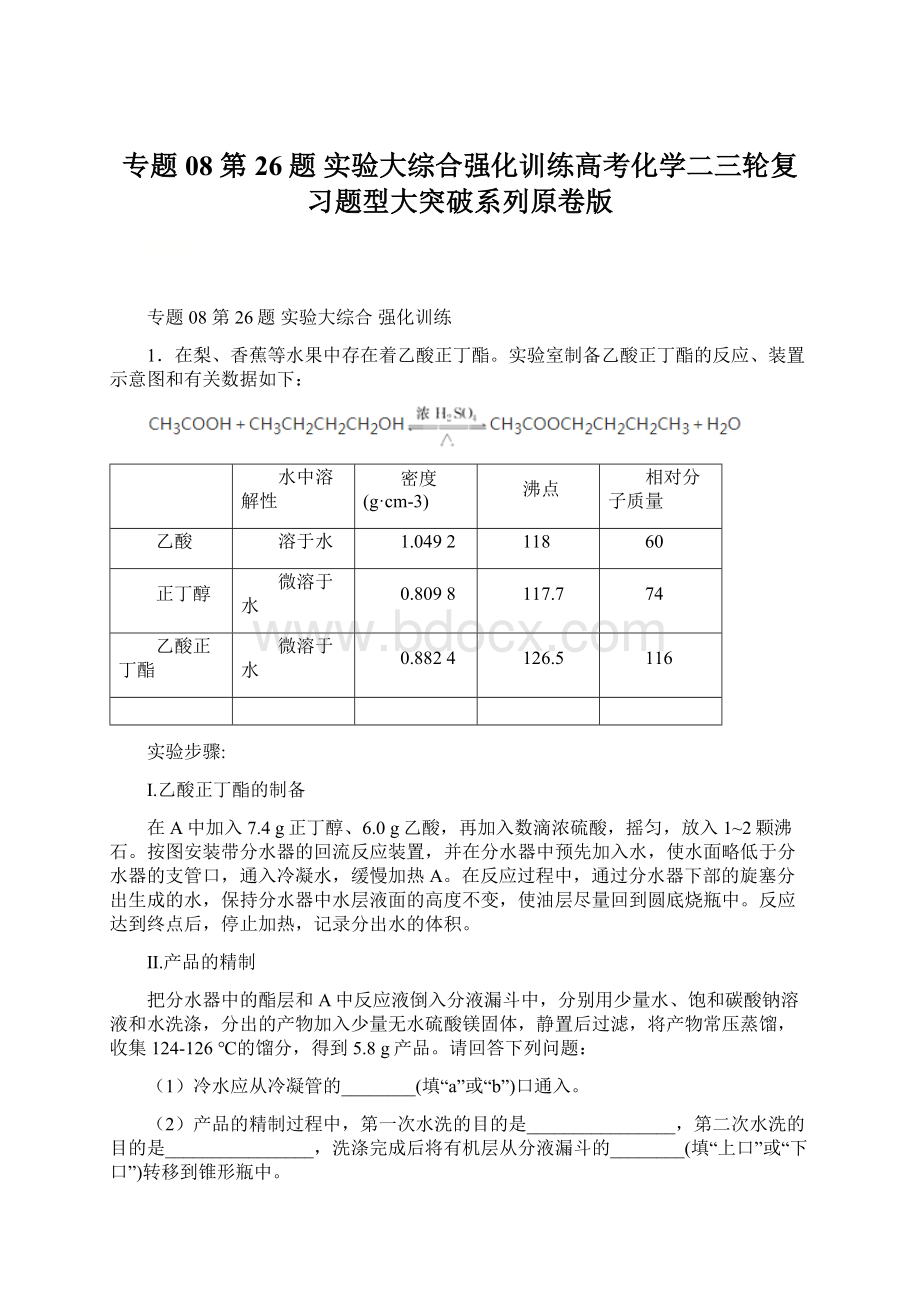
实验室制备乙酸正丁酯的反应、装置示意图和有关数据如下:
水中溶解性
密度(g·cm-3)
沸点
相对分子质量
乙酸
溶于水
1.0492
118
60
正丁醇
微溶于水
0.8098
117.7
74
乙酸正丁酯
微溶于水
0.8824
126.5
116
实验步骤:
Ⅰ.乙酸正丁酯的制备
在A中加入7.4g正丁醇、6.0g乙酸,再加入数滴浓硫酸,摇匀,放入1~2颗沸石。
按图安装带分水器的回流反应装置,并在分水器中预先加入水,使水面略低于分水器的支管口,通入冷凝水,缓慢加热A。
在反应过程中,通过分水器下部的旋塞分出生成的水,保持分水器中水层液面的高度不变,使油层尽量回到圆底烧瓶中。
反应达到终点后,停止加热,记录分出水的体积。
Ⅱ.产品的精制
把分水器中的酯层和A中反应液倒入分液漏斗中,分别用少量水、饱和碳酸钠溶液和水洗涤,分出的产物加入少量无水硫酸镁固体,静置后过滤,将产物常压蒸馏,收集124-126℃的馏分,得到5.8g产品。
请回答下列问题:
(1)冷水应从冷凝管的________(填“a”或“b”)口通入。
(2)产品的精制过程中,第一次水洗的目的是________________,第二次水洗的目的是________________,洗涤完成后将有机层从分液漏斗的________(填“上口”或“下口”)转移到锥形瓶中。
(3)本实验提高产品产率的方法是_________________________________________。
(4)判断反应终点的依据是_______________________________________________。
(5)该实验过程中,生成乙酸正丁酯的产率是_______________________________。
2.碘化钠在医疗及食品方面有重要的作用。
实验室用NaOH、单质碘和水合肼(N2H4·H2O)为原料制备碘化钠。
已知:
水合肼具有还原性。
回答下列问题:
(1)水合肼的制备反应原理为:
CO(NH2)2(尿素)+NaClO+2NaOH=N2H4·H2O+NaCl+Na2CO3
①制取次氯酸钠和氢氧化钠混合液的连接顺序为__________(按气流方向,用小写字母表示)。
若该实验温度控制不当,反应后测得三颈瓶内ClO-与ClO3-的物质的量之比为5:
1,则氯气与氢氧化钠反应时,被还原的氯元素与被氧化的氯元素的物质的量之比为____。
②制备水合肼时,应将__________滴到_________中(填“NaClO溶液”或“尿素溶液”),且滴加速度不能过快。
③尿素的电子式为__________________
(2)碘化钠的制备:
采用水合肼还原法制取碘化钠固体,其制备流程如图所示:
在“还原”过程中,主要消耗反应过程中生成的副产物IO3-,该过程的离子方程式为___。
(3)测定产品中NaI含量的实验步骤如下:
a.称取10.00g样品并溶解,在500mL容量瓶中定容;
b.量取25.00mL待测液于锥形瓶中,然后加入足量的FeCl3溶液,充分反应后,再加入M溶液作指示剂:
c.用0.2000mol·L−1的Na2S2O3标准溶液滴定至终点(反应方程式2Na2S2O3+I2=Na2S4O6+2NaI),重复实验多次,测得消耗标准溶液的体积为15.00mL。
①M为____________(写名称)。
②该样品中NaI的质量分数为_______________。
3.化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:
该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I、摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水搅拌、过滤。
并进行如下实验
(1)请完成表格中的填空:
实验步骤
实现现象
反应的离子方程式
往滤渣中加入过量NaOH溶液。
①______________
过滤,往所得滤液中通入过量二氧化碳,
②_________
③______________
继续加入过量稀盐酸
④_________
II、牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
依据实验过程回答下列问题:
(2)实验过程中先后两次鼓入空气,第二次鼓入空气的目的是:
______。
(3)C中反应生成BaCO3的化学方程式是_________________。
(4)下列各项措施中,不能提高测定准确度的是________(填标号)。
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A—B之间增添盛有浓硫酸的洗气装置
D.在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)、实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g。
则样品中碳酸钙的质量分数为_______。
(6)某同学提出将C中的Ba(OH)2换成浓H2SO4,通过测定D装置反应前后的质量差也可以测定CaCO3的含量,假设反应前D装置的质量为m1,实验结束后D装置的质量为m2,则样品中CaCO3的质量为_______。
实验证明按此测定的结果偏高,原因是______。
4.二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发粘、遇冷变硬的性质。
查阅资料可知S2Cl2具有下列性质:
物理性质
毒性
色态
挥发性
熔点
沸点
剧毒
金黄色液体
易挥发
-76℃
138℃
化学性质
①300℃以上完全分解;
②S2Cl2+Cl2
2SCl2;
③遇高热或与明火接触,有引起燃烧的危险;
④受热或遇水分解放热,放出腐蚀性烟气;
Ⅰ.制取少量S2Cl2
实验室可利用硫与少量氯气在110~140℃反应制得S2Cl2粗品。
(1)仪器m的名称为___,装置A中发生反应的离子方程式为______________。
(2)装置连接顺序:
A→___→___→___→E→D。
______________
(3)为了提高S2Cl2的纯度,实验的关键是控制好温度和__________________。
(4)若D中所装试剂为碱石灰,则该装置的作用为______________。
II.测定产品中SO2Cl2的含量,实验步骤如下:
①取1.8g产品加入足量Ba(OH)2溶液,充分振荡、过滤、洗涤,将所得溶液均放入锥形瓶中;
②向锥形瓶中加入硝酸酸化,再加入0.2000mol·L-1的AgNO3溶液l00.00mL;
③向其中加入2mL硝基苯,用力摇动,使沉淀表面被有机物覆盖;
④加入NH4Fe(SO4)2指示剂,用0.1000mol·L-1NH4SCN溶液滴定过量Ag+,终点所用体积为10.00mL。
已知:
Ksp(AgCl)=3.2×10-10;Ksp(AgSCN)=2×10-12
(5)滴定终点的现象为_____________________________。
(6)产品中SO2Cl2的质量分数为__________,若步骤③不加入硝基苯则所测SO2Cl2含量将________(填“偏高”、“偏低”或“无影响”)。
5.实验室需要0.1mol/LNaOH溶液450mL和0.5mol/LH2SO4溶液450mL。
根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是______(填序号)。
仪器C的名称是________。
本实验所需玻璃仪器E的规格和名称是________。
(2)下列操作中,容量瓶所不具备的功能有________(填序号)
A.配制一定体积准确浓度的标准溶液B.长期贮存溶液
C.用来加热溶解固体溶质D.量取220mL溶液
(3)在配制NaOH溶液的实验中,其他操作均正确,若定容时仰视刻度线,则所配制溶液的浓度将________0.1mol/L(填“大于”“等于”或“小于”,下同)。
若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度将________0.1mol/L。
(4)根据计算得知:
所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为________mL(计算结果保留一位小数)。
如果实验室有10mL、25mL、50mL规格的量筒,应选用________mL的最好。
(5)如果定容正确的操作是_________________________。
(6)引流需要玻璃棒,其正确的放置方式_________________________
6.有学生用五氧化二磷作为乙醇脱水制乙烯的催化剂,进行相关实验。
按右表所示的量和反应条件在三颈瓶中加入一定量P2O5,并注入95%的乙醇,并加热,观察现象。
实验
P2O5
95%乙醇量
加热方式
实验1
2g
4mL
酒精灯
实验2
2g
4mL
水浴70℃
实验结果如下:
实验
实验现象
三颈瓶
收集瓶
试管
实验1
酒精加入时,立刻放出大量的白雾,开始有气泡产生,当用酒精灯加热时,气泡加快生成并沸腾,生成粘稠状液体。
有无色液体
溶液褪色
实验2
酒精加入时,有少量白雾生成,当用水浴加热时,不产生气泡,反应一个小时,反应瓶内生成粘稠状液体
有无色液体
溶液不褪色
根据上述资料,完成下列填空。
(1)写出乙醇制乙烯的化学方程式______________________________________。
(2)上图装置中冷凝管的作用是___________,进水口为(填“a”或“b”)______,浓硫酸的作用是_____________。
(3)实验1使溴的四氯化碳溶液褪色的物质是___________。
(4)实验2中,水浴加热所需仪器有________、________(加热、夹持仪器、石棉网除外)。
(5)三颈瓶、收集瓶中的液体经检验为磷酸三乙酯,写出三颈瓶中生成磷酸的化学方程式
_____________________,P2O5在实验1中的作用是______________________。
(6)根据实验1、2可以推断:
①以P2O5作为催化剂获得乙烯的反应条件是____________
②P2O5与95%乙醇在加热条件下可以发生的有机反应的类型是________反应。
7.苯胺
是重要的化工原料。
某兴趣小组在实验室里进行苯胺的相关实验。
已知:
①
和NH3相似,与盐酸反应生成易溶于水的盐
②用硝基苯制取苯胺的反应原理:
+3Sn+12HCl
+3SnCl4+4H2O
③有关物质的部分物理性质见下表:
I.比较苯胺与氨气的性质
(1)将分别蘸有浓氨水和浓盐酸的玻璃棒靠近,产生白烟,反应的化学方程式为____;用苯胺代替浓氨水重复上述实验,却观察不到白烟,原因是____。
Ⅱ.制备苯胺
往图1所示装置(夹持装置略,下同)的冷凝管口分批加入20mL浓盐酸(过量),置于热水浴中回流20min,使硝基苯充分还原;冷却后,往三颈烧瓶中滴入一定量50%NaOH溶液,至溶液呈碱性。
(2)冷凝管的进水口是____(填“a”或“b”);
(3)滴加NaOH溶液的主要目的是析出苯胺,反应的离子方程式为____。
Ⅲ.提取苯胺
i.取出图1所示装置中的三颈烧瓶,改装为图2所示装置。
加热装置A产生水蒸气,烧瓶C中
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题08 第26题 实验大综合强化训练高考化学二三轮复习题型大突破系列原卷版 专题 08 26 实验 综合 强化 训练 高考 化学 三轮 复习 题型 突破 系列 原卷版
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 如何打造酒店企业文化2刘田江doc.docx
如何打造酒店企业文化2刘田江doc.docx
