 江西铜鼓届高三理科实验班第五次理科综合能力测试化学部分试题.docx
江西铜鼓届高三理科实验班第五次理科综合能力测试化学部分试题.docx
- 文档编号:28584673
- 上传时间:2023-07-19
- 格式:DOCX
- 页数:13
- 大小:156.03KB
江西铜鼓届高三理科实验班第五次理科综合能力测试化学部分试题.docx
《江西铜鼓届高三理科实验班第五次理科综合能力测试化学部分试题.docx》由会员分享,可在线阅读,更多相关《江西铜鼓届高三理科实验班第五次理科综合能力测试化学部分试题.docx(13页珍藏版)》请在冰豆网上搜索。
江西铜鼓届高三理科实验班第五次理科综合能力测试化学部分试题
理科综合能力测试[化学部分]
第Ⅰ卷
(选择题,每小题6分,共48分)
在下列各题的四个选项中,只有一个选项是符合题目要求的。
以下数据可供解题时参考:
相对原子质量:
H1,C12,O16,Na23,Al27,S32,Cl35.5,Fe56,Zn65
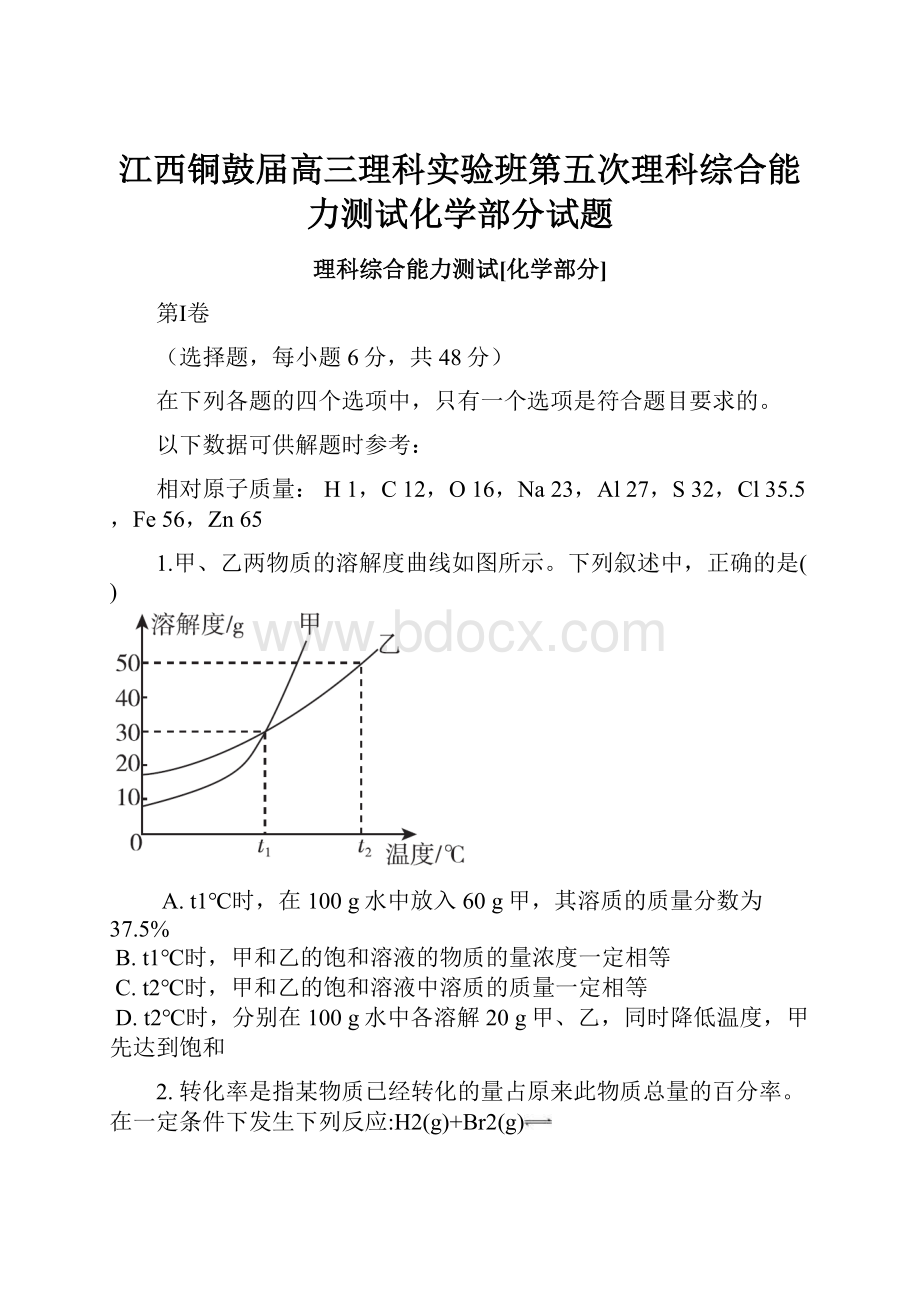
1.甲、乙两物质的溶解度曲线如图所示。
下列叙述中,正确的是( )
A.t1℃时,在100 g水中放入60 g甲,其溶质的质量分数为37.5%
B.t1℃时,甲和乙的饱和溶液的物质的量浓度一定相等
C.t2℃时,甲和乙的饱和溶液中溶质的质量一定相等
D.t2℃时,分别在100 g水中各溶解20 g甲、乙,同时降低温度,甲先达到饱和
2.转化率是指某物质已经转化的量占原来此物质总量的百分率。
在一定条件下发生下列反应:
H2(g)+Br2(g)
2HBr(g)。
固定容积为2 L的容器内充入H2(g)和Br2(g)分别为3 mol和2 mol,达到反应限度时,HBr的浓度为1.56 mol/L。
则Br2的转化率为( )
A.78% B.52%
C.39% D.0.78 mol/L
3.下列关于有机物的说法中正确的是 ( )
①棉花、蚕丝和人造丝的主要成分都是纤维素 ②淀粉、油脂、蛋白质在一定条件下都能发生水解 ③除去溴苯中的少量溴:
加入NaOH溶液,振荡、静置分层后,除去水层 ④除去乙酸乙酯中残留的乙酸,加过量饱和Na2CO3溶液振荡后,静置分液 ⑤塑料、橡胶和光导纤维都是合成高分子材料 ⑥石油的分馏、裂化和煤的干馏都是化学变化
A.①⑤⑥ B.①②③⑤
C.②③④ D.③④⑤⑥
4.短周期元素X、Y、Z、W、Q在周期表中相对位置如图所示。
下列说法正确的是( )
A.工业上常用电解法生产Z、Q的单质
B.形成的简单离子的半径大小顺序:
r(Z)>r(Q)>r(Y)
C.Z的最高价氧化物对应水化物是三元弱酸
D.最简单气态氢化物的热稳定性:
W>X
5.下列关于氧化物及过氧化物的说法中正确的是( )
A.因为H2O2和Na2O2都是过氧化物,所以二者化学键的类型完全相同
B.标准状况下,2.24 L NO2和N2O4组成的混合气体中,原子总数是分子总数的3倍
C.NO、NO2、SO2、SO3都是酸性氧化物
D.常温常压下,5.6 L SO2与足量的O2混合,充分反应后,生成的SO3物质的量小于0.25 mol
6.下列说法正确的是 ( )
A.水的离子积KW只与温度有关,但外加酸、碱、盐一定会影响水的电离程度
B.Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关
C.常温下,在0.01 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使溶液的pH减小,c(N
)/c(NH3·H2O)的比值增大
D.室温下,CH3COOH的Ka=1.7×10-5,NH3·H2O的Kb=1.7×10-5,CH3COOH溶液中的c(H+)与NH3·H2O中的c(OH-)相等
7.在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2 L密闭容器中发生下述反应:
PCl3(g)+ Cl2(g)
PCl5(g)
PCl3(g)
Cl2(g)
PCl5(g)
初始浓度(mol·L-1)
2.0
1.0
0
平衡浓度(mol·L-1)
c1
c2
0.4
A.若升高温度,反应的平衡常数减小,则正反应为吸热
B.反应5 min内,v(PCl3)=0.08 mol·L-1·min-1
C.当容器中Cl2为1.2 mol时,可逆反应达到平衡状态
D.平衡后移走2.0 mol PCl3和1.0 mol Cl2,在相同条件下再达平衡时,c(PCl5)<0.2 mol·L-
8. “天宫一号”飞行器在太空工作期间必须有源源不断的电源供应。
其供电原理是白天太阳能帆板发电,将一部分电量直接供给天宫一号,另一部分电量储存在镍氢电池里,供黑夜时使用。
下图为镍氢电池构造示意图(氢化物电极为储氢金属,可看做H2直接参加反应)。
下列说法正确的是 ( )
A.充电时阴极区电解质溶液pH降低
B.在使用过程中此电池要不断补充水
C.放电时NiOOH在电极上发生氧化反应
D.充电时阳极反应为Ni(OH)2-e-+OH-
NiOOH+H2O
第Ⅱ卷
(非选择题,共4小题,共52分)
9、I.X、Y、Z、M、N为短周期的五种主族元素,其中X、Z同主族,Y、Z同周期,M与X,Y既不同族,也不同周期。
X原子最外层电子数是核外电子层数的三倍,Y的最高化合价与其最低化合价的代数和等于6。
N是短周期主族元素中原子半径最大的非金属元素。
(1)请写出M的元素符号:
____________,Z的原子结构示意图:
____________。
M与X两元素可形成两种液态化合物,其化学式分别为 。
(2)请写出N元素在周期表中的位置 ;与N同族的短周期元素L,其最高价氧化物的电子式为 。
(3)Y与Z相比,非金属性较强的元素是____ __ __,(填元素符号)可以证明该结论的实验事实是 。
II.下列转化关系中,X、Y是生活中用途广泛的两种金属单质,A、B是氧化物,A为红棕色固体,C、D、E是中学常见的三种化合物。
分析转化关系回答问题。
(1)请写出反应①的化学方程式:
________________________________。
(2)由D到E的离子方程式_________________________________。
(3)若试剂a是NaOH溶液,写出单质X与NaOH溶液反应的离子方程式 。
(4)若试剂b是H2SO4,工业上用E、H2SO4和NaNO2为原料制取高效净水剂Y(OH)SO4,已知还原产物为NO,则该反应的化学方程式是________________________________。
(5)工业上电解熔融的B制取X时,若阳极产生的气体在标准状况下的体积为33.6L,则阴极产物的质量为______________。
10.(14分)氯化铁和高铁酸钾都是常见的水处理剂。
下图为制备氯化铁及进一步将其氧化制备高铁酸钾的工艺流程。
请回答下列问题:
(1)氯化铁有多种用途,请用离子方程式表示下列用途的原理。
①氯化铁做净水剂 。
②用FeCl3溶液(32%~35%)腐蚀铜印刷线路板 。
(2)吸收剂X的化学式为 ;氧化剂Y的化学式为 。
(3)碱性条件下反应①的离子方程式为 。
(4)过程②将混合溶液搅拌半小时,静置,抽滤获得粗产品。
该反应的化学方程式为2KOH+Na2FeO4
K2FeO4+2NaOH,请根据复分解反应原理分析反应发生的原因 。
(5)K2FeO4在水溶液中易发生反应:
4Fe
+10H2O
4Fe(OH)3+8OH-+3O2↑。
在提纯K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用 (填序号)。
A.H2O
B.稀KOH溶液、异丙醇
C.NH4Cl溶液、异丙醇
D.Fe(NO3)3溶液、异丙醇
(6)可用滴定分析法测定粗K2FeO4的纯度,有关反应离子方程式:
①Fe
+Cr
+2H2O
Cr
+Fe(OH)3↓+OH-
②2Cr
+2H+
Cr2
+H2O
③Cr2
+6Fe2++14H+
2Cr3++6Fe3++7H2O
现称取1.980 g粗高铁酸钾样品溶于适量氢氧化钾溶液中,加入稍过量的KCrO2,充分反应后过滤,滤液定容于250 mL容量瓶中。
每次取25.00 mL加入稀硫酸酸化,用0.1000 mol/L的(NH4)2Fe(SO4)2标准溶液滴定,三次滴定消耗标准溶液的平均体积为18.93 mL。
则上述样品中高铁酸钾的质量分数为 。
11.如图所示是用于气体制备、干燥(或除杂质)、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去,各装置可重复使用也可不用)。
请根据下列要求回答问题。
(1)若用A—C—D—B组合进行氢气还原氧化铜实验。
分液漏斗中的试剂是盐酸,C中试剂是水,其作用是
;A中反应开始一段时间后,再加热B。
加热B之前的实验操作是 。
(2)为验证氯气不能使干燥的红布条褪色,置红布条于B中,按A—C—B—D连接成实验装置体系。
A锥形瓶中试剂选用高锰酸钾晶体,则分液漏斗中的液体是 (填名称);C中试剂是 (填名称)。
已知高锰酸钾反应生成+2价的锰离子,写出此法制备氯气的离子方程式 。
(3)为了进行氨的催化氧化实验,若锥形瓶中盛装足量的Na2O2粉末,分液漏斗中盛装浓氨水,慢慢打开分液漏斗的活塞,产生的气体通过红热的铂粉,各仪器装置按气流方向从左到右连接顺序是(填字母) ;装置B中发生反应的化学方程式为 。
12、一氯甲烷,也叫甲基氯,常温下是无色气体,密度为0.9159克/厘米3,熔点为-97.73℃,沸点为-24.2℃,18℃时在水中的溶解度为280毫升/毫升水,与乙醚、丙酮或苯互溶,能溶于乙醇。
在实验室里可用下图装置制取一氯甲烷:
制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸。
试填写下列空白:
(1)制备一氯甲烷的化学方程式 ,
(2)装置b的作用是 ;
(3)已知卤代烃能发生碱性水解,转化为醇。
装置e中可能发生的反应方程式为 ;
(4)检验气体产物CH3Cl的方法是:
在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃燃烧现象有明显区别)。
CH3Cl燃烧的化学方程式是 ;
(5)实验中实际按甲醇和浓盐酸1︰2(物质量之比)进行反应的理由是 ;
(6)某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇~浓盐酸的混和液的量比正常情况下多(装置的气密性没有问题),其原因是 ;
(7)实验结束后,d中收集到的液体中含有。
参考答案及评分标准
1.【答案】D
【解析】本题考查学生对溶解度的掌握情况及影响溶解度的因素。
温度不同溶解度不同,不同物质的溶解度受温度的影响情况不一样。
温度对甲物质的溶解度影响更大一
些。
2.【答案】A
【解析】对反应过程进行分析:
H2(g)+Br2(g)
2HBr(g)
初始(mol) 3 2 0
平衡(mol) 1.56×2
反应(mol) 1.56 1.56 3.12
则Br2的转化率为
×100%=78%
3.【答案】C
【解析】①错误,蚕丝的主要成分是蛋白质;⑤错误,光导纤维的主要成分是SiO2,为无机非金属材料;⑥错误,石油的分馏是物理变化。
4.【答案】A
【解析】本题考查元素周期表及周期律。
X、Y、Z、W、Q分别为C、F、Al、Si、Cl。
A项,电解氧化铝制得铝,电解饱和食盐水制得氯气,正确;B项,Y-为F-,Z3+为Al3+,Q-为Cl-,简单离子的半径大小顺序:
r(Cl-)>r(F-)>r(Al3+),错误;C项,Al(OH)3是两性氢氧化物,错误;D项,CH4比SiH4稳定,错误。
5.【答案】D
【解析】本题考查常见的氧化物及过氧化物的性质和组成。
A项H2O2中是共价键,Na2O2
中既有离子键又有共价键,故A错;B项分子数是0.1 mol,但是因为两种分子中的原子个数不同,所以原子数不能确定;C项NO不是酸性氧化物;D项因为常温常压下,5.6 L SO2气体的物质的量一定小于0.25 mol,而SO2与O2的反应是可逆的,所以生成的SO3物质的量必定小于0.25 mol,D正确。
【失分警示】注意对每种物质的具体情况进行详细的分析,不能只是以组成类别相似就判定为性质和结构一定相同。
6.【答案】C
【解析】本题考查了KW、Ksp及弱电解质的电离平衡常数。
A中,向水中加入不水解的中性盐时,不会影响水的电离平衡常数KW,错误;B中,Ksp只与温度和难溶电解质的性质有关,与相关离子浓度无关,错误;C中,向氨水中加入氯化铵固体,增大铵根离子浓度,氨水的电离平衡逆向移动,c(OH-)减小,溶液pH减小,但其平衡常数不变,c(N
)/c(NH3·H2O)=Kb/(OH-),比值增大,正确;D中,当氨水与醋酸等浓度时,相应的OH-与H+浓度相等,错误。
7.【答案】A
【解析】本题考查化学平衡的知识。
升高温度,反应的平衡常数减小,则此反应的正反应放热,A错。
8.【答案】D
【解析】本题考查电解的相关知识。
A选项充电时阴极区氢离子被还原pH升高;B选项在使用过程中不需补充水;C选项放电时NiOOH在电极上得电子发生还原反应。
9、
I.(7分,每空1分)
(1)H;略;H2O、H2O2
(2)第三周期第IVA族; ;
(3)Cl;Cl2+H2S=S↓+2HCl(其他答案合理也给分)
II.(7分)
(1)Fe2O3+2Al
2Fe+Al2O3(1分)
(2)Fe+2Fe3+=3Fe2+(1分)
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑(1分)
(4)2FeSO4+H2SO4+2NaNO2=2Fe(OH)SO4+Na2SO4+2NO↑(2分)(5)54g(2分)
10.【答案】
(1)①Fe3++3H2O
Fe(OH)3(胶体)+3H+(2分)
②2Fe3++Cu
2Fe2++Cu2+(2分)
(2)FeCl2 NaClO(各1分)
【解析】氯气与吸收剂X反应之后生成了氯化铁,所以X为FeCl2;Y是氢氧化钠与氯气反应之后的产物,而且具有强氧化性,应该是NaClO。
(3)2Fe3++3ClO-+10OH-
2Fe
+3Cl-+5H2O(2分)
(4)K2FeO4溶解度小,析出晶体,促进反应进行(2分)
(5)B(2分)
【解析】用稀KOH溶液可以使4Fe
+10H2O
4Fe(OH)3+8OH-+3O2↑平衡向着逆向移动,用异丙醇可以防止高铁酸钾溶解,所以选B。
(6)63.1%(2分)
【解析】利用关系式法:
Fe
~Cr
~1/2Cr2
~3Fe2+
所以,高铁酸钾的质量分数=(0.1×18.93×10-3×1/3×10×198)/1.98=63.1%。
11.【答案】
(1)吸收氢气中的HCl(或除去HCl) 检验氢气纯度(或验纯H2)
(2)浓盐酸 浓硫酸 2Mn
+16H++10Cl-
2Mn2++5Cl2↑+8H2O
(3)ADBD(D盛装碱石灰)或ADBC(C盛装氢氧化钠溶液) 4NH3+5O2
4NO+6H2O
【解析】
(1)因H2和空气的混合气体在点燃或加热时会发生爆炸,所以在加热前要验纯,以防出现安全事故。
(2)生成氯气利用氧化还原反应,一般选择由浓盐酸提供氯离子,用浓硫酸对氢气进行干燥。
(3)过氧化钠可以与浓氨水中的水反应生成O2并放出热量,升高温度,加速浓氨水的挥发。
尾气排入大气会造成污染,要对其进行吸收处理。
12、【答案】
(1)CH3OH+HCl
CH3Cl+H2O
(2)防止倒吸,保证安全(3)NaOH+HCl=NaCl+H2O
(4)2CH3Cl+3O2
2CO2+2H2O+2HCl
(5)可使甲醇充分反应,转化成一氯甲烷
(6)甲醇沸点较低(64.7℃),受热时易挥发,致使一部分未反应而逸出
(7)甲醇、盐酸、一氯甲烷
【解析】试题分析:
(1)在催化剂的作用下,甲醇和氯化氢发生取代反应生成一氯甲烷,反应的化学方程式使CH3OH+HCl
CH3Cl+H2O。
(2)由于氯化氢极易挥发,而氯化氢又极易溶解在水中,所以装置b的作用是防止倒吸,保证安全。
(3)卤代烃能发生碱性水解,转化为醇。
由于在生成醇的同时,还生成氯化氢,则装置e中可能发生的反应方程式为NaOH+HCl=NaCl+H2O。
(4)根据一氯甲烷的组成元素可知,一氯甲烷燃烧的生成物应该是CO2、水和氯化氢,则CH3Cl燃烧的化学方程式是2CH3Cl+3O2
2CO2+2H2O+2HCl。
(5)实验中实际按甲醇和浓盐酸1︰2(物质量之比)进行反应,显然盐酸是过量的,则可以提高甲醇的转化率,可使甲醇充分反应,转化成一氯甲烷。
(6)根据已知条件可知,甲醇沸点较低(64.7℃),受热时易挥发,致使一部分未反应而逸出,所以收集到一定体积的气体产物所消耗的甲醇~浓盐酸的混和液的量比正常情况下多。
(7)由于甲醇和盐酸都是易挥发的,因此实验结束后,d中收集到的液体中含有甲醇、盐酸、一氯甲烷。
考点:
考查物质制备的有关实验设计、操作、评价以及有关反应式的书写
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 江西 铜鼓 届高三 理科 实验 第五 综合 能力 测试 化学 部分 试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《彩云国物语》人物解析之红黎深转.docx
《彩云国物语》人物解析之红黎深转.docx
