 自来水行业中余氯氨氮.docx
自来水行业中余氯氨氮.docx
- 文档编号:28514349
- 上传时间:2023-07-18
- 格式:DOCX
- 页数:11
- 大小:244.78KB
自来水行业中余氯氨氮.docx
《自来水行业中余氯氨氮.docx》由会员分享,可在线阅读,更多相关《自来水行业中余氯氨氮.docx(11页珍藏版)》请在冰豆网上搜索。
自来水行业中余氯氨氮
自来水行业中余氯、氯胺类消毒剂的监测
一、常识:
在分析余氯、氯胺类消毒剂成分监测技术之前,我们首先来看一下消毒机理与其中的一些化学反应,因为这些是介绍监测技术的前提。
可能大家都已经很熟悉了,但还是希望大家都仔细看一遍,理清一下思路。
如果里面有什么错误,也请大家能提出来,一起探讨。
1、氯的消毒作用
常用氯系消毒剂有氯、次氯酸钠、漂白粉、漂白精等。
它们的杀菌机制基本相同,主要靠水解产物次氯酸起作用。
氯在水中迅速水解为次氯酸,而次氯酸为弱酸,在水中部分电离。
根据次氯酸的电离常数式Ka=[H+][OCl--]/[HOCl],可得pH值与OCl、HOCl两者相对含量的关系式:
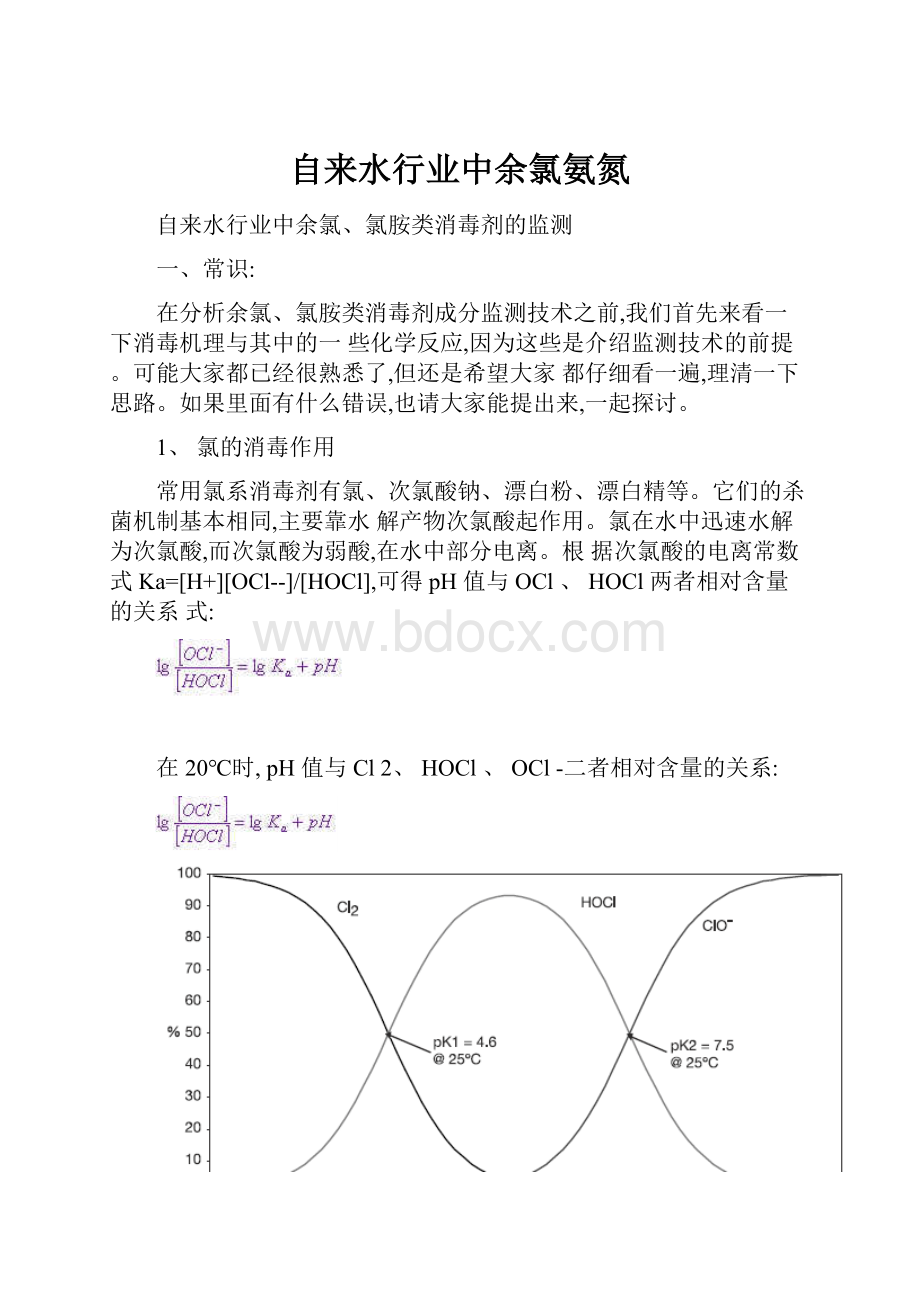
在20℃时,pH值与Cl2、HOCl、OCl-二者相对含量的关系:
实践表明:
pH值约低,氯的杀菌作用愈强。
由此可推断,氯的消毒作用主要依靠HOCl,而OCl-的作用较弱。
究其原因,可能是因为HOCl呈电中性,易接近带负电的菌体,并透过细胞壁而进入菌体,通过氧化作用破坏细菌的酶系统而使细菌死亡;而OCl-带有负电荷,不易接近带负电荷的菌体,难于发挥其杀菌作用。
当水中含有氨态氮时(这是很常见的,投氯后生成各种氯胺:
Cl2+H2OHOCl+HCl;
NH+HOCl
3NHCl+HO
22NHCl+HOCl
2NHCl+H22O
NHCl2+
HOClNCl+H32O
氯胺亦有消毒作用,称为化合氯;而把HOCl、OCl-称为游离氯。
在平衡状态时水中各种
氯胺的比例决定于pH值、(氯/氨值和温度。
一般说来,当pH>9时,一氯胺占优势;当pH=7.0时,一氯胺与二氯胺近似等量;当pH<6.5时,主要为二氯胺;只有当pH<4.4时才产生三氯胺。
实验表明,氯胺在酸性条件下有较强的杀菌作用。
由此可知,二氯胺的消毒作用比一氯胺强。
至于三氯胺,其消毒作用极差,又具有恶臭味,在通常的水处理条件下不大可能生成,因而对消毒处理意义不大。
氯胺在水中的消毒作用,实质上是依靠其水解产物HOCl。
只有当水中的HOCl因消毒而消耗后,氯胺才不断水解释放出HOCl继续起消毒作用。
因此,氯胺的消毒作用比较缓慢,需要较长的接触时间和较大的投药量。
但是氯胺消毒有其独特的优点:
(1氯胺较稳定,在水中的存留期长,逐渐释放出HOCl,消毒作用持久;(2能减少三卤甲烷和氯酚的产生,可使氯酚臭味减轻;(3防止管网中铁细菌的繁殖。
2、投氯量及投氯点
氯化消毒时,为获得可靠而持久的消毒效果,投氯量应满足部分的要求:
(1杀灭细菌以达到指定的消毒指标及氧化有机物等所消耗的"需氯量";(2抑制水中残存致病菌的再度繁殖所需的"余氯量"。
余氯量的规定还提供了确定投氯量和判定消毒效果的简易方法。
下面分别讨论不同情况下投氯量与余氯量之间的关系。
(1水中不含氨氮和含氨有机物,只有其他需氧物质(如
细菌、有机物、还原性无机物等时,投氯量等于需氯
量b与余氯量c之和。
投氯量与余氯量之关系如右图中
OMP曲线所示。
45o倾斜线(虚线表示需氯量为零的假
想情况。
(2若水中需氯杂质主要为氨氮及含氨有机物时,
投氯量与余氯量的关系如右中OMABP曲线所示。
曲
线与虚线间的垂直距离表示需氯量;曲线与横坐标
间的垂直距离表示余氯量。
OM段表示水中其它杂质
消耗氯,余氯量为零,此时消毒效果不可靠;MA
段,表示氯与氨生成氯胺(主要是一氯胺,有化合
余氯存在,所以有一定消毒效果,余氯量极少,一
氯胺基本可代表总氯,A点的Cl:
N=5:
1;AB段表
示,部分氯胺被投入的氯氧化分解为不起消毒作用
的N、NO、NO等。
化合余氯减少,最后到折点B,
22化合余氯量降至最小值,此时余氯仍然很少。
B点的
Cl:
N=9:
1;BP线表示,此时已经没有消耗氯的杂
质了,所投之氯全部用于增加游离余氯量,消毒效
果最好。
消毒处理时投氯量的控制视原水水质和消毒要求不同而异。
对给水处理来说,若氨氮含量较低(小于0.3mg/L,通常投氯量超过折点B,维持一定游离余氯量,此即"折点氯化法"。
若胺氮含量较高(大于0.5mg/L,投氯量控制在峰点A以前即可,这时的化合余氯量以足够消毒。
不同废水的水质和消毒要求差别很大,应通过实验确定投氯量。
一般城市污水沉淀后出水的投氯量约为6~24mg/L,二级生化处理出水约为3~9mg/L,二级生化加过滤处理之出水,约为1~5mg/L。
氯与废水应充分混合,接触时间约为1h(氯胺消毒为2h。
废水经加氯消毒后,1h后的余氯量应不小于0.5mg/L;但余氯的多少,还应考虑接纳水体的安全;例如水体含氯量达0.1mg/L时,有使河流中鱼类死亡的危险。
二、建立模型,分析实际水体中含有的成分
我们以一个实际加氯点前水样:
水体中有微生物,有一定的氨氮,来分析一下出厂水中应该有哪些成分。
由常识部分我们已经知道,当这样的水体进行氯消毒时,随着氯的加入量:
1氯与水反应生成次氯酸,次氯酸不停的被微生物消耗,直至微生物全部被杀死之前,水体
中不会有HOCl。
这个时候,主要的化学反应是:
Cl+H22OHOCl+HCl
此时,水体中的成分有:
Cl-NH3
如果一家自来水厂工艺没有控制好,导致加氯量不足,就会导致以上的情况。
这个时候,该自来水厂在出厂水中监测不到余氯,但能监测到氨氮。
2随着氯加入量不断增加,微生物全部被杀死,此时过量的氯与水反应生成次氯酸,次氯酸
与氨反应生成一氯胺、二氯胺甚至三氯胺,其中的成分根据pH值、温度的不同而不同。
这个时候,主要的化学反应是:
Cl2+H2
OHOCl+HCl;
NH+HOCl3NHCl+H
O22NHCl+HOCl2NHCl+H22O此时,水体中的成分有Cl-HOClOCl-NHNH32Cl(NHCl2微量
如果按照常识中所提到的,有些自来水厂加氯量可能就是控制在这一段,那么该自来水厂的出厂水中,实际能监测到的成分有极少量余氯(HOClOCl
-,氨氮,一氯胺。
在这一段中,一氯胺总氯里面的大部分,余氯含量不高。
3随着氯加入量不断增加,过量的氯将部分氯胺氧化分解为不起消毒作用的N、
NO、N22O
等,化合余氯减少。
这个时候,主要的化学反应是:
Cl2+H2OHOCl+HCl;
NH+HOCl3NHCl+HO22NHCl+HOCl2NHCl+H22O
此时,水体中的成分有Cl-HOClOCl-NHCl(NHCl微量
22如果按照常识中所提到的,有些自来水厂加氯量由于失误控制在了这一段,那么该自来
水厂的出厂水中,实际能监测到的成分有极少量余氯(HOClOCl-,一氯胺。
在这一段中,一氯胺占总氯里面的大部分,余氯含量不高。
于前一阶段相比,没有了氨氮是其显著特点。
4随着加氯量的继续增加,此时过量的氯已经将各种氯胺全部氧化(也有可能由于接触时间、
环境等原因没有完全将其反应完,但理想状态下,应该是反应完全的,水体中主要化学反应为:
Cl
2+H2OHOCl+HCl;
此时,水体中的成分有:
Cl-
HOClOCl-以极少量的Cl2
一般来水,自来水厂的消毒过程都是控制在这一步,也就是说,出厂水中只有游离余氯存在,极少有符合余氯,氨氮值也很难监测得到。
各物质成分的含量,随着氯加入变化的曲线可用下图形象的表达:
红色:
总氯
黑色:
一氯胺
黄色:
氨氮
绿色:
余氯
三、HACH实验室及在线仪器中监测余氯、总氯、氨氮、氯胺等方法分析
1、实验室仪器
1余氯
DPD法:
经典的余氯分析方法,应用的原理是DPD(N,N-diethyl-p-phenylenediamine与余氯反应,生成紫红色化合物。
反应方程式如下:
2总氯
DPD法:
经典的余氯分析方法,应用的原理是碘化钾KI先与复合余氯反应生成碘,DPD(N,N-diethyl-p-phenylenediamine与余氯和碘I反应,生成紫红色化合物。
反应方程式如下:
2
滴定法:
也是经典方法,应用的原理是总氯与碘化钾在一定条件下反应生成碘,使用滴定液(一般是硫代硫酸钠,用电位滴定的方法确定滴定终点,从而计算出总氯量。
反应方程式如下:
3氨氮:
纳氏试剂法:
经典方法,测量原理:
碘化汞和碘化钾的碱性溶液,与氨反应生成淡红棕色胶态化合物,该颜色在较宽的波长内具强烈吸收。
在425nm波长下比色。
反应方程式:
水杨酸法:
原理:
在五氰络铁(III酸钠[sodiumnitrosopentacyanofrer-rate(III或称硝普纳sodiumnitroprusside]存在下铵与水杨酸盐和次氯酸离子反应生成蓝色化合物在约697nm
用分光光度计加以测定在pH11.7有硝普钠存在下氯胺与水杨酸钠发生反应所有样品中的氯胺都定量地被测定。
化学方程式如下:
靛酚法:
原理:
一氯氨与酚溶液反应,生成深蓝色之靛酚。
在水样中加入次氯酸盐(Hypochlorite)及可以将所有游离氨转化为一氯胺,氯氨再与酚溶液反应,两者的差值即为游离氨浓度。
4)一氯氨:
靛酚法:
原理:
氯氨与酚溶液反应,生成深蓝色之靛酚。
2、在线仪器:
1)余氯:
CL17:
DPD法。
同实验室方法。
9184sc:
膜电极法,根据下图,膜电极测得水体pH,温度及HOCl值,反推OCl-及Cl2
2)总氯:
Cl17:
DPD,同实验室。
3)氨氮:
8810,Amtaxsc:
氨气敏电极法,原理:
调解样品碱性逐出氨(NH3),然后通过测定膜电极+,但测定时间的控制也会影响到平衡pH值变化测定氨氮。
它测量的是游离氨氮(NH4,NH3)反应中氯胺向游离氨方向移动,因此时间很重要。
AmtaxCompact:
酸碱指示剂法,原理:
调解样品碱性逐出氨到测量池,通过酸碱指示剂的颜色变化来指示氨氮浓度。
它测定的是游离氨氮(NH4+,NH3)Amtaxinter2:
水杨酸法(同实验室部分)。
根据其原理可知,inter2测定的是总氨氮(游离氨复合胺的总和)APA6000:
靛酚法(也叫酚盐法):
原理同实验室部分。
根据其原理可知,APA6000可测得游+,精确测量。
离氨(NH4,NH3)4)氯氨:
APA6000:
靛酚法(也叫酚盐法):
原理同实验室部分。
根据其原理可知,APA6000可测得一氯胺,精确测量。
四、问题分析:
到现在为止,我们都已经碰到了很多用户的困扰,尤其是氨氮仪器。
根据上面的内容,对我遇到的问题,我可以做出一些合理的解释。
1、在去年7月份,我曾经与任军到乍浦自来水厂,做了一次实验是产品与inter2对比。
用户的问题是在出水口位置适中检测不到氨氮值,而在原水中是有中等含量的氨氮的。
由于inter2使用水杨酸法,因此由于氨氮与余氯反应生成氯胺导致检测不出来的解释是不合理的。
可能的原因是加氯量在B点后,大量的氨氮已经被氯氧化,因此氨氮浓度非常低,甚至低于检测线。
这可以通过与业主讨论一下他们的工艺,并且在出水口检测一下余氯值已得到确认。
2、杨工的问题:
8810为什么数据不稳定。
这个问题很复杂,但大致有三方面原因。
A.出厂水的氨氮值确实比较低的,在接近检测线的情况下,数据不稳定是正常的。
B.,如果是采用了氯氨消毒,那么氨气敏电极法本身缺陷。
由于采用逐出法,这样在逐出过程中实际上打破了很多化学平衡。
虽然说8810只能监测游离氨,但其取样逐出氨的方式使得NH3+HOClNH2Cl+H2ONH2Cl+HOClNHCl2+H2ONHCl2+HOClNCl3+H2O这几个化学反应相反方向进行(虽然速度比较缓慢),不可避免导致数据始终是漂移的,而且以向上偏移为主。
C.气敏电极法内主要是一根pH电极,pH电极本身基线漂移就比较厉害,需要时常校准,认为把基线拉下来。
3、杨工问题:
8810和INTER2氨氮仪监测的是总氨?
还是自由氨?
8810测自由氨,inter2测总氨。
4、谭经理的关于上海杨树谱水厂出水口检测不出氨氮,往下游搬迁一段就正常的问题。
由于氨氮是自然界中天然滋长的物质,只需要有腐败植物、死亡的微生物或其他氮源,都有可能在细菌的作用下产生氨氮。
因此搬迁到下游能测得氨氮值并不能说明太多问题。
可
以考虑一下在那个点同时测量一下余氯值,是否在正常值?
极有可能这个时候余氯已经被消耗光了。
5、程总提到的两个例子。
其实我们的仪器在原水监测都是没有问题的,出问题的是在加氯点后。
因此用户拿实验室产品去和在线仪器比较,即使原理不同,也能得到有相关性的数据。
当然,以上有些解释是纯粹的理论上的,比如第四个问题,我只是根据问题预计上海杨树谱水厂以氯消毒为主,加氯量控制在B点以后,如果不是的话,那解释就完全不对了。
以上不对的地方还请大家指正,一起探讨。
如有其他问题,也可以根据上面的模型分析一下,应该能得到比较合理的解释的。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 自来水 行业 余氯
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
