 化学寒假作业8《化学》必修一附答案 1.docx
化学寒假作业8《化学》必修一附答案 1.docx
- 文档编号:28384142
- 上传时间:2023-07-10
- 格式:DOCX
- 页数:15
- 大小:128.13KB
化学寒假作业8《化学》必修一附答案 1.docx
《化学寒假作业8《化学》必修一附答案 1.docx》由会员分享,可在线阅读,更多相关《化学寒假作业8《化学》必修一附答案 1.docx(15页珍藏版)》请在冰豆网上搜索。
化学寒假作业8《化学》必修一附答案1
人教版2016年高一化学寒假作业8《化学》必修一
一、选择题(本题共7道小题)
1.
Cu与足量的浓硝酸反应产生气体,用排水法收集aL此气体(标况),从理论上讲,被还原的硝酸的物质的量是下列中的( )
A.
molB.
molC.
molD.
mol
2.
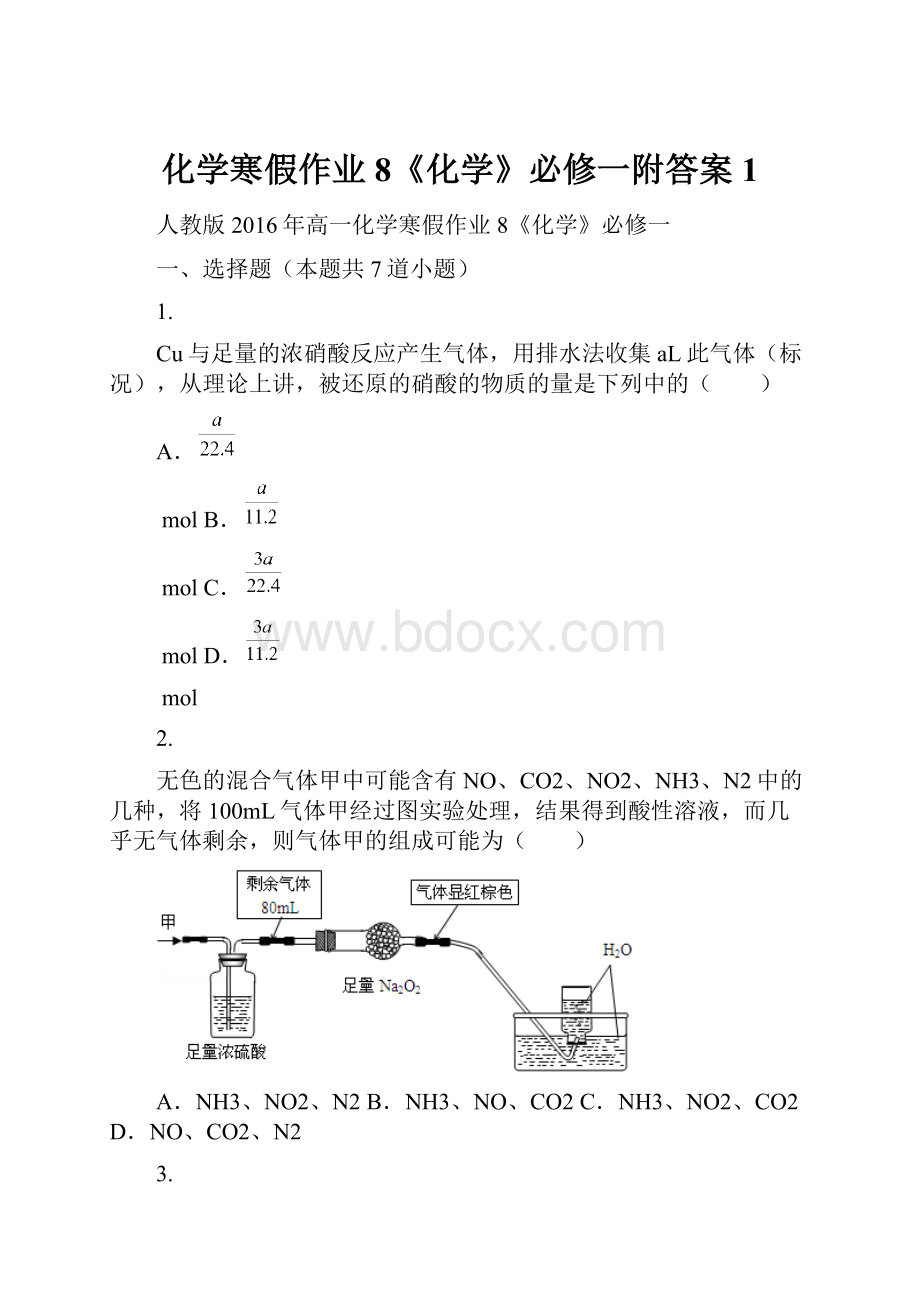
无色的混合气体甲中可能含有NO、CO2、NO2、NH3、N2中的几种,将100mL气体甲经过图实验处理,结果得到酸性溶液,而几乎无气体剩余,则气体甲的组成可能为( )
A.NH3、NO2、N2B.NH3、NO、CO2C.NH3、NO2、CO2D.NO、CO2、N2
3.
能把Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶无色溶液加以区别的一种试剂是(必要时可加热)( )
A.BaCl2B.NaOHC.Ba(OH)2D.AgNO3
4.
利用图所示装置进行以下实验,能得到相应实验结论的是( )
选项
①
②
③
实验结论
A
稀硫酸
石灰石
澄清石灰水
制二氧化碳并吸收尾气
B
浓硫酸
蔗糖
溴水
浓硫酸具有脱水性、氧化性
C
稀盐酸
Na2SO3
H2S溶液
SO2具有还原性
D
浓硝酸
Na2CO3
Na2SiO3溶液
酸性:
硝酸>碳酸>硅酸
5.
足量的铝与20mL1.0mol/L的下列物质反应,产生气体物质的量最少的是
A.氢氧化钠溶液B.稀硫酸C.盐酸D.稀硝酸
6.锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水.当生成amol硝酸锌时,被还原的硝酸的物质的量为()
A.
amolB.
amol
C.amolD.2amol
7.
用下列实验装置进行相应实验,能达到实验目的是(夹持装置未画出)( )
A.
用装置甲检验溶液中是否有K+
B.
用装置乙制取并收集少量NH3
C.
用装置丙进行喷泉实验
D.
用装置丁加热熔融NaOH固体
二、填空题(本题共3道小题)
8.
(16分)氮及其化合物在化学实验中有广泛应用:
(1)请写出实验室用Cu和稀硝酸反应制备NO的离子方程式:
;
(2)请设计实验,检验某可溶性固体物质中含有NH4+的操作、现象、结论:
;
(3)实验室可用(NH4)2Cr2O7受热分解产生N2、Cr2O3和H2O来制备N2,请写出该分解反应的化学方程式:
;
(4)有人发现重铬酸铵分解产物不仅含N2、Cr2O3和H2O,还含有NH3和O2,并指出伴随有显著的副反应发生:
2(NH4)2Cr2O7
2Cr2O3+4NH3↑+2H2O+3O2↑;设计如图所示实验装置,并通过实验方法验证了NH3和O2的存在(忽略空气中O2的干扰).
限选试剂:
Na2S溶液、Na2SO3溶液、FeSO4溶液;
限选仪器:
试管、玻璃导管、漏斗、烧杯、胶头滴管
①图中试管口玻璃纤维的作用是;
②根据实验目的,选择一种试剂和最佳的仪器补全该实验装置(在方框中画图并标注所选试剂);
③写出该法验证NH3和O2存在的实验原理的化学方程式:
.
9.
使用如图所示装置进行化学小实验,请填写下列空白:
(1)若①中放一片湿润的红色石蕊试纸,②装有浓氨水,可观察到的实验现象为
(2)若①装有AlCl3溶液,②装有浓氨水,可观察到的实验现象为
(3)若①装有浓硝酸,②装有浓氨水,可观察到的实验现象为
(4)若①装有浓硝酸,②装有Na2SO3溶液,实验时有无色气体产生,该气体逐渐变为红棕色,用化学方程式表示无色气体变为红棕色的原因 .
10.
(12分)氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。
完成下列填空:
实验室设计了如图所示的实验装置,进行“氨的催化氧化”等实验。
图1
(1)A处是气体发生装置,A中所用试剂只能从下列物质中选取:
①硝酸铵 ②碳酸氢铵 ③氯化铵 ④熟石灰 ⑤氢氧化钠
若A中制取气体时只用了一种试剂,该试剂可以是____________(选填上述编号),此时A处的装置应为______________(选填下列编号)。
图2
至此,完成了对图1中装置的补充。
某同学从安全与环保的角度考虑,该装置存在两处明显的缺陷,你认为这两处缺陷是_________________、_____________________。
(2)写出图1装置B中发生反应的化学方程式(写一个即可);
在图1中,若A、B处试剂足量,则装置E中发生反应的离子方程式为:
_________________________________________________。
(3)写出图1装置C中发生反应的化学方程式
试卷答案
1.
考点:
氧化还原反应的计算.
专题:
守恒法;氧化还原反应专题.
分析:
Cu和浓硝酸反应生成NO2,NO2和水反应方程式为3NO2+H2O=2HNO3+NO,通过排水法收集到的气体是NO,根据方程式知,NO体积是二氧化氮体积的
,如果用排水法收集aLNO,则二氧化氮体积为3aL,n(NO2)=
=
mol,根据N原子守恒计算被还原硝酸物质的量.
解答:
解:
Cu和浓硝酸反应生成NO2,NO2和水反应方程式为3NO2+H2O=2HNO3+NO,通过排水法收集到的气体是NO,根据方程式知,NO体积是二氧化氮体积的
,如果用排水法收集aLNO,则二氧化氮体积为3aL,n(NO2)=
=
mol,根据N原子守恒得被还原n(HNO3)=n(NO2)=
mol,
故选C.
点评:
本题考查氧化还原反应方程式的有关计算,为高频考点,明确排水法收集到的气体成分是解本题关键,注意原子守恒的灵活运用,题目难度不大.
2.B
考点:
常见气体的检验;氨的化学性质;氮的氧化物的性质及其对环境的影响.
专题:
物质检验鉴别题.
分析:
二氧化氮是红棕色的气体,浓硫酸可以和氨气反应,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,氮气不溶于水.
解答:
解:
二氧化氮是红棕色的气体,所以一定不存在,甲气体经过足量的浓硫酸,溢出剩余气体80毫升,说明一定有NH3存在,二氧化碳可以和过氧化钠反应生成碳酸钠和氧气,一氧化氮无色,与氧气立即反应变为红棕色的二氧化氮,通过足量的过氧化钠后气体显红棕色,说明有NO、CO2,排水法收集气体,广口瓶被上升的水注满,说明没有N2.
故选B.
点评:
本题考查学生常见气体的检验和性质,是一道气体的鉴别题目,难度不大
3.C
考点:
物质的检验和鉴别的实验方案设计.
专题:
元素及其化合物.
分析:
Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶无色溶液分别与Ba(OH)2反应,现象分别为:
白色沉淀、刺激性气味的气体、无现象、既有沉淀又有刺激性气味的气体,现象各不相同,以此来解答.
解答:
解:
A.BaCl2与Na2SO4、(NH4)2SO4两瓶无色溶液反应,均生成白色沉淀,现象相同,无法区别,故A错误;
B.NaOH与NH4NO3、(NH4)2SO4两瓶无色溶液反应,均生成刺激性气味的气体,现象相同,无法区别,故B错误;
C.Na2SO4、NH4NO3、KCl、(NH4)2SO4四瓶无色溶液分别与Ba(OH)2反应,现象分别为:
白色沉淀、刺激性气味的气体、无现象、既有沉淀又有刺激性气味的气体,现象各不相同,能够区别,故C正确;
D.AgNO3与Na2SO4、KCl、(NH4)2SO4三瓶无色溶液反应,均生成白色沉淀,现象相同,不能区别,故D错误;
故选C.
点评:
本题考查物质的鉴别区分,明确物质的性质及发生的反应中的现象是解答本题的关键,注意把握物质的性质,利用不同现象来区分,题目难度不大
4.B
考点:
化学实验方案的评价.
专题:
实验评价题.
分析:
A.稀硫酸与石灰石反应生成微溶的硫酸钙,反应不能顺利进行;
B.浓硫酸可使蔗糖碳化,并发生氧化还原反应生成二氧化硫气体;
C.生成二氧化硫与硫化氢发生氧化还原反应;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与硅酸钠溶液反应生成.
解答:
解:
A.稀硫酸与石灰石反应生成微溶的硫酸钙,附在固体而使反应不能顺利进行,应用稀硫酸和碳酸钠反应制备二氧化碳气体,故A错误;
B.浓硫酸可使蔗糖碳化,并发生氧化还原反应生成二氧化硫气体,通过高锰酸钾溶液的颜色变化证明浓硫酸的强氧化性,故B正确;
C.生成二氧化硫与硫化氢发生氧化还原反应,生成硫,二氧化硫表现氧化性,故C错误;
D.浓硝酸与碳酸钠反应生成二氧化碳,但浓硝酸易挥发,硝酸、碳酸均可与硅酸钠溶液反应生成,应先除杂,否则不能证明碳酸>硅酸,故D错误.
故选B.
点评:
本题考查化学实验方案的评价,为高频考点,涉及气体的制备、浓硫酸的性质、酸性比较、氧化还原反应等,把握化学反应原理及实验装置中的反应为解答的关键,注意实验操作的可行性、评价性分析,题目难度不大.
5.D
【解析】铝与氢氧化钠溶液或盐酸或稀硫酸均是产生氢气,且都是铝作还原剂,所以产生的氢气相等。
铝与稀硝酸反应生成硝酸铝、NO和水,氮元素的化合价从+5价降低到+2价,所以产生的NO最少,答案选D。
6.A
解:
根据题意知,锌和稀硝酸反应方程式为4Zn+10HNO3=4Zn(NO3)2+NH4NO3+3H2O,生成amol硝酸锌时转移电子的物质的量=amol×(2﹣0)=2amol,根据氧化还原反应中得失电子守恒得,被还原的硝酸的物质的量=
=0.25amol,
故选A.
7.B
考点:
化学实验方案的评价.
分析:
A.观察K的焰色反应应透过蓝色的钴玻璃;
B.浓氨水与生石灰混合可生成氨气,氨气的密度比空气的密度小;
C.氯气不易溶于食盐水;
D.瓷坩埚中的二氧化硅与NaOH反应.
解答:
解:
A.观察K的焰色反应应透过蓝色的钴玻璃,由图可知,缺少蓝色的钴玻璃,故A错误;
B.浓氨水与生石灰混合可生成氨气,氨气的密度比空气的密度小,则图中固液反应不加热装置及向下排空气法均合理,故B正确;
C.氯气不易溶于食盐水,则图中装置不能形成喷泉实验,故C错误;
D.瓷坩埚中的二氧化硅与NaOH反应,仪器选择不合理,应使用铁坩埚,故D错误;
故选B.
点评:
本题考查化学实验方案的评价,为高频考点,涉及焰色反应、气体的制备及收集、物质的性质等,把握物质的性质及反应原理为解答的关键,侧重分析与实验能力的考查,注意装置的作用及实验的评价性分析,题目难度不大
8.
(1)3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O;
(2)取少量待测固体(或先配制成浓溶液亦可)于试管中,加入过量浓的NaOH溶液,加热,在试管口放置湿润的红色石蕊试纸,产生无色有刺激性气味的气体,且试纸变蓝,则原溶液含有NH4+;
(3)(NH4)2Cr2O7
Cr2O3+N2↑+4H2O;
(4)①缓冲气流,防止固体被气流带进入导管,堵塞导管;
②
;
③2NH3+2H2O+FeSO4=Fe(OH)2↓+(NH4)2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3)(或8NH3+10H2O+4FeSO4+O2=4Fe(OH)3↓+4(NH4)2SO4).
考点:
性质实验方案的设计;铵离子检验;硝酸的化学性质.
分析:
(1)铜与稀硝酸反应氧化还原反应生成硝酸铜、NO气体和水;
(2)检验铵根离子的方法一般为:
向铵盐中进入氢氧化钠、加热,用湿润的红色石蕊试纸检验是否有变蓝,从而判断是否含有铵根离子;
(3)反应中Cr元素和N元素的化合价发生变化,根据化合价升降相等配平并写出该反应的化学方程式;
(4)①反应中固体容易堵塞导管,且生成气体的气流不稳定,据此判断使用玻璃纤维的目的;
②氨气极易溶于水,需要使用防倒吸装置吸收氨气,检验氨气和氧气,需要选用硫酸亚铁溶液,据此设计方案并画出装置图;
③氨气与硫酸亚铁反应生成白色的氢氧化亚铁沉淀,据此证明存在氨气;氢氧化亚铁与氧气反应生成红褐色的氢氧化铁沉淀,据此判断反应中生成了氧气.
解答:
解:
(1)铜与稀硝酸反应生成硝酸铜、一氧化氮气体和水,反应的离子方程式为3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O,
故答案为:
3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O;
(2)通常用强碱溶液和湿润的红色石蕊试纸检验铵根离子,其操作方法、现象及结论为:
取少量待测固体(或先配制成浓溶液亦可)于试管中,加入过量浓的NaOH溶液,加热,在试管口放置湿润的红色石蕊试纸,产生无色有刺激性气味的气体,且试纸变蓝,则原溶液含有NH4+,
故答案为:
取少量待测固体(或先配制成浓溶液亦可)于试管中,加入过量浓的NaOH溶液,加热,在试管口放置湿润的红色石蕊试纸,产生无色有刺激性气味的气体,且试纸变蓝,则原溶液含有NH4+;
(3)实验室可用(NH4)2Cr2O7受热分解产生N2、Cr2O3和H2O来制备N2,(NH4)2Cr2O7中铬元素的化合价为+6,氮元素的化合价为﹣3,反应后分别生成Cr2O3、N2,铬元素化合价变化至少为:
(6﹣3)×2=6,N元素化合价至少升高:
[0﹣(﹣3)]×2=6,则化合价变化的最小公倍数为6,所以Cr2O3、N2的系数都是1,然后利用质量守恒配平可得(NH4)2Cr2O7
Cr2O3+N2↑+4H2O,
故答案为:
(NH4)2Cr2O7
Cr2O3+N2↑+4H2O;
(4)①反应中固体容易堵塞导管,且生成气体的气流不稳定,所以使用玻璃纤维缓冲气流,防止固体被气流带进入堵塞导管,
故答案为:
缓冲气流,防止固体被气流带进入导管,堵塞导管;
②检验氨气和氧气,发生的反应必须具有明显现象,如颜色变化、沉淀等,氨气能够与硫酸亚铁溶液反应生成氢氧化亚铁沉淀:
2NH3+2H2O+FeSO4=Fe(OH)2↓+(NH4)2SO4,氢氧化亚铁在溶液中遇到氧气能够被氧化成红褐色的氢氧化铁:
4Fe(OH)2+O2+2H2O=4Fe(OH)3),所以用硫酸亚铁检验;氨气极易溶于水,需要用倒置的漏斗吸收氨气,据此画出的检验氨气和氧气的装置图为
故答案为:
;
③根据②的分析可知,检验氨气的反应原理为:
2NH3+2H2O+FeSO4=Fe(OH)2↓+(NH4)2SO4;检验氧气的反应方程式为4Fe(OH)2+O2+2H2O=4Fe(OH)3),
故答案为:
2NH3+2H2O+FeSO4=Fe(OH)2↓+(NH4)2SO4、4Fe(OH)2+O2+2H2O=4Fe(OH)3)(或8NH3+10H2O+4FeSO4+O2=4Fe(OH)3↓+4(NH4)2SO4).
点评:
本题考查了性质实验方案的设计与评价,题目难度中等,明确常见物质的性质及检验方案的设计原则为解答关键,注意掌握化学实验基本操作方法及其应用,试题充分考查了学生的分析、理解能力及灵活应用基础知识的能力.
9.
1.石蕊试纸变蓝2. ①中有白色沉淀3.烧杯中有白烟生成
4.2NO+O2=2NO2
考点:
氨的化学性质;硝酸的化学性质;镁、铝的重要化合物.
专题:
元素及其化合物.
分析:
(1)依据浓氨水具有挥发性,氨气为碱性气体解答;
浓氨水以挥发,氨气与水反应生成一水合氨,与氯化铝反应生成氢氧化铝沉淀;
(3)浓硝酸、浓氨水易挥发,硝酸与氨气反应生成硝酸铵;
(4)无色一氧化氮不稳定,与氧气反应生成红棕色的二氧化氮.
解答:
解:
(1)浓氨水具有挥发性,挥发出的氨气为碱性气体,能够与水反应生成一水合氨,一水合氨电离生成氢氧根离子,能够使石蕊试纸变蓝,
故答案为:
石蕊试纸变蓝;
浓氨水以挥发,氨气与水反应生成一水合氨,与氯化铝反应生成氢氧化铝沉淀;
故答案为:
①中有白色沉淀生成;
(3)浓硝酸、浓氨水易挥发,硝酸与氨气反应生成硝酸铵,所以会看到产生大量白烟;
故答案为:
烧杯中有白烟生成;
(4)一氧化氮不稳定,与氧气反应生成红棕色的二氧化氮,化学方程式:
2NO+O2=2NO2,故答案为:
2NO+O2=2NO2.
点评:
本题通过实验现象的描述考查了物质的性质,熟悉浓氨水、硝酸的性质是解题关键,题目难度不大
10.
(1)②;d;D中液体可能会倒吸;缺少尾气处理装置,会污染环境
(2)2Na2O2+2H2O=4NaOH+O2或2Na2O2+2CO2=2Na2CO3+O2
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
(3)4NH3+5O2=4NO+6H2O
【解析】
(1)铵盐受热分解产生氨气,过氧化钠在此装置中可以吸收二氧化碳和水,所以制取氨气的药品可以用NH4HCO3或(NH4)2CO3,药品均为固体,选择的装置符合加热固体制气体,再结合选项,药品应为NH4HCO3,对应②;
氨气极易溶于水,实验会倒吸;氨气有毒,需要尾气处理,故答案为:
②;d;D中液体可能会倒吸;缺少尾气处理装置,会污染环境
(2)NH4HCO3分解产生氨气、二氧化碳和水,装置B中的过氧化钠在此装置中可以吸收二氧化碳和水,化学方程式为2Na2O2+2H2O=4NaOH+O2和2Na2O2+2CO2=2Na2CO3+O2;
氨气的催化氧化反应得到的一氧化氮迅速被氧气氧化为二氧化氮,二氧化氮溶于水形成硝酸,金属铜和稀硝酸反应生成硝酸铜和一氧化氮,则装置E中发生反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;故答案为:
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(3)C中发生的是NH3的催化氧化反应,故答案为:
4NH3+5O2=4NO+6H2O。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 化学寒假作业8化学必修一附答案 寒假 作业 必修 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
