 几种重要的金属.docx
几种重要的金属.docx
- 文档编号:28048221
- 上传时间:2023-07-07
- 格式:DOCX
- 页数:16
- 大小:113.19KB
几种重要的金属.docx
《几种重要的金属.docx》由会员分享,可在线阅读,更多相关《几种重要的金属.docx(16页珍藏版)》请在冰豆网上搜索。
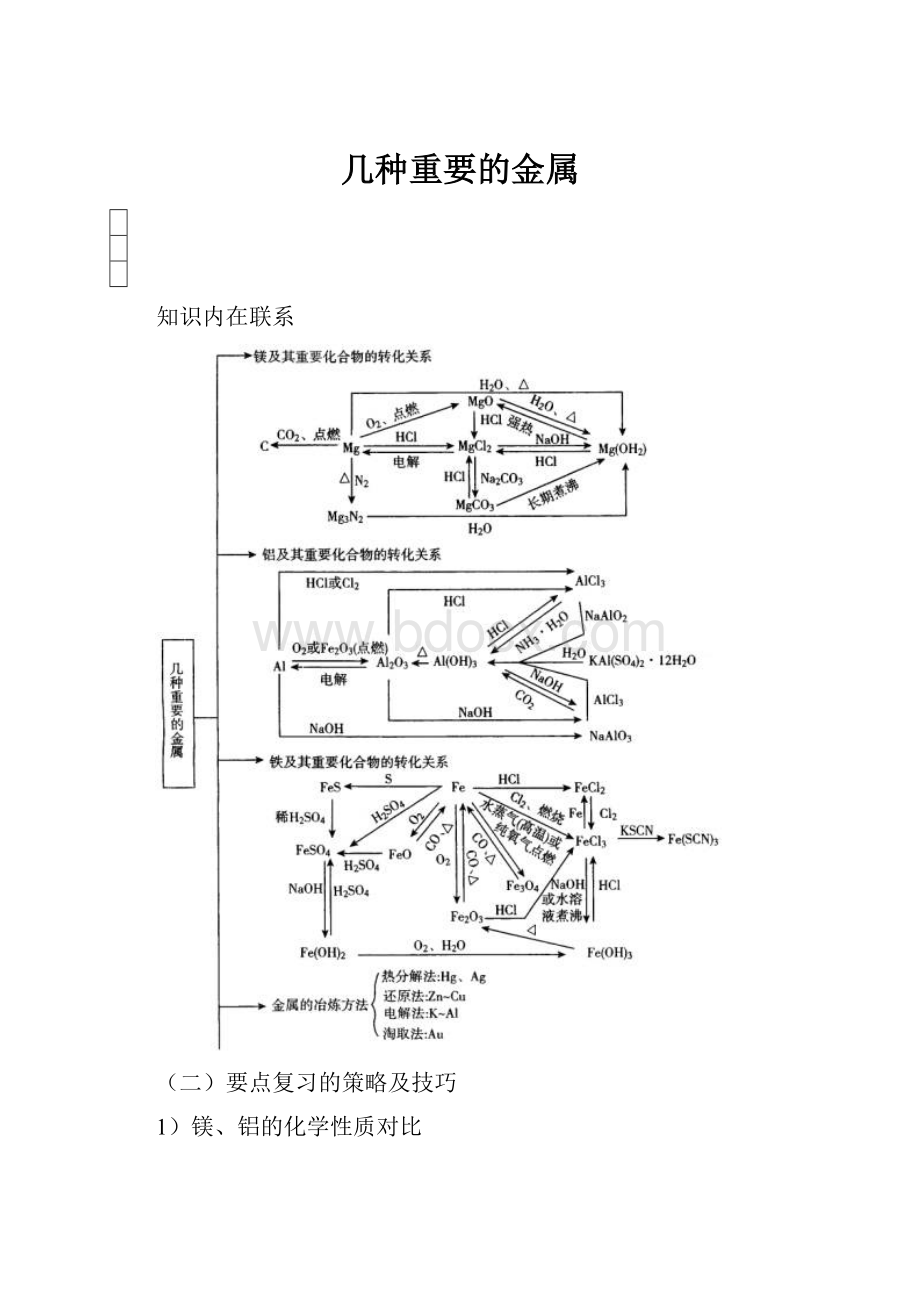
几种重要的金属
知识内在联系
(二)要点复习的策略及技巧
1)镁、铝的化学性质对比
镁的化学性质
铝的化学性质
与O2反应
常温下生成氧化膜,
2Mg+O2
MgO
常温下生成致密的氧化膜
4Al+3O2
Al2O3
与某些非金属反应
Mg+Cl2
MgCl2 Mg+S
MgS
3Mg+N2
Mg3N2
2Al+3Cl2
2AlCl3
2Al+3S
Al2S3
与H2O的反应
Mg+2H2O
Mg(OH)2+H2
2Al+3H2O
Al2O3+3H2
与某些氧化物反应
2Mg+CO2
C+2MgO
8Al+3Fe3O4
Al2O3+9Fe
与非氧化性酸反应
Mg+2H+=Mg2++H2↑
2Al+6H+=2Al3++3H2↑
与碱溶液反应
不反应
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
(2)氧化镁与氧化铝性质的比较
①相同点:
MgO和Al2O3都属于高熔点氧化物,常用作耐火材料。
它们都难溶于水。
②不同点:
MgO可缓慢与水反应生成Mg(OH)2,而Al2O3不与水反应。
MgO是碱性氧化物,只与酸反应,不与碱反应。
Al2O3是典型的两性氧化物,即能与酸反应又能与强碱反应。
Al2O3与酸反应生成铝盐:
Al2O3+6HCl=2AlCl3+3H2O
Al2O3与碱反应生成偏铝酸盐:
Al2O3+2NaOH=2NaAlO2+H2O。
(3)氢氧化铝的两性
Al(OH)3+3H+=Al3++3H2OAl(OH)3+OH-=
+2H2O
由于Al(OH)3是两性氢氧化物,因此实验室常用铝盐和氨水反应来制备:
Al3++3NH3·H2O=Al(OH)3↓+
(5)Al3+、Al(OH)3和
相互转化规律
①铝盐与碱反应
实验操作
往AlCl3溶液中滴加NaOH溶液
往NaOH溶液中滴加AlCl3溶液边滴边振荡
实验现象
先产生沉淀,后沉淀消失
产生沉淀,沉淀随即消失得透明澄清溶液后产生沉淀且不消失
离子
方程式
Al3++3OH-=Al(OH)3↓
Al(OH)3+OH-==AlO2-+2H2O
Al3++3OH-=Al(OH)3↓
Al(OH)3+OH-=AlO2-+2H2O
3AlO2-+Al3++6H2O=4Al(OH)3↓
图象
②偏铝酸根与酸反应
实验
往NaAlO2溶液中滴加HCl溶液
往HCl溶液中滴加NaAlO2溶液边滴边振荡
往NaAlO2溶液中通入CO2
现象
先产生沉淀,后沉淀消失
产生沉淀,随即沉淀消失
最后又生成沉淀且不消失
产生沉淀且不消失
离子
方程式
+H++H2O=Al(OH)3↓
Al(OH)3+3H+=Al3++3H2O
AlO2-+H++H2O=Al(OH)3↓
Al(OH)3+3H+=Al3++3H2O
Al3++
+6H2O
=4Al(OH)3↓
+3H2O+CO2
=2Al(OH)3↓+
+2H2O+CO2
=Al(OH)3↓+
图象
(3)镁盐铝盐的混合溶液与强碱反应
实验
往AlCl3和MgCl2的混合溶液中滴加NaOH溶液,边滴边振荡
现象
先产生沉淀,后沉淀部分溶解
离子
方程式
Mg2++2OH-=Mg(OH)2↓Al3++3OH-=Al(OH)3↓
Al(OH)3+OH-=
+2H2O
图象
(6)镁铝的工业制法
练1、海水的综合利用可以制备金属镁,其流程如下图所示:
(1)若在空气中加热MgCl2·6H2O,生成的是Mg(OH)Cl或MgO,写出有关反应的化学方程式。
______________________________________________
用电解法制取金属镁时,需要无水氯化镁。
在干燥的HCl气流中加热MgCl2·6H2O时,能得到无水MgCl2,其原因是_________________________。
(2)Mg(OH)2沉淀中混有的Ca(OH)2应怎样除去?
写出实验步骤。
______________________________________________________
(3)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明在这三种情况下使用玻璃棒的目的:
溶解时:
____________________________________________________。
过滤时:
_____________________________________________________。
蒸发时:
____________________________________________________。
练2、铝和氢氧化钾都是重要的工业产品。
请回答:
(1)工业冶炼铝的化学方程式是____________________。
(2)铝与氢氧化钾溶液反应的离子方程式是____________________。
(3)工业品氢氧化钾的溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如图所示。
①该电解槽的阳极反应式是____________________。
②通电开始后,阴极附近溶液pH会增大,请简述原因____________________。
③除去杂质后的氢氧化钾溶液从液体出口__________(填写“A”或“B”)导出。
2、铁和铁的化合物
(1)铁在周期表中的位置及原子结构
铁位于第四周期第Ⅷ族,属过渡元素。
铁元素是一种变价元素,通常显示+2价、+3价,+2价铁不稳定,易转化为+3价。
其化合物及其水溶液往往带有颜色。
(2)金属铁的性质及存在
①物理性质:
铁不仅具有金属晶体的物理性质,而且能被磁铁吸引。
②化学性质
a.与非金属反应
(铁与弱氧化剂反应生成低价铁的化合物)
b.与酸反应
a.和非氧化性酸反应放出H2:
Fe+2H+=Fe2++H2↑
b.氧化性酸:
常温下浓H2SO4、浓HNO3使铁、铝钝化,故在室温时铁铝不溶于浓H2SO4和浓HCO3。
③与水反应:
3Fe+4H2O(气)
Fe3O4+4H2
c.铁的存在
铁在自然界中分布较广。
在地壳中含量约占5%,仅次于铝。
分布在地壳中的铁均以化合态存在,游离态的铁只能在陨石中得到。
铁矿石的种类较多,重要的有:
赤铁矿(Fe2O3),磁铁矿(Fe3O4),褐铁矿(2Fe2O3·3H2O)和菱铁矿(FeCO3)。
(3)铁的氧化物和氢氧化物
①铁的氧化物
化学式
FeO
Fe2O3
Fe3O4
俗名
-
铁红
磁性氧化铁
色态
黑色粉末
红棕色固体
黑色晶体
价态
+2
+3
+2价,+3价
水溶性
不溶
不溶
不溶
与酸的反应
FeO+2H+=
Fe2++H2O
Fe2O3+6H+=
2Fe3++3H2O
Fe3O4+8H+=
Fe2++2Fe3++4H2O
与CO的反应
FexOy+yCO
xFe+yCO2
②铁的氢氧化物
氢氧化物
氢氧化亚铁
氢氧化铁
化学式
Fe(OH)2
Fe(OH)3
化学性质
Fe(OH)2+2H+=Fe2++2H2O
4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe(OH)3+3H+=Fe3++3H2O
2Fe(OH)3
Fe2O3+3H2O
制法
可溶性碱与亚铁盐溶液反应
Fe2++2OH-=Fe(OH)2↓
可溶性碱与铁盐溶液反应
Fe3++3OH-=Fe(OH)3↓
(4)Fe2+和Fe3+的性质
a.Fe3+的鉴别:
鉴别Fe3+的试剂:
KSCN溶液
鉴别离子方程式:
Fe3++3SCN-=Fe(SCN)3(红色)
b.Fe2+和Fe3+性质对比
Fe2+
Fe3+
溶液颜色
淡绿色
棕黄色
加碱溶液
白色沉淀迅速变成灰绿色最后变成红褐色
红褐色沉淀
加KSCN溶液
无明显现象
溶液变红色
c.Fe2+既有氧化性又有还原性,以还原性为主
4Fe2++O2+4H+=4Fe3++2H2O(Fe2+被氧化)
2Fe2++H2O2+2H+=2Fe3++2H2O
d.Fe3+具有较强的氧化性,与S2-、I-、
等能发生氧化还原反应
2Fe3++S2-=2Fe2++S↓
2Fe3++2I-=2Fe2++I2
e.Fe3+是典型的弱碱阳离子,与
等在溶液中发生双水解反应
2Fe3++
+3H2O=2Fe(OH)3↓+3CO2↑
f.Fe3+遇苯酚溶液呈紫色,可用于检验Fe3+:
Fe3++6C6H5OH→[Fe(C6H5O)6]3-+6H+
(紫色)
g.亚铁盐、铁盐的实验室保存方法:
亚铁盐溶液——隔绝空气加入少量铁屑以防止Fe2+被氧化,滴入少量相应的酸溶液以防止Fe2+水解。
铁盐溶液——加入少量相应的酸溶液以防止Fe3+水解。
0 +2 +3
(5)铁三角(Fe、Fe、Fe)的转化关系
①Fe只有还原性,可以被氧化成Fe2+和Fe3+,Fe3+只有氧化性,可被还原成Fe2+,Fe2+既有氧化性又有还原性,遇到较强氧化剂时可被氧化成Fe3+,遇较强还原剂时被还原为单质Fe。
练3、对FeSO4溶液进行如下实验,指出实验现象,写出有关反应的离子方程式或化学方程式。
⑴滴入氯水
2Fe2++Cl2=2Fe3++2Cl-;溶液变黄色
⑵长久露置在空气中
4Fe2++4H++O2=4Fe3++2H2O;变黄
⑶滴入稀HNO3
3Fe2++4H++
=3Fe3++NO↑+2H2O;溶液变黄
⑷滴入3%H2O2溶液
2Fe2++H2O2+2H+=2Fe3++2H2O;变黄
⑸滴入酸性KMnO4溶液
5Fe2++8H++
=5Fe3++Mn2++4H2O;紫色消失
练4、对FeCl3溶液进行如下实验,指出实验现象,写出有关反应的离子方程式。
⑴加Cu粉振荡
2Fe3++Cu=2Fe2++Cu2+;溶液颜色变浅
⑵加还原Fe粉振荡
2Fe3++Fe=3Fe2+;溶液颜色变浅
⑶滴入KI溶液后再加CCl4振荡静置
2Fe3++2I-=2Fe2++I2;溶液分层;上层无色下层紫色
⑷滴加Na2S溶液
2Fe3++S2-=2Fe2++S↓;溶液变浑浊
⑸通入H2S
2Fe3++H2S=2Fe2++S↓+2H+;溶液变浑浊
⑹通入SO2
2Fe3++SO2+2H2O=2Fe2++
+4H+;溶液颜色变浅
②Fe2+、Fe3+转化成单质铁一般是高温时利用还原剂(H2、C、CO、Al)进行还原生成。
(6)铁的冶炼
练5、硫铁矿在高温下被空气氧化产生二氧化硫:
4FeS2+11O2=8SO2+2Fe2O3。
设空气中N2、O2的含量分别为0.800和0.200(体积分数,以下气体含量均用体积分数表示),试完成下列各题:
(1)1.00molFeS2完全氧化,需要空气的体积(标准状况)为________L。
(2)55L空气和足量FeS2完全反应后,气体体积(同温同压)变为_______L。
(3)用空气氧化FeS2产生的气体混合物中,O2的含量为0.0800,计算SO2的含量。
(4)设FeS2的氧化产生的气体混合物为100L,其中O2为aL,SO2为bL。
①写出a与b的关系式。
②在下图中画出a和b的关系曲线(FeS2氧化时,空气过量20%)
说明:
为方便作图,纵坐标用13b表示
3、金属的冶炼
(1)冶炼原理
金属元素在自然界中以化合态形式存在,所以转化成零价单质只能是含金属元素的化合物得电子被还原:
。
根据Mn+氧化性强弱的差异,来确定金属的冶炼方法。
(2)金属的冶炼方法
金属的活动性决定该元素在自然界的存在形式。
一般活泼的金属在自然界中以化合态存在,而活动性很差的金属则以游离态存在于自然界中,如金以单质形式存在,采用物理方法富集冶炼。
在以化合态存在的金属元素中,因活动性不同,采用的方法也不同。
①热分解法:
某些不活泼金属的化合物在受热时即可分解生成金属单质。
2HgO
2Hg+O2↑ 2Ag2O
4Ag+O2↑ HgS+O2
Hg+SO2
②热还原法:
用还原剂(C、CO、H2、Al等)还原金属氧化物,适合于金属活动性介于Zn~Cu之间的金属的冶炼。
a.碳还原法因碳资源丰富且价廉,故Sn、Pb、Zn、Fe常用此法冶炼:
SnO2+2C
Sn+2CO↑ZnCO3
ZnO+CO2↑ZnO+C
Zn+CO↑
b.用H2作还原剂,其特点是得到的金属较纯。
WO3+3H2
W+3H2O(H2作还原剂,适用于冶炼高纯度金属)
c.用Al作还原剂。
Cr2O3+2Al
2Cr+Al2O3(Al作还原剂,适用于冶炼难熔金属)
电解法:
是最强有力的氧化还原手段,适合于冶炼用普通还原剂难以还原的金属(活动性在Al以前的金属)。
2Al2O3
4Al+3O2↑ 2NaCl
2Na+Cl2↑
(3)金属的回收和资源保护
a.废旧金属的最好处理方法是回收利用。
b.回收利用废旧金属的意义是减少垃圾量,防止污染环境且缓解资源短缺的矛盾。
二、典例剖析
例1、0.1mol镁粉分别在足量的O2、CO2、N2中燃烧,生成固体的质量依次为W1、W2、W3。
下列关系式正确的是( )
A.W2>W1>W3 B.W1=W2>W3
C.W1=W2=W3 D.W3>W2>W1
例2、甲、乙两烧杯中各盛有100mL3mol·L-1的盐酸和氢氧化钠溶液,向两烧杯中分别加入等质量的铝粉,反应结束后测得生成的气体体积比为甲︰乙=1︰2,则加入铝粉的质量为( )
A.5.4g B.3.6g
C.2.7g D.1.6g
例3、在FeCl3、CuCl2、FeCl2的混合溶液中,Fe3+,Cu2+和Fe2+的物质的量之比为3︰2︰1,现加入适量铁粉,使溶液中三种离子物质的量浓度之比变化为1︰2︰4,则参加反应的铁粉与原溶液Fe3+的物质的量之比为( )
A.2︰1 B.1︰2
C.1︰3 D.1︰4
例4、将氯化铝溶液和氢氧化钠溶液等体积混合,得到的沉淀物中铝元素的质量与溶液中所含铝元素的质量相等,则原氯化铝溶液和氢氧化钠溶液的物质的量浓度之比可能是( )
A.1︰3 B.2︰3
C.1︰4 D.2︰7
例5、铁及铁的化合物应用广泛,如FeCl3可用作催化剂、印刷电路铜板腐蚀剂和外伤止血剂等。
(1)写出FeCl3溶液腐蚀印刷电路铜板的离子方程式:
_____________________________。
(2)若将
(1)中的反应设计成原电池,请画出原电池的装置图,标出正、负极,并写出电极反应式。
正极反应___________________________
负极反应___________________________
(3)腐蚀铜板后的混合溶液中,若Cu2+、Fe3+和Fe2+的浓度均为0.10mol·L-1。
请参照下表给出的数据和药品,简述除去CuCl2溶液中Fe3+和Fe2+的实验步骤_______________。
氢氧化物开始
沉淀时的pH
氢氧化物沉淀
完全时的pH
Fe3+
Fe2+
Cu2+
1.9
7.0
4.7
3.2
9.0
6.7
提供的药品:
Cl2浓H2SO4NaOH溶液CuOCu
(4)某科研人员发现劣质不锈钢在酸中腐蚀缓慢,但在某些盐溶液中腐蚀现象明显。
请从上表提供的药品中选择两种(水可任选),设计最佳实验,验证劣质不锈钢易被腐蚀。
有关反应的化学方程式:
___________________________________;
劣质不锈钢腐蚀的实验现象:
_______________________________。
例6、标准状况下,取甲、乙、丙各30.0mL相同浓度的盐酸,然后分别慢慢加入组成相同的镁铝合金粉未,得到下表中有关数据(假设反应前后溶液体积不发生变化)。
实验序号
甲
乙
丙
合金质量/mg
255
385
459
气体体积/mL
280
336
336
请回答:
(1)甲组实验中,盐酸_________;乙组实验中盐酸_________。
(选填“过量”“适量”或“不足量”)
(2)盐酸的物质的量浓度为_________。
(3)合金中Mg、Al的物质的量之比为_________。
(4)丙实验之后,向容器中加入一定量1.00mol·L-1NaOH溶液,能使合金中的铝粉恰好完全溶解,再过滤出不溶性固体,求所得溶液中各溶质的物质的量浓度。
(要求写出计算过程)
例7、现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为amol,Cu的物质的量分数为x。
研成粉末后,全部投入含bmolHNO3的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)用微粒符号填写下列空白(列举出全部可能的情况)。
①
②
③
④
⑤
⑥
残留固体成分
溶液中的金属离子
(2)当溶液中金属离子只有Fe2+、Cu2+时,则b的取值范围是(用a、x表示)______________。
(3)当x=0.5时,溶液中Fe3+与Fe2+的物质的量相等时,在标准状况下共产生672mL气体。
求a、b的值。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 重要 金属
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《贝的故事》教案4.docx
《贝的故事》教案4.docx
