 1001平衡和电化学.docx
1001平衡和电化学.docx
- 文档编号:2795316
- 上传时间:2022-11-15
- 格式:DOCX
- 页数:26
- 大小:309.12KB
1001平衡和电化学.docx
《1001平衡和电化学.docx》由会员分享,可在线阅读,更多相关《1001平衡和电化学.docx(26页珍藏版)》请在冰豆网上搜索。
1001平衡和电化学
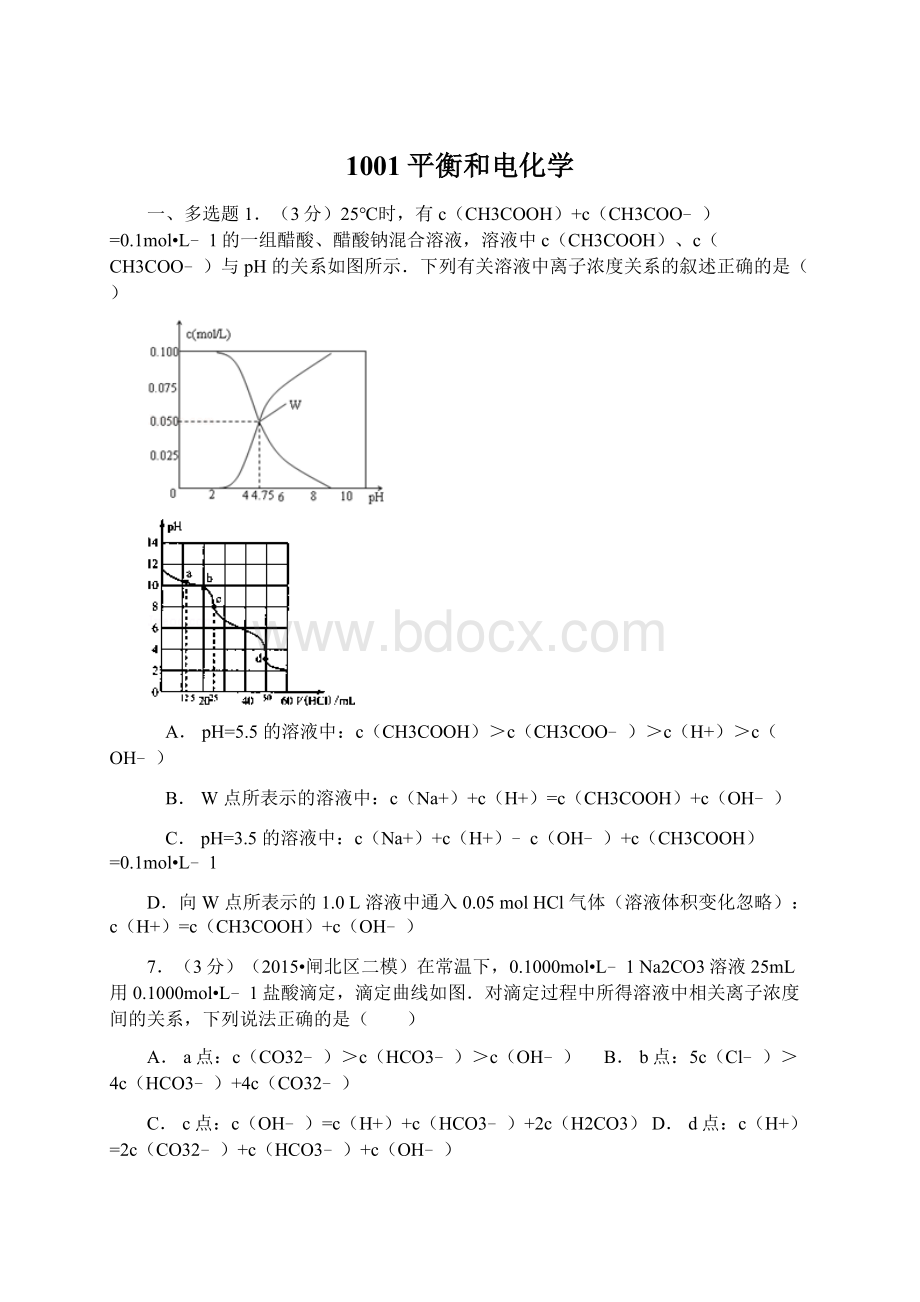
一、多选题1.(3分)25℃时,有c(CH3COOH)+c(CH3COO﹣)=0.1mol•L﹣1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO﹣)与pH的关系如图所示.下列有关溶液中离子浓度关系的叙述正确的是( )
A.pH=5.5的溶液中:
c(CH3COOH)>c(CH3COO﹣)>c(H+)>c(OH﹣)
B.W点所表示的溶液中:
c(Na+)+c(H+)=c(CH3COOH)+c(OH﹣)
C.pH=3.5的溶液中:
c(Na+)+c(H+)﹣c(OH﹣)+c(CH3COOH)=0.1mol•L﹣1
D.向W点所表示的1.0L溶液中通入0.05molHCl气体(溶液体积变化忽略):
c(H+)=c(CH3COOH)+c(OH﹣)
7.(3分)(2015•闸北区二模)在常温下,0.1000mol•L﹣1Na2CO3溶液25mL用0.1000mol•L﹣1盐酸滴定,滴定曲线如图.对滴定过程中所得溶液中相关离子浓度间的关系,下列说法正确的是( )
A.a点:
c(CO32﹣)>c(HCO3﹣)>c(OH﹣) B.b点:
5c(Cl﹣)>4c(HCO3﹣)+4c(CO32﹣)
C.c点:
c(OH﹣)=c(H+)+c(HCO3﹣)+2c(H2CO3)D.d点:
c(H+)=2c(CO32﹣)+c(HCO3﹣)+c(OH﹣)
2.(3分)(2012•腾冲县校级模拟)常温下,下列溶液的pH或微粒的物质的量浓度关系不正确的是( )
A.在醋酸的稀溶液中存在电离平衡:
CH3COOH⇌CH3COO﹣+H+,加水一定能使电离平衡右移,氢离子浓度增大
B.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,混合液的pH等于7,则反应后的混合液:
2c(R2﹣)+c(HR﹣)=c(Na+)
C.将0.2mol/L的某一元酸HA溶液和0.1mol/LNaOH溶液等体积混合后溶液pH大于7,则反应后的混合液:
2c(OH﹣)=2c(H+)+c(HA)﹣c(A﹣)
D.某物质的溶液中由水电离出的c(H+)=1×10﹣amol/L,若a>7时,则该溶液的pH一定为14﹣a
二、单选题3.(3分)把0.05molNaOH固体分别加入到下列100mL溶液中,溶液导电能力变化不大的是( )
A.自来水B.0.5mol•L﹣1HCl溶液C.0.5mol•L﹣1CH3COOH溶液D.0.5mol•L﹣1氨水
4.(3分)(2013秋•海珠区校级期中)下列叙述中能说明某物质是弱电解质的是( )
A.熔融状态下不导电 B.不是离子化合物,而是共价化合物
C.水溶液的导电能力很差 D.溶液中溶质分子和电离出的离子共存
5.(3分)(2012•永州模拟)下列各组离子在指定溶液中能大量共存的是( )
①无色溶液中:
K+、Na+、MnO﹣4、SO2﹣4②pH=11的溶液中:
CO2﹣3、Na+、AlO﹣2、NO﹣3
③加入Al能放出H2的溶液中:
Cl﹣、HCO﹣3、SO2﹣4、NH+4
④由水电离出的c(OH﹣)=10﹣13mol•L﹣1的溶液中:
Na+、Ba2+、Cl﹣、Br一
⑤有较多Fe3+的溶液中:
Na+、H+、SCN﹣、HCO﹣3⑥酸性溶液中:
Fe2+、Al3+、NO﹣3、I﹣、Cl﹣.
A.①②B.③⑥C.②④D.⑤⑥
6.(3分)下列溶液中离子可以大量共存的是( )
A.加Zn能放出H2的溶液:
Cl﹣、
、
、
B.透明溶液:
K+、Na+、
、
C.pH=11的溶液:
、Na+、Al3+、
D.使石蕊试液变红的溶液:
Na+、Ba2+、Cl﹣、S2﹣
8.(3分)25℃时,下列说法正确的是( )
A.pH=12的NaOH溶液中,c(H+)=10﹣12mol•L﹣1,将溶液稀释为原体积的10倍后c(H+)=
mol•L﹣1=10﹣13mol•L﹣1
B.pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后,因生成的CH3COONa水解,所以由水电离出的c(H+)>10﹣7mol•L﹣1
C.pH=2的盐酸、pH=2的醋酸中由水电离出的c(H+)均为10﹣12mol•L﹣1
D.pH=11和pH=13的NaOH溶液等体积混合后,溶液中的c(H+)=
mol•L﹣1
9.(3分)现有常温下的四种溶液:
①0.01mol/L醋酸溶液、②0.01mol/LHCl溶液、③pH=12的氨水、④pH=12的NaOH溶液.下列说法正确的是( )
a.水的电离程度①中最小,③中最大b.水的电离程度①中最大,②③④相等
c.将②③等体积混合,所得的溶液中由水电离出来的c(OH﹣)<1×10﹣7mol/L
d.将①③等体积混合,所得的溶液中由水电离出来的c(OH﹣)>1×10﹣7mol/L.
A.aB.bC.bcD.bd
10.(3分)(2012秋•故城县期末)现有等pH或等物质的量浓度的盐酸和醋酸溶液,分别加入足量镁,产生H2的体积(同温同压下测定)的变化图示如下:
其中正确的是( )
A.①③B.②④C.①②③④D.都不对
11.(3分)(2009•湘桥区校级三模)在体积均为1L,pH均等于2的盐酸和醋酸溶液,分别投入0.23gNa,则下图中比较符合反应事实的曲线是( )
A.
B.
C.
D.
12.(3分)(2010•山东)某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示.据图分析,下列判断错误的是( )
A.Kap[Fe(OH)3]<Kap[Cu(OH)2] B.加适量NH4CL固体可使溶液由a点变到b点
C.c、d两点代表的溶液中c(H+)与c(OH﹣)乘积相等
D.Fe(OH)3、Cu(OH)2分别在b、c两点代表的溶液中达到饱和
13.(3分)25℃时,某难溶性碱MOH在水中的沉淀溶解平衡曲线如图所示(单位:
mol•L﹣1).下列说法正确的是( )
A.该碱在25℃时的Ksp为2×10﹣10 B.a点的Ksp大于b点的Ksp
C.通过蒸发可使溶液由b点变为c点
D.25℃时,要使c(M+)为0.1mol•L﹣1的溶液形成沉淀,溶液的pH至少要升高到5
14.(3分)(2015春•宣威市校级月考)下列说法正确的是( )
A.25℃时,在pH=4的盐酸和NH4Cl溶液中,由水电离出的H+浓度相等
B.25℃时,pH=3和pH=5的盐酸等体积混合后,溶液的pH=4
C.25℃时,pH=9和pH=11的NaOH溶液等体积混合后,溶液的pH=10
D.25℃时,pH=3.6的某橙汁中的c(H+)是pH=5.6的某西瓜汁中的c(H+)的100倍
15.(3分)25℃时,pH=a的某一元酸与pH=b的氨水、烧碱溶液分别等体积混合后得到甲、乙两溶液,若a+b=14,则关于甲、乙两溶液pH的判断正确的是( )
A.甲的pH可能大于7、等于7或小于7 B.甲的pH不可能小于7
C.乙的pH可能大于7、等于7或小于7 D.乙的pH不可能小于7
16.(3分)(2013•贵州一模)室温下,水的电离达到平衡:
H2O═H++OH﹣.下列叙述正确的是( )
A.将水加热,平衡向正反应方向移动,Kw不变
B.向水中加入少量盐酸,平衡向逆反应方向移动,c(H+)增大
C.向水中加入少量NaOH固体,平衡向逆反应方向移动,c(OH﹣)降低
D.向水中加入少量CH3COONa固体,平衡向正反应方向移动,c(OH﹣)=c(H+)
17.(3分)(2012•菏泽二模)已知100℃时,水的离子积常数Kw=1×l0﹣12,对于该温度下pH=1的硫酸,下列叙述正确的是( )
A.向该溶液中加入同温同体积pH=13的Ba(OH)2溶液,反应后溶液呈中性
B.该溶液中硫酸电离出的c(H+)与水电离出的c(H+)之比为10﹣10
C.等体积的该硫酸与室温下pH为1的硫酸中和碱的能力相同
D.该溶液中水电离出的c(H+)是同温下pH为3的硫酸中水电离出的c(H+)的100倍
18.(3分)(2008•上海)某酸性溶液中只有Na+、CH3COO﹣、H+、OH﹣四种离子.则下列描述正确的是( )
A.该溶液可由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液可由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO﹣)>c(Na+)>c(OH﹣)>c(H+)
D.加入适量氨水,c(CH3COO﹣)一定大于c(Na+)、c(NH4+)之和
19.(3分)某溶液中由水电离产生的c(H+)=1×10﹣13mol/L,则该溶液中一定可以大量共存的离子是( )
A.K+、Na+、
、Cl﹣B.K+、Na+、
、S2
C.Ca2+、
、
、Cl﹣D.Fe2+、Fe3+、
、Cl﹣
20.(3分)(2013•忻州二模)体积相同的盐酸和醋酸两种溶液,n(Cl﹣)=n
=0.01mol,下列叙述错误的是( ) A.它们与NaOH完全中和时,醋酸所消耗的NaOH多
B.它们分别与足量CaCO3反应时,放出的CO2一样多
C.两种溶液的pH相同 D.分别用水稀释相同倍数后,n(Cl﹣)<n
21.(3分)(2012•郴州校级二模)用A、B、C、D四种酸进行下列实验:
①25℃时,pH=a的酸A与pH=b的NaOH溶液等体积混合,混合后测得溶液的pH=7,且a+b>14;
②酸B与NaCl不反应,能与Na2CO3反应生成CO2;
③向物质的量浓度为10﹣2mol•L﹣1的C溶液中滴加甲基橙试液,溶液呈黄色;
④酸D的钠盐不止一种,向两种D的钠盐水溶液中分别滴加紫色石蕊试液时,一个显红色,一个显蓝色.
从上述实验数据和现象中,可以用来确定是弱酸的实验是( )
A.②③B.①③④C.②③④D.全部
22.(3分)(2009•金安区校级模拟)下列溶液中有关微粒的物质的量浓度关系正确的是( )
A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):
c(Na+)=c(HRO3﹣)+2c(RO32﹣)
B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:
c(Na+)>c(Cl﹣)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):
①<③<②
D.等体积等物质的量浓度的NaClO(aq)与NaCl(aq)中离子总数多少:
N后<N前
23.(3分)(2014•大东区校级一模)常温下,0.1mol•L﹣1某一元酸(HA)溶液中
,下列叙述正确的是( )
A.该一元酸溶液的pH=1 B.该溶液中由水电离出的c(H+)=1×10﹣11mol•L﹣1
C.该溶液中水的离子积常数为1×10﹣22
D.用pH=11的NaOH溶液V1L与V2L0.1mol•L﹣1该一元酸(HA)溶液混合,若混合溶液的pH=7,则V1<V2
24.(3分)常温下,0.1mol•L﹣1某一元酸(HA)溶液中
=1×10﹣8.下列叙述正确
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 1001 平衡 电化学
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 铝散热器项目年度预算报告.docx
铝散热器项目年度预算报告.docx
