 土壤基本性质.docx
土壤基本性质.docx
- 文档编号:27928240
- 上传时间:2023-07-06
- 格式:DOCX
- 页数:46
- 大小:104.12KB
土壤基本性质.docx
《土壤基本性质.docx》由会员分享,可在线阅读,更多相关《土壤基本性质.docx(46页珍藏版)》请在冰豆网上搜索。
土壤基本性质
第二章土壤基本性质
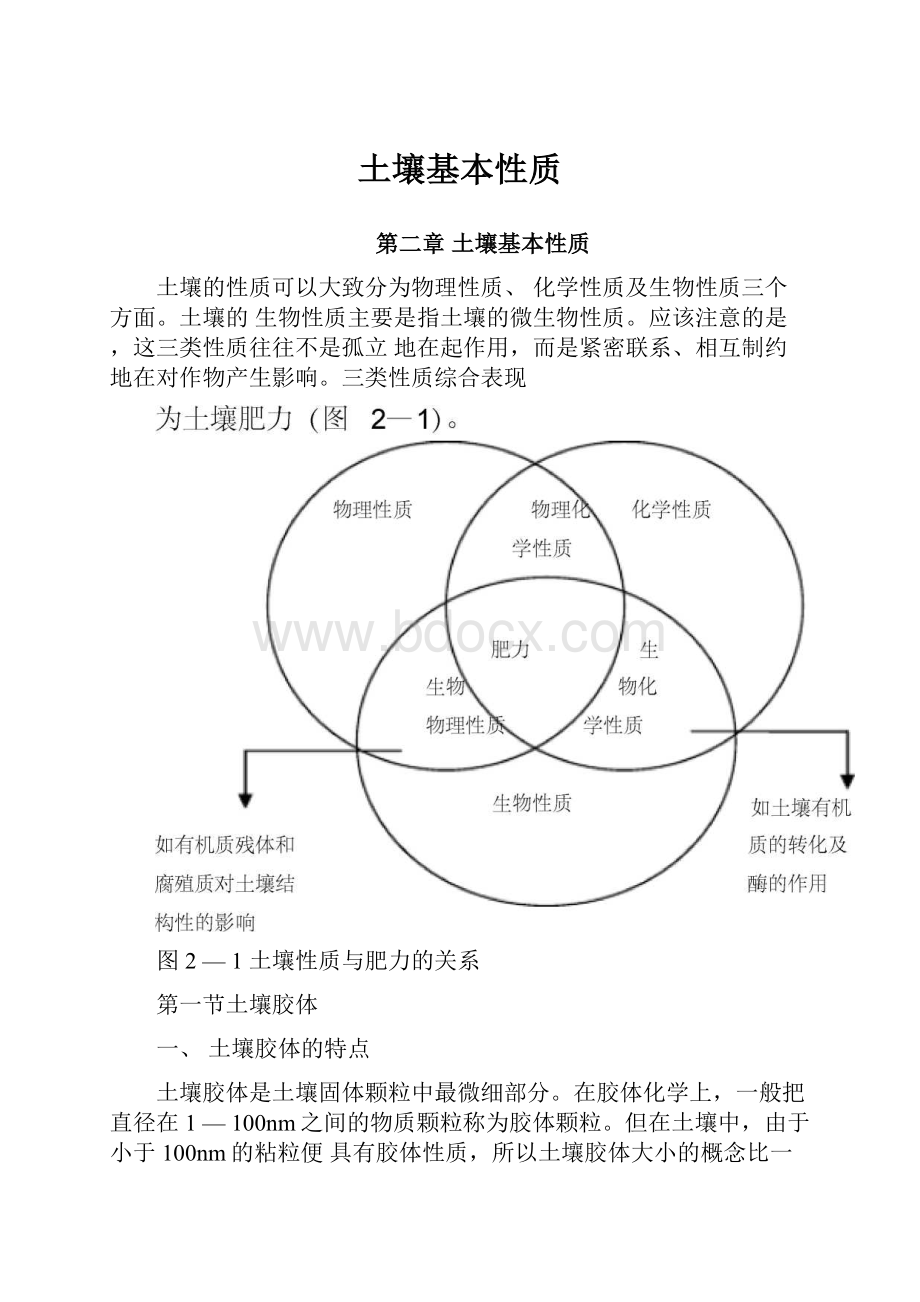
土壤的性质可以大致分为物理性质、化学性质及生物性质三个方面。
土壤的生物性质主要是指土壤的微生物性质。
应该注意的是,这三类性质往往不是孤立地在起作用,而是紧密联系、相互制约地在对作物产生影响。
三类性质综合表现
图2—1土壤性质与肥力的关系
第一节土壤胶体
一、土壤胶体的特点
土壤胶体是土壤固体颗粒中最微细部分。
在胶体化学上,一般把直径在1—100nm之间的物质颗粒称为胶体颗粒。
但在土壤中,由于小于100nm的粘粒便具有胶体性质,所以土壤胶体大小的概念比一般规定的胶体颗粒的上限大10倍。
土壤溶液中有胶体微粒分散存在时,叫做土壤胶体溶液。
二、土壤胶体的种类
土壤胶体按其成分不同,可以分以下三类:
(一)无机胶体
无机胶体主要是极细微的土壤粘粒,包括成分简单的含水氧化物(含水氧化铁、氧化铝、氧化硅)和成分复杂的各种层状铝硅酸盐(高岭石、蒙脱石、水云母等),它们大部分是次生矿物。
含水氧化物和层状铝硅酸盐这两类矿物都是岩石风化和成土过程的产物,都能影响土壤肥力特性,就广义而言统称为黏土矿物。
(二)有机胶体
有机胶体主要是腐殖质,它是土壤有机质腐殖化过程的产物。
由于腐殖质分子大,功能团多,解离后带负电量大,对土壤保肥供肥能力有深刻的影响。
有机胶体是极好的胶结剂,可以把土粒胶结在一起形成良好的土壤结构。
(三)有机无机复合胶体
土壤中的无机胶体和腐殖质胶体绝大部分都结合在一起,形成有机无机复合
胶体。
土壤中的有机和无机胶体可以通过多种方式进行结合,但大多数是通过多
价离子(如钙、镁、铁、铝等)或功能团(如氨基、羧基、酚羟基、醇羟基等)将带负电荷的粘粒矿物和腐殖质连结成有机无机复合胶体的。
土壤中的微生物一般都吸附在有机胶体和无机胶体颗粒的表面,被此结合成具有活性的土团及土壤结构。
西南农学院的研究结果认为,微生物也是复合胶体的一个组成部分,土壤复合胶体应是土壤微生物一有机一无机复合胶体。
这种复合胶体借助于微生物体内酶和体外酶以及植物根的分泌物,植物遗体及有机肥料等带入的大量酶的活动,在一定温度范围内,通过各类物质的代谢作用,可以调节土体内部热、水、肥,维持其动态平衡,是维持土壤与植物的生理协调的物质基础。
三、土壤胶体的构造
土壤胶体微粒的构造可分为三部分:
微粒核、决定电位离子层和补偿离子层。
决定电位离子层和补偿离子层总称为双电层,见图2—2。
(一)微粒核(胶核)
微粒核是胶体微粒的核心部分,它是由组成胶体微粒的基本物质(黏土矿物、腐殖质、蛋白质等)的分子群所组成。
(二)决定电位离子层(双电层内层)
决定电位离子层是固定在微粒表面并决定胶体微粒电荷和电位的一层离子。
它是由微粒核表面分子解离或从溶液中吸附某些离子而形成。
它能使胶体微粒带
电,带电的性质(电荷的符号)决定其吸附阳离子或阴离子,其带电量决定吸附离子的数量。
(三)补偿离子层(双电层外层)
决定电位离子层的存在,必然吸附与其电荷相反的离子围绕在其周围,形成补偿电子层。
这一层离子带着和决定电位离子层电性相反而电量相等的电荷。
补偿离子层按其被决定电位层吸附力的强弱和活动情况,又可分为两层,这两层是逐步过渡的。
1•非活性层
靠近决定电位离子层,所受吸力很强,被吸附很紧,不能自由活动的离子层。
2•扩散层
离决定电位离子层较远,疏散在胶粒的外围,由非活性层逐渐过渡到这一层。
由于决定电位离子层对它的吸力不强,所以它有较大的活动性,呈扩散分布的状态,故叫扩散层。
扩散层的离子可与溶液中的离子互相代换,很容易参加土壤的离子代换作用等多种过程。
此层为胶体微粒的最外层,由这一层逐渐过渡到胶粒间溶液。
四、土壤胶体的性质
土壤胶体对土壤肥力有重大影响,其实质是因为它具有下列主要特性:
(一)胶体具有巨大的表面能
任何物质的分子与分子之间有着互相吸引的力,在物质内部,任何分子都受
到周围分子的同等吸力,因此它所受到的各方面的力是均衡的,这些均衡的力相互抵消,而合力就等于零,所以对其它分子的能量没有影响。
但在物体表面上的分子,在它的周围,并不是相同的分子,所以它受到不均衡的吸力。
在它与液体或气体接触的一面,因液体或气体分子对它的吸力小,在这种情况下,分子的合力不等于零,因而,致使表面上的分子,对外表现出有剩余能量,这种能量是由于表面的存在而产生,所以叫做表面能。
表面能的大小取决于物体的表面积,换句话说是取决于比面。
所谓比面就是
指每单位重量物体的表面积,可以用下式表示:
比面
面积
重量
⑴…
设有半径为r的球形土粒,式,则得:
4n33
比面二一=
3
4/3n&652.65
它的重量应为4/3n3,球形面积为4n3,代入
(1)
11
3-=1.13(——平方厘米/克),,
(2)
rr
从
(2)式中可以看出比面与颗粒半径成反比。
例如半径为0.1厘米的1克
砂粒,比面只有11.3平方厘米,而半径为0.0001厘米的1克粘粒,它的比面可达11,300平方厘米。
由此可见,一定重量的物体,颗粒越细,总表面积越大,表面能也越大。
土壤胶体微粒半径很小,比面很大,巨大的比面,使它产生了巨大的表面能。
所以土壤越细,所含胶体微粒越细,表面能越大,吸附分子态物质能力也越强。
(二)胶体具有带电性
胶体颗粒一般都带有电性,土壤胶体也不例外。
土壤胶体带电的主要原因是由于微粒核表面分子本身的解离所致。
_
土壤有机胶体含有羧基(一COOH)、羟基(一OH)和酚基(C—OH),它们在周围溶液中解离出若干数量的氢离子,解离后形成一COO—与O-留在核面上,而使决定电位离子层带负电荷,见图2—3。
一般情况,含水氧化硅胶体外层为硅酸分子(H2SQ3)发生解离:
H2SiO3=HHSiO3一
H十+Si
它们在碱性溶液中则解离出氢离子,使土壤胶体带负电荷。
其解离式为:
FeOH3HCI=FeOH2CLH?
O
FeOH2Cl「=FeOCl一H2O
这样Fe(OH)2+或FeO+构成决定电位的离子层,而Cl-构成补偿离子层,见图2—4。
它们在碱性溶液中则解离出氢离子,使土壤胶体带负电荷。
其解离式为:
-+
Fe(OH)3+NaOH=Fe(OH)2ONa+H2O
Fe(OH)2O-被固定在微粒核表面,构成决定电位离子层,而Na+则构成补偿
离子层。
这种随着土壤PH值而改变,既能带正电,又能带负电的胶体称为两性胶体。
土壤中粘土矿物多带负电荷。
有机无机复合胶体虽然保留各种组成的原来性质,但由于土壤中含量较多的硅酸和粘土矿物都带有负电荷,而富集于表土的有
机胶体也带有负电荷,所以有机无机复合胶体表现出带多量的负电荷。
综上所述,土壤胶体大多数是带负电荷的,因此补偿离子层多由阳离子组成。
由于土壤胶体带电,所以才能吸收、保持许多离子态养分,既能避免流失、又可随时供应植物吸收利用。
(三)胶体的凝聚和分散作用土壤胶体有两种不同的状态:
一种是胶体微粒均匀散布在水中,呈高度分散的溶胶;另一种是胶体微粒彼此联结凝聚在一起而呈絮状的凝胶。
土壤胶体溶液,如受某些因素的影响,使胶体微粒下沉,由溶胶变成凝胶,这种作用叫胶体的凝聚作用。
反之凝胶分散或呈溶胶状态,叫做胶体的分散作用。
土壤胶体所以呈凝胶状态,且具有相当的稳定性,这是由于胶体微粒的带电性和水膜的存在而引起的。
因为同一种胶粒,带有相同的电荷,促使胶粒相互排斥,而水膜又能阻碍胶粒互相粘结,因而使胶体呈溶胶状态。
如果减少土壤水分,促使胶体水膜变薄和提高电解质浓度,或直接加入电解质,以中和胶体的电性,必然会促使胶体粘粒结成较大的颗粒而凝聚。
土壤中带负电荷的胶粒占多数,所以土壤溶液中的离子能使带负电的胶粒凝聚。
实验证明,阳离子的价数越高,半径越大,所产生的凝聚作用越强。
土壤中常见的阳离子,按凝聚力的大小,依次排列如下:
Fe3+>Al3+>Ca2+>Mg2+>NH4+>K+>N扌
当土壤干燥和冻结时,土壤溶液所含电解质的浓度增加,同样会引起胶体的凝聚。
此外,土壤中带有相反电荷的胶体,相互接触时也会凝结作用。
溶胶变成凝胶后,如果反复用水冲洗,容易发生分散作用变成溶胶,这种凝聚叫做可逆凝聚。
一般由一价的阳离子(N6、k+、nh4+)在高浓度时所引起的凝聚为可逆凝聚。
二价及三价阳离子(Mg2+、Ca2+、Al3+、)所引起的凝聚则比较难于进行分散。
它们所形成的土壤结构具有相当的稳定性,特别是Ca2+和腐殖质共同作用下,所形成的土壤结构更好。
土壤胶体是溶胶状态时,土壤结构不良,耕性很差,湿时泥泞,干时结块,影响土壤的通气透水性,对植物生育和土壤耕作都是不利的。
相反呈凝胶状态时,土壤具有良好的结构和耕性,养分也易于保存。
所以在生产上,常施用钙质肥料(如石灰、石膏)改善胶体性质,以及通过排水、晒田、冰冻等方法提高土壤溶液中离子浓度和通过深耕晒垡、冻垡等措施促进胶体脱水,改善土壤结构。
土壤肥力的特点不仅在于土壤具有供应水、肥的能力,更重要的是具有协调供水、肥的能力,满足作物生长所需要的水分、养分等生活条件,让作物吃饱、喝足、住得舒服。
要能达到这样的要求,良好的耕作是一重要前提,而有机无机复合胶体则是形成土壤良好结构的重要物质基础。
第二节土壤交换吸收性能
浑浊的水通过土壤会变清,粪水、臭气通过土壤,臭味会消失或减弱,海水通过土壤会变淡等现象说明,土壤对施入的肥料、盐分或微小颗粒有吸收和保持的能力。
土壤吸持各种离子、分子、气体和粗悬浮体的能力称为土壤的吸附性能。
它是土壤能保存营养物质并不断地向植物提供养分的主要原因。
各种吸收作用都
有各自的特点,其中机械的吸收性能是指土壤孔隙对较大的颗粒的阻留作用;物
理吸收性能是指土壤细粒靠表面能对分子态物质的吸收;化学吸收性能是指土壤溶液中的可溶性养分与土壤中某些物质起化学反应,形成难溶性物质的作用;而生物吸收性能则是指植物和微生物对土壤中可溶态养分的选择吸收作用。
还有交
换吸收性能是指土壤溶液中的离子态养分与土壤胶体上的离子进行交换后而被
保存在土壤中的作用。
它对土壤养分的吸收和释放起着更为重要的作用
一、土壤的阳离子交换吸收作用土壤胶体多数带负电荷,扩散层的阳离
子和土壤溶液中的阳离子进行交换,称为阳离子交换吸收作用。
反应过程如下:
+
H
+
—K
小2+
Ca
土
—K+
+
K
壤
—K+
+5KCl二
小2+
Ca
胶
-Ca2+
+
K
体
+土
KK+
K
KL
壤+
[+壤
+体
+2CaCb+HCI
Ca2+
(一)阳离子交换吸收作用的特征由反应式可知,阳离子交换有两个基
本特征:
1•可逆反应阳离子交换是可逆反应。
所谓可逆反应,是指反应同时向两个方向进行,如AB+CDAD+CB。
在一般情况下,反应很快达到平衡,然而反应的任何一个方面都不能彻底完成。
土壤在自然状况下,不是单纯吸收某一种离子,而是吸收两种或两种以上的离子。
被土壤胶体吸附的任何一种阳离子,不可能被全部代换到溶液中去。
2.等当量交换在阳离子交换过程中,离子间以离子价为根据做等量交换。
如一个当量的钙离子可被一个当量的钾离子所代替,钙离子的当量是40/2=20,
而钾离子的当量是39.1/1=39.1,即20克的钙离子可以代换39.1克的钾离子。
如果用两价的钙离子去交换一价的钾离子时,一个摩尔离子的钙可以代换两个摩尔离子的钾。
(二)阳离子交换能力一个阳离子把其它阳离子从胶体微粒上代换出来的能力,称为阳离子交换能力。
各种阳离子交换能力的大小顺序是:
Fe3+>Al3+>
+2+■_2+.・・・4+.,+-.+
H>Ca>Mg>NH、K>Na。
阳离子交换能力的大小受以下三种情况所支配:
1•离子价数离子交换能力随离子价数的增加而增大。
这时由于离子的电荷愈多,与胶体间的电性引力也愈强,因而交换能力增大。
2•阳离子半径和水化程度在电荷价数相等的离子中,离子半径愈大,其水
化半径趋于减小,则交换能力愈强。
因为在离子半径增大时,单位表面积的电荷量(即电荷密度)减小,电场强度减弱,所以对极性分子的水的吸引力小,离子外围的水膜薄,水化半径减小,以致同负胶粒间的距离较近,相互吸引力较大,并且具有较强的交换能力。
但是,H+的交换能力比两价的Ca2+、Mg2+大,这是因为H+半径极小,水化能力极弱,运动速度又大,因而交换能力强(表2—1)。
表2—1离子半径、水化程度与交换能力的关系
离子
价数
原子量
0
交换能力
离子半径
(A)
未水化
水化
H+
1
1.008
—
—
1
Ca2+
2
40.08
1.06
10.00
2
Mg2+
2
24.32
0.78
13.30
3
K+
1
39.10
1.33
5.32
4
nh4+
1
10.01
1.43
5.37
5
Na+
1
23.00
0.98
7.90
6
3•离子的浓度交换作用受质量作用定律的支配,即离子浓度愈大,交换能力愈强。
即使某一种离子的交换能力小,但在它的浓度增加后,也能交换胶体上交换能力强的其它离子。
例如在钙质土上施用硫酸铵时,高浓度的NH4+可以交
换出土壤胶体上的一部分Ca2+,从而NH4+得以保存下来。
因此,生产上可以通过增加土壤中某些有益阳离子的数量来控制和调节阳离子交换的方向,以便有目
的地调节土壤养分和改良土壤性质。
(三)阳离子交换量(代换量或吸收容量)土壤吸收阳离子能力的大小通
常以阳离子交换量来衡量。
阳离子交换量是指每百克干土所能吸收的全部交换性阳离子(包括H+与盐基离子)的毫克当量数(me)。
土壤交换量的大小是衡量土壤保肥能力等的主要指标。
交换量大的土壤,保肥性强,在植物的生育过程中不易脱肥,一次的施肥量可以多些。
交换量小的土壤,为了防止养分流失,一次施用化肥的数量不能太多。
一般认为,大于20me/100g干土的土壤为保肥力强的土壤;10—20me/100g干土,保肥力中等;小于10me/100g干土时,为保肥力弱的土壤。
不同土壤的阳离子交换量大小主要决定于下列条件:
1.胶体的数量和种类土壤质地愈细,胶体的物质愈多,土壤的交换量也愈
大。
一般砂土的交换量约为1—5me/100g土,砂壤土为7—8me/100g土,壤土为15—18me/100g土,而粘土则多大25—30me/100g土。
而有机胶体的交换量可达200—500me/100g土。
表2—2不同土壤胶体的阳离子交换量(me/100g土)
胶体种类
蒙脱石
伊利石
高岭石
含水氧化铁、铝
有机胶体
一般范围
60—100
20—40
3—15
极微
200—500
平均
80
30
10
—
350
2•土壤酸碱度(PH值)一般在土壤PH值下降时,H+增多,胶体上的H+不易解离,以致胶体所带负电荷的量较少,阳离子交换量随之降低。
反之,土壤溶液愈趋碱性,H+的解离愈多,胶粒的负电荷也愈多,亦即交换量愈大。
由于土壤胶体电性通常随着PH值而变化,所以测定阳离子交换量时一般都控制在PH7的条件下进行。
我国各地土壤类型不同,各自的交换量和吸收性阳离子的组成亦异。
如南方的红壤,随着粘粒含量很高,但开垦以后,腐殖质含量不多,粘粒矿物以高岭石及水化氧化铁、铝为主,加上处于高温多雨的热带、亚热带气候下,土体受到高度淋溶,盐基离子大量损失,致使吸收的离子有相当数量的日+和Al3+,土壤呈
酸性和强酸性反应,交换量很低,一般不超过5—8me/100g土。
在华北或西北干旱地区,土壤腐殖质含量不高,粘粒矿物以蒙脱石、水化云母为主。
由于降水量少,淋溶较弱,吸收的离子以钙、镁为主,土壤呈中性或微碱性反应,交换量较高,可达16—20me/100g土或更高。
碱化土或碱土的阳离子组成中有相当数量的Na+。
据此,土壤吸收的阳离子的组成基本上分为三种类型,以Ca2+为主的中性或微碱性土壤类型;Na+占一定比例的碱化土和碱土类型;以H+、Al3+为主的酸性土壤类型。
(四)土壤盐基饱和度土壤交换性阳离子包括致酸离子如H+、AI3+和盐基离子Ca2+、Mg2+、Na、K+、NH4+等。
当胶体所吸附的阳离子都是盐基离子时,土壤呈盐基饱和状态,称为盐基饱和土壤。
如果除盐基离子外,还有部分H+(或AI3+)离子,则为盐基不饱和土壤。
交换性阳离子中盐基离子所占的百分数称为
盐基饱和度
盐基饱和度(%)二
交换性盐基离子量交换性阳离子总量
100
例:
土壤的阳离子交换量为13.6me/100g土(表2—3),而交换性盐基离子
总量为3.6me/100g土,则该土壤的盐基饱和度为:
3.6100=26.5(%)
13.6
表2—3土壤阳离子交换量计算示例
交换性阳离子
每百克干土中
”0离子克数
摩尔原子量(即
摩尔离子量)
离子价
离子的克当量
每百克干土中
当量数
毫克当量数
H
+
0.01
1
1
1
0.01
10
盐
Ca2+
0.04
40
2
20
0.002
2
基
Mg2+
0.012
24
2
12
0.001
1
离
K+
0.0156
39
1
39
0.0004
0.4
子
Na+
0.0046
23
1
23
0.0002
0.2
阳离子交换量
H++Ca2+
+Mg2++K++Na=(me)/100g干土
13.6
由此可知,交换量大的土壤,如果盐基饱和度很低,则只能说明这种土壤保
持养分的潜力很大,但不能说明含有较多的养分,相反说明该土壤酸度大,需要采取有效措施进行改良。
肥沃的土壤不仅阳离子交换量大,而且盐基饱和度也高。
盐基饱和度大的土壤,它的盐基离子分布在扩散层的也多,易于被植物吸收。
一般认为,盐基饱和度以保持在70—90%时较为理想。
具有较高盐基饱和度和阳离子交换量的土壤,不仅有利于养分的积蓄和保存,而且在施肥量较多的情况下,也不会引起“烧苗”,又能不断解吸,供应植物吸收。
盐基饱和度的大小与雨量、母质和植被有密切关系。
一般干旱地区的土壤盐基饱和度高,多雨地区盐基饱和度低。
我国从南到北,从东到西,除少数土壤外,盐基饱和度逐渐增高。
大致以北纬33°为界,此线以南,除少数受母质影响外,一般盐基饱和度都低。
如有的红壤、黄壤,盐基饱和度在20%^下,甚至小于10%呈强酸性。
此线以北,除少数受针叶林植被影响外,多数为饱和度很高的土壤,例如东北的黑土,盐基饱和度可达80—95%以上。
二、土壤的阴离子交换吸收作用
(一)阴离子交换吸收作用阴离子交换吸收作用是指土壤中带正电荷胶体所吸收的阴离子相互交换的作用。
它同阳离子交换作用一样,一般也是可逆反应,迅速达到平衡,并受质量作用定律的支配,平衡转移也与离子浓度有关。
但是土壤中的阴离子交换吸收常和化学固定作用等交织在一起,很难截然分开。
例如PO43-可以被土壤中的Ca2+、Fe3+ftAl3+等化学固定,又能和粘粒表面的OH-相交换而固定在粘粒矿物上。
土
—OH-
土
—O
壤
—OH+KH2PO4
—►
壤
—O—P=O+KOH+2H2O
—OH
—O
(二)土壤对阴离子的交换吸收能力土壤中的阴离子依其被土壤吸收的难
易可分为三类:
1•易被土壤吸收的阴离子,如磷酸根离子(HPO4-、HPO42-、PO43-)、硅酸
根离子(HSiO『、SiO32-)及某些有机酸的阴离子,这类离子常与阳离子起化学反应,产生难溶性化合物。
2•很少被吸收,甚至不能被吸收的阴离子,如Cl-、NO3-、NO2-等。
由于它们不能和溶液中的阳离子形成难溶性盐类,而且不被土壤负电荷吸收,所以极易随水流失。
3•介于上述两者之间的阴离子,如SO42-、CO32-、HCO3-以及某些有机酸的阴离子。
由于土壤吸收SO42-、CO32-的能力较弱,在土壤含有大量Ca2+,且气候比较干燥的条件下,它们能起化学反应,形成难溶性的CaSC4或CaCO3。
影响土壤对阴离子交换吸收力的因素主要有:
1•离子价数阴离子的价数愈高,吸收力愈强。
阴离子吸收力的顺序是:
Cl-、NO3->SO42->PO43-。
Cl-、NO3-很少被吸收。
2•土壤胶体种类及其组成一般来说,含高岭石,水化氧化铁、铝较多的土
壤,对阴离子的吸收作用较大。
(三)土壤阴离子交换量土壤能保持的交换性阴离子的数量称为阴离子交
换量,也以每百克干土的毫克当量数表示。
土壤阴离子交换量与土壤粘粒矿物成分及土壤酸碱度有关。
土壤中含水氧化铁、铝胶体数量增多,则阴离子交换量加大。
例如在PH5时,含水氧化铁、铝的阴离子交换量可达100-150me/100g土.
三、离子交换吸收对土壤肥力的影响
(一)使土壤具有保肥、供肥性能土壤的保肥与供肥作用主要是通过离子交换实现的。
土壤胶体与土壤溶液间能进行可逆的离子交换,既能吸收保蓄养分,减少流失,又能交换出离子态养分,供植物吸收利用。
土保肥
_2++
壤=Ca+2NH4u
供肥
NH4+
NH4+
小2+
+Ca
土壤保肥性能和土壤吸收性能有着不可分割的联系。
一般讲,土壤中养分的
保存主要靠粘粒矿物和腐殖质。
我国土壤中分布最广的粘粒矿物是蒙脱石、伊利石和高岭石。
据中科院南京土壤研究所资料,华南、华中地区和丘陵山区红壤中的粘粒矿物以高岭土为主;江西、云南、四川等省的紫色土是以伊利石为主;在冲积物和沉积物上形成的水稻土因地区而有差异,如珠江下游地区以高岭石和伊利石为主,长江中下游和海河下游地区则以蒙脱石和伊利石为主;我国北方地区
则以伊利石为主。
由于这些粘土矿物表面都带有负电荷,所以能吸附保存各种阳离子态的养料,如Ca2+、Mg2+、N6、K+、NH4+等。
粘粒矿物种类不同,所带电荷量也不等,它们保存阳离子态养分的能力也有差异(表2—1,1—2)。
蒙脱石保存阳离子态养料的能力最大,伊利石次之,高岭石为最小。
此外,高岭石表面还有交换性Al3+,不易被肥料中低价离子如NH4+或K+所代替,所以它的保肥能力更小。
腐殖质胶体带负电荷,可以保存阳离子态养料。
由于土壤形成过程中自然条件等的不同,所形成的腐殖质的组成和功能团的含量也有差异,从而影响它的保
肥性能,一般讲,它的阳离子交换量每百克约为350me,较等量蒙脱石高3—7倍,较高岭石大30—50倍。
由于土壤有保肥性,施肥后肥料中的阳离子就能和土壤胶体上所吸附的阳离子进行交换。
因此在施用化学肥料时,不仅要了解作物的需要,而且还要考虑到
土壤的质地和粘粒矿物的种类及腐殖质的含量等。
一般讲,土壤质地较粘重,粘
粒矿物以蒙脱石或伊利石为主以及腐殖质含量较多的土壤,保肥能力较强,即使
一次施肥较多,养料也不致流失。
反之,土壤质
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 土壤 基本 性质
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #2机组现场施工用电布置措施.docx
#2机组现场施工用电布置措施.docx
