 《有机化学》第四版第五章 芳烃.docx
《有机化学》第四版第五章 芳烃.docx
- 文档编号:274800
- 上传时间:2022-10-08
- 格式:DOCX
- 页数:24
- 大小:902.91KB
《有机化学》第四版第五章 芳烃.docx
《《有机化学》第四版第五章 芳烃.docx》由会员分享,可在线阅读,更多相关《《有机化学》第四版第五章 芳烃.docx(24页珍藏版)》请在冰豆网上搜索。
《有机化学》第四版第五章芳烃
第五章芳烃芳香性
思考题
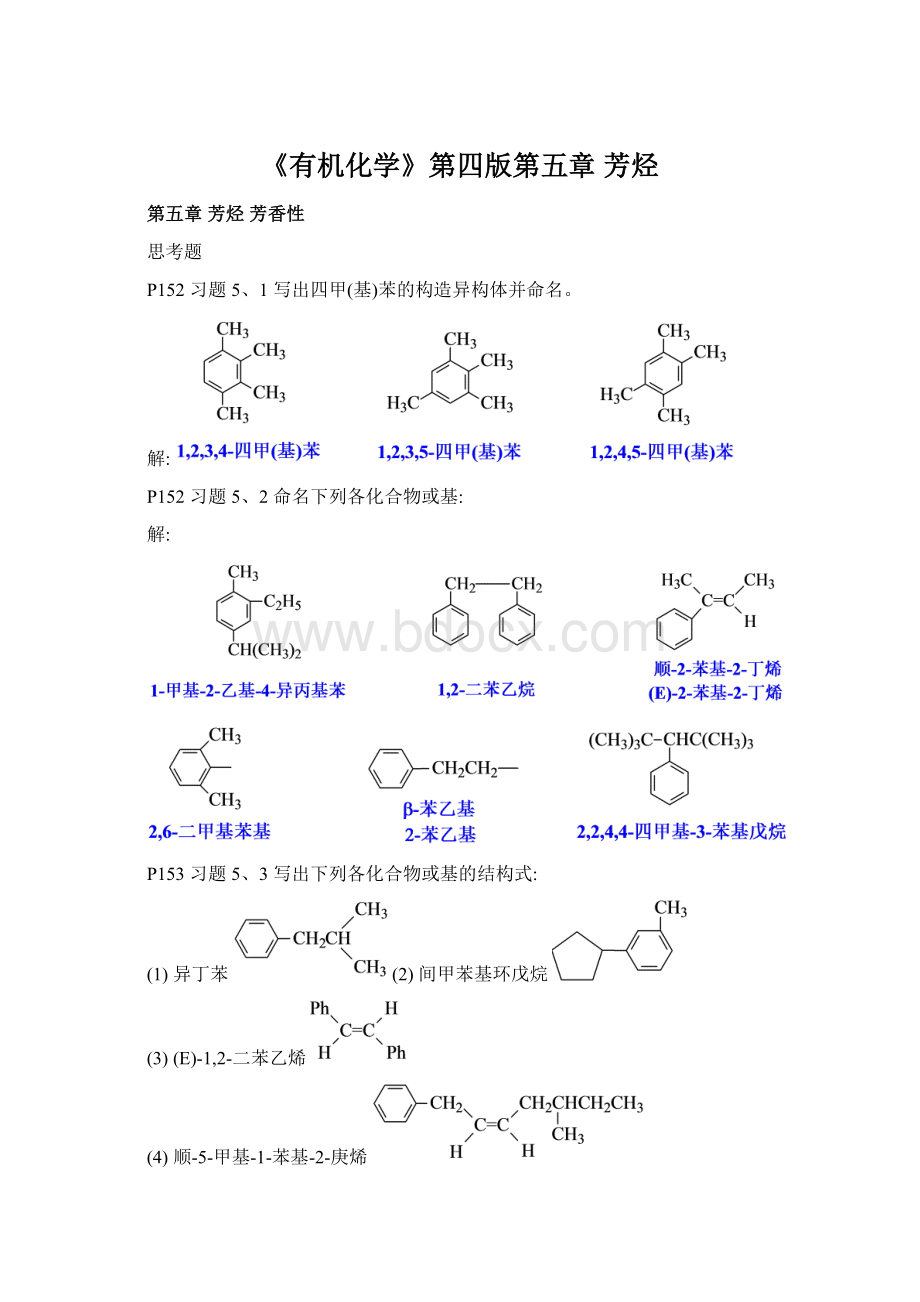
P152习题5、1写出四甲(基)苯的构造异构体并命名。
解:
P152习题5、2命名下列各化合物或基:
解:
P153习题5、3写出下列各化合物或基的结构式:
(1)异丁苯
(2)间甲苯基环戊烷
(3)(E)-1,2-二苯乙烯
(4)顺-5-甲基-1-苯基-2-庚烯
(5)二苯甲基(6)3-苯基-2-丙烯基
P156习题5、4甲苯的沸点比苯高30、5℃,而熔点低~100℃,为什么?
解:
甲苯的相对分子质量大于苯,分子间色散力大于苯,因比甲苯的沸点也高于苯;
但苯分子的对称性好,晶格能大于甲苯,因此苯的熔点高于苯。
P161习题5、5写出乙苯与下列试剂作用的反应式(括号内就是催化剂):
(1)Cl2(FeCl3)
(2)混酸(3)正丁醇(BF3)
(4)丙烯(无水AlCl3)(5)丙酸酐(CH3CH2CO)2O(无水AlCl3)
(6)丙酰氯CH3CH2COCl(无水AlCl3)
解:
(1)
(2)
(3)
(4)
(5)
(6)
P161习题5、6由苯与必要的原料合成下列化合物:
(1)
解:
(2)叔丁苯
解:
(3)
解:
(4)
解:
P164习题5、7试以苯与必要的原料合成正丙苯。
解:
P164习题5、8在氯化铝的存在下,苯与新戊基氯作用,主要产物就是2-甲基-2-苯基丁烷,而不就是新戊基苯。
试解释之。
写出反应机理。
解:
C+稳定性:
>>
P164习题5、8写出下列反应的产物:
P166习题5、10在日光或紫外光照射下,苯与氯加成生成六氯化苯,就是一个自由基链反应。
写出反应机理。
解:
P166习题5、11写出六氯化苯最稳定的构象式。
解:
从理论上说,六氯化苯最稳定的构象式应该就是;
P168习题5、12写出下列反应的产物或反应物的构造式:
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
P173习题5、13苯甲醚在进行硝化反应时,为什么主要得到邻与对硝基苯甲醚?
试从理论上解释之。
解:
硝基上邻位时,活性中间体的结构及稳定性如下:
其中(II)的共价键数目较多,且满足八隅体,较为稳定,对真实结构的贡献也最大。
导致真实结构的能量降低,从而使硝化反应的活化能降低,反应速度增大。
硝基上对位时,活性中间体的结构及稳定性如下:
其中(III)的共价键数目较多,且满足八隅体,较为稳定,对真实结构的贡献也最大。
导致真实结构的能量降低,稳定性增大,从而使硝化反应的活化能降低,反应速度增大。
硝基上间位时,没有类似的能量较低的共振结构式,不能使反应活化能降低,反应速度增大。
因此,苯甲醚在硝化时,主要得到邻、对位产物。
P175习题5、14苯磺酸在进行硝化反应时,为什么得到间硝基苯磺酸?
试从理论上解释之。
解:
+NO2进攻间位时,活性中间体的结构及稳定性如下:
其中没有能量特别高共振结构式,不会使活性中间体的真实结构的能量有太多的升高。
进攻邻位时,会有下列能量特别高的共振结构式出现:
(正电荷直接与吸电子基HO3S―相连)
使活性中间体的真实结构能量大大升高,稳定性大大降低,从而使邻位的硝化反应的活化能升高,反应速率降低。
进攻对位时,会有下列能量特别高的共振结构式出现:
(正电荷直接与吸电子基HO3S―相连)
使活性中间体的真实结构能量大大升高,稳定性大大降低,从而使对位的硝化反应的活化能升高,反应速率降低。
P176习题5、15解释下列事实:
反应
o-
p-
氯化
39
55
硝化
30
70
溴化
11
87
磺化
1
99
解:
从上到下,反应新引入的基团体积增大,使邻位取代反应的空间障碍增大,因此邻位取代产物比例减小;而对位取代的空间障碍相对较小一些,所以,对位取代产物比例增大。
P177习题5、16写出下列化合物一溴化的主要产物。
(1)
(2)(3)
(4)(5)
(6)
P177习题5、17完成下列反应式:
P179习题5、18由苯及必要的原料合成下列化合物:
(1)
解:
(2)
解:
(3)
解:
(4)
解:
P179习题5、19以较好的产率由苯与无机试剂制备4-硝基-1,2-二溴苯。
解:
P185习题5、20完成下列反应式:
(1)
(2)
(3)
(4)
P185习题5、21能否由2-甲基萘氧化制备2-萘甲酸?
说明理由。
解:
不能用2-甲基萘氧化制备2-萘甲酸,2-甲基萘氧化的产物更可能就是邻苯二甲酸(酐)。
因为萘环不及苯环稳定,能与氧化剂反应,且氧化反应总就是发生在电子云密度较大的环上。
P185习题5、22为什么萘剧烈氧化生成邻苯二甲酸酐后,不易再进一步被氧化?
答:
因为①稳定性:
苯环>萘环(离域能:
苯150、48kJ/mol,萘245、98)
②邻苯二甲酸酐相当于苯环带有两个吸电子的酰基,使苯环上电子云密度降低,不易发生氧化反应。
P187习题5、23完成下列反应式:
(1)
(2)
P193习题5、24应用Huckel规则判断下列化合物、离子与自由基就是否有芳香性?
(1)
(2)(3)
无无无
(4)(5)(6)
有有无
课后习题
(一)写出分子式为C9H12的单环芳烃的所有同分异构体并命名。
解:
(二)命名下列化合物:
(1)
(2)(3)
(4)(5)(6)
(7)(8)(9)
解:
(1)3-对甲苯基戊烷
(2)(Z)-1-苯基-2-丁烯(3)4-硝基-2-氯甲苯
(4)1,4-二甲基萘(5)8-氯-1-萘甲酸(6)1-甲基蒽
(7)2-甲基-4-氯苯胺(8)3-甲基-4羟基苯乙酮(9)4-羟基-5-溴-1,3-苯二磺酸
(三)完成下列各反应式:
解:
红色括号中为各小题所要求填充的内容。
(1)
(2)
(3)
(4)
(5)
(6)
(7)
(8)
(9)
(10)
(11)
(12)
(13)
(14)
(15)
(16)
(四)用化学方法区别下列各组化合物:
(1)环己烷、环己烯与苯
(2)苯与1,3,5-己三烯
解:
(1)
(2)
(五)写出下列各反应的机理:
(1)
解:
(2)
解:
(3)
解:
(4)
(六)己知硝基苯(Ph—NO2)进行亲电取代反应时,其活性比苯小,—NO2就是第二类定位基。
试部亚硝基苯(Ph—NO)进行亲电取代反应时,其活性比苯大还就是小?
—NO就是第几类定位基?
解:
由于氧与氮的电负性均大于碳,在亚硝基苯中存在下列电动去的转移:
所以亚硝基苯(Ph—NO)进行亲电取代反应时,其活性比苯小,—NO就是第二类定位基。
(七)写出下列各化合物一次硝化的主要产物:
解:
蓝色箭头指向为硝基将要进入的位置:
(1)
(2)(3)
(4)(5)(6)
(7)(8)(9)
(10)(11)(12)
(13)(14)
(15)(16)
(17)(18)
讨论:
A.(10)的一元硝化产物为而不就是,因为与前者相关的σ-络合物中正电荷分散程度更大,反应活化能更低:
B.(13)的一元硝化产物为而不就是,就是因为前者的空间障碍小,热力学稳定。
(八)利用什么二取代苯,经亲电取代反应制备纯的下列化合物?
(1)
(2)(3)(4)
解:
可用下列二取代苯分别制备题给的各化合物:
(1)
(2)(3)(4)
(九)将下列各组化合物,按其进行硝化反应的难易次序排列:
(1)苯、间二甲苯、甲苯
(2)乙酰苯胺、苯乙酮、氯苯
解:
(1) 间二甲苯>甲苯>苯
解释:
苯环上甲基越多,对苯环致活作用越强,越易进行硝化反应。
(2)乙酰苯胺>氯苯>苯乙酮
解释:
连有致活基团的苯环较连有致钝集团的苯环易进行硝化反应。
对苯环起致活作用的基团为:
—NH2,—NHCOCH3且致活作用依次减小。
对苯环起致钝作用基团为:
—Cl,—COCH3且致钝作用依次增强。
(十)比较下列各组化合物进行一元溴化反应的相对速率,按由大到小排列。
(1)甲苯、苯甲酸、苯、溴苯、硝基苯
(2)对二甲苯、对苯二甲酸、甲苯、对甲基苯甲酸、间二甲苯
解:
(1)一元溴化相对速率:
甲苯>苯>溴苯>苯甲酸>硝基苯
解释:
致活基团为—CH3;致钝集团为—Br,—COOH,—NO2,且致钝作用依次增强。
(2)间二甲苯>对二甲苯>甲苯>对甲基苯甲酸>对苯二甲酸
解释:
—CH3对苯环有活化作用且连接越多活化作用越强。
两个甲基处于间位的致活效应有协同效应,强于处于对位的致活效应;—COOH有致钝作用。
(十一)在硝化反应中,甲苯、苄基溴、苄基氯与苄基氟除主要的到邻与对位硝基衍生物外,也得到间位硝基衍生物,其含量分别为3%、7%、14%与18%。
试解释之。
解:
这就是-F、-Cl、-Br的吸电子效应与苄基中―CH2―的给电子效应共同作用的结果。
电负性:
F>Cl>Br>H
邻、对位电子云密度:
甲苯>苄基溴>苄基氯>苄基氟
新引入硝基上邻、对位比例:
甲苯>苄基溴>苄基氯>苄基氟
新引入硝基上间位比例:
甲苯<苄基溴<苄基氯<苄基氟
(十二)在硝化反应中,硝基苯、苯基硝基甲烷、2-苯基-1-硝基乙烷所得间位异构体的量分别为93%、67%与13%。
为什么?
解:
硝基就是强的吸电子基(-I、-C),它使苯环上电子云密度大大降低,新引入基上间位。
(十三)甲苯中的甲基就是邻对位定位基,然而三氟甲苯中的三氟甲基就是间位定位基。
试解释之。
解:
由于氟的电负性特别大,导致F3C-就是吸电子基,对苯环只有吸电子效应,而无供电子效应,具有间位定位效应。
(十四)在AlCl3催化下苯与过量氯甲烷作用在0℃时产物为1,2,4-三甲苯,而在100℃时反应,产物却就是1,3,5-三甲苯。
为什么?
解:
前者就是动力学控制反应,生成1,2,4-三甲苯时反应的活化能较低;后者就是热力学控制反应,得到的1,3,5-三甲苯空间障碍小,更加稳定。
(十五)在室温下,甲苯与浓硫酸作用,生成约95%的邻与对甲苯磺酸的混合物。
但在150~200℃较长时间反应,则生成间位(主要产物)与对位的混合物。
试解释之。
(提示:
间甲苯磺酸就是最稳定的异构体。
)
解:
高温条件下反应,有利于热力学稳定的产物(间甲苯磺酸)生成。
(十六)将下列化合物按酸性由大到小排列成序:
(1)
(2)(3)
(4)(5)
解:
(3)>
(1)>(5)>
(2)>(4)
各化合物失去H+后得到的碳负离子稳定性顺序为:
(3)>
(1)>(5)>
(2)>(4)。
碳负离子越稳定,H+越易离去,化合物酸性越强。
(十七)下列反应有无错误?
若有,请予以改正。
(1)
解:
错。
右边苯环由于硝基的引入而致钝,第二个硝基应该进入电子云密度较大的、左边的苯环,且进入亚甲基的对位。
(2)
解:
错
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 有机化学 有机化学第四版第五章 芳烃 第四 第五
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 国企会计岗位笔试试题及答案解析(分享).docx
国企会计岗位笔试试题及答案解析(分享).docx
 行政事业单位内部审计流程图(按照新内部审计准则).xls
行政事业单位内部审计流程图(按照新内部审计准则).xls
![机动车检测人员试题库[含答案].doc](/Images/s.gif)