 必修二实验报告.docx
必修二实验报告.docx
- 文档编号:27351027
- 上传时间:2023-06-29
- 格式:DOCX
- 页数:9
- 大小:17.17KB
必修二实验报告.docx
《必修二实验报告.docx》由会员分享,可在线阅读,更多相关《必修二实验报告.docx(9页珍藏版)》请在冰豆网上搜索。
必修二实验报告
必修二实验报告
实验报告
学年第学期学科年级班
实验类别:
□演示□分组□观察□体验□探究
实验日期:
年月日
实验题目:
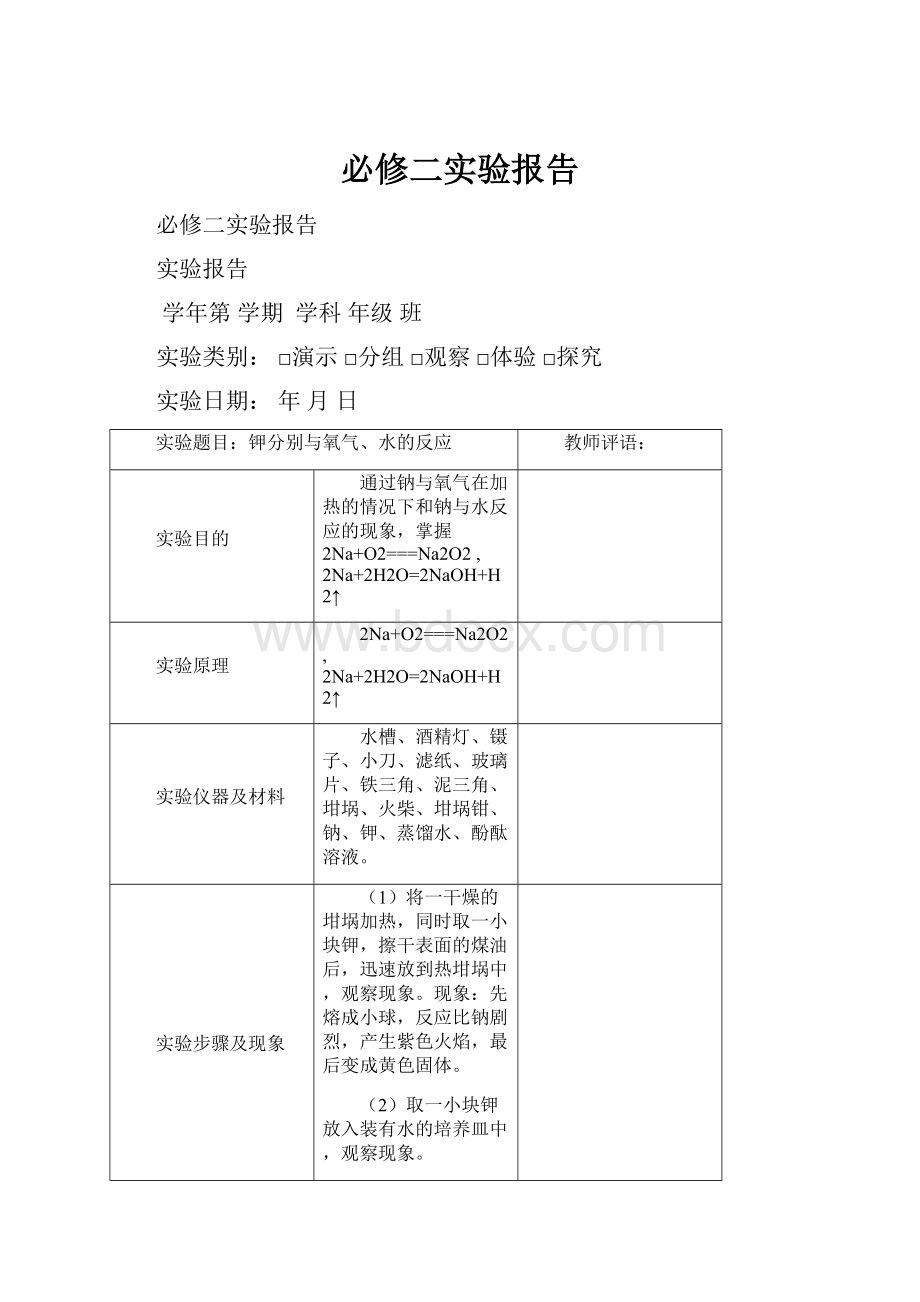
钾分别与氧气、水的反应
教师评语:
实验目的
通过钠与氧气在加热的情况下和钠与水反应的现象,掌握2Na+O2===Na2O2,2Na+2H2O=2NaOH+H2↑
实验原理
2Na+O2===Na2O2,2Na+2H2O=2NaOH+H2↑
实验仪器及材料
水槽、酒精灯、镊子、小刀、滤纸、玻璃片、铁三角、泥三角、坩埚、火柴、坩埚钳、钠、钾、蒸馏水、酚酞溶液。
实验步骤及现象
(1)将一干燥的坩埚加热,同时取一小块钾,擦干表面的煤油后,迅速放到热坩埚中,观察现象。
现象:
先熔成小球,反应比钠剧烈,产生紫色火焰,最后变成黄色固体。
(2)取一小块钾放入装有水的培养皿中,观察现象。
现象:
熔成小球,并产生轻微的爆炸,在水面很快消失。
实验结果
2Na+O2===Na2O2,2Na+2H2O=2NaOH+H2↑
注:
实验类别请在□内“√”
实验报告
学年第学期学科年级班
实验类别:
□演示□分组□观察□体验□探究
实验日期:
年月日
实验题目:
1、镁与水的反应
2、镁、铝与盐酸反应
教师评语:
实验目的
掌握镁与水反应的现象和反应方程式;掌握镁、铝与盐酸反应的现象、反应方程式。
实验原理
Mg+2H2O==Mg(OH)2+H2↑Mg+2HCl==MgCl2+H2↑2Al+6HCl==2AlCl3+H2↑
实验仪器及材料
试管、胶头滴管、砂纸、酒精灯、试管夹、火柴、美带酚酞溶液、铝片、稀盐酸、蒸馏水。
实验步骤及现象
(1)取一小段用砂纸除去表面的氧化膜的镁放入试管中,向试管中加入2ml水,并滴入2滴酚酞溶液。
观察现象。
过一会儿加热试管至水沸腾,观察现象。
现象:
与冷水反应缓慢(产生气泡较少),与沸水反应迅速,溶液变红。
(2)取一小段镁带和一小片铝,用砂纸磨去它们表面的氧化膜,分别放入两支试管,再各加入2ml1mol/L盐酸。
观察发生的现象。
现象:
镁:
产生气泡,反应剧烈;铝:
产生气泡,反应相对于镁慢。
实验结果
Mg+2H2O==Mg(OH)2+H2↑Mg+2HCl==MgCl2+H2↑2Al+6HCl==2AlCl3+H2↑
注:
实验类别请在□内“√”
实验报告
学年第学期学科年级班
实验类别:
□演示□分组□观察□体验□探究
实验日期:
年月日
实验题目:
1、Ba(OH)2•8H2O晶体与NH4Cl晶体反应
2、盐酸与氢氧化钠溶液反应温度的变化
教师评语:
实验目的
1、掌握Ba(OH)2•8H2O晶体与NH4Cl晶体反应
2、掌握酸碱中和反应为放热反应
实验原理
Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑+H2O
HCl+NaOH==NaCl+H2O
实验仪器及材料
小烧杯、玻璃片、胶头滴管、氢氧化钡晶体、氯化铵晶体、蒸馏水、玻璃棒。
量筒、温度计、稀盐酸(2mol/L)、氢氧化钠(2mol/L)。
实验步骤及现象
(1)将约20gBa(OH)2•8H2O晶体研细后与约10gNH4Cl晶体一起放入烧杯中,并将烧杯放在滴有几滴水的玻璃片或小木板上,用玻璃棒快速搅拌,闻气味,用手接触烧杯壁底部,试着用手拿起烧杯,观察现象。
现象:
有刺激性气味气体产生;感觉到烧杯变凉;玻璃片和烧杯粘在一起。
(2)将50ml烧杯加入20ml2mol/L的盐酸,测其温度。
另用量筒取20ml2mol/LNaOH溶液,测其温度,并缓缓倾入烧杯中,边加边用玻璃棒搅拌。
观察反应中溶液温度的变化过程,并记录。
现象:
中和后温度变高。
实验结果
Ba(OH)2·8H2O+2NH4Cl==BaCl2+2NH3↑+H2O
HCl+NaOH==NaCl+H2O
注:
实验类别请在□内“√”
实验报告
学年第学期学科年级班
实验类别:
□演示□分组□观察□体验□探究
实验日期:
年月日
实验题目:
原电池反应原理
教师评语:
实验目的
掌握原电池反应原理和构成条件。
实验原理
氧化还原反应的实质是电子的转移,原电池就是利用电子的转移原理制成的,还利用的电解质溶液把得电子和失电子的反应分开进行,产生原电池的正负极.电流的方向是从正极流向负极,电子的方向从负极流向正极.所以负极是失去电子,正极是得电子
实验仪器及材料
烧杯、电流计、铜片、锌片、导线、稀硫酸。
实验步骤及现象
将锌片和铜片用导线连接(导线中间接入一个电流表),平行插入盛有稀硫酸的烧杯中,观察现象。
现象:
铜片上有气泡冒出;锌片逐渐溶解;电流表的指针发生偏转。
实验结果
化学能转化为电能的一种装置叫做原电池。
注:
实验类别请在□内“√”
实验报告
学年第学期学科年级班
实验类别:
□演示□分组□观察□体验□探究
实验日期:
年月日
实验题目1、温度对化学反应速率的影响
2、催化剂对化学反应速率的影响
教师评语:
实验目的
掌握温度对化学反应速率的影响及催化剂对化学反应速率的影响
实验原理
温度对化学反应速率快慢的影响及催化剂对化学反应速率快慢的影响
实验仪器及材料
试管、胶头滴管、双氧水(5%)、氯化铁(1mol/L)冷水、热水、火柴、木条。
实验步骤及现象
(1)在2支试管中装入2-3ml约5%H2O2溶液,分别滴入1-2滴1mol/LFeCl3溶液。
待试管中均有适量的气泡出现时,将其中一支试管放入盛有5℃的冷水中,另一支放入盛有40℃的热水中,观察现象,待放入热水的试管出现大量气泡时,用代火星的木柴检验气体。
现象:
热水中产生气泡快,带火星木柴复燃;冷水中产生气泡少。
(2)在3支试管中各加入2-3ml5%H2O2溶液,在向其中2支试管中加入少量的MnO2粉末、1-2滴1mol/LFeCl3溶液。
观察现象。
现象:
均能使气泡冒出的速率增大
实验结果
温度对化学反应速率有影响
催化剂对化学反应速率有影响
注:
实验类别请在□内“√”
实验报告
学年第学期学科年级班
实验类别:
□演示□分组□观察□体验□探究
实验日期:
年月日
实验题目:
1、乙醇与金属钠的反应
2、乙醇的氧化反应
教师评语:
实验目的
1、掌握乙醇与金属钠的反应
2、乙醇的氧化反应
实验原理
2Na+2C2H5OH→2C2H5ONa+H2↑2CH3CH2OH+O2→2CH3CHO+2H2O
实验仪器及材料
试管、带尖嘴导管的单孔胶塞、试管夹、小烧杯、澄清石灰水、镊子、小刀、滤纸、玻璃片、、酒精灯、螺旋状铜丝、钠、乙醇、坩埚钳。
实验步骤及现象
(1)在盛有少量的无水乙醇试管中,加入一小块新切的、用滤纸擦干表面煤油的钠,在试管口迅速塞上配有医用注射针头的单口塞,用小试管倒扣在针头之上,收集并验纯气体,然后点燃,并把一干燥的小烧杯罩在火焰上,片刻在烧杯壁上出现液滴后,迅速倒转烧杯,向烧杯中加入少量澄清石灰水,观察想象。
现象:
钠块开始沉于试管底部,未熔化,慢慢有气泡产生,钠快浮上来最后消失,点燃产生淡蓝色火焰。
(2)向一支试管中加入3-5ml乙醇,取一根10-15cm长的铜丝,下端绕成螺旋状,在酒精灯上灼烧至红热,插入乙醇,反复几次。
观察现象,小心闻试管中液体产生的气味。
现象:
铜丝:
红色变黑色又变红色,有刺激性气味产生。
实验结果
2Na+2C2H5OH→2C2H5ONa+H2↑2CH3CH2OH+O2→2CH3CHO+2H2O
注:
实验类别请在□内“√”
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 必修 实验 报告
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《C12343098汽轮机操作规程》要点.docx
《C12343098汽轮机操作规程》要点.docx
