 高中化学重庆高二竞赛测试模拟试题6含答案考点及解析.docx
高中化学重庆高二竞赛测试模拟试题6含答案考点及解析.docx
- 文档编号:27270025
- 上传时间:2023-06-28
- 格式:DOCX
- 页数:23
- 大小:192.86KB
高中化学重庆高二竞赛测试模拟试题6含答案考点及解析.docx
《高中化学重庆高二竞赛测试模拟试题6含答案考点及解析.docx》由会员分享,可在线阅读,更多相关《高中化学重庆高二竞赛测试模拟试题6含答案考点及解析.docx(23页珍藏版)》请在冰豆网上搜索。
高中化学重庆高二竞赛测试模拟试题6含答案考点及解析
2018-2019年高中化学重庆高二竞赛测试模拟试题【6】含答案考点及解析
班级:
___________姓名:
___________分数:
___________
题号
一
二
三
四
五
六
总分
得分
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
评卷人
得 分
一、选择题
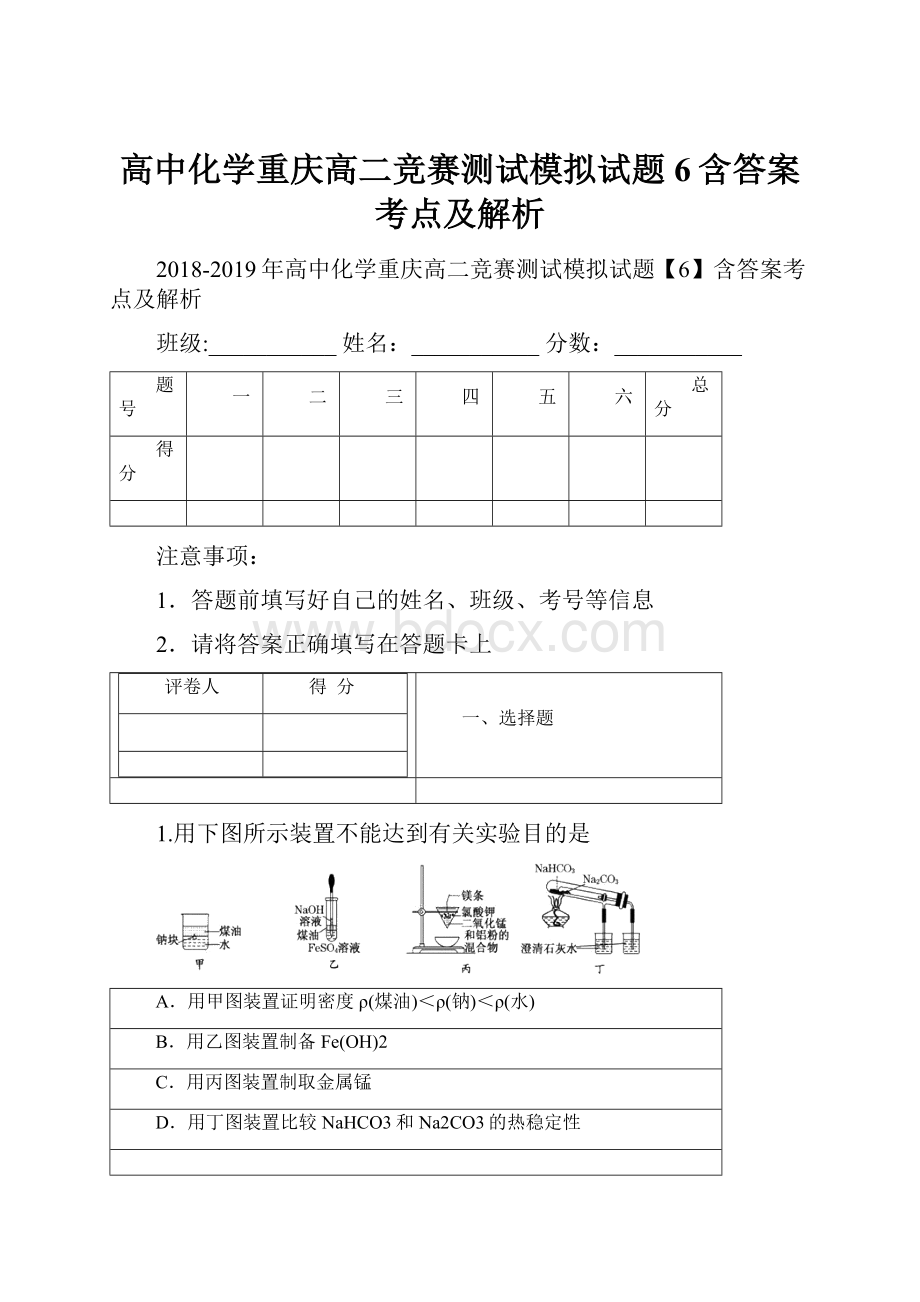
1.用下图所示装置不能达到有关实验目的是
A.用甲图装置证明密度ρ(煤油)<ρ(钠)<ρ(水)
B.用乙图装置制备Fe(OH)2
C.用丙图装置制取金属锰
D.用丁图装置比较NaHCO3和Na2CO3的热稳定性
【答案】D
【解析】
试题分析:
A、金属钠在水和煤油界面上下移动,证明密度ρ(煤油)<ρ(钠)<ρ(水),正确;B、氢氧化亚铁容易被氧气氧化,所以制备时应避免与空气接触,煤油覆盖在溶液表面和滴管插入液面以下均是防止氧气进入,正确;C、铝热反应可以制备熔点高的金属如锰等,正确;D、套管实验,加热时大试管温度高小试管温度低,温度高先分解不能比较NaHCO3和Na2CO3的热稳定性,应把NaHCO3和Na2CO3药品互换放置,错误。
考点:
考查钠元素单质及其化合物的性质、实验方案的分析评价。
2.下列物质属于强电解质且该状态下能导电的是( )
(1)氯化钠溶液;
(2)氯化铵固体;(3)铜;(4)石墨;(5)熔融NaOH;(6)稀硫酸;(7)乙酸;
A.
(1)
(2)(5)(6)
B.(5)
C.
(2)(5)
D.
(1)(3)(4)(5)(6)
【答案】B
【解析】
试题分析:
(1)氯化钠溶液能够导电,但是是混合物,错误;
(2)氯化铵固体是电解质,但是不能导电,错误;(3)铜是金属单质,不是电解质,能够导电;错误;(4)石墨是非金属单质,不是电解质,能够导电;错误;(5)熔融NaOH是电解质,能够导电,正确;(6)稀硫酸是混合物,不是电解质,能够导电,错误;(7)乙酸是电解质,不能导电,错误。
考点:
考查物质的分类的知识。
3.用相同浓度的标准盐酸滴定相同体积、相同pH的
、NaOH和NH3·H2O三种碱溶液,当恰好中和时,滴定消耗盐酸的体积依序为V1、V2、V3,则V1、V2、V3三者的大小关系正确的是
A.V3>V2>V1
B.V3=V2=V1
C.V1=V2>V3
D.V3>V2=V1
【答案】D
【解析】
试题分析:
由于Ba(OH)2、NaOH是强碱,完全电离,而NH3·H2O是弱碱,部分电离,因此当溶液的pH相同时,c(OH-)相同,随着盐酸的滴加,未电离的NH3·H2O会继续电离,最终溶液电离产生的n(OH-):
Ba(OH)2=NaOH 故选项是D。 考点: 考查等pH的强碱、弱碱的中和能力大小比较的知识。 4.下图表示蛋白质分子的一部分,图中A、B、C、D标出分子中不同的键,当蛋白质发生水解反应时,断裂的键是( )。 【答案】C 【解析】蛋白质发生水解反应时,断裂的键是肽键,可简记为从哪个位置形成,易从哪个位置断开。 5.下列溶液中各微粒的浓度关系不正确的是 A.0.1mol/LHCOOH溶液中: c(HCOO-)+c(OH-)=c(H+) B.1L0.1mol/LCuSO4·(NH4)2SO4·6H2O的溶液中c(SO42->c(NH4+)>c(Cu2+)>c(H+)>c(OH-) C.0.1mol/LNaHCO3溶液中: c(Na+)+c(H+)+c(H2CO3)>c(HCO3-)+c(CO32-)+c(OH-) D.等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液中: c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) 【答案】D 【解析】 试题分析: A、因HCOOH溶液不显电性,共有HCOO-、OH-、H+三种离子,则电荷守恒式为c(HCOO-)+c(OH-)=c(H+),故A正确;B、CuSO4•(NH4)2SO4•6H2O的物质的量为0.1mol,则n(SO42-)=n(NH4+)>n(Cu2+),但在溶液中因铵根离子和铜离子的水解使溶液显酸性,则c(H+)>c(OH-),因铵根离子水解则c(SO42-)>c(NH4+))>c(Cu2+),水解的程度很弱,则c(SO42-)>c(NH4+))>c(Cu2+)>c(H+)>c(OH-),故B正确;C、因NaHCO3溶液不显电性,电荷守恒式为c(Na+)+c(H+)=c(HCO3-)+2c(CO32-)+c(OH-)①,物料守恒式为c(Na+)=c(H2CO3)+c(HCO3-)+c(CO32-)②,则①-②可得c(H+)=c(CO32-)+c(OH-)-c(H2CO3)③,该溶液中因碳酸氢根离子水解显碱性,则c(OH-)>c(H+),即c(Na+)+c(H+)+c(H2CO3)=c(HCO3-)+2c(CO32-)+c(OH-)+c(H+)-c(CO32-)-c(OH-)=c(HCO3-)+c(CO32-)+c(H+)>c(HCO3-)+c(CO32-)+c(OH-),故C正确;D、等体积、等物质的量浓度,则NaX和弱酸HX的物质的量相等,HX的电离大于NaX的水解,则c(X-)>c(Na+),故D错误;故选D. 考点: 溶液各微粒的浓度关系 6.在水溶液中,因发生水解反应而不能大量共存的一组离子是 A.CO32-、OH-、Na+、H+ B.Al3+、Na+、AlO2-、Cl- C.Ba2+、HCO3-、K+、SO42- D.S2-、H+、SO42-、Cu2+ 【答案】B 【解析】 试题分析: 离子间如果发生化学反应,则不能大量共存,反之是可以的。 A、CO32-、OH-与H+均发生复分解反应而不能大量共存,A不符合题意;B、Al3+与AlO2-水解相互促进生成氢氧化铝白色沉淀而不能大量共存,B正确;C、Ba2+与SO42-发生复分解反应而不能大量共存,C不符合题意;D、S2-与H+、Cu2+均发生复分解反应而不能大量共存,D不符合题意,答案选B。 考点: 考查离子共存的正误判断 7.室温下,下列各组离子在指定溶液中一定能大量共存的是 A.pH=1的溶液中: Fe3+、NO3-、Cl-、Na+ B.由水电离的c(H+)=10-12mol·L-1的溶液中: Cl-、CO32-、K+、SO32- C.c(OH-)/c(H+)=1012的溶液中: SO32-、NH4+、NO3-、K+ D.能使甲基橙呈红色的溶液中: Na+、AlO2-、NO3-、HCO3- 【答案】A 【解析】 试题分析: pH=1的溶液为强酸性溶液,Fe3+、NO3-、Cl-、Na+这四种离子都可以大量共存,故A正确,为本题的答案;由水电离的c(H+)=10-12mol·L-1的溶液可以是强酸性溶液,也可以是强碱性溶液,若溶液为强酸性溶液,则CO32-、SO32-都不可以大量共存,故B不正确;c(OH-)/c(H+)=1012的溶液为强碱性溶液,NH4+不能再强碱性溶液中大量共存,故C错误;能使甲基橙呈红色的溶液中为酸性溶液,AlO2-、HCO3-不能在酸性溶液中大量共存,故D不正确。 考点: 离子共存 点评: 本题考查了离子共存的问题,离子共存问题是高考考查的重点和难点,该题综合性好,有一定的难度,注意的是由水电离的c(H+)=10-12mol·L-1的溶液可以是酸性溶液,也可以是碱性溶液。 8.在NH4+离子中存在4个N-H共价键,则下列说法正确的是( ) A.四个共价键的键长完全相同 B.四个共价键的键长完全不同 C.原来的三个N-H的键长完全相同,但与由配位键形成的N-H键不同。 D.四个N-H键键长相同,但键能不同 【答案】A 【解析】 试题分析: 在NH4+离子中存在4个N-H共价键的键长是完全相同的,答案选A。 考点: 考查NH4+离子中化学键的判断 点评: 该题是基础性试题的考查,难度不大。 记住NH4+离子的结构特点,并能灵活运用即可。 9.甲型H1N1流感对人们生活产生了很大影响,一旦发现流感病人,隔离、消毒极为重要,常用消毒剂有过氧乙酸、漂白粉、甲醛等。 关于甲醛,下列说法错误的是( ) A.常温下甲醛为气体,故可作为熏蒸消毒剂 B.甲醛可使蛋白质变性,故可杀灭病毒 C.甲醛与漂白粉混用,效果更好 D.甲醛氧化可得甲酸,甲酸氧化的产物为CO2和H2O 【答案】C 【解析】 试题分析: 漂白粉具有强氧化性,能氧化甲醛,所以甲醛与漂白粉混用,效果差,选项C不正确,其余选项都是正确的,答案选C。 考点: 考查甲醛的结构和性质 点评: 该题是常识性试题的考查,主要是考查学生对甲醛结构、性质的熟悉了解程度,意在调动学生的学习兴趣,激发学生的学习积极性。 该题难度不大,记住即可。 10.要鉴别己烯中是否混有少量甲苯,正确的实验方法是 ( ) A.先加足量的酸性高锰酸钾溶液,然后再加入溴水 B.先加足量溴水,然后再加入酸性高锰酸钾溶液 C.点燃这种液体,然后再观察火焰的颜色 D.加入浓硫酸与浓硝酸后加热 【答案】B 【解析】 试题分析: 加入浓溴水,乙烯与溴发生加成反应而使溴水褪色,苯酚可发生取代反应生成白色三溴苯酚沉淀,加入酸性高锰酸钾可与甲苯反应而褪色,可鉴别。 故选B。 考点: 有机物的鉴别 点评: 本题考查有机物的鉴别,题目难度不大,本题注意把握有机物的官能团的性质,为解答该类题目的关键。 评卷人 得 分 二、实验题 11.(3分)下列实验操作不正确的是 (填字母代号)。 A.在催化剂存在的条件下,苯和溴水发生反应可生成无色、比水重的液体溴苯。 B.将铜丝弯成螺旋状,在酒精灯上加热变黑后,立即伸入盛有无水乙醇的试管中,完成乙醇氧化为乙醛的实验。 C.醇中含有少量水可加入生石灰再蒸馏制得无水乙醇。 D.验证蔗糖的水解产物时,将蔗糖和稀H2SO4溶液混合,水浴加热使其充分水解,然后用稀的NaOH溶液使其呈碱性后,再滴加银氨溶液。 F.验证溴乙烷水解产物时,将溴乙烷和氢氧化钠溶液混合,充分振荡溶液、静置、待液体分层后,滴加硝酸银溶液。 G.实验室蒸馏石油时温度计水银球插入石油中测量温度,收集60℃~150℃馏分得到汽油。 【答案】AFG 【解析】A不正确,应该是液溴。 溴乙烷水解在碱性条件下进行,而溴离子检验需要在酸性条件下进行,所以F不正确。 蒸馏时温度计的水银球应该放在蒸馏烧瓶的支管出口处,G不正确,其余都是正确的,答案选AFG。 评卷人 得 分 三、填空题 12.化合物A最早发现于酸牛奶中,它是内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。 A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。 在浓硫酸存在下,A可发生如下图所示的反应。 试写出: (1)化合物A含有的官能团的名称: ___________________________ (2)化合物的结构简式: B_________ D_________ (3)化学方程式: A E__________ A F____________ (4)反应类型: A E__________,A F___________ 【答案】 【解析】 试题分析: (1)A既能和醇,也能和羧酸发生酯化反应,这说明A分子中含有羟基和羧基。 又因为A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应,所以根据有机物A的化学式可知,该有机物的结构简式应该是CH3CHOHCOOH。 (2)A能和乙醇或乙酸发生酯化反应,所以生成物B和D的结构简式分别是CH3CHOHCOOC2H5、CH3COOCH(CH3)COOH。 (3)E能使溴水褪色,说明E分子中含有碳碳双键,这说明A生成E的反应式醇的消去反应,反应的化学方程式是 。 A分子中含有羟基和羧基,所以根据F的化学式可知,该反应2分子A的酯化反应,反应的化学方程式是 。 考点: 考查有机物结构简式、官能团、有机反应类型的判断以及方程式的书写 点评: 该题是高考中的常见题型,属于中等难度的试题。 试题贴近高考,综合性强,在注重对基础知识巩固与训练的同时,侧重对学生能力的培养与解题方法的指导与训练。 该类试题能较全面地考查学生的有机化学基础知识和逻辑思维能力、创造思维能力,提高学生的应试能力。 该题的关键是记住常见官能团的结构、性质以及相互之间的转化,然后灵活运用即可。 13.已知: ①无水氯化钙可与乙醇形成难溶于水的CaCl2·6C2H5OH. ②有关有机物的沸点见下表: 试剂 乙醚 乙醇 乙酸 乙酸乙酯 沸点(℃) 34.5 78.3 118 77.1 某课外活动小组设计的实验室制取较多量乙酸乙酯的装置如图所示,A中放有乙醇、无水醋酸和浓硫酸,B中放有饱和碳酸钠溶液.试回答: (1)A中浓硫酸的作用是________;若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式: ______________________. (2)B中球形管的两个作用是________、________.若反应前向B中溶液滴加几滴酚酞,呈红色,产生此现象的原因是__________________________(用离子方程式表示);反应结束后B中的现象是______________________________. 【答案】 (1)催化剂、吸水剂 (2)冷凝蒸气 防止倒吸 溶液分层,上层无色油状液体,下层溶液颜色变浅 【解析】 试题分析: (1)酯化反应是可逆反应,所以在酯化反应中,浓硫酸起催化剂和吸水剂的作用。 酯化反应中羧酸提供羟基,醇提供氢原子,所以反应的化学方程式是 。 (2)由于乙酸和乙醇都是易挥发的,所以生成的乙酸乙酯中混有乙酸和乙醇。 又因为二者和水都是互溶的,所以B中球形管的两个作用是冷凝蒸气 防止倒吸;碳酸钠是强碱弱酸盐,水解呈碱性,因此反应前向B中溶液滴加几滴酚酞,呈红色。 乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,有香味,在上层。 乙酸和碳酸钠反应而使溶液红色变浅,即下层溶液颜色变浅。 考点: 考查乙酸乙酯制备实验的有关判断 点评: 该题是中等难度的试题,试题基础性强,难易适中,侧重对学生基础知识的巩固与训练,有利于培养学生的创新思维能力,以及规范、严谨的实验设计与操作能力。 该题主要是从乙酸乙酯制取实验的原理、操作、装置、现象上进行分析,以实验基本操作为中心,通过是什么、为什么和怎样做重点考查实验基本操作的规范性和准确性及灵活运用知识解决实际问题的能力。 14.我国是个农业大国,农业是立国之本,“农村、农业、农民”是党中央新时期农村工作的重心,化肥与农药的发展起着巨大的推动作用,请回答下列问题: (1)农作物生长过程中不可缺少的微量元素有Fe、Mn、B、Cu、Mo等,它们或是酶的组成成分,或能提高酶的活性,是农作物体内营养物质的形成和新陈代谢不可缺少的。 常用铜肥是胆矾,在盐碱地(土壤pH>7)施用胆矾时宜将溶液________(填“喷在叶片上”或“随水灌入土壤中”),主要理由是_______________________________________________________ ________________________________________________________________________。 (2)农药波尔多液是一种常用的杀菌剂,常用配方为胆矾、生石灰、水,按质量比1∶0.56∶100混合,分析其防治病虫害的原因________________________________________。 (3)拟除虫菊酯是一种高效、低毒,对昆虫有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊酯的结构简式如图: 其分子式为________________________,则下列对该化合物的叙述正确的是________(填字母代号)。 A.该化合物属于芳香烃 B.该化合物属于卤代烃 C.该化合物在碱性条件下失去药效 D.该化合物在一定条件下可发生加成反应 【答案】 (1)喷在叶片上 Cu2+在碱性条件下生成不溶物,农作物根部不易吸收 (2)Cu2+在碱性条件下使菌体蛋白质变性 (3)C23H21NO3Br2 CD 【解析】 试题分析: (1)胆矾的水溶液显酸性,在碱性土壤中,由于Cu2+与碱性物质结合生成不易被农作物吸收的不溶物,所以宜在农作物叶面喷施。 (2)Cu2+为重金属离子,其药效体现在能使细菌的蛋白质变性,而达到杀菌效果。 当胆矾、生石灰、H2O的质量比为1∶0.56∶100时,其中n(Cu2+)∶n(Ca2+)= ∶ =2∶5,当波尔多液的有效成分为CuSO4·xCu(OH)2·yCa(OH)2时,且x=1,由于CuSO4与Ca(OH)2反应生成Cu(OH)2,可结合: CuSO4+Ca(OH)2===Cu(OH)2↓+CaSO4 反应前 2 5 0 0 反应后 1 1 所以CuSO4·Cu(OH)2·yCa(OH)2中y=5-1=4。 (3)拟除虫菊酯是一种酯类化合物,所以该化合物不属于烃类,该化合物具有酯的性质,在碱性条件下水解而失效,该化合物中含 ,苯环及—C≡N能发生加成反应,其分子式为C23H21NO3Br2。 考点: 考查胆矾在农业生产中的应用、波尔多液配制、性能和有机物分子式判断、性质 点评: 该题是中等难度的试题,试题综合性强,难易适中,注重考查学生灵活运用基础知识解决实际问题的能力。 关于有机物的结构和性质解题的关键是准确判断出分子中含有的官能团,然后在根据相应官能团的结构和性质,灵活分析、判断即可。 该题有利于培养学生严谨的逻辑思维能力和发散思维能力。 15.(8分)已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如下图所示(反应条件和部分产物已省略)。 请回答: (1)若A为金属单质,B、C为非金属单质,且常温下B、C均为无色气体,D为黑色固体,则B的化学式为______,A和E在一定条件下反应生成D的化学方程式为 ___________ __。 (2)若A为非金属单质,且常温下为黄绿色气体,B为金属单质,C为不含氧元素的酸,且C的组成中含有与A相同的元素。 则C的化学式为___________,A和E在一定条件下反应生成D的离子方程式 _____ __。 【答案】(8分) (1)O2(2分) 3Fe+4H2O Fe3O4+4H2↑(2分) (2)C: HCl(2分) 2Fe2++Cl2=2Fe3++2Cl(2分) 【解析】 (1)常见的气体非金属单质有H2、O2、N2,而常见的金属A及其化合物D呈黑色,可猜测到铁的氧化物Fe3O4,进一步可确定: A为铁,B为氧气,C为氢气 (2)A为黄绿色的气体单质,即氯气;C为含有氯元素的非含氧酸,即盐酸; 金属B与盐酸生成E可与氯气反应生成D,可知B为具有变价的活泼金属铁; 16.(10分)呋喃是一种有氯仿气味的液体,用于有机合成,结构简式为, 它的蒸气或者具有 结构的有机物的蒸气遇到用盐酸浸湿的松木片时发生显绿色的反应,叫做松片反应. (1)请写出与 互为同分异构体的具有松片反应的有机物的结构简式(2种)_______________________,________________________ (2)呋喃甲醛又叫做糠醛,可由玉米芯经化学处理而得,结构简式为 ,它用于塑料、清漆、医药和香烟香料.糠醛在一定条件下与足量的氢气反应得到的有机物的结构简式为______________;糠醛与银氨溶液反应的化学方程式为______________。 (3)糠醛与苯酚在一定条件下发生缩聚反应,生成糠醛树脂,其结构简式为________. 【答案】(10分) (1) (2) (3) 【解析】 (1)解此题的第一步需知道 的分子式, 的分子式为C7H8O,所以,符合条件的同分异构体的结构简式有: (2) (3)此题的意图为考查苯酚与甲醛反应: 糠醛与苯酚反应方程式为: 评卷人 得 分 四、计算题 17.某抗酸药每片含碳酸钙500mg,氢氧化镁174mg,每片该药可中和多少克溶质质量分数为7.3%盐酸? 【答案】8g 【解析】试题分析: 每片含碳酸钙500mg,氢氧化镁174mg 则碳酸钙的物质的量是0.5g÷100g/mol=0.005mol 氢氧化镁的物质的量是0.174g÷58g/mol=0.003mol 所以根据方程式可知 CaCO3+2HCl=CaCl2+CO2↑+H2O 1mol 2mol 0.005mol0.01mol Mg(OH)2+2HCl=MgCl2+2H2O 1mol 2mol 0.003mol 0.006mol 所以消耗氯化氢的物质的量是0.016mol 氯化氢的质量是0.016mol×36.5g/mol=0.584g 则盐酸的质量是0.584g÷7.3%=8g 考点: 考查根据方程式进行的有关计算 点评: 该题是基础性试题的考查,难度不大。 试题贴近生活实际,有利于调动学生的学习兴趣,有助于培养学生规范的答题能力。 明确反应的原理是答题的根据 18.有两种气态链烃的混合气体,已知它们都能使溴水褪色且分子中碳原子数均小于5;1体积该混合气体完全燃烧后,可得到3.6体积CO2和3体积水蒸气,气体体积均是在相同温度和压强下测定的。 通过计算和推理,确立这两种烃的分子式以及它们在混合气体中的体积比。 【答案】混合烃是由C4H6和C3H6组成,体积比为3∶2 【解析】解: 这两种均能使溴水褪色,它们都是不饱和烃。 若这两种烃都是烯烃,则燃烧后生成等体积的CO2和H2O(气),可见不合题意,舍去;若这两种烃都是炔烃或二烯烃,或一种为炔烃,一种为二烯烃,则1体积混合气体燃烧后,生成的CO2比H2O(气)应多1体积,也不符合题意,舍去,故混合气体应由一种烯烃与一种炔烃(或二烯烃)组成。 设1体积混合气体中含炔烃(或二烯烃)CnH2n-2为x体积,含烯烃CmH2m为(1–x)体积,根据元素守恒可得: nx+(1-x)m=3.6……① x(n-1)+m(1-x)=3……② 解①和②得x=0.6,故混和气体中CnH2n-2与CmH2m的体积比为: 0.6: (1-0.6)=3∶2. 将x=0.6代人①或②得6n+4m=36 讨论: ①当n=2时,m=6(不合题意,舍去); ②n=3时,m=4.5(不合题意,舍去) ③n=4时,m=3(合理) ∴混合烃是由C4H6和C3H6组成,体积比为3∶2. 19.某有机物A与氢气的相对密度是30,取有机物A6.0g完全燃烧后,生成0.2molCO2和0.2molH2O。 此有机物既可与金属钠反应,又可与氢氧化钠和碳酸钠反应。 (1)计算该有机物的分子式。 (2)根据该有机物的性质,写出其结构简式。 【答案】 (1)C2H4O2 (2)CH3COOH 【解析】 20.㈠已知: 2H2(g)+O
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 重庆 竞赛 测试 模拟 试题 答案 考点 解析
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《崔万志演讲观后感》.docx
《崔万志演讲观后感》.docx
