 自动电位滴定测定氯化锂.docx
自动电位滴定测定氯化锂.docx
- 文档编号:26829676
- 上传时间:2023-06-23
- 格式:DOCX
- 页数:12
- 大小:20.34KB
自动电位滴定测定氯化锂.docx
《自动电位滴定测定氯化锂.docx》由会员分享,可在线阅读,更多相关《自动电位滴定测定氯化锂.docx(12页珍藏版)》请在冰豆网上搜索。
自动电位滴定测定氯化锂
合化理化建议表
江西赣锋锂业股份有限公司合理化建议表
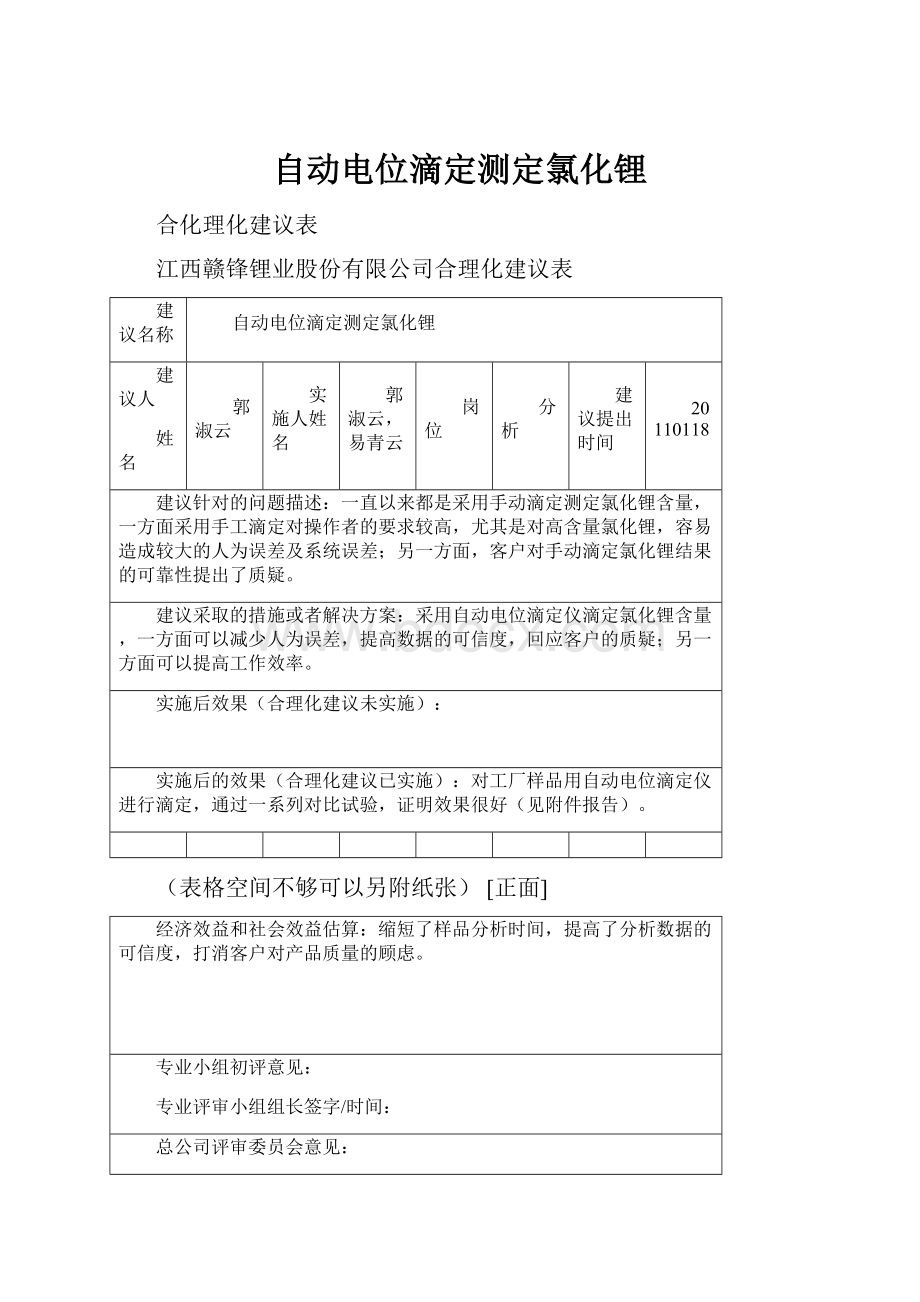
建议名称
自动电位滴定测定氯化锂
建议人
姓名
郭淑云
实施人姓名
郭淑云,易青云
岗位
分析
建议提出时间
20110118
建议针对的问题描述:
一直以来都是采用手动滴定测定氯化锂含量,一方面采用手工滴定对操作者的要求较高,尤其是对高含量氯化锂,容易造成较大的人为误差及系统误差;另一方面,客户对手动滴定氯化锂结果的可靠性提出了质疑。
建议采取的措施或者解决方案:
采用自动电位滴定仪滴定氯化锂含量,一方面可以减少人为误差,提高数据的可信度,回应客户的质疑;另一方面可以提高工作效率。
实施后效果(合理化建议未实施):
实施后的效果(合理化建议已实施):
对工厂样品用自动电位滴定仪进行滴定,通过一系列对比试验,证明效果很好(见附件报告)。
(表格空间不够可以另附纸张)[正面]
经济效益和社会效益估算:
缩短了样品分析时间,提高了分析数据的可信度,打消客户对产品质量的顾虑。
专业小组初评意见:
专业评审小组组长签字/时间:
总公司评审委员会意见:
办公室主任签字/时间:
终审意见:
评审委员会主任签字/时间:
附件:
自动电位滴定测定氯化锂研究
1.实验方法参数设置:
1.1套用盐酸滴定度测定方法参数设置:
1.1.1在此设置下,称取样品加入100ml烧杯中,再加入80ml水,我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.1121
5.4
16.2641
0.118(*1)
-89.4
2
0.1107
6.9
16.5176
0.11468
-86.1
3
0.1040
(*2)
(*2)
0.11543
(*2)
4
0.1039
9.3
15.6408
0.11367
-93.5
5
0.1019
6.4
13.4322
0.12981
-71.6
6
0.1059
5.7
14.4689
0.12524
-77.4
注:
*1:
开始设定结果保留小数点后3位,后来改为5位;
*2:
结果除了滴定度其余项没有记录下来。
滴定现象及结论:
银电极表面附着一层白色的氯化银沉淀,怀疑影响电极灵敏度,实验结果来看平行性差,从后面几个实验终点电位来看,怀疑未达到滴定终点;滴定曲线无突跃。
1.1.2在此设置下,改变样品测定条件,称取样品加入100ml烧杯中,加入80ml水,再加入20滴1+1硝酸,我们进行了3组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.1020
5.2
14.0358
0.12435
166.5
2
0.1213
6.3
18.2598
0.11367
164.5
6
0.1288
超过最大进样量20ml,无结果
滴定现象及结论:
滴定过程出现大量絮状沉淀,电极表层无氯化银沉淀层附着,滴定终点电位变为正值;滴定曲线无突跃。
1.2改变滴定参数为《电位滴定理论与实践》106页中条件:
在此设置下,称取样品加入100ml烧杯中,加入80ml水,再加入20滴1+1硝酸,我们进行了3组实验,实验数据如下表所示:
编号
样品质量(g)
ER.rec设置
EP设置
1
0.1121
均滴定不到1ml自动停止滴定
all
1
5
0.1019
greatest
1
3
0.1059
greatest
9
实验现象及结论:
实验中我们不断改变ER.rec和EP设置,但是滴定都是在没有到达终点的时候就自动停止了,说明我们设置的终点确定条件仍然有问题,考虑改变EPC值。
1.3改变滴定参数为EP.C30,min.waitingtime2s,转速7,ER.recgreatest,EP9:
1.3.1在此设置下,称取样品加入100ml烧杯中,加入80ml水,再加入20滴1+1硝酸,我们进行了3组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.0817
76.0
13.8064
0.10126
38.8
2
0.0812
73.5
13.7411
0.10112
23.1
3
0.0809
73.6
13.5585
0.10210
40.6
实验现象及结论:
实验结果平行性较好,滴定曲线无突跃。
1.3.2在此设置下,我们将最小进样量改为10μl,称取样品加入100ml烧杯中,加入80ml水,再加入20滴1+1硝酸,我们进行了3组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.0933
71.8
15.6781
0.10183
38.4
2
0.0937
73.2
15.7700
0.10167
44.4
3
0.0938
69.6
15.8530
0.10125
4.6(?
)
4
0.0937
验证3号终点电位,没有异常
实验现象及结论:
实验结果平行性还可以,滴定曲线出现突跃,可以认为实验参数设置基本可以确定下来,剩下的就是实验条件的进一步优化。
2.硝酸银滴定度测定:
1.1按照上面确定的参数,滴定硝酸银滴定度:
1.1.1称取一定量于550℃烧1h的氯化钠样品加入100ml烧杯中,加入80ml水,再加入20滴1+1硝酸,我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.0988
74.6
16.5604
0.10209
25.2
2
0.0998
74.9
16.7213
0.10213
26.9
3
0.1023
74.2
17.2788
0.10131
32.0
4
0.1040
73.8
17.5421
0.10145
31.0
5
0.0956
68.1
16.3025
0.10032
-10.0
6
0.0994
73.1
17.1017
0.09946
20.9
实验现象及结论:
测定结果越来越小,偏差越来越大,开始怀疑是银环上附着的氯化银沉淀所致,因此在做最后一个实验前擦拭干净银环测定,结果还是减小的,因此排除此怀疑。
后来怀疑是滴定头上的小孔被阻塞导致试剂不畅通所致,待验证。
1.2拆下滴定头的小塞子进行实验:
1.2.1称取一定量样品加入100ml烧杯中,加入80ml水,再加入20滴1+1硝酸,我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.0934
75.5
15.5195
0.10298
-2.9
2
0.0921
77.8
15.2457
0.10337
22.7
3
0.0946
79.9
15.7578
0.10273
40.0
4
0.0904
78.9
14.8916
0.10388
29.9
5
0.0922
78.0
15.3677
0.10266
36.8
6
0.0978
77.9
16.2119
0.10323
31.4
实验现象及结论:
测定结果平行性还是不好,我们取下滴定管的小塞子不能根本解决此问题,考虑其他办法。
我们首先考虑减少沉淀的量,将硝酸银浓度降低。
1.3硝酸银浓度稀释五倍改为约0.02mol/L:
1.3.1称取一定量样品加入100ml烧杯中,加入80ml水,再加入20滴1+1硝酸,我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.0254
样品量太大,未滴定到终点
2
0.0284
3
0.0192
56.5
15.7873
0.02081
-2.1
4
0.0125
56.3
10.5959
0.02019
2.3
5
0.0145
57.2
11.9787
0.02071
-0.4
6
0.0126
57.1
10.1983
0.02114
0.1
实验现象及结论:
没有装上滴定管的小塞子,对溶液体积有影响,平行性不是很好,所以以后将滴定管塞子装上,由于硝酸银稀释了,应该不会再阻塞滴定头;同时考虑到称取的样品量太小,采用称大样分取的方法减小误差。
1.4滴定头塞子装上,硝酸银浓度约0.02mol/L:
1.4.1称取0.3013g氯化钠样品定容于250ml容量瓶中,分取10.0ml样品,加入80ml水,再加入20滴1+1硝酸,我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.012052
57.7
9.9006
0.02083
41.5
2
0.012052
57.7
9.9275
0.02077
39.1
3
0.012052
58.0
9.9220
0.02079
40.1
4
0.012052
58.4
9.9107
0.02081
41.0
5
0.012052
57.2
9.9451
0.02074
34.7
6
0.012052
57.9
9.9280
0.02077
39.5
实验现象及结论:
统计6组实验数据均值为0.02079mol/L,标准偏差为0.15%,结果满足要求,说明方法已经基本可行。
1.5滴定头塞子装上,硝酸银浓度约0.02mol/L:
1.5.1称取0.3032g于550℃烧1h的氯化钠样品定容于250ml容量瓶中,分取10.0ml样品,加入80ml水,再加入20滴1+1硝酸,我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.012128
58.6
9.9165
0.02093
41.0
2
0.012128
61.0
10.0156
0.02072
29.1
3
0.012128
59.1
10.0138
0.02072
38.1
4
0.012128
59.5
9.9835
0.02079
38.9
5
0.012128
58.6
9.9823
0.02079
33.5
6
0.012128
59.4
9.9837
0.02079
38.9
实验现象及结论:
统计后5组实验数据均值为0.02076mol/L,标准偏差为0.18%,结果满足要求。
1.6硝酸银滴定氯化锂样品:
1.6.1同样测定条件下,用该硝酸银标准溶液滴定氯化锂样品(手动滴定结果为97.08%),我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
百分含量(%)
终点电位(mv)
1
0.00838448
60.4
9.2703
97.30
37.8
2
63.3
9.2549
97.14
35.6
3
61.8
9.2536
97.12
42.4
4
60.6
9.2992
97.60
38.8
5
62.3
9.2636
97.23
36.7
6
59.4
9.2997
97.61
32.3
担心滴定头被阻塞影响实验结果,清洗滴定头后继续滴定3组样品,实验数据如下:
编号
样品质量(g)
ERC
EP1(ml)
百分含量(%)
终点电位(mv)
1
0.00838448
61.2
9.2608
97.20
39.7
2
0.00838448
58.0
9.3028
97.64
38.7
3
0.00838448
59.5
9.2675
97.27
49.7
实验现象及结论:
统计后5组实验数据均值为0.02076mol/L,标准偏差为0.18%,结果满足要求。
1.6.2同样测定条件下,用该硝酸银标准溶液滴定氯化锂样品(手动滴定结果为97.23%),我们进行了6组实验,实验数据如下表所示:
编号
样品质量(g)
ERC
EP1(ml)
百分含量(%)
终点电位(mv)
1
0.00797824
60.0
8.8713
97.85
41.9
2
57.7
8.8697
97.83
46.4
3
58.7
8.8858
98.01
44.7
4
54.7
8.8696
97.83
50.0
5
55.9
8.8766
97.91
51.7
6
55.5
8.8806
97.95
44.3
担心滴定头被阻塞影响实验结果,清洗滴定头后滴定3组样品,实验数据如下:
编号
样品质量(g)
ERC
EP1(ml)
百分含量(%)
终点电位(mv)
1
0.00838448
61.2
9.2608
97.20
39.7
2
0.00838448
58.0
9.3028
97.64
38.7
3
0.00838448
59.5
9.2675
97.27
49.7
实验现象及结论:
用自动电位滴定仪测定的结果与手动操作结果有一定偏差,考虑因为硝酸银标准溶液经过一次稀释造成误差,以及自动电位滴定样品是经过手动滴定样品二次稀释的样品,也造成了一部分误差,所以考虑减小这些误差。
考虑将硝酸银换回约0.1mol/L,同时将烧杯由100ml换为250ml。
1.7硝酸银浓度约0.1mol/L:
1.7.1称取1.5150g氯化钠样品定容于250ml容量瓶中,分取10.0ml样品于250ml烧杯,加入200ml水,再加入20滴1+1硝酸,进行了6组实验,实验数据如下:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.0606
67.5
10.2238
0.10143
32.4
2
64.5
10.2087
0.10158
48.0
3
65.2
10.2120
0.10154
40.9
4
64.6
10.2114
0.10155
34.4
5
65.8
10.2458
0.10121
40.9
6
65.5
10.1974
0.10169
40.6
实验现象及结论:
实验数据平行性还可以,考虑标定硝酸银标准溶液。
1.7.2称取2.5088g于550℃烘1h的氯化钠样品定容于250ml容量瓶中,分取10.0ml样品于250ml烧杯,加入200ml水,再加入20滴1+1硝酸,进行了4组实验,实验数据如下:
编号
样品质量(g)
ERC
EP1(ml)
Titer(mol/L)
终点电位(mv)
1
0.100352
67.1
16.9036
0.10159
5.2
2
0.100352
68.0
16.9139
0.10152
10.2
3
0.100352
67.0
16.8996
0.10161
11.5
0.100352
69.0
16.9013
0.10160
17.8
实验现象及结论:
实验数据平行性还可以,不过与手动滴定标定结果(0.10221mol/L)偏差较大,我们在实验时排除了人为误差,最终确定该误差是手动滴定的滴定管造成的系统误差,因此可以解释两者的差异。
3.自动电位滴定结果与手动滴定结果验证:
为了验证自动电位滴定结果的可靠性,我们将最有经验的操作者的手动滴定结果与电位滴定结果(2个平行样)相对照,如下表所示:
编号
手动滴定
电位滴定
电位滴定2次平行测定
1
98.05%
97.91%
97.96%
97.86%
2
96.89%
96.83%
96.78%
96.83%
3
31.73%
31.70%
31.77%
31.68%
4
31.77%
31.74%
31.78%
31.70%
5
99.44%
99.40%
99.48%
99.33%
结论:
由上面表中对比数据我们可以看出手动滴定结果与电位滴定结果偏差很小,在允许的偏差范围之内,虽然用熟练的操作者来减小了手动滴定的人为误差,但是由于存在滴定管的系统误差和指示剂指示判断终点误差,理论上手动滴定结果会比电位滴定结果偏高一点,上面的试验结果也是如此,2次电位滴定的平行性也很好,可以采用自动电位滴定测定氯化锂含量。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 自动 电位 滴定 测定 氯化锂
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《C12343098汽轮机操作规程》要点.docx
《C12343098汽轮机操作规程》要点.docx
