 《氯及其化合物》上课课件.ppt
《氯及其化合物》上课课件.ppt
- 文档编号:2668173
- 上传时间:2022-11-06
- 格式:PPT
- 页数:48
- 大小:2.04MB
《氯及其化合物》上课课件.ppt
《《氯及其化合物》上课课件.ppt》由会员分享,可在线阅读,更多相关《《氯及其化合物》上课课件.ppt(48页珍藏版)》请在冰豆网上搜索。
【考纲通鉴考纲通鉴】1.1.掌握氯气的性质,了解氯气的用途。
掌握氯气的性质,了解氯气的用途。
2.2.掌握氯气的实验室制法(原理、装置、收集、掌握氯气的实验室制法(原理、装置、收集、检验及尾气处理)检验及尾气处理)3.3.次氯酸的性质(强氧化性、不稳定性、弱酸性)次氯酸的性质(强氧化性、不稳定性、弱酸性)44制取漂白粉的原理及漂白粉的性质、变质等。
制取漂白粉的原理及漂白粉的性质、变质等。
1.1.(11)如)如图所示,将所示,将氯气依次通气依次通过盛有干燥有色布条的广口瓶盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可和盛有潮湿有色布条的广口瓶,可观察到的察到的现象象是是__。
(22)为防止防止氯气尾气气尾气污染空气,根据染空气,根据氯水水显酸性的性酸性的性质,可可用用氢氧氧化化钠溶溶液液吸吸收收多多余余的的氯气气,原原理理是是(用用化化学学方方程程式式表表示示)_。
根根据据这一一原原理理,工工业上上常常用用廉廉价价的的石石灰灰乳乳吸吸收收工工业氯气气尾尾气气制制得得漂漂白白粉粉,漂漂白白粉粉的的有有效效成成分分是是_(填填化化学学式式),长期期露露置置于于空空气气中中的的漂漂白白粉粉,加加稀稀盐酸酸后后产生生的的气体是气体是_(用字母代号填)。
(用字母代号填)。
AAOO22BBClCl22CCCOCO22DDHClOHClO(33)据据“北北方方网网”报道道,20042004年年44月月1515日日至至1616日日,位位于于重重庆市市江江北北区区的的天天原原化化工工总厂厂相相继发生生氯气气泄泄漏漏和和爆爆炸炸事事故故。
截截至至记者者发稿稿时,已已有有99人人在在事事故故中中失失踪踪死死亡亡,33人人受受伤,1515万万人人被被紧急急疏疏散散。
当当人人们逃逃离离爆爆炸炸现场时,可可以以用用浸浸有有一一定定浓度度的的某某种种物物质的的水水溶溶液液的的毛毛巾巾捂捂住住鼻鼻子子,最最适适宜宜采采用用的的该物物质是是。
AANaOHBNaOHBNaClCNaClCKBrDKBrDNaNa22COCO33第一课时第一课时氯气的物理性质氯气的物理性质和制法和制法学习目标学习目标1.掌握氯元素在周期表的位置及原掌握氯元素在周期表的位置及原子结构子结构2.掌握氯气的分子结构与物理性质掌握氯气的分子结构与物理性质3.掌握氯气的工业制法和实验室制掌握氯气的工业制法和实验室制法法(一一)、氯在周期表中的位置和分子结构:
、氯在周期表中的位置和分子结构:
氯在周期表中位于氯在周期表中位于族,原子结构示意图族,原子结构示意图为为。
其最外层有。
其最外层有个个电子,在化学反应中表现出较强的电子,在化学反应中表现出较强的性。
性。
其单质的电子式为其单质的电子式为,结构式,结构式为为。
第第AA7氧化氧化氯气氯气(Cl2)
(二)氯气的物理性质
(二)氯气的物理性质l通常情况下,氯气呈通常情况下,氯气呈色有色有气气味的有毒气体(注意闻有毒气体的操作);味的有毒气体(注意闻有毒气体的操作);溶于水,氯水呈溶于水,氯水呈色(常温常压下,色(常温常压下,11体积水可溶解体积水可溶解体积氯气);易体积氯气);易(常压下(常压下-34.6-34.6变为液体);密度比空气变为液体);密度比空气密度密度。
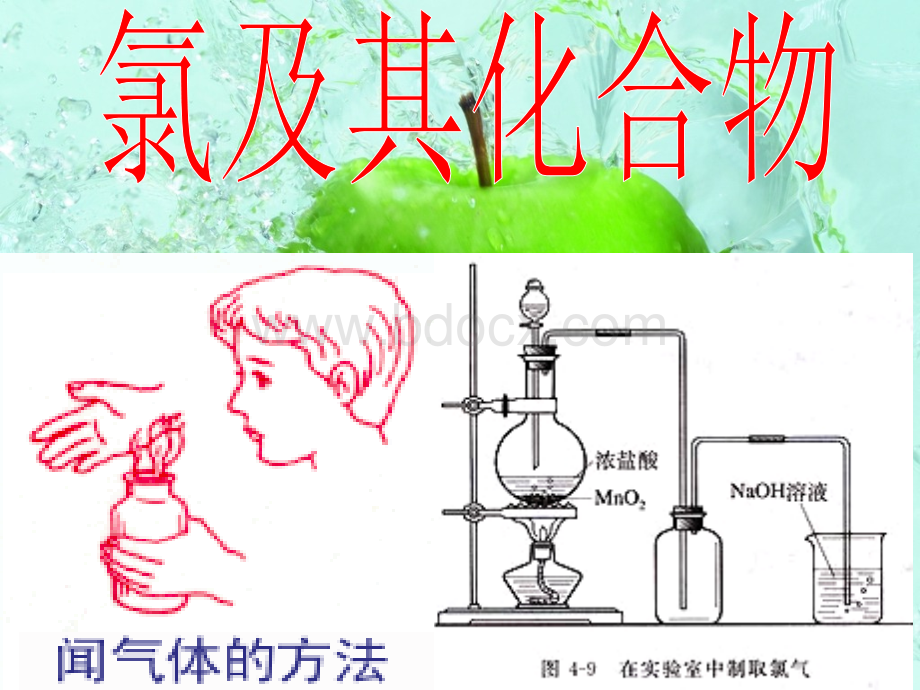
黄绿刺激性能浅黄绿液化大闻气味的方法是:
左手持瓶伸直,右手在瓶口轻轻扇动,仅让少量的氯气分子飘入鼻孔。
(三)(三).氯气的制备氯气的制备:
1.工业制备:
(氯碱工业)工业制备:
(氯碱工业)2NaCl+2H2O2NaOH+Cl2+H2电解电解+-精制精制饱和食盐水饱和食盐水水水(含少量含少量NaOH)Cl2H2NaOH溶液溶液淡盐水淡盐水Na+装置装置l阳极:
阳极:
金属钛网金属钛网(涂有涂有钛钌等氧化物钛钌等氧化物)l阴极:
阴极:
碳钢网碳钢网(涂有镍涂有镍涂层涂层)l阳离子交换膜:
阳离子交换膜:
只允只允许阳离子通过,阻止许阳离子通过,阻止阴离子和气体通过。
阴离子和气体通过。
l阴极室产物:
阴极室产物:
NaOH、H2l阳极室产物:
阳极室产物:
Cl2离子交换膜法离子交换膜法制烧碱制烧碱含氯含氯漂白剂漂白剂有机合成、造纸有机合成、造纸玻璃、肥皂玻璃、肥皂纺织、印染纺织、印染有机合成有机合成氯化物合成氯化物合成农药农药金属冶炼金属冶炼有机合成有机合成HCl盐酸盐酸电解饱和食盐水电解饱和食盐水以氯碱工业为基础的化工生产以氯碱工业为基础的化工生产H2NaOH湿氯气湿氯气湿氢气湿氢气液碱液碱Cl22.实验室制备实验室制备:
MnO2作氧化剂,作氧化剂,可用可用KMnO4、KClO3、K2Cr2O7、Ca(ClO)2等替代等替代.
(1)原理原理:
nO2+4HCl(浓浓)=MnCl2+Cl2+2H2O浓盐酸作用浓盐酸作用:
还原性、酸性还原性、酸性.
(2)
(2)实验装置实验装置:
(33)收集方法:
)收集方法:
;(44)验满:
)验满:
;(55)洗气:
除)洗气:
除:
通过盛有:
通过盛有的的洗气瓶;除洗气瓶;除:
通过盛有:
通过盛有的洗的洗气瓶;气瓶;(66)检验:
检验:
;(77)尾气吸收:
用)尾气吸收:
用溶液吸收多余的溶液吸收多余的氯气。
氯气。
向上排空气法;排饱和食盐水的方法向上排空气法;排饱和食盐水的方法集气瓶充满黄绿色说明已集满集气瓶充满黄绿色说明已集满HClHCl饱和食盐水饱和食盐水水蒸汽水蒸汽浓硫酸浓硫酸能使湿润的淀粉能使湿润的淀粉KIKI试纸变蓝试纸变蓝NaOHNaOH实验装置改进实验装置改进除除氯氯化化氢氢气气体体干干燥燥,除除水水蒸蒸气气收收集集气气体体除除尾尾气气,防防污污染染1.1.足量足量MnOMnO22和含和含4mol4molHClHCl的浓盐酸加热制得的浓盐酸加热制得ClCl22物质的量物质的量1mol1mol(填小于或等于或大于)(填小于或等于或大于)2.2.该反应该反应要缓缓加热,温度不超过要缓缓加热,温度不超过90,要用,要用分液漏斗不能用长颈漏斗。
分液漏斗不能用长颈漏斗。
盐酸是挥发性酸,温度再高盐酸是挥发性酸,温度再高ClCl22中中HClHCl含量高含量高3.3.若实验室没有浓盐酸,可用什么代替?
写出若实验室没有浓盐酸,可用什么代替?
写出化学方程式化学方程式NaClNaCl固体和浓固体和浓HH22SOSO442NaCl+MnO2NaCl+MnO22+3H+3H22SOSO44=22NaHSONaHSO44+MnSO+MnSO44+Cl+Cl22+2H+2H22OO亦可用亦可用NaClNaCl和和NaHSONaHSO44固体代替固体代替(小于小于)注意:
注意:
气体净化装置(除杂,干燥装置)气体净化装置(除杂,干燥装置)A中只能装中只能装液体液体干燥剂,并且干燥剂,并且长进短出长进短出ACBB中只能装中只能装固体固体干燥剂,并且干燥剂,并且大进小出大进小出C中只能装中只能装固体固体干燥剂,进出无限制干燥剂,进出无限制尾气处理装置尾气处理装置ABB:
可用于处理极易溶于水的气体,如:
可用于处理极易溶于水的气体,如HCl、NH3等等A:
可用于处理在水中溶解度不大的气体,如:
可用于处理在水中溶解度不大的气体,如Cl2、CO2等等迁移体验11、浓盐酸不具有的性质是(、浓盐酸不具有的性质是()AA、不稳定性、不稳定性BB、强酸性、强酸性CC、氧化性、氧化性DD、还原性、还原性22、实实验验室室用用二二氧氧化化锰锰与与浓浓盐盐酸酸反反应应制制取取ClCl22,下下列叙述正确的是(列叙述正确的是()AA、二氧化锰只表现出还原性、二氧化锰只表现出还原性BB、盐酸只表现出还原性、盐酸只表现出还原性CC、盐酸只表现出酸性、盐酸只表现出酸性DD、盐酸表现出酸性和还原性、盐酸表现出酸性和还原性AADD第二课时第二课时氯气化学性质氯气化学性质学习目标:
重点掌握氯气的学习目标:
重点掌握氯气的化学性质化学性质氯气的化学性质氯气的化学性质l氯气的化学性质非常活泼,是一种活泼的非金属单质,具有较强的氧化性。
2NaCl22NaCl(产生白烟)(产生白烟)CuCl2CuCl22Fe3Cl22FeCl3(产生棕色的烟,溶于水溶液呈黄色)产生棕色的烟,溶于水溶液呈黄色)(产生棕黄色的烟,溶于水溶液呈蓝绿色)产生棕黄色的烟,溶于水溶液呈蓝绿色)(与变价金属反应,均使金属氧化至高价态)(与变价金属反应,均使金属氧化至高价态)注:
注:
常温下干燥的氯气或液氯不能与铁发生反应,常温下干燥的氯气或液氯不能与铁发生反应,所以工业上常把所以工业上常把干燥的液氯储存在钢瓶中干燥的液氯储存在钢瓶中。
1跟金属反应跟金属反应(三三)氯气的化学性质氯气的化学性质思考:
思考:
氯气、硫与变价金属铁和铜反应的区别:
氯气、硫与变价金属铁和铜反应的区别:
(用化学反应式表示)或举例说明氯气的氧(用化学反应式表示)或举例说明氯气的氧化性比硫强化性比硫强小结:
小结:
氯气的氧化性很强,将金属氧化为高价氯气的氧化性很强,将金属氧化为高价2P+3Cl22PCl3(小液滴小液滴)2P+5Cl22PCl5(固体小颗粒固体小颗粒)点燃点燃点燃点燃
(2)
(2)与磷反应:
与磷反应:
烟:
固体小颗粒烟:
固体小颗粒雾:
小液滴雾:
小液滴白色烟雾白色烟雾2.2.与非金属的反应与非金属的反应
(1)
(1)与氢气的反应与氢气的反应H2+Cl2=2HCl点燃或光照点燃或光照点燃发出苍白色火焰,点燃发出苍白色火焰,瓶口有白雾。
瓶口有白雾。
光照会发生爆炸。
光照会发生爆炸。
3.与水的反应与水的反应Cl2+H2OHClHClO新制氯水新制氯水呈呈浅黄绿色浅黄绿色,成分是:
,成分是:
分子:
分子:
Cl2、H2O、HClO离子:
离子:
H、Cl、ClO、OH久置氯水久置氯水:
无色溶液,实际是稀盐酸无色溶液,实际是稀盐酸离子:
离子:
H、Cl、少量、少量OH.2HClO=2HCl+O2HClO=2HCl+O22光光在常温下,在常温下,11体积水约溶解体积水约溶解22体体积的氯气。
氯气的水溶液叫积的氯气。
氯气的水溶液叫“氯水氯水”。
次氯酸:
次氯酸:
是一种强氧化剂,能杀死水里的病菌,是一种强氧化剂,能杀死水里的病菌,所以,自来水常用氯气所以,自来水常用氯气(在在1L水中通入约水中通入约0.002gCl2)来杀菌消毒;还能使某些染料和有来杀菌消毒;还能使某些染料和有机色素褪色,可用作棉、麻、纸张的漂白剂。
机色素褪色,可用作棉、麻、纸张的漂白剂。
Cl2Cl22NaOHNaClNaClOH2O2Cl22Ca(OH)2CaCl2+Ca(ClO)22H2O由于上述反应生成由于上述反应生成2HClO2HCl+O2,故漂白粉露置在空气中,久置无效。
故漂白粉露置在空气中,久置无效。
Ca(ClO)2CO2H2OCaCO32HClOCa(ClO)22HCl(稀稀)CaCl22HClO4、跟碱反应跟碱反应工业上用工业上用和和制得漂白粉。
制得漂白粉。
漂白粉的漂白原理是:
漂白粉的漂白原理是:
常用于常用于。
除去多余的氯气除去多余的氯气氯气氯气石灰乳石灰乳44、与碱反应:
、与碱反应:
2NaOH+Cl2NaOH+Cl22=NaClNaCl+NaClONaClO+H+H22OO2Ca(OH)2Ca(OH)22+2Cl+2Cl22=CaCl=CaCl22+Ca(ClO)+Ca(ClO)22+2H+2H22OO漂白粉主要成分漂白粉主要成分:
CaClCaCl22+Ca(ClO)+Ca(ClO)22,有效成分是有效成分是:
Ca(ClO)Ca(ClO)22杀菌原理杀菌原理:
Ca(ClO)Ca(ClO)22+H+H22O+COO+CO22=CaCO=CaCO33+2HClO2HClO(HClOHClO强氧化剂强氧化剂)5.5.与其他还原性物质反应:
与其他还原性物质反应:
2Fe2Fe2+2+Cl+Cl22=2Fe=2Fe3+3+2Cl+2Cl-SOSO22+Cl+Cl22+2H+2H22O=HO
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 氯及其化合物 及其 化合物 上课 课件
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 12处方点评管理规范实施细则_精品文档.doc
12处方点评管理规范实施细则_精品文档.doc
 17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
17种抗癌药纳入国家基本医疗保险工伤保险和生育保险药品目录_精品文档.xls
