 专题11 原电池装置原理及其应用.docx
专题11 原电池装置原理及其应用.docx
- 文档编号:26677281
- 上传时间:2023-06-21
- 格式:DOCX
- 页数:13
- 大小:326.22KB
专题11 原电池装置原理及其应用.docx
《专题11 原电池装置原理及其应用.docx》由会员分享,可在线阅读,更多相关《专题11 原电池装置原理及其应用.docx(13页珍藏版)》请在冰豆网上搜索。
专题11原电池装置原理及其应用
专题原电池装置、原理及其应用
【高频考点解读】
1.了解原电池的工作原理,能写出电极反应和电池反应方程式。
2.了解常见化学电源的种类及其工作原理。
【热点题型】
题型一原电池原理
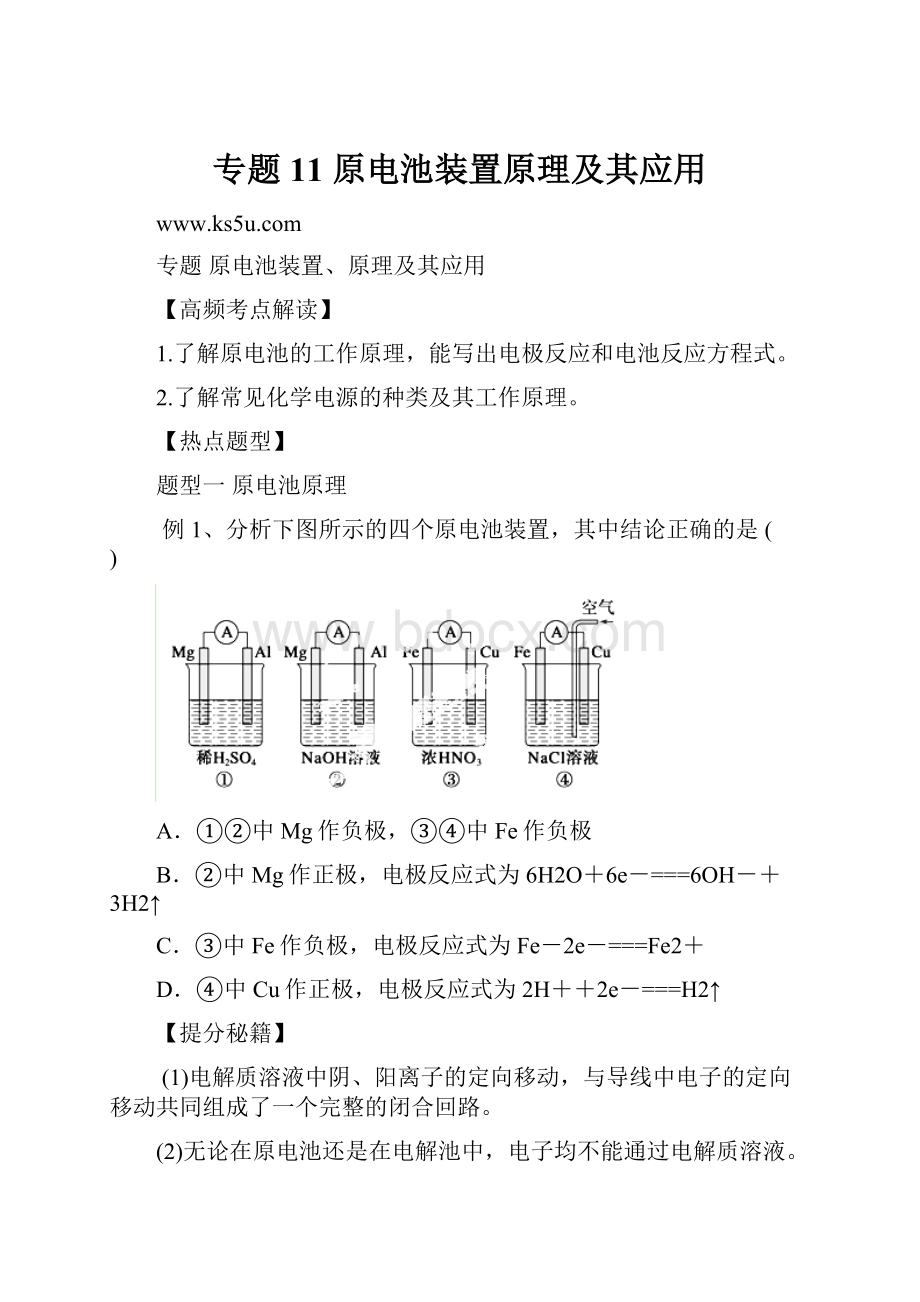
例1、分析下图所示的四个原电池装置,其中结论正确的是( )
A.①②中Mg作负极,③④中Fe作负极
B.②中Mg作正极,电极反应式为6H2O+6e-===6OH-+3H2↑
C.③中Fe作负极,电极反应式为Fe-2e-===Fe2+
D.④中Cu作正极,电极反应式为2H++2e-===H2↑
【提分秘籍】
(1)电解质溶液中阴、阳离子的定向移动,与导线中电子的定向移动共同组成了一个完整的闭合回路。
(2)无论在原电池还是在电解池中,电子均不能通过电解质溶液。
(3)原电池的负极失去电子的总数等于正极得到电子的总数。
(4)原电池电极的“正”极与“负”极与电极材料的性质有关,也与电解质溶液有关。
【举一反三】
一种基于酸性燃料电池原理设计的酒精检测仪,负极上的反应为CH3CH2OH-4e-+H2O===CH3COOH+4H+。
下列有关说法正确的是( )
A.检测时,电解质溶液中的H+向负极移动
B.若有0.4mol电子转移,则在标准状况下消耗4.48L氧气
C.电池反应的化学方程式为CH3CH2OH+O2===CH3COOH+H2O
D.正极上发生的反应为O2+4e-+2H2O===4OH-
【热点题型】
题型二化学电源
例2、铅蓄电池是典型的可充电电池,它的正负极极板是惰性材料,
请回答下列问题(不考虑氢、氧的氧化还原):
(1)电解液中H2SO4的浓度将变______________________;
当外电路通过1mol电子时,理论上负极板的质量增加__________g。
(2)在完全放电耗尽PbO2和Pb时,若按上图连接,电解一段时间后,则在A电极上生成________,B电极上生成____________,此时铅蓄电池的正负极的极性将________。
【热点题型】
题型三电极反应式的书写
例3、 有人设计以Pt和Zn为电极材料,埋入人体内作为某种心脏病人的心脏起搏器的能源。
它依靠跟人体内体液中含有的一定浓度的溶解氧、H+和Zn2+进行工作,试写出该电池的两极反应式。
【热点题型】
题型四原电池原理的应用
例4、燃料在电池中直接被氧化而产生电能的装置叫燃料电池,它是一种高效低污染的新型电池。
燃料电池所用燃料可以是氢气,也可以是其他燃料,如甲醇、肼等。
肼分子(H2N—NH2)可以在氧气中燃烧生成氮气和水,利用肼、氧气与KOH溶液组成碱性燃料电池,请写出该电池反应的电极反应式和总反应式:
______________________;
并指出电解质溶液中OH-向哪极移动:
________________________________。
【提分秘籍】
5.探究金属腐蚀的快慢规律
(1)不同类型的腐蚀规律
电解原理引起的腐蚀>原电池原理引起的腐蚀>化学腐蚀>有防护措施的腐蚀
(2)电化学腐蚀规律
①对同一种金属来说,腐蚀的快慢:
强电解质溶液>弱电解质溶液>非电解质溶液。
②活动性不同的两金属:
活动性差别越大,活动金属腐蚀越快。
③对同一种电解质溶液来说,电解质溶液浓度越大,腐蚀越快,且氧化剂的浓度越高,腐蚀越快。
④对于不同氧化剂来说,氧化性越强,金属腐蚀越快。
【举一反三】
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。
①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少。
据此判断这四种金属活动性由大到小的顺序是( )
A.①③②④B.①③④②C.③④②①D.③①②④
【随堂巩固】
1.为探究原电池的形成条件和反应原理,某同学设计了如下实验,并记录了实验现象:
①向一定浓度的稀硫酸中插入锌片,看到有气泡生成;
②向上述浓度的稀硫酸中插入铜片,没有气泡生成;
③将锌片与铜片上端接触并捏住,一起插入上述浓度的稀硫酸中,看到铜片上有气泡生成,且生成气泡的速率比实验①中快;
④在锌片和铜片中间接上电流计,再将锌片和铜片插入上述浓度的稀硫酸中,发现电流计指针偏转。
下列关于以上实验设计及现象的分析,不正确的是( )。
A.实验①、②说明锌能与稀硫酸反应而铜不能
B.实验③说明发生原电池反应时会加快化学反应速率
C.实验③说明在该条件下铜可以与稀硫酸反应生成氢气
D.实验③、④说明该原电池中铜为正极、锌为负极
3.如图,在盛有稀H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )。
A.外电路的电流方向为:
X→外电路→YB.若两电极分别为铁和碳棒,则X为碳棒,Y为铁
C.X极上发生的是还原反应,Y极上发生的是氧化反应
D.若两电极都是金属,则它们的活动性顺序为X>Y
4.右图所示是一种酸性燃料电池酒精检测仪,具有自动吹气流量侦测与控制的功能,非常适合进行现场酒精检测。
下列说法不正确的是( )。
A.该电池的负极反应式为:
CH3CH2OH+3H2O-12e-===2CO2↑+12H+
B.该电池的正极反应式为:
O2+4e-+4H+===2H2O
C.电流由O2所在的铂电极经外电路流向另一电极
D.微处理器通过检测电流大小而计算出被测气体中酒精的含量
5.镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运等特点。
研究的燃料电池可分为镁—空气燃料电池,镁—海水燃料电池,镁—过氧化氢燃料电池,镁—次氯酸盐燃料电池。
如图为镁—次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )。
A.放电过程中OH-移向正极B.电池的总反应式为Mg+ClO-+H2O===Mg(OH)2↓+Cl-
C.镁电池中镁均为负极,发生氧化反应
D.镁—过氧化氢燃料电池,酸性电解质中正极反应为:
H2O2+2H++2e-===2H2O
6.如图所示,杠杆AB两端分别挂有体积相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中滴入浓CuSO4溶液,一段时间后,下列有关杠杆的偏向判断正确的是( )。
A.杠杆为导体或绝缘体时,均为A端高B端低B.杠杆为导体或绝缘体时,均为A端低B端高
C.当杠杆为导体时,A端低B端高;杠杆为绝缘体时,A端高B端低
D.当杠杆为导体时,A端高B端低;杠杆为绝缘体时,A端低B端高
7.据报道,以硼氢化合物NaBH4(B元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图所示。
下列说法错误的是( )。
A.电池放电时Na+从b极区移向a极区B.电极b采用MnO2,MnO2既作电极材料又有催化作用
C.该电池的负极反应为:
BH4-+8OH--8e-===BO2-+6H2O
D.每消耗3molH2O2,转移的电子为3mol
8.
(1)高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。
高铁电池的总反应为:
3Zn+2K2FeO4+8H2O
3Zn(OH)2+2Fe(OH)3+4KOH。
请回答下列问题:
①高铁电池的负极材料是________。
②放电时,正极发生________(填“氧化”或“还原”)
反应:
已知负极反应为Zn-2e-+2OH-===Zn(OH)2,则正极反应为________________________________________________________________。
③放电时,________(填“正”或“负”)极附近溶液的碱性增强。
(2)某种燃料电池的工作原理示意如图所示,a、b均为惰性电极。
①使用时,空气从________口通入(填“A”或“B”);
②假设使用的“燃料”是甲醇,a极的电极反应式为_______________________________________;
③假设使用的“燃料”是水煤气(成分为CO、H2),如用这种电池电镀铜,待镀金属的质量增加6.4g,则至少消耗标准状况下水煤气的体积为________。
9.
(1)分析如图所示的四个装置,回答下列问题:
①装置a和b中铝电极上的电极反应式分别为________________、________________。
②装置c中产生气泡的电极为________电极(填“铁”或“铜”),装置d中铜电极上的电极反应式为_______________________________________________________________________________________。
(2)观察如图所示的两个装置,图1装置中铜电极上产生大量的无色气泡,图2装置中铜电极上无气体产生,而铬电极上产生大量的有色气体。
根据上述现象试推测金属铬具有的两种重要化学性质为________________、__________________。
(3)如图是甲烷燃料电池原理示意图,回答下列问题:
①电池的负极是________(填“a”或“b”)电极,该极的电极反应式为:
________________________________________________________________。
②电池工作一段时间后电解质溶液的pH________(填“增大”“减小”或“不变”)。
【热点题型】
题型一原电池原理
【举一反三】
【热点题型】
题型二化学电源
题型三电极反应式的书写
【热点题型】
题型四原电池原理的应用
总反应式:
N2H4+O2===N2+2H2O OH-向负极移动
【举一反三】
【随堂巩固】1.
2.
3.
4.
5.
6.
7.
8.
9.
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题11 原电池装置原理及其应用 专题 11 原电池 装置 原理 及其 应用
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《爱和自由》读书心得15篇.docx
《爱和自由》读书心得15篇.docx
