 高考化学《铁及其化合物的综合》专项训练及答案.docx
高考化学《铁及其化合物的综合》专项训练及答案.docx
- 文档编号:25567793
- 上传时间:2023-06-09
- 格式:DOCX
- 页数:21
- 大小:192.46KB
高考化学《铁及其化合物的综合》专项训练及答案.docx
《高考化学《铁及其化合物的综合》专项训练及答案.docx》由会员分享,可在线阅读,更多相关《高考化学《铁及其化合物的综合》专项训练及答案.docx(21页珍藏版)》请在冰豆网上搜索。
高考化学《铁及其化合物的综合》专项训练及答案
2020-2021高考化学《铁及其化合物的综合》专项训练及答案
一、高中化学铁及其化合物练习题(含详细答案解析)
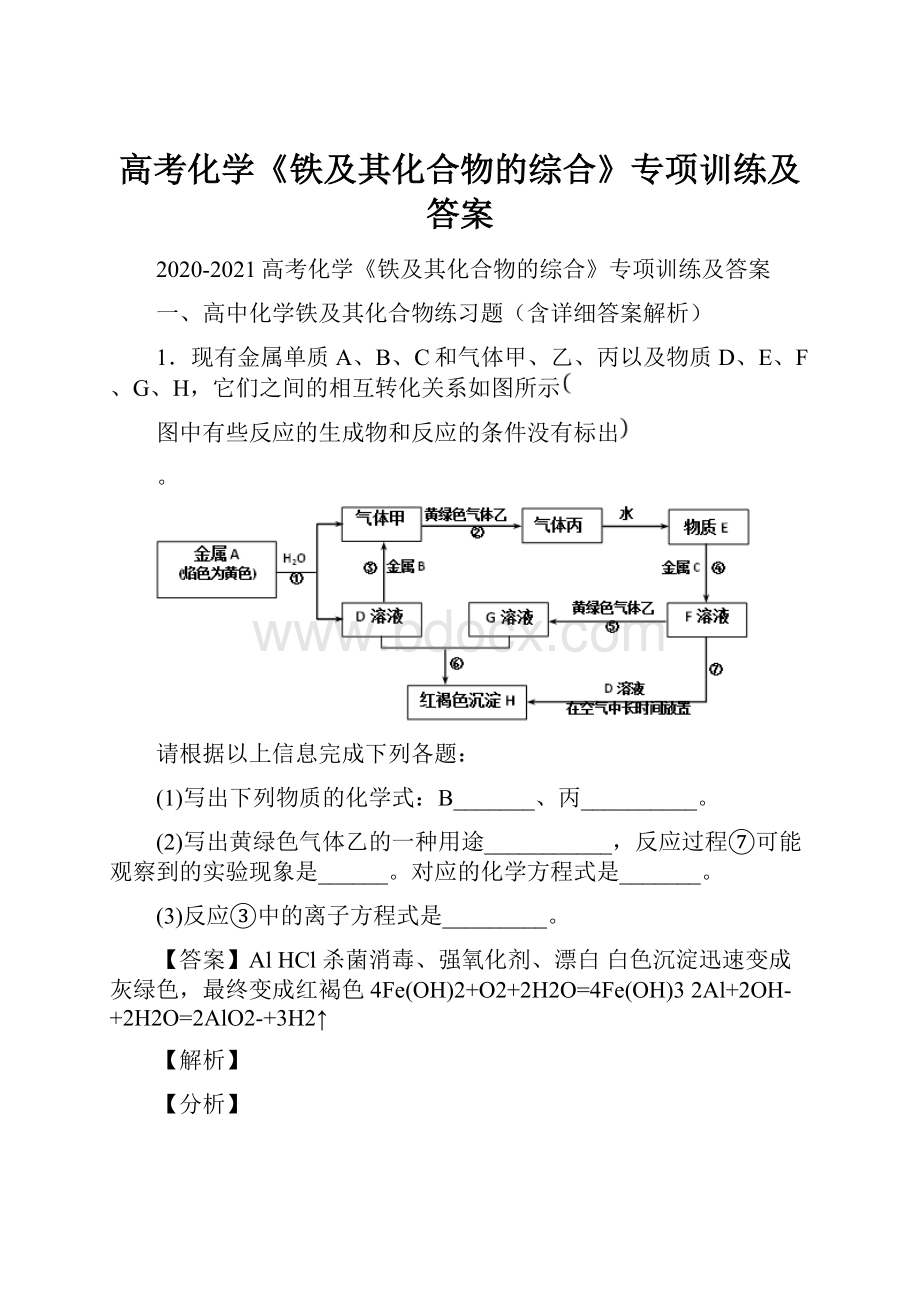
1.现有金属单质A、B、C和气体甲、乙、丙以及物质D、E、F、G、H,它们之间的相互转化关系如图所示
图中有些反应的生成物和反应的条件没有标出
。
请根据以上信息完成下列各题:
(1)写出下列物质的化学式:
B_______、丙__________。
(2)写出黄绿色气体乙的一种用途___________,反应过程⑦可能观察到的实验现象是______。
对应的化学方程式是_______。
(3)反应③中的离子方程式是_________。
【答案】AlHCl杀菌消毒、强氧化剂、漂白白色沉淀迅速变成灰绿色,最终变成红褐色4Fe(OH)2+O2+2H2O=4Fe(OH)32Al+2OH-+2H2O=2AlO2-+3H2↑
【解析】
【分析】
金属A颜色反应为黄色证明A为金属Na,Na与水反应生成气体甲为H2,D为NaOH;金属B和氢氧化钠溶液反应产生H2,说明B为金属Al,黄绿色气体乙为Cl2,气体甲是H2,H2和Cl2反应生成丙为HCl,HCl溶于水得到的物质E为盐酸溶液,盐酸与金属C反应产生F溶液是金属氯化物,该氯化物与Cl2还可以反应产生G,G与NaOH溶液反应生成红褐色沉淀H为Fe(OH)3,则G为FeCl3,推断物质F为FeCl2;判断C为Fe,以此解答该题。
【详解】
根据上述分析可知A是Na,B是Al,C为Fe,气体甲是H2,气体乙是Cl2,气体丙是HCl;D是NaOH,E是盐酸,F是FeCl2,G是FeCl3,H是Fe(OH)3。
(1)根据上述分析可知,物质B是Al,丙是HCl;
(2)黄绿色气体乙是Cl2,该物质可以与水反应产生HCl和HClO,HClO具有强氧化性,可作氧化剂,氧化一些具有还原性的物质,也用于杀菌消毒或用于物质的漂白;
(3)FeCl2与NaOH溶液发生反应:
FeCl2+2NaOH=Fe(OH)2↓+2NaCl,Fe(OH)2具有还原性,容易被溶解在溶液中的氧气氧化,发生反应:
4Fe(OH)2+O2+2H2O=4Fe(OH)3,固体由白色迅速变为灰绿色,最后变为红褐色,因此可观察到的实验现象是白色沉淀迅速变成灰绿色,最终变成红褐色;
(4)反应③是Al与NaOH溶液发生反应产生NaAlO2和H2,反应的离子方程式为:
2Al+2OH-+2H2O=2AlO2-+3H2↑。
【点睛】
本题是无机物推断,物质的颜色及转化关系中特殊反应是物质推断的突破口,再结合转化关系推断,需要学生熟练掌握元素化合物知识,试题培养了学生的分析能力及逻辑推理能力。
2.A、B、C均为中学化学常见的纯净物,它们之间存在如下转化关系:
其中①②③均为有单质参与的反应。
(1)若A是常见的金属,①③中均有同一种黄绿色气体参与反应,B溶液遇KSCN显血红色,且②为化合反应,写出反应②的离子方程式_________________________。
(2)如何检验上述C溶液中的阳离子?
______________________。
(3)若B是太阳能电池用的光伏材料,①②③为工业制备B的反应。
C的化学式是____________,属于置换反应____________,(填序号)写出反应①的化学方程式____________________。
【答案】Fe+2Fe3+=3Fe2+取少量溶液于试管,加KSCN溶液,无明显现象,再加氯水,溶液变成血红色,则证明含Fe2+SiCl4①③2C+SiO2
Si+2CO↑
【解析】
【分析】
(1)由转化关系可知A为变价金属,则A应为Fe,B为氯化铁,C为氯化亚铁,②为Fe与氯化铁的反应;
(3)B是太阳能电池用的光伏材料,可知B为Si,①为C与二氧化硅的反应,①②③为工业制备B的反应,则C为SiCl4,③中SiCl4与氢气反应,提纯Si,以此解答该题。
【详解】
(1)A是常见的金属,①③中均有同一种气态非金属单质参与反应,且②为化合反应,则该非金属气体为Cl2,B为氯化铁,则反应②的离子方程式为2Fe3++Fe=3Fe2+;
(2)由分析知C为氯化亚铁,检验Fe2+的操作方法是取少量溶液于试管,加KSCN溶液,无明显现象,再加氯水,溶液变成血红色,则证明含Fe2+;
(3)B是太阳能电池用的光伏材料,可知B为Si,①为C与二氧化硅的反应,①②③为工业制备B的反应,则C为SiCl4,其中②为Si和Cl2化合生成SiCl4,③中SiCl4与氢气反应,提纯Si,则反应①的化学方程式为SiO2+2C
Si+2CO↑,其中属于置换反应的有①③。
3.A、B、C、D四种化合物,其中A、C、D焰色反应均为黄色,而B的焰色反应为紫色,A、C和盐酸反应均得到D,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,若B的溶液滴加到硫酸亚铁溶液会先后出现白色沉淀→灰绿色沉淀→红褐色沉淀E。
试推断:
(1)A:
__、B:
__、C:
__、D:
__、E:
__;
(2)固体C加热得到A的化学反应方程式__;
(3)得到红褐色沉淀E的化学反应方程式__。
【答案】Na2CO3KOHNaHCO3NaClFe(OH)32NaHCO3=Na2CO3+H2O+CO2↑4Fe(OH)2+2H2O+O2=4Fe(OH)3
【解析】
【分析】
A、C、D为盐且焰色反应均为黄色,说明都含有钠元素的化合物;B是碱且透过钴玻璃观察焰色反应为紫色,判断为含K元素,A、C和盐酸反应均得到D的溶液,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,可以判断,无色无味的气体是CO2,A为Na2CO3,C为NaHCO3,D为NaCl;若B的溶液滴加到硫酸亚铁溶液会先后出现白色沉淀→灰绿色沉淀→红褐色沉淀E,说明B为氢氧化钾,E为氢氧化铁,据此分析解答。
【详解】
A、C、D为盐且焰色反应均为黄色,说明都含有钠元素的化合物;B是碱且透过钴玻璃观察焰色反应为紫色,判断为含K元素,A、C和盐酸反应均得到D的溶液,将固体C加热可得到A,若在A的溶液中通入一种无色无味气体,又可制得C,可以判断,无色无味的气体是CO2,A为Na2CO3,C为NaHCO3,D为NaCl,若B的溶液滴加到硫酸亚铁溶液会先后出现白色沉淀→灰绿色沉淀→红褐色沉淀E,说明B为氢氧化钾,综上所述:
A:
Na2CO3、B:
KOH、C:
NaHCO3 D:
NaCl、E:
Fe(OH)3;
(1)有分析可知:
A:
Na2CO3、B:
KOH、C:
NaHCO3 D:
NaCl、E:
Fe(OH)3;
(2)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水的化学方程式为2NaHCO3=Na2CO3+H2O+CO2↑;
(3)氢氧化亚铁具有还原性,能够与氧气、水反应生成氢氧化铁,方程式:
4Fe(OH)2+O2+2H2O=4Fe(OH)3。
4.中学化学常见物质A、B、C、D、E有如下转化(已知A、B、C、D、E均含有同一元素):
请写出:
(1)B→C+D的离子方程_______________________;
(2)E→F化学方程式__________________________。
(3)若A→B过程的反应不是化合反应,该反应可能的化学方程式___________________。
(4)D通过化合反应转化为C的离子方程式为____________________________________。
【答案】
【解析】
【分析】
由F是红褐色物质,可知F是Fe(OH)3;E能氧化为Fe(OH)3,E是Fe(OH)2;逆推可知C含有Fe2+、D含有Fe3+,则A是Fe;B中的铁元素有+2、+3两种,B是Fe3O4。
【详解】
根据以上分析,
(1)Fe3O4与盐酸反应生成氯化亚铁和氯化铁,反应的离子方程
;
(2)氢氧化亚铁和氧气反应生成氢氧化铁,反应化学方程式为
;
(3)若Fe→Fe3O4过程的反应不是化合反应,则为铁和水蒸气高温条件下生成四氧化三铁和氢气,反应可能的化学方程式为
;
(4)Fe3+和Fe通过化合反应生成Fe2+,反应的离子方程式为
。
5.图中A~J均为中学化学中常见的物质,它们之间有如下转化关系。
其中A、D为金属单质。
(反应过程中生成的水及其他产物已略去)
请回答以下问题:
(1)B是__________,H是_______________。
(填化学式)
(2)写出J与D反应转化为G的离子方程式_________________________________。
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学方程式 _______。
【答案】Fe2O3Fe(OH)22Fe3++Fe=3Fe2+2Al+2OH-+2H2O=2AlO2-+3H2↑
【解析】
【分析】
A、D为常见金属单质,B、C为金属氧化物,反应条件是高温进行,可以判断为铝热反应,可以推断A为Al,D为Fe,B为铁的氧化物,结合C与氢氧化钠反应证明C为Al2O3,E为AlCl3,F为NaAlO2,通过转化关系判断,G为FeCl2,H为白色沉淀Fe(OH)2,I为红褐色沉淀Fe(OH)3,B为Fe2O3,J为FeCl3,依据判断结果分析解答问题。
【详解】
A、D为常见金属单质,B、C为金属氧化物,反应条件是高温进行,可以判断为铝热反应,可以推断A为Al,D为Fe,B为铁的氧化物,结合C与氢氧化钠反应证明C为Al2O3,E为AlCl3,F为NaAlO2,通过转化关系判断,G为FeCl2,H为白色沉淀Fe(OH)2,I为红褐色沉淀Fe(OH)3,B为Fe2O3,J为FeCl3;
(1)依据分析判断可知B为:
Fe2O3;H的化学式为:
Fe(OH)2;故答案为:
Fe2O3;Fe(OH)2;
(2)反应“J+D→G”的离子方程式为铁和三氯化铁的氧化还原反应,离子方程式为:
2Fe3++Fe=3Fe2+;故答案为:
2Fe3++Fe=3Fe2+;
(3)A为Al在常温下也可与NaOH溶液反应生成F为偏铝酸钠,反应的化学方程式为:
2Al+2OH-+2H2O=2AlO2-+3H2↑;故答案为:
2Al+2OH-+2H2O=2AlO2-+3H2↑。
6.已知A是一种常见金属,部分反应物或生成物已略去。
试根据图中转化关系,回答下列问题。
(1)B的俗名为____。
(2)保存C溶液时需加入少量A的原因是____,A与水蒸气反应的化学方程式为____,该反应类型属于____(填基本反应类型)
(3)E生成F可观察到的现象____,化学方程式为____。
(4)写出B→C化学方程式为____,C→D的离子方程式为____。
【答案】磁性氧化铁防止Fe2+被O2氧化3Fe+4H2O
Fe3O4+4H2置换反应白色沉淀迅速变成灰绿色,最终变成红褐色4Fe(OH)2+2H2O+O2=4Fe(OH)3Fe3O4+8HCl=FeCl2+2FeCl3+4H2O2Fe2++Cl2=2Fe3++2Cl-
【解析】
【分析】
A是一种常见金属,燃烧后生成的氧化物B与盐酸反应能够生成两种氯化物,符合条件的常见金属是铁,所以由图中转化关系得,A为Fe,B为Fe3O4,C为FeCl2,D为FeCl3,X为H2,E为Fe(OH)2,F为Fe(OH)3,G为Fe2O3。
【详解】
(1)由分析可知B为Fe3O4,俗名为磁性氧化铁,故答案为:
磁性氧化铁;
(2)因为Fe2+极易被O2氧化,所以保存FeCl2溶液时需加入少量Fe,Fe与水蒸气反应的化学方程式为3Fe+4H2O
Fe3O4+4H2,该反应属于置换反应,故答案为:
防止Fe2+被O2氧化;3Fe+4H2O
Fe3O4+4H2;置换反应;
(3)Fe(OH)2沉淀在空气中被氧化生成Fe(OH)3,可观察到的现象是白色沉淀迅速变成灰绿色,最终变成红褐色,化学方程式为:
4Fe(OH)2+2H2O+O2=4Fe(OH)3;故答案为:
白色沉淀迅速变成灰绿色,最终变成红褐色;4Fe(OH)2+2H2O+O2=4Fe(OH)3;
(4)Fe3O4与盐酸反应得化学方程式为Fe3O4+8HCl=FeCl2+2FeCl3+4H2O,FeCl2与Cl2反应得离子方程式为2Fe2++Cl2=2Fe3++2Cl-,故答案为:
Fe3O4+8HCl=FeCl2+2FeCl3+4H2O;2Fe2++Cl2=2Fe3++2Cl-。
7.A~G各物质间的关系如下图,其中B、D为气态单质。
请回答下列问题:
(1)物质C和E的名称分别为________、________;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为__________________________;
若只能在加热情况下进行,则反应物A应为________;
(3)写出D转化为G的化学方程式_____________________________________;
(4)新配制的F溶液应加入________以防止其转化为G。
检验G溶液中阳离子的常用试剂是________,实验现象为________________________________________。
【答案】浓盐酸四氧化三铁2H2O2
2H2O+O2↑KClO32Fe+3Cl2
2FeCl3铁粉KSCN溶液溶液变为血红色
【解析】
【分析】
本题的突破点是MnO2,在中学化学中MnO2参与的反应主要是氧气和氯气的制备,所以依据框图的转化特点可知B是氧气,D是氯气,C是浓盐酸,E是四氧化三铁,F是氯化亚铁,G是氯化铁;Fe2+具有还原性,因此配制时需要加入铁粉防止被氧化;利用有关元素化合物知识,从质量守恒的角度书写化学方程式。
【详解】
(1)在中学化学中MnO2参与的反应主要是氧气和氯气的制备,所以依据框图的转化特点可知B是氧气,D是氯气,C是浓盐酸,E是四氧化三铁,F是氯化亚铁,G是氯化铁;
(2)MnO2参与制备氧气的反应有两种,一种是MnO2做催化剂的条件下,常温下H2O2分解制得氧气,其反应方程式为2H2O2
2H2O+O2↑;另一种是由MnO2做催化剂的条件下,加热KClO3分解制得氧气,所以A为KClO3;
(3)D为Cl2,G为FeCl3,Fe在氯气中燃烧生成FeCl3的化学方程式为2Fe+3Cl2
2FeCl3;
(4)Fe2+具有还原性,易被空气中的氧气所氧化,因此新配制的氯化亚铁溶液需要加入铁粉防止被氧化成Fe3+;检验FeCl3溶液中阳离子的常用试剂是KSCN溶液,实验现象为滴加KSCN溶液后,溶液变为血红色。
8.以下物质相互转化
试回答:
(1)写出B的化学式________________;D的名称________________。
(2)写出由E转变成F的化学方程式________________。
(3)写出用KOH鉴别G溶液的离子方程式________________;向G溶液加入A的有关离子方程式________________。
【答案】FeCl2氯化钾4Fe (OH)2+O2+2H2O═4Fe (OH)3Fe3++3OH-═Fe (OH)3↓2Fe3++Fe═3Fe2+
【解析】
【分析】
D和硝酸银溶液反应生成白色沉淀H,H不溶于稀硝酸,所以H是氯化银,则D中含有氯离子,D和硝酸银混合溶液进行焰色反应呈紫色,则D中含有钾元素,所以D是氯化钾,白色沉淀E和氧气反应生成红褐色沉淀F,则F是氢氧化铁,E是氢氧化亚铁,氢氧化铁和盐酸反应生成氯化铁溶液,所以G是氯化铁,氯化铁和A反应生成B,B和C反应生成氯化钾和氢氧化亚铁,所以A是铁,B是氯化亚铁,C是氢氧化钾,据此分析解答。
【详解】
根据上述分析,A是铁,B是氯化亚铁,C是氢氧化钾,D是氯化钾,E是氢氧化亚铁,F是氢氧化铁,G是氯化铁,H是氯化银。
(1)B是氯化亚铁,化学式为FeCl2;D是氯化钾,故答案为:
FeCl2;氯化钾;
(2)E是氢氧化亚铁,F是氢氧化铁,氢氧化亚铁和氧气、水反应生成氢氧化铁,反应的化学方程式为:
4Fe (OH)2+O2+2H2O═4Fe (OH)3,故答案为:
4Fe (OH)2+O2+2H2O═4Fe (OH)3;
(3)用KOH鉴别G溶液时铁离子和氢氧根离子反应生成氢氧化铁,离子方程式为:
Fe3++3OH-═Fe (OH)3↓,向G溶液加入A是铁离子和铁反应生成亚铁离子,离子方程式为:
2Fe3++Fe═3Fe2+,故答案为:
Fe3++3OH-═Fe (OH)3↓;2Fe3++Fe═3Fe2+。
9.已知A、B、C均为含铁化合物,请根据以下四种物质的转化过程回答相关问题:
Fe
A
B
C
(1)反应①、③中属于氧化还原反应的是________________(填序号)。
(2)向B的溶液中滴入几滴KSCN溶液后,可观察到的现象是__________。
(3)反应②的离子方程式为_____________。
【答案】①溶液呈血红色2Fe2++Cl2=2Fe3++2Cl-
【解析】
【分析】
根据铁的化学性质及图中的转化过程分析知,A为氯化亚铁,B为氯化铁,C为氢氧化铁,据此分析解答;根据铁离子的检验方法分析实验现象;根据氯气的氧化性书写相关反应的离子方程式。
【详解】
(1)反应①为铁和盐酸反应生成氯化亚铁和氢气,属于置换反应,是氧化还原反应,③是氯化铁与氢氧化钠溶液反应生成氢氧化铁沉淀和氯化钠,属于复分解反应,是非氧化还原反应,故答案为:
①;
(2)B为氯化铁溶液,铁离子遇到KSCN形成血红色溶液,故答案为:
溶液呈血红色;
(3)反应②是氯化亚铁被氯气氧化生成氯化铁,反应的离子方程式为2Fe2++Cl2=2Fe3++2Cl-,故答案为:
2Fe2++Cl2=2Fe3++2Cl-。
10.已知有以下物质相互转化。
试回答:
(1)写出B的化学式__________,D的化学式__________。
(2)写出由E转变成F的化学方程式_______________________。
(3)写出用KSCN鉴别G现象___________;向G溶液加入A的有关离子反应方程式___________。
【答案】
(1)FeCl2;KCl
(2)4Fe(OH)2+O2+2H2O===4Fe(OH)3
(3)溶液变血红色;Fe+2Fe3+=3Fe2+。
【解析】
试题分析:
白色沉淀E在空气中转化为红褐色沉淀F,可推知E为Fe(OH)2、F为Fe(OH)3,F与盐酸反应得到G溶液,则G为FeCl3,G与A反应得到B、B与C反应得到E与,可推知B为FeCl2,A为Fe,C为碱,反应得到D为氯化物,D溶液与硝酸银、硝酸混合得到白色沉淀H为AgCl,反应得到的溶液进行焰色反应呈紫色,可以K元素,故D为KCl、C为KOH。
(1)由上述分析可知,B为FeCl2,D为KCl,故答案为FeCl2;KCl;
(2)E转变成F的化学方程式为:
4Fe(OH)2+O2+2H2O=4Fe(OH)3,故答案为4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)用KSCN鉴别FeCl3溶液的现象为:
溶液呈血红色,向FeCl3溶液加入Fe的离子方程式为:
Fe+2Fe3+=3Fe2+故答案为血红色;Fe+2Fe3+=3Fe2+。
考点:
考查了无机物推断、Fe、Cl、K元素化合物的性质的相关知识。
11.某兴趣活动小组利用物质间的互变,设计成一个平面魔方,如右图所示:
已知①A、B、C、D、G含有同种元素。
②
纯A(单质)
B溶液
D固体
G溶液
颜色
银白色
黄色
红棕色
浅绿色
③E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,也能将一种氧化物氧化为F,F是含有三种元素的化合物,与A反应生成E、G。
依据以上信息填空:
(1)写出D的化学式:
______________。
(2)G生成C的过程中所出现的现象为_____________写出对应的离子方程式_________________
(3)写出反应A→B的化学方程式:
_______________________。
(4)B→F的离子方程式为__________;G与次氯酸反应的离子方程式为________________。
【答案】Fe2O3先产生白色沉淀,迅速变为灰绿色,最后变为红褐色Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)32Fe+3Cl2
2FeCl32Fe3++SO2+2H2O=2Fe2++SO42-+4H+2Fe2++2HClO=2Fe3++Cl-+H2O+ClO-
【解析】
【分析】
根据信息,D固体是红棕色,则D为Fe2O3;A、B、C、D、G含有相同元素,且G溶液为浅绿色,则G中含有Fe2+;C可以生成Fe2O3,推出C为Fe(OH)3;A为单质,银白色,则A为Fe,B溶液为黄色,说明含有Fe3+;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,推出B为含有Cl-,则B为FeCl3;E是通常情况下密度最小的气体,E为H2,F能和Fe反应生H2和Fe2+,且属于三种元素的化合物,则F为H2SO4,
【详解】
(1)D为Fe2O3;
(2)G中含有Fe2+,C为Fe(OH)3,因此离子反应方程式为Fe2++2OH-=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3,现象是先产生白色沉淀,迅速变为灰绿色,最后变为红褐色;
(3)A为Fe,B为FeCl3,则反映式为2Fe+3Cl2
2FeCl3;
(4)F为H2SO4,因此氧化物是SO2,2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,利用次氯酸的强氧化性,把Fe2+氧化成Fe3+,即2Fe2++2HClO=2Fe3++Cl-+H2O+ClO-。
12.在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液(含有Fe2+、Fe3+、Cu2+)处理和资源回收很有意义,下列是回收金属铜和刻蚀液再生的流程图,回答下列问题:
(1)沉淀A中含有的单质是_________。
(2)通入的气体C的化学式是________。
(3)滤液与气体C反应生成刻蚀液的离子方程式:
_________________。
【答案】Fe、CuCl22Fe2++Cl2=2Fe3++2Cl-
【解析】
【分析】
废液中含有Fe2+、Fe3+、Cu2+,废液中加入过量铁屑后发生反应:
Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu;过滤后得到的沉淀A为Fe、Cu;滤液中含有Fe2+,滤液中通入气体C,得到刻蚀液FeCl3溶液,则气体C为氯气;沉淀A与过量盐酸反应,Fe与盐酸反应生成氯化亚铁,而铜不反应,则沉淀B为Cu,据此进行解答。
【详解】
根据上述分析可知沉淀A为Fe、Cu,沉淀B为Cu,滤液含有Fe2+,气体C为Cl2。
(1)废液中含有Fe2+、Fe3+、Cu2+,向废液中加入过量Fe屑,发生反应Fe+2Fe3+=3Fe2+、Fe+Cu2+=Fe2++Cu,所以沉淀A中含有过量的Fe和反应产生的Cu,即沉淀A中含有的金属单质是Fe、Cu;
(2)A中含有Fe、Cu,向A中加入盐酸,铁溶解生成FeCl2,而Cu不溶解,过滤得到沉淀B是Cu
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 铁及其化合物的综合 高考 化学 及其 化合物 综合 专项 训练 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《初级会计实务》试题题库大全及答案详解.docx
《初级会计实务》试题题库大全及答案详解.docx
