 化学竞赛习题及解析化学反应速率.docx
化学竞赛习题及解析化学反应速率.docx
- 文档编号:25457057
- 上传时间:2023-06-08
- 格式:DOCX
- 页数:13
- 大小:111.14KB
化学竞赛习题及解析化学反应速率.docx
《化学竞赛习题及解析化学反应速率.docx》由会员分享,可在线阅读,更多相关《化学竞赛习题及解析化学反应速率.docx(13页珍藏版)》请在冰豆网上搜索。
化学竞赛习题及解析化学反应速率
化学反应速率习题(竞赛部分)
姓名班级学号
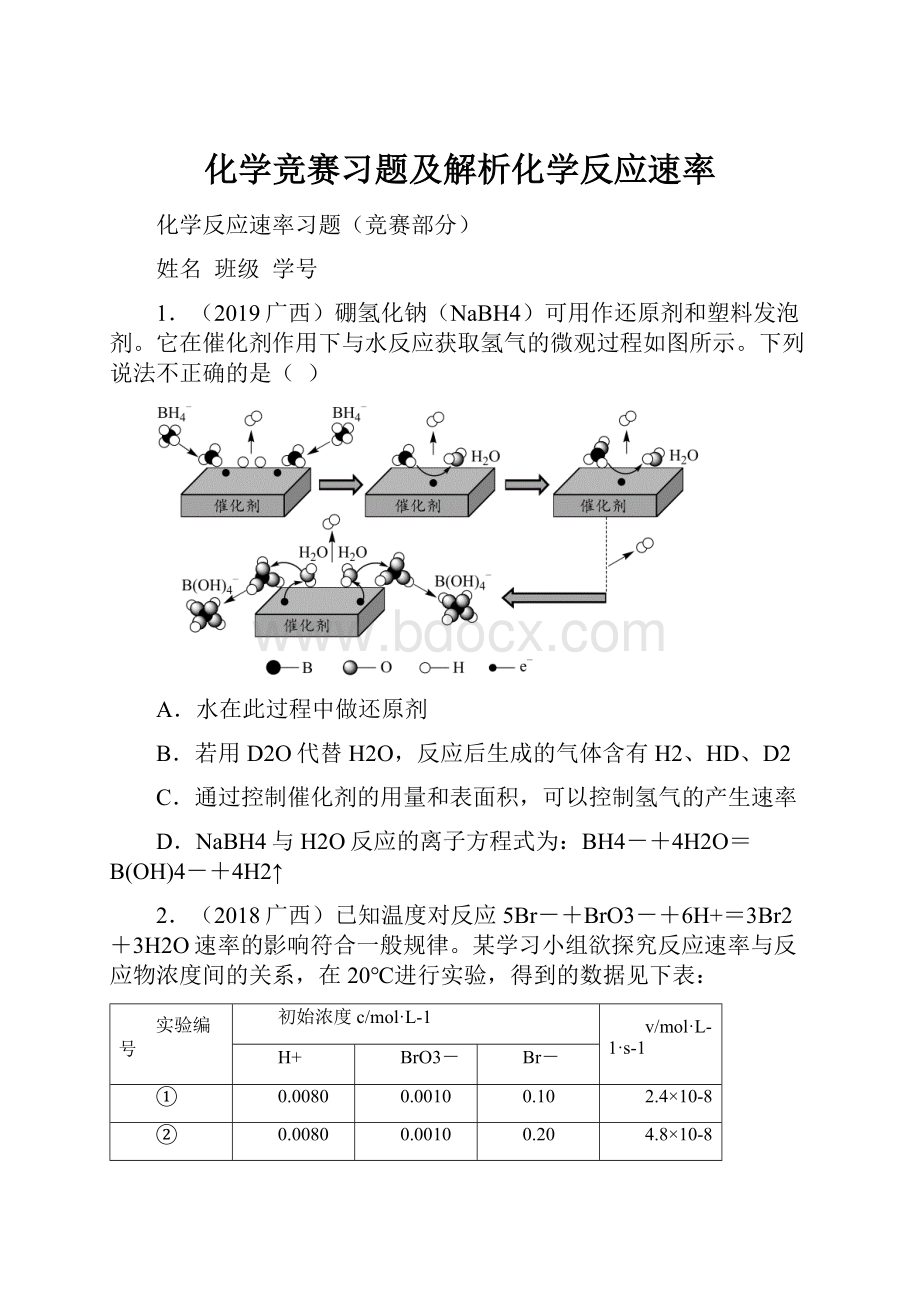
1.(2019广西)硼氢化钠(NaBH4)可用作还原剂和塑料发泡剂。
它在催化剂作用下与水反应获取氢气的微观过程如图所示。
下列说法不正确的是()
A.水在此过程中做还原剂
B.若用D2O代替H2O,反应后生成的气体含有H2、HD、D2
C.通过控制催化剂的用量和表面积,可以控制氢气的产生速率
D.NaBH4与H2O反应的离子方程式为:
BH4-+4H2O=B(OH)4-+4H2↑
2.(2018广西)已知温度对反应5Br-+BrO3-+6H+=3Br2+3H2O速率的影响符合一般规律。
某学习小组欲探究反应速率与反应物浓度间的关系,在20℃进行实验,得到的数据见下表:
实验编号
初始浓度c/mol·L-1
v/mol·L-1·s-1
H+
BrO3-
Br-
①
0.0080
0.0010
0.10
2.4×10-8
②
0.0080
0.0010
0.20
4.8×10-8
③
0.0040
0.0010
0.20
1.2×10-8
④
0.0080
0.0020
0.10
4.8×10-8
⑤
0.0040
0.0020
0.40
b
下列推测正确的是()
A.表格中的b=4.8×10-8
B.编号①实验若在35℃进行,则反应速率v在(2.4×10-8~4.8×10-8)mol·L-1·s-1范围内
C.对于编号④实验若将H+浓度改为0.0800mol·L-1,BrO3-浓度增加一倍,则反应速率约为9.5×10-7mol·L-1·s-1
D.反应速率与反应物浓度满足v=kc(BrO3-)·c(Br-)·c2(H+),其中k=3.75L3·mol-3·s-1
3.(2018湖北)某探究小组利用丙酮的溴代反应(CH3COCH3+Br2
CH3COCH2Br+HBr)来研究反应物浓度与反应速率的关系。
反应速率v(Br2)通过测定溴的颜色消失所需要的时间来确定。
在一定温度下,获得如下实验数据。
分析实验数据所得出的结论错误的是()
实验序号
初始浓度c/mol·L-1
溴颜色消失所需时间/s
CH3COCH3
HCl
Br2
①
0.80
0.20
0.0010
290
②
1.60
0.20
0.0010
145
③
0.80
0.40
0.0010
145
④
0.80
0.20
0.0020
580
A.增大c(Br2),v(Br2)增大B.实验②和③的v(Br2)相等
C.增大c(CH3COCH3),v(Br2)增大D.增大c(HCl),v(Br2)增大
4.一定温度下,按下式发生分解反应:
N2O5(g)
2NO2(g)+1/2O2(g)。
实验测得的数据如下表:
时间/s
0
500
1000
1500
2000
2500
3000
c(N2O5)/mol·L-1
5.00
3.52
2.4
1.75
1.23
0.87
0.61
(1)求各时间间隔内N2O5分解的平均反应速率。
(2)求1000s时,生成NO2的瞬时反应速率。
5.(2016北京)某二级反应2A→C,若A的起始浓度为a,产物C的浓度x随时间t的变为关系为:
,其中k为反应速率常数。
请写出反应半衰期(反应物浓度消耗一半所需要的时间)的表达式。
6.有化学反应:
①A(g)+B(g)
2D(g);②C(g)+G(g)
2H(g),其中E1、E2为该反应的活化能。
(1)vA、vD分别是用物质A、D表示反应①的化学反应速率,则vA与vD的关系为。
(2)对于反应②,若起始浓度c(C)=amol·L-1,c(G)=2amol·L-1,c(H)=0mol·L-1。
则用各物质表示的反应速率与时间的关系示意图正确的是(填序号)
(3)若E1>E2,将两反应的温度分别从500℃升至1000℃,则反应①的速度增加值Δv1与反应②速度的增加值Δv2相比,其关系为。
7.已知在320℃时反应SO2Cl2(g)→SO2(g)+Cl2(g)是一级反应,速率常数为2.2×10-5s-1。
问:
(1)10.0gSO2Cl2分解一半需要多长时间?
(2)2.00gSO2Cl2经2h后还剩余多少?
8.HgCl2和C2O42-在室温下发生下列反应:
2HgCl2(aq)+C2O42-(aq)=2Cl-(aq)+2CO2(g)+Hg2Cl2(s)
由Hg2Cl2沉淀量可计算反应速率,4次实验数据如下:
实验一
实验二
实验三
实验四
c(HgCl2)/mol·L-1
0.105
0.105
0.052
0.052
c(C2O42-)/mol·L-1
0.15
0.30
0.30
0.15
dc(C2O42-)/dt
mol·L-1·s-1
1.8×10-5
7.1×10-5
3.5×10-5
8.9×10-6
试求:
(1)HgCl2、C2O42-及总反应的级数各是多少?
(2)速率常数。
(3)当c(HgCl2)=0.020mol·L-1、c(C2O42-)=0.22mol·L-1时的反应速率。
9.一个密闭容器中,在504℃二甲醚发生反应:
CH3—O—CH3(g)→CH4(g)+H2(g)+CO(g)。
测得二甲醚分压力随时间的变化如下:
t/s
0
390
777
1195
3155
p(CH3—O—CH3)/kPa
41.6
35.2
29.9
24.9
10.5
试求:
(1)证明该反应为一级反应。
(2)速率常数。
(3)在1000s时气体总压力。
10.某抗生素在人体血液中呈现简单级数的反应,若给病人在上午8时注射一针抗生素,然后在不同时刻t测定抗生素在血液中的浓度c(以mg/100cm3表示),得到如下数据:
t/h
4
8
12
16
c/(mg/100cm3)
0.480
0.326
0.222
0.151
(1)确定反应级数。
(2)求反应的速率常数k和半衰期t1/2。
(3)若抗生素在血液中浓度不低于0.37mg/100cm3才有效,问大约何时该注射第二针?
11.338K时N2O5气相分解的速率常数为0.29min-1,活化能为103.3kJ·mol-1求353K时的速率常数k及半衰期t1/2。
12.分解反应的速率常数和温度的关系见下表。
按下表计算此分解反应的活化能是多少?
T/K
318
328
338
k/s-1
4.98×10-4
1.60×10-3
4.87×10-3
13.某酶催化反应的活化能为51kJ·mol-1,若正常人的体温为37.0℃,问病人发烧至39.5℃时,酶催化反应速率增加的百分数为多少?
14.在不同温度下,测定H2+I2=2HI的反应速率常数如下表所示:
T/K
556
629
666
700
781
k/(mol-1·L·s-1)
4.45×10-5
2.52×10-3
1.41×10-2
6.43×10-2
1.24
试求:
(1)用作图法求反应的活化能。
(2)300℃、400℃时的速率常数各是多少?
15.2ICl+H2=2HCl+I2的反应机理若是:
①ICl+H2=HCl+HI(慢)
②ICl+HI=HCl+I2(快)
试推导速率方程式。
16.次氯酸根离子和碘离子在碱性溶液中发生反应:
ClO-+I-=IO-+Cl-
若反应机理为:
①ClO-+H2O
HClO+OH-(快)
②I-+HClO=HIO+Cl-(慢)
③HIO+OH-=IO-+H2O(快)
试推导速率方程式。
参考答案及解析
题号
1
2
3
答案
A
AD
A
4.
(1)2.96×10-3,2.24×10-3,1.30×10-3,1.04×10-3,0.72×10-3,0.52×10-3
(单位:
mol·L-1·s-1)
(2)
时间/s
0
500
1000
1500
2000
2500
3000
c(N2O5)/mol·L-1
5.00
3.52
2.4
1.75
1.23
0.87
0.61
lgc(N2O5)
0.699
0.546
0.380
0.240
0.089
-0.060
-0.215
所以该反应为一级反应:
lgc=lgc0-kt/2.303
斜率=-k/2.303=(0.089-0.699)/(2000-0)=-0.000305s-1
k=0.000305×2.303s-1=7.0×10-4s-1
v(N2O5)=k·c(N2O5)=7.0×10-4s-1·2.4mol·L-1=1.68×10-3mol·L-1·s-1
v(NO2)=2v(N2O5)=3.36×10-3mol·L-1·s-1
5.当A剩余一半时,即x=a/4,则t1/2=1/2ak
6.
(1)vA=1/2vD
(2)D
(3)Δv1>Δv2
lgk与-Ea/2.303T成正比,斜率为-Ea/2.303,Ea越大,斜率的绝对值越大,升高温度时(横坐标变小),k增大值越大,反应速率增大越多。
7.
(1)t1/2=0.693/k=3.2×104s
(2)由lg(c/c0)=-kt/2.303可知lg(xg/2.00g)=-2.2×10-5s-1×3600s×2/2.303
x=1.7
8.
(1)-dc(C2O42-)/dt=kcm(HgCl2)·cn(C2O42-)
代入实验二、三数据,得到m=1
代入实验一、二数据,得到n=2
对HgCl2为一级,对C2O42-为二级,总反应级数为3
(2)-dc(C2O42-)/dt=kc(HgCl2)·c2(C2O42-)
将实验一数据代入可知:
k=7.6×10-3mol-2·L3·s-1
(3)-dc(C2O42-)/dt=7.6×10-3mol-2·L6·s-1·c(HgCl2)·c2(C2O42-)
代入数据可知:
-dc(C2O42-)/dt=7.4×10-6mol·L-1·s-1
9.
t/s
0
390
777
1195
3155
p(CH3—O—CH3)/kPa
41.6
35.2
29.9
24.9
10.5
lg(p/kPa)
1.62
1.55
1.48
1.40
1.02
(1)以lgp对t作图得一直线,说明该反应是一级反应。
(2)lgp=lgp0-kt/2.303
斜率=-k/2.303=(1.40-1.48)/(1195-777)=-1.9×10-4s-1
k=1.9×10-4×2.303s-1=4.4×10-4s-1
(3)lg(p/kPa)=lgp0-kt/2.303=1.62-1.9×10-4×1000=1.43
p=27kPa
CH3—O—CH3(g)→CH4(g)+H2(g)+CO(g)
起始压强(kPa)41.6000
反应压强(kPa)14.614.614.614.6
1000s压强(kPa)2714.614.614.6
p总=27+14.6+14.6+14.6=70.8(kPa)
10.
(1)
t/h
4
8
12
16
c/(mg/100cm3)
0.480
0.326
0.222
0.151
lg[c(mg/100cm3)]
-0.319
-0.487
-0.654
-0.821
以lgc对t作图得一直线,说明该反应是一级反应。
(2)lgc=lgc0-kt/2.303
斜率=-k/2.303=(-0.654+0.487)/(12-8)=-0.0418h-1
k=0.0418×2.303h-1=0.0962h-1
t1/2=0.693/k=7.20h
(3)以第4小时浓度为c0:
lgc=lgc0-kt’/2.303lg0.37=lg0.48-0.0962t’/2.303
t’=lg(0.48/0.37)×2.303/0.0962h-1=2.7h
t=2.7h+4h=6.7h
11.
(1)
T1=338K、T2=353K、k1=0.29min-1、Ea=103.3kJ·mol-1
由阿累尼乌斯公式:
可得:
根据公式代入实验值,解得k2=1.392min-1
(2)根据公式t1/2=0.693/k代入k2=1.392min-1,解得t1/2=0.4978min
12.
由阿累尼乌斯公式:
可得:
根据公式代入实验值,解得Ea=101.2kJ·mol-1
13.
由阿累尼乌斯公式:
可得:
k1/k2=1.17。
反应速率增加了17%。
14.
T-1×10-3(K-1)
1.80
1.59
1.50
1.43
1.28
lgk/(mol-1·L·s-1)
-4.35
-2.60
-1.85
-1.19
-0.09
(1)斜率=[-0.09-(-4.35)]/(1.28×10-3-1.80×10-3)=-8.20×103
R=8.314J·mol-1·K-1
斜率=-Ea/2.303R=-8.20×103Ea=157kJ·mol-1
(2)
573K时,作图得A点,即:
lgk/(573K)=-4.00k=1.0×10-4mol-1·L·s-1
673K时,作图得B点,即:
lgk/(673K)=-1.70k=2.0×10-2mol-1·L·s-1
15.反应速率由较慢的一步所决定,即:
-dc(H2)/dt=kc(H2)·c(ICl)
16.
反应是可逆反应,速率快,很容易建立平衡,故:
由反应①可知:
K=c(HClO)·c(OH-)/c(ClO-)
c(HClO)=K·c(ClO-)/c(OH-)a
反应是控速步,故速率方程为:
v=k1c(I-)·c(HClO),将a代入可得:
v=k1c(I-)·K·c(ClO-)/c(OH-)=kc(I-)·c(ClO-)/c(OH-)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 竞赛 习题 解析 化学反应 速率
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《爱和自由》读书心得15篇.docx
《爱和自由》读书心得15篇.docx
