 届枣庄二中高三化学二轮复习第四周过关练习题.docx
届枣庄二中高三化学二轮复习第四周过关练习题.docx
- 文档编号:25017843
- 上传时间:2023-06-03
- 格式:DOCX
- 页数:14
- 大小:274.63KB
届枣庄二中高三化学二轮复习第四周过关练习题.docx
《届枣庄二中高三化学二轮复习第四周过关练习题.docx》由会员分享,可在线阅读,更多相关《届枣庄二中高三化学二轮复习第四周过关练习题.docx(14页珍藏版)》请在冰豆网上搜索。
届枣庄二中高三化学二轮复习第四周过关练习题
2017届枣庄二中高三化学二轮复习第四周过关练习题
学校:
___________姓名:
___________班级:
___________考号:
___________
一、选择题
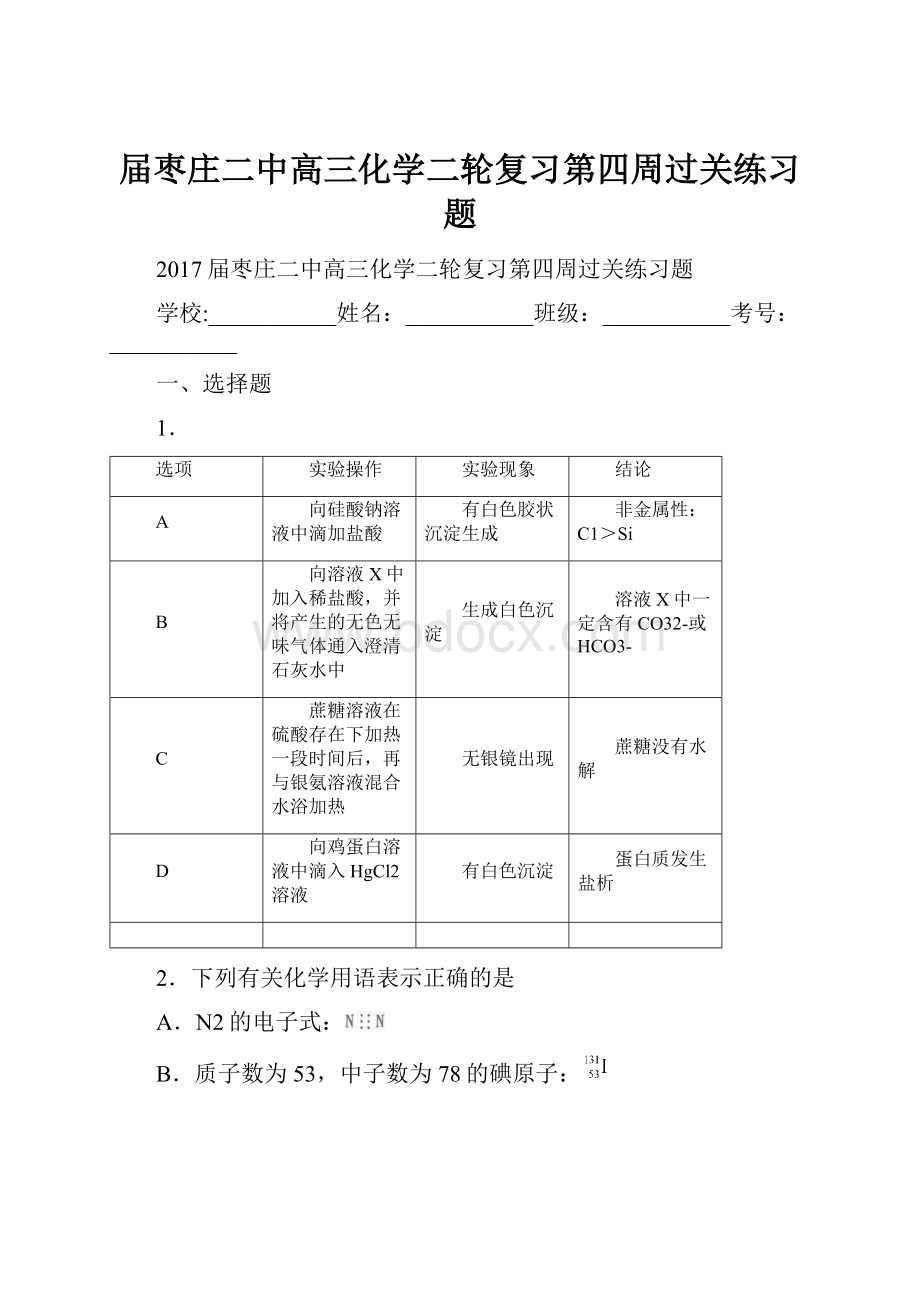
1.
选项
实验操作
实验现象
结论
A
向硅酸钠溶液中滴加盐酸
有白色胶状沉淀生成
非金属性:
C1>Si
B
向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中
生成白色沉淀
溶液X中一定含有CO32-或HCO3-
C
蔗糖溶液在硫酸存在下加热一段时间后,再与银氨溶液混合水浴加热
无银镜出现
蔗糖没有水解
D
向鸡蛋白溶液中滴入HgCl2溶液
有白色沉淀
蛋白质发生盐析
2.下列有关化学用语表示正确的是
A.N2的电子式:
B.质子数为53,中子数为78的碘原子:
C.S2-的结构示意图:
D.乙烯的分子式:
CH2=CH2
3.NA表示阿伏加德罗常数,下列说法正确的是()
A.标准状况下,11.2LCCl4所含原子数目为2.5NA
B.常温常压下,64gSO2中含有的原子数为3NA
C.将1molCl2通入水中能生成1molHClO
D.2L0.1mol•L﹣1K2SO4溶液中含K+物质的量为0.2mol
4.下列物质分类正确的是()
A.SO2、SiO2、CO均为酸性氧化物
B.稀豆浆、硅酸、氯化铁溶液均为胶体
C.烧碱、冰醋酸、四氯化碳均为电解质
D.漂白粉、水玻璃、氨水均为混合物
5.能正确表示下列化学反应的离子方程式的是
A.氧化钙与稀盐酸反应:
CaO+2H+=Ca2++H2O
B.稀氨水中通入少量二氧化碳:
2OH-+CO2=CO32-+H2O
C.将铜屑加入硝酸银溶液中:
Cu+Ag+=Cu2++Ag
D.过量Ca(HCO3)2溶液与少量NaOH反应:
2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O
6.从海藻灰中可以提取碘的主要反应为:
2I-+Cl2=2Cl-+I2,下列说法正确的是)()
A.该反应属于置换反应B.I-具有氧化性
C.1mol氯气转移了1mol电子D.Cl2是还原剂
7.某温度下,将Cl2通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合液,经测定ClO-与ClO3-的浓度之比为1∶1,则Cl2与NaOH溶液反应时被还原的氯元素与被氧化的氯元素的物质的量之比为
A.4∶1B.11∶3C.3∶1D.21∶5
8.根据下列反应判断有关物质还原性由强到弱的顺序是()
H2SO3+I2+H2O===H2SO4+2HI
2FeCl3+2HI===2FeCl2+2HCl+I2
3FeCl2+4HNO3===2FeCl3+NO↑+2H2O+Fe(NO3)3。
A.I->Fe2+>H2SO3>NO
B.H2SO3>I->Fe2+>NO
C.Fe2+>I->H2SO3>NO
D.NO>Fe2+>H2SO3>I-
9.CuSO4、Fe2(SO4)3、H2SO4的混合溶液100mL,已知溶液中阳离子的浓度相同(不考虑水解),且SO42-的物质的量浓度为6mol•L-1,则此溶液最多溶解铁粉的质量为()
A.5.6gB.11.2gC.22.4gD.33.6g
10.足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。
若向所得硝酸铜溶液中加入5mol·L-1NaOH溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是
A.60mLB.45mLC.30mLD.15mL
11.今有甲、乙、丙、丁、戊5种物质,在一定条件下,它们能按图方式进行转化:
其推断正确的是
选项
甲
乙
丙
丁
戊
A
NH3
O2
NO
H2O
NO2
B
Mg
CO2
C
MgO
CO
C
C
H2O
CO
H2
C2H5OH
D
FeBr2
Cl2
FeCl2
Br2
FeCl3
二、填空题
12.假定元素周期表是有限的,根据已知的元素周期表的某些事实和理论可归纳出一些假说。
(1)已知元素周期表中的各周期可排元素种类如下:
周期
1
2
3
4
5
6
7
元素种类
2
8
8
18
18
32
32
人们预测元素周期表第八周期将来也会排满,那么该周期排满后的元素种数是。
A.18B.32C.50D.无法判断
(2)根据周期表中每个周期非金属元素的种数(把稀有气体元素看做非金属元素),预测周期表中应该有种非金属元素,还有种未发现。
未发现的非金属元素处于周期族。
(3)小明同学所在的化学探究小组,在查阅相关资料后归纳出元素周期表的另一种画法——三角形元素周期表的一部分,图上标有第ⅦA族和碳、钾两种元素的位置。
回答下列问题:
①请在图中将过渡元素所在的位置涂黑。
②画出B元素价电子排布图。
13.合成氨是最重要的化工生产之一,回答下列问题:
I.氢气通常用生产水煤气的方法制得。
其中CO(g)+H2O(g)
CO2(g)+H2(g)△H<0,在850℃时,平衡常数K=1。
(1)若升高温度到950℃时,达到平衡时K_________1(填“>”“<”或“=”)
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0molCO、3.0molH2O、1.0molCO2和xrnolH2,则:
①当x=5.0时,上述平衡向_________(填正反应或逆反应)方向进行。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是_____________。
(3)在850℃时,若设x=5.0mol和x=6.0mol,其它物质的投料不变,当上述反应达到平衡后,测得H2的体积分数分别为a%、b%,则a_______b(填“大于”、“小于”或“等于”)。
II.氨和尿素【CO(NH2)2】溶液都可以吸收硝酸工业尾气中的NO、NO2,将其转化为N2。
(4)尿素与NO、NO2三者等物质的最反应为:
CO(NH2)2+NO+NO2=CO2+2N2+2H2O
该反应中的氧化剂为________(写化学式)。
若反应生成标况下N233.6L,则转移电子的数目为___________。
(5)已知:
N2(g)+O2(g)=2NO(g)△H1=akJ·mol-1
N2(g)+3H2(g)=2NH3(g)△H2=bkJ•mol-1
2H2(g)+O2(g)=2H2O(g)△H3=ckJ•mol-1
则4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g)△H=__________。
III.(6)合成氨盐也是氨的重要用途,测定其中的含氮量可以采用“甲醛法”。
即4NH4++6HCHO(CH2)6N4+4H++6H2O。
现有一种纯净的铵盐,可能是硝酸铵、硫酸铵或碳酸铵中的一种。
称取2g该铵盐溶于水,加入足量的甲醛溶液后,再加人水配成100mL溶液,取出10mL,滴入酚酞后再逐滴滴入0.lmol/L的NaOH溶液,当滴到25mL时溶液呈粉红色,且在半分钟内不褪色,则该铵盐中氮的质量分数是_________。
14.下图表示氮及其化合物在一定条件下的转化关系:
(1)根据反应I,在500℃、20MPa时,将N2和H2通入到体积为2L的密闭容器中,反应过程中各种物质的物质的量变化如右图所示:
(1)10min内用NH3表示该反应的平均速率,v(NH3)=。
(2)在10~20min内NH3浓度变化的原因可能是(填字母)。
a.加了催化剂
b.降低温度
c.增加NH3的物质的量
(3)该可逆反应达到平衡的标志是_______(填字母)。
a.3v(H2)正=2v(NH3)逆
b.混合气体的密度不再随时间变化
c.容器内的总压强不再随时间而变化
d.N2、H2、NH3的分子数之比为1∶3∶2
(4)第一次平衡时,平衡常数K1=(用数学表达式表示)。
(5)反应I:
N2(g)+3H2(g)
2NH3(g)ΔH=–92.4kJ•mol-1
如图所示反应I中平衡混合气中NH3的体积分数随温度或压强变化的曲线,图中L(L1、L2)、X分别代表温度或压强。
其中X代表的是____________(填“温度”或“压强”),判断L1、L2的大小关系并说明理由_______。
(6)反应II其中一步反应为
2NH3(g)+3Cl2(g)=N2(g)+6HCl(g)ΔH=–462kJ•mol-1
已知:
断开1molH–N键与断开1molH–Cl键所需能量相差约为_________kJ。
15.草酸钴可用于指示剂和催化剂的制备.用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取COC2O4•2H2O工艺流程如下:
已知:
①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
沉淀物
Fe(OH)3
Al(OH)3
Co(OH)2
Fe(OH)2
Mn(OH)2
完全沉淀的pH
3.7
5.2
9.2
9.6
9.8
(1)浸出过程中加入Na2SO3的目的是.
(2)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀.试用离子方程式和必要的文字简述其原理:
_________
(3)萃取剂对金属离子的萃取率与pH的关系如右图1.萃取剂的作用是;其使用的适宜pH范围是.
A.2.0~2.5B.3.0~3.5C.4.0~4.5
(4)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀.已知Ksp(MgF2)=7.35×10﹣11、Ksp(CaF2)=1.05×10﹣10,当加入过量NaF后,所得滤液
=.
(5)已知:
NH3•H2O
NH4++OH﹣Kb=1.8×10﹣5;
H2C2O4
H++HC2O4﹣Ka1=5.4×10﹣2;
HC2O4﹣
H+C2O42﹣Ka2=5.4×10﹣5
则该流程中所用(NH4)2C2O4溶液的pH7(填“>”或“<”或“=”)
(6)CoC2O4•2H2O热分解质量变化过程如图2所示(其中600℃以前是隔绝空气加热,600℃以后是在空气中加热);A、B、C均为纯净物;C点所示产物的化学式是_____________________
16.如图所示3套实验装置,分别回答下列问题。
(1)装置1为铁的吸氧腐蚀实验。
一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应为_________________。
(2)装置2中的石墨是极________(填“正”或“负”),该装置发生的总反应的离子方程式为________________________。
(3)装置3中甲烧杯盛放100mL0.2mol/L的NaCl溶液,乙烧杯盛放100mL0.5mol/L的CuSO4溶液。
反应一段时间后,停止通电。
向甲烧杯中滴入几滴酚酞溶液,观察到石墨电极附近首先变红。
①电源的M端为极____________(填“正”或“负”),甲烧杯中铁电极的电极反应为__________。
②乙烧杯中电解反应的化学方程式为___________________________。
③停止电解,取出Cu电极,洗涤、干燥、称量、电极增重0.64g,甲烧杯中产生的气体标准状况下体积为___________mL。
三、实验题
17.蛇纹石矿可以看做由MgO、Fe2O3、Al2O3、SiO2组成。
由蛇纹石制取碱式碳酸镁的实验步骤如下图所示
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是________________。
氢氧化物
Fe(OH)3
Al(OH)3
Mg(OH)2
开始沉淀pH
1.5
3.3
9.4
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表)Ca(OH)2不能过量,若Ca(OH)2过量可能会导致溶解、沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入______(填入物质的化学式),然后(依次填写实验操作名称)。
(4)现设计一个实验,确定产品aMgCO3·bMg(OH)2·cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:
浓硫酸、碱石灰):
①样品称量②高温分解
③___________________。
④____________________。
⑤MgO称量
(5)18.2g产品完全分解后,产生6.6gCO2和8.0gMgO,由此可知,产品的化学式中:
a=__________________,b=_______________,
c=。
四、推断题
18.对二甲苯(英文名称p﹣xylene,缩写为PX)是化学工业的重要原料。
(1)写出PX的结构简式____________________。
(2)增塑剂(DEHP)存在如图所示的转化关系,其中A是PX的一种同分异构体。
①B的苯环上存在2种等效氢,则B的结构简式是_______________________。
②C分子有1个碳原子连接乙基和正丁基,DEHP的结构简式是_______________。
(3)F是B的一种同分异构体,具有如下特征:
a.是苯的邻位二取代物;
b.遇FeCl3溶液显示特征颜色;
c.能与碳酸氢钠溶液反应。
写出F与NaHCO3溶液反应的化学方程式________________________。
参考答案
1.B
2.B
3.B
4.D
5.A
6.A
7.C
8.B
9.C
10.A
11.B
12.
(1)C;
(2)23;一,七,ⅦA;
(3)①
;②
。
【答案】
(1)<(1分)
(2)①逆反应(2分)②0≤x<3(2分)
(3)小于(2分)
(4)NO、NO2(2分)4.5NA(2分)
(5)(3c-2a-2b)KJ•mol-1(2分)(6)17.5%(2分)
14.
(1)v(NH3)=0.005mol/(L·min)
(2)a(3)c(4)
(5)压强;L1<L2,合成氨的反应是放热反应,压强相同时,温度升高,平衡逆向移动,氨的体积分数减小(6)41
15.
(1)还原Fe3+、Co3+为Fe2+、Co2+.
(2)加入的碳酸钠(或CO32﹣)与H+反应,c(H+)降低,使Fe3+和Al3+(用R3+代替)的水解平衡R3++3H2O⇌R(OH)3+3H+,向右移动,而产生氢氧化物沉淀(直接用用双水解解释也给分)
(3)除去溶液中的Mn2+;B(1分)(4)0.7(5)<
(6)Co3O4(或CoO•Co2O3)
16.
(1)O2+4e-+2H2O=4OH-;
(2)正,Fe3++Cu=2Fe2++Cu2+
(3)①正,Fe-2e-=Fe2+②2CuSO4+2H2O
2Cu+O2↑+2H2SO4③224
17.
(1)Fe3+、Al3+
(2)Al(OH)3Mg(OH)2
(3)NaOH或Ca(OH)2过滤、洗涤、灼烧
(4)③用浓硫酸吸收水蒸气④称量碱石灰吸收CO2前后的质量
(5)313
据元素守恒可知:
n(CO2)=n(MgCO3)==0.15mol。
镁元素守恒可知:
n[Mg(OH)2]=n(MgO)-n(MgCO3)=-0.15mol=0.05mol。
根据前后质量守恒可求n(H2O)=0.15mol,则a∶b∶c=3∶1∶3,即为最小整数比,可得。
18.
(1)
(2)①
;②
(3)
+NaHCO3→
+CO2↑+H2O
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 枣庄 中高 化学 二轮 复习 四周 过关 练习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《初级会计实务》试题题库大全及答案详解.docx
《初级会计实务》试题题库大全及答案详解.docx
