 中考化学流程图综合练习题附答案.docx
中考化学流程图综合练习题附答案.docx
- 文档编号:24870156
- 上传时间:2023-06-02
- 格式:DOCX
- 页数:20
- 大小:151.59KB
中考化学流程图综合练习题附答案.docx
《中考化学流程图综合练习题附答案.docx》由会员分享,可在线阅读,更多相关《中考化学流程图综合练习题附答案.docx(20页珍藏版)》请在冰豆网上搜索。
中考化学流程图综合练习题附答案
一、中考初中化学流程图
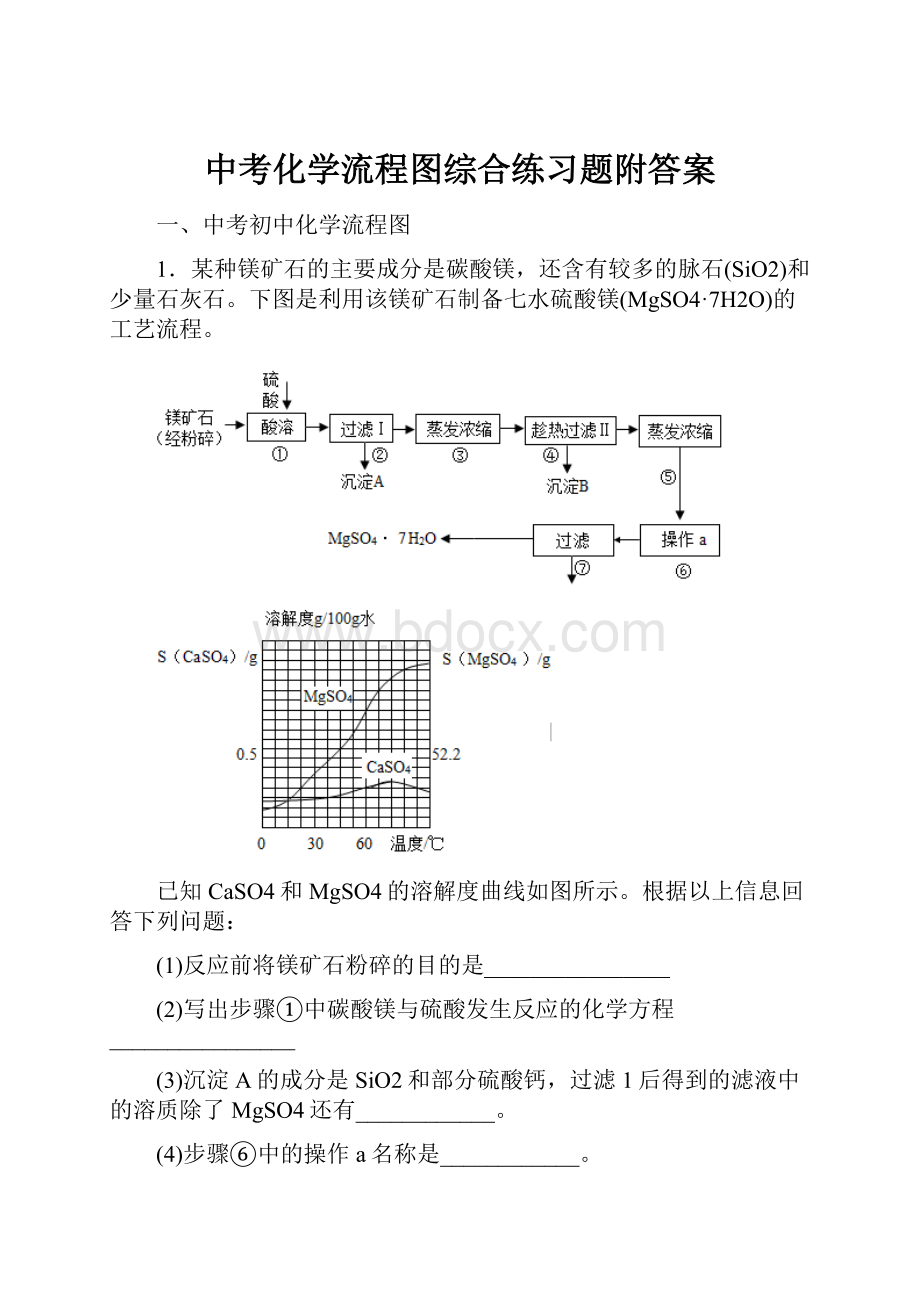
1.某种镁矿石的主要成分是碳酸镁,还含有较多的脉石(SiO2)和少量石灰石。
下图是利用该镁矿石制备七水硫酸镁(MgSO4·7H2O)的工艺流程。
已知CaSO4和MgSO4的溶解度曲线如图所示。
根据以上信息回答下列问题:
(1)反应前将镁矿石粉碎的目的是________________
(2)写出步骤①中碳酸镁与硫酸发生反应的化学方程________________
(3)沉淀A的成分是SiO2和部分硫酸钙,过滤1后得到的滤液中的溶质除了MgSO4还有____________。
(4)步骤⑥中的操作a名称是____________。
【答案】增大反应物的接触面积,加快反应速率,使反应进行得更充分MgCO3+H2SO4=MgSO4+H2O+CO2↑CaSO4降温结晶
【解析】
【分析】
【详解】
(1)因为自然界中开采出来的镁矿石是块状的,如果不将其粉碎,稀硫酸只能和块状镁矿石的表面接触,接触面积较小,反应速率较慢。
因此反应前将镁矿石粉碎的目的是:
增大反应物的接触面积,加快反应速率,使反应进行得更充分;
(2)步骤①中碳酸镁与硫酸反应产生硫酸钠、水和二氧化碳,其化学方程式是:
:
MgCO3+H2SO4=MgSO4+H2O+CO2↑
(3)沉淀A的成分是SiO2和部分硫酸钙,过滤1后得到的滤液中的溶质除了MgSO4还有硫酸钙(CaSO4)。
因为硫酸钙微溶于水,大部分变为沉淀,但有少部分溶解在水中。
(4)从题中提供的溶解度曲线可知,硫酸镁的溶解度受温度影响加大,故步骤⑥中将溶液浓缩蒸发,然后降温结晶,就会有七水硫酸镁晶体析出。
因此操作a的名称是:
降温结晶。
2.随着世界工业经济的发展、人口的剧增、人类欲望的无限上升和生产生活方式的无节制,世界气候面临越来越严重的问题,二氧化碳排放量越来越大,全球灾难性气候变化屡屡出现,已经严重危害到人类的生存环境和健康安全。
以下流程是通过控制化学反应的条件来促进或抑制化学反应,实现“低碳”,从而更好地通过化学反应为人类造福。
根据上述流程回答下列问题:
(1)上述流程中可循环利用的物质是___________。
(2)“低碳”是全世界的主题,这里的“碳”主要是指_____________气体。
(3)甲醇(CH3OH)完全燃烧除了生成二氧化碳外,还生成一种常温下为液态的化合物,发生反应的化学方程式为_______________。
(4)证明液化石油气、汽油、甲醇等燃料燃烧产物中含有二氧化碳的方法是(用化学方程式表示)_______________。
【答案】二氧化碳二氧化碳
【解析】
【分析】
【详解】
(1)根据流程图,可循环利用的物质是二氧化碳。
(2)“低碳”就是较低的二氧化碳排放,这里的“碳”主要是指二氧化碳气体。
(3)甲醇(CH3OH)完全燃烧生成二氧化碳和水,发生反应的化学方程式为
。
(4)检验二氧化碳的方法是通入澄清石灰水,其化学方程式为
。
3.实验室以一种工业废渣(主要成分为MgCO3、MgO和SiO2)为原料制备MgCO3•3H2O.其主要实验过程如图:
已知:
SiO2不溶于水,常温下不与硫酸、碳酸钠反应。
(1)“酸溶”时发生反应的化学方程式为_____和_____。
(2)“过滤Ⅱ”所得滤液中含有的主要离子有_____(填离子符号)。
(3)“反应”步骤前后均有过滤,能否省去“过滤Ⅰ”只进行“过滤Ⅱ”。
_____(填“能”或“否”),理由是_____。
(4)“酸溶”时所加硫酸溶液不宜过量太多的原因是_____。
【答案】MgO+H2SO4=MgSO4+H2OMgCO3+H2SO4=MgSO4+H2O+CO2↑Na+、SO42﹣、CO32﹣否导致产品不纯避免制备产品消耗更多的碳酸钠
【解析】
【分析】
氧化镁和硫酸反应生成硫酸镁和水,碳酸镁和硫酸反应生成硫酸镁、水和二氧化碳。
【详解】
(1)“酸溶”时是氧化镁和硫酸反应生成硫酸镁和水,化学方程式为
,碳酸镁与硫酸反应生成硫酸镁、水和二氧化碳,化学方程式为
。
(2)滤液I为生成的硫酸以及生成的硫酸镁的混合溶液,和过量碳酸钠反应,生成硫酸钠以及碳酸镁,还剩余碳酸钠,所以“过滤Ⅱ”所得滤液中含有的主要离子有
。
(3)“反应”步骤前后均有过滤,不能省去“过滤Ⅰ”只进行“过滤Ⅱ”,会导致得到的产品因为混油二氧化硅而不纯。
(4)“酸溶”时所加硫酸溶液不宜过量太多的原因是过量的硫酸需要加入碳酸钠进行去除,所以是避免制备产品消耗更多的碳酸钠。
4.用金属铁制备自来水新型消毒、净水剂Na2FeO4的流程如下,请回答下列问题:
(1)固体B中的物质是_______;Na2FeO4属于______(填“酸”、“碱”、“盐”、“氧化物”).
(2)操作Ⅰ的名称是________;该操作能使A、B分离的原因是_________.
(3)反应②的基本反应类型为:
_______;反应③的化学方程式为:
________.
(4)溶液C中的溶质组成存在_________种可能性.
【答案】Fe和Cu盐过滤A是液体,B是固体(合理皆可)复分解反应2Fe(OH)2+H2O2=2Fe(OH)3三
【解析】
【分析】
【详解】
(1)由反应的流程可知,过量的铁粉与硫酸铜反应,生成了硫酸亚铁和铜,由于铁是过量的,在过滤后得到的固体B是Cu,Fe的混合物;Na2FeO4是金属离子和酸根离子构成的化合物,属于盐。
故填:
Fe和Cu;盐;
(2)由上述反应①得到是固液的混合物,要将固液分开,应进行的操作是过滤。
故填:
过滤;A是液体,B是固体(合理皆可);
(3)反应②是硫酸亚铁与氢氧化钠反应生成氢氧化亚铁和硫酸钠,反应的方程式是:
FeSO4+2NaOH=Fe(OH)2↓+Na2SO4,该反应是两种化合物交换成分生成另外两种化合物,属于复分解反应;反应③是氢氧化亚铁被过氧化氢氧化为氢氧化铁,方程式是:
2Fe(OH)2+H2O2=2Fe(OH)3。
故填:
复分解反应;2Fe(OH)2+H2O2=2Fe(OH)3;
(4)若氢氧化钠溶液与硫酸亚铁溶液恰好完全反应,所得溶液中只有一种溶质——硫酸钠;若氢氧化钠过量,则有两种溶质﹣﹣硫酸钠和氢氧化钠;若硫酸亚铁过量,则有两种溶质﹣﹣硫酸钠和硫酸亚铁。
故填:
三。
【点睛】
本题给出了制取物质的反应流程图,对于这类题目,需要搞清楚每一步反应物、生成物,清楚工艺流程原理.再结合有关的知识分析解答有关的问题。
5.现有一包粗盐,主要成分是氯化钠,其中含少量的硫酸钠、氯化钙和沙子,小轩设计了如图工艺流程,制得精盐。
(1)在①-⑤的操作中,属于蒸发操作的是______(填序号),蒸发操作中用于提供热源的仪器是______。
(2)向反应池1中加过量的x是_____溶液(填序号)。
aKOHbNaOHcBa(OH)2dCa(OH)2
(3)固体B中含有的物质有_______(写物质名称,至少写两种)。
(4)第④步加足量盐酸的目的是________。
(5)写出反应池2中所发生的化学方程式:
①____、②______。
【答案】⑤酒精灯c硫酸钡、碳酸钡(或碳酸钙)除去过量的NaOH和Na2CO3Na2CO3+Ba(OH)2=BaCO3↓+2NaOHNa2CO3+CaCl2=CaCO3↓+2NaCl
【解析】
【分析】
【详解】
(1)操作⑤是从溶液中获取晶体,即蒸发操作;蒸发操作中用于提供热源的仪器是酒精灯;故填:
⑤;酒精灯;
(2)加入试剂x是为了除去硫酸钠,所以加入的是氢氧化钡溶液,硫酸钠和氢氧化钡反应生成硫酸钡沉淀和氢氧化钠;故填:
c;
(3)先加入过量的氢氧化钡溶液除去硫酸钠,二者反应生成硫酸钡沉淀和氢氧化钠;然后再加入过量的碳酸钠,碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,所以过滤后得到的固体B中含有硫酸钡、碳酸钡和碳酸钙三种物质;故填:
硫酸钡、碳酸钡(或碳酸钙);
(4)在第④步操作中,向滤液中滴加足量盐酸的目的是除去加入的过量的NaOH和Na2CO3;故填:
除去过量的NaOH和Na2CO3;
(5)反应池2中碳酸钠与氢氧化钡反应生成碳酸钡沉淀和氢氧化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,故填:
Na2CO3+Ba(OH)2=BaCO3↓+2NaOH;Na2CO3+CaCl2=CaCO3↓+2NaCl。
【点睛】
合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础。
6.国拥有丰富的海洋资源,我们可以从海水中提取食盐,并以此为原料制得具有广泛用途的产品。
(1)海水晒盐是利用了____________的方法使食盐晶体析出,得到粗盐。
(2)某制碱工厂以粗盐为原料制纯碱,部分工艺流程如下:
(3)流程I中为了除去杂质,依次加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是___________(填字母编号)。
A加入三种溶液的顺序不能调整
B加入三种溶液可将粗盐水中的SO42-、Mg2+、Ca2+转化为沉淀
C按流程I所加溶液的顺序除杂,过滤后得到四种沉淀
(4)在流程I中,加入氢氧化钠溶液时发生反应的化学方程式是____________。
(5)写出流程Ⅲ中发生反应的化学方程式______________。
【答案】蒸发结晶BCMgCl2+2NaOH═Mg(OH)2↓+2NaCl2NaHCO3
Na2CO3+H2O+CO2↑
【解析】
【分析】
【详解】
(1)由于氯化钠的溶解度受温度的影响不大,所以海水晒盐是利用了蒸发结晶的方法使食盐晶体析出,得到粗盐。
(3)A.加入的三种溶液中,碳酸钠溶液必须在氯化钡溶液后面加入,而氢氧化钠溶液可以颠倒顺序,因为碳酸钠可以出去粗盐中的氯化钙和过量的氯化钡,该选项说法不正确;
B.加入氯化钡可将溶液中硫酸根离子转化为硫酸钡沉淀,加入氢氧化钠溶液可将粗盐中镁离子转化为氢氧化镁沉淀,加入碳酸钠溶液可将粗盐中的钙离子转化为碳酸钙沉淀,三种溶液将粗盐水中的SO42-、Mg2+、Ca2+转化为沉淀,该选项说法正确;
C.按流程I所加溶液的顺序除杂,过滤后得到四种沉淀,即硫酸钡沉淀、氢氧化镁沉淀、碳酸钙沉淀和碳酸钡沉淀,该选项说法正确。
(4)在流程I中,加入氢氧化钠溶液能与氯化镁反应生成了氢氧化镁沉淀和氯化钠,发生反应的化学方程式是:
MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(5)流程Ⅲ中碳酸氢钠受热分解生成碳酸钠、二氧化碳和水,发生反应的化学方程式是:
2NaHCO3
Na2CO3+H2O+CO2↑。
故答案为:
(1)蒸发结晶;
(3)BC;
(4)MgCl2+2NaOH═Mg(OH)2↓+2NaCl;
(5)2NaHCO3
Na2CO3+H2O+CO2↑。
【点睛】
合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础。
7.人类的生产生活离不开金属.
(1)金属铁、铝常用来制作炊具,主要是利用其_______________性.
(2)人类每年从自然界提取大量的金属,其中提取量最大的是铁.赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的化学方程式为______________________________________.
(3)我国钢铁年产量很高,但因锈蚀造成的损失也很惊人.工业上常用稀盐酸除去铁锈,该反应的化学方程式为___________________________________________.
(4)从含有CuSO4、ZnSO4、FeSO4的废水中回收重要原料硫酸锌和有关金属,实验过程如下.
请回答:
写出步骤①中发生反应的化学方程式__________________________________________;固体D的化学式为_____;以上物质A~G中,含有锌元素的是_______(填字母序号)
【答案】导热
6HCl+Fe2O3=2FeCl3+3H2OZn+FeSO4=Fe+ZnSO4Zn+CuSO4=ZnSO4+CuFe;ABCEG
【解析】
【分析】
【详解】
(1)作炊具,主要是利用金属的导热性.
(2)用赤铁矿(主要成分为Fe2O3)和一氧化碳炼铁的反应物是一氧化碳和氧化铁,写在等号的左边,生成物铁和二氧化碳写在等号的右边,根据得失氧进行配平,反应条件是高温写在等号的上边,所以化学方程式为:
.
(3)盐酸除铁锈的反应物是盐酸和氧化铁写在等号的左边,生成物氯化铁和水写在等号的右边,用观察法配平即可,所以方程式是:
6HCl+Fe2O3=2FeCl3+3H2O.(4)根过量A是加入的锌,锌与硫酸亚铁反应生成铁和硫酸锌,所以方程式是:
Zn+FeSO4═Fe+ZnSO4;锌与硫酸铜反应生成铜和硫酸锌,所以方程式是:
Zn+CuSO4═ZnSO4+Cu;由于锌与硫酸亚铁反应生成铁盒硫酸锌,锌与硫酸铜反应生成铜和硫酸锌,且加入的锌是过量的,所以固体B中含有锌、铁、铜;溶液C是硫酸锌溶液;固体B用磁铁把铁吸引出来,所以固体D是铁;固体E中含有锌和铜,由于锌能与硫酸反应,铜与硫酸不反应,所以加入的溶液F是稀硫酸,溶液G是硫酸锌溶液;所以含有锌元素的有ABCEG.
考点:
金属的物理性质及用途;金属活动性顺序及其应用;一氧化碳还原氧化铁;酸的化学性质.
8.我市拥有丰富的海洋资源,开发利用这些宝贵的资源有力地促进了我市经济的发展。
从海水中提取出的粗盐中除了NaCl外,还含有泥沙等杂质。
请完善下列实验室中除去泥沙等杂质的实验步骤,井回答相关问题:
(1)其中操作a、b.的名称分别是___________,_____________;在操作a中要用到的玻璃仪器有烧杯、玻璃棒、____________(填仪器名称)。
在操作b过程中,当____________时,停止加热。
(2)上述除去泥沙后的澄清滤液中,还含有钙、镁等阳离子。
要想知道该滤液是硬水还是软水,可加入_____________;进行检验。
(3)海水提取出粗盐后的母液中,还含有较多的氯化镁,用氯化铁可制得金属镁。
工业上从母液中提取氯化镁的过程如下:
反应Ⅰ的化学方程式为______________;物质X是______________(填名称)。
(4)工业上可用电解饱和NaCl溶液的方法制得烧碱、氯气和氢气。
请写出该反应的化学方程式:
____________;
(5)从下列装置中选择并组装一套制取干燥二氧化碳气的装置,正确的连接顺序为___________(用接口处字母填写)
(6)写出一个在实验室中用加热法制取氧气的化学方程式:
_________________。
【答案】过滤蒸发漏斗蒸发皿中出现较多固体肥皂水
稀盐酸
a
g
f
c
或
。
【解析】
【分析】
【详解】
(1)含有泥沙的粗盐初步提纯的过程有三步:
溶解、过滤和蒸发,所以操作a、b分别是过滤和蒸发。
过滤操作用到的仪器有烧杯、漏斗和玻璃棒。
蒸发时,当蒸发皿中出现较多固体时停止加热。
故填:
过滤;蒸发;漏斗;蒸发皿中出现较多固体。
(2)上述除去泥沙后的澄清滤液中,还含有钙、镁等阳离子。
要想知道该滤液是硬水还是软水,可加入肥皂水进行检验,当出现较多泡沫和少量浮渣时是软水,当出现较多浮渣和少量泡沫时为硬水。
故填:
肥皂水。
(3)海水提取出粗盐后的母液中,还含有较多的氯化镁,工业上通过加入熟石灰来使氯化镁转化为氢氧化镁沉淀,反应的方程式为:
,再将氢氧化镁沉淀通过加入稀盐酸转化成氯化镁。
故填:
;稀盐酸。
(4)工业上可用电解饱和NaCl溶液的方法制得烧碱、氯气和氢气。
反应物是氯化钠和水,生成物是氢氧化钠、氯气和氢气,方程式为:
。
故填:
。
(5)制取干燥二氧化碳气体的装置,需要固液不加热型的发生装置和浓硫酸做试剂的干燥装置,还有向上排空气法收集气体的收集装置。
故填:
a
g
f
c。
(6)实验室中用加热法制取氧气的化学方程式可以是加热高锰酸钾制氧气或加热氯酸钾与二氧化锰的混合物制氧气。
故填:
或
。
9.制备波尔多液。
某农场需要大量的波尔多液,农场工人就地取材,利用农场废弃的铜渣(只含有铜和一定量的铁),化工厂的废硫酸和农场附近山上的石灰石来制作波尔多液。
下面是制作波尔多液的工艺流程图(注:
所加试剂及操作均省略):
请据图回答下列问题:
(1)写出上述流程1~6中发生化学变化的化学反应方程式:
1______________________。
2______________________。
3______________________。
4______________________。
5______________________。
6______________________。
其中属于复分解反应的是_____________(填流程图中的数字编号)。
(2)喷洒波尔多液后,果农的手上和衣服上会残留一些用水洗不掉的蓝色斑点,这些蓝色斑点属于________(填“酸”、“碱”、“盐”或“氧化物”),在家中洗去衣服上蓝色斑点的是方法是___________________________________。
【答案】CaCO3
CaO+CO2↑CaO+H2O=Ca(OH)2H2SO4+Fe=FeSO4+H2↑2Cu+O2
2CuOCuO+H2SO4=CuSO4+H2OCa(OH)2+CuSO4=Cu(OH)2↓+CaSO4⑤⑥碱用食醋浸泡后用水冲洗
【解析】
【详解】
1、高温煅烧石灰石反应原理:
CaCO3
CaO+CO2↑符合“一变多”,属于分解反应;
2、生石灰与水反应:
CaO+H2O=Ca(OH)2符合“多变一”,属于化合反应;
3、铜渣中含有少量铁,用稀硫酸将铁除去:
H2SO4+Fe=FeSO4+H2↑符合“单质+化合物=新单质+新化合”,属于置换反应;
4、铜加热变为氧化铜:
2Cu+O2
2CuO符合“多变一”,属于化合反应;
5、氧化铜与硫酸反应原理:
CuO+H2SO4=CuSO4+H2O,符合“化合物+化合物=新化合物+新化合物”,反应物离子交换成分,属于分解反应;
6、氢氧化钙与硫酸铜反应原理:
Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4符合“化合物+化合物=新化合物+新化合物”,反应物离子交换成分,属于分解反应;
其中属于复分解反应的是:
⑤⑥;
(2)喷洒波尔多液后,果农的手上和衣服上会残留一些用水洗不掉的蓝色斑点,这些蓝色斑点是氢氧化铜,属于碱性物质,在家中洗去衣服上蓝色斑点的是方法是:
用食醋浸泡后用水冲洗;
10.煤是社会生产、生活中最重要的能源,工业上常把煤进行气化和液化处理,使煤变成清洁能源。
煤气化和液化流程示意图如下:
(1)第①步操作发生的是_____________(填“物理”或“化学”)变化。
(2)第②步是精炼煤与水蒸气的反应,化学方程式为______________________________。
(3)第③步反应的基本类型属于________________________________。
(4)含硫化合物洗液经过提炼后,可用来制硫酸,过程是:
含硫化合物氧化得到SO2,SO2进一步氧化得到X,X与水反应得到H2SO4,则X的化学式为_______________。
(5)从“绿色化学”的角度分析,“煤的汽化和煤的液化”生产流程的优点______。
【答案】物理C+H2O(气)
CO+H2化合反应SO3原料全部被产品消纳(或原料全部转化为产品,或原子利用率100%等),实现“零排放”(或不对环境造成污染等)
【解析】
【分析】
【详解】
(1)该过程没有新的物质生成,只是简单的分离,是物理变化;
(2)煤的主要成分是碳与水反应生成一氧化碳与氢气,反应的化学方程式为:
C+H2O(气)
CO+H2;
(3)该过程中反应物是两种,生成物是一种,符合化合反应的特点,第③步反应的基本类型属于化合反应;
(4)二氧化硫再次氧化可生成三氧化硫,与水反应会生成硫酸,X的化学式为SO3;
(5)绿色化学主要是指反应时反应物全部会转化成生成物,同时实现无排放的过程。
该生产流程的优点是原料全部被产品消纳(或原料全部转化为产品,或原子利用率100%等),实现“零排放”(或不对环境造成污染等)。
11.化工厂用废硫酸制备K2SO4的流程如下:
(1)生产上将CaCO3研成粉末的目的是_______欲达此目的,还可采用的方法是__________(任写一条)
(2)上述流程中,还可循环使用的物质是___(填写化学式).
(3)写出反应①中主要的化学方程式_______
(4)反应③中相关物质的溶解度如下表所示,反应③在常温下可实现的原因是______
物质
KCl
K2SO4
NH4Cl
(NH4)2SO4
溶解度/g(20℃)
34.2
11.1
37.2
75.4
(5)洗涤反应③所得晶体最适宜的试剂是___________(填序号)
AH2OB饱和K2SO4溶液C二者均可
(6)检验K2SO4晶体是否洗涤干净的方法是____________
【答案】加快反应速率搅拌CO2和CaCO3H2SO4+CaCO3=CaSO4+CO2↑+H2O常温下K2SO4的溶解度小B取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,除去硫酸根,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净。
【解析】
【详解】
(1)将CaCO3研成粉末,可以增大反应物的接触面积,其目的是加快反应速率,欲达此目的,还可采用的方法是将反应物混合后充分搅拌;(或其他合理答案)
(2)观察上述流程,发现二氧化碳和碳酸钙既是反应物也是生成物,故可循环使用的物质有CO2和CaCO3;
(3)①中主要的化学方程式:
H2SO4+CaCO3=CaSO4+CO2↑+H2O;
(4)根据复分解反应发生的条件,反应Ⅲ中虽然没有不溶物,但常温下K2SO4的溶解度小,在生成物中会以沉淀的形式出现,故反应可以进行;
(5)洗涤反应③所得晶体最适宜的试剂是饱和硫酸钾溶液,不用水而用饱和K2SO4溶液洗涤反应Ⅲ所得晶体的目的是减少K2SO4的溶解;
(6)银离子和氯离子结合生成氯化银沉淀,为检验此晶体是否洗涤干净,可取最后一次洗涤液,先加入过量的Ba(NO3)2溶液,振荡、静置,目的是除去硫酸根离子,再向上层清液中滴加AgNO3溶液,如果没有白色沉淀,说明洗涤干净。
12.以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:
氯化铵和硫酸钠的溶解度随温度变化如上图所示。
回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl_____g。
(2)实验室进行蒸发浓缩用到的主要仪器有_____、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为_____。
(4)不用其他试剂,检查NH4Cl产品是否纯净的方法及操作是_____。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是_____。
【答案】11.7g蒸发皿3
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 中考 化学 流程图 综合 练习题 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《包装概论》课后习题汇总.docx
《包装概论》课后习题汇总.docx
