 银川市医疗器械经营和使用环节飞行检查信息汇总表模板.docx
银川市医疗器械经营和使用环节飞行检查信息汇总表模板.docx
- 文档编号:24795863
- 上传时间:2023-06-01
- 格式:DOCX
- 页数:190
- 大小:29.97KB
银川市医疗器械经营和使用环节飞行检查信息汇总表模板.docx
《银川市医疗器械经营和使用环节飞行检查信息汇总表模板.docx》由会员分享,可在线阅读,更多相关《银川市医疗器械经营和使用环节飞行检查信息汇总表模板.docx(190页珍藏版)》请在冰豆网上搜索。
银川市医疗器械经营和使用环节飞行检查信息汇总表模板
附件1:
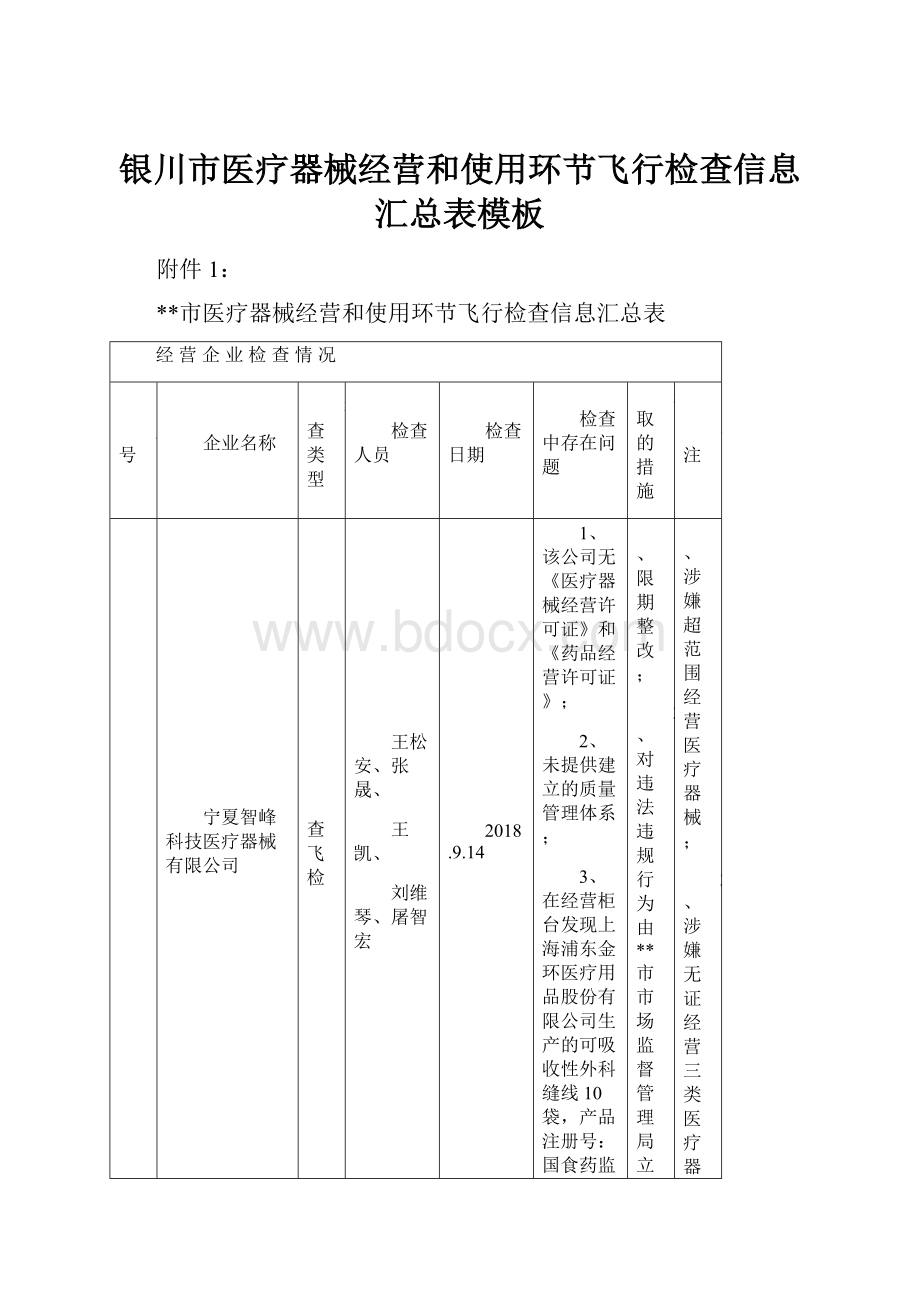
**市医疗器械经营和使用环节飞行检查信息汇总表
经营企业检查情况
序号
企业名称
检查类型
检查人员
检查日期
检查中存在问题
采取的措施
备注
1
宁夏智峰科技医疗器械有限公司
督查飞检
王松安、张晟、
王凯、
刘维琴、屠智宏
2018.9.14
1、该公司无《医疗器械经营许可证》和《药品经营许可证》;
2、未提供建立的质量管理体系;
3、在经营柜台发现上海浦东金环医疗用品股份有限公司生产的可吸收性外科缝线10袋,产品注册号:
国食药监械(准)字2013第********号,规格:
4-090cm紫色,批号:
66S1116B;发现湖北仙明医疗器械有限公司生产的一次性使用无菌注射器(带针)300支,批号:
********,注册证号:
国械注准********,涉嫌无证经营三类医疗器械;
4、在经营柜台发现云南白药创可贴7盒(每盒100片装),批号:
PEE1741,涉嫌无证经营药品;
5、在经营柜台发现三诺血糖试条20余盒,早早孕试条200人份,涉嫌超范围经营。
1、限期整改;
2、对违法违规行为由**市市场监督管理局立案调查。
1、涉嫌超范围经营医疗器械;
2、涉嫌无证经营三类医疗器械。
2
宁夏富宏信宇医疗科技有限公司
督查飞检
王松安、张晟、
王凯、
刘维琴
2018.9.14
1、检查时质量负责人不在现场;2、经营场所与经营范围和经营规模不相适应;3、现场抽取扬州洋生医药科技有限公司生产的一次性使用骨穿包,规格型号:
16#,生产日期********,无法提供产品资质及相关证明文件;4、三类医疗器械席地存放;5、在该公司二楼办公区域存放三类医疗器械一次性使用无菌注射器(带针)。
限期整改
3
宁夏新中科医疗器械有限公司
督查飞检
冯琳、张晟、
沈明辉
王凯
2018.9.14
1、检查时质量负责人不在现场;2、柜台内三类医疗器械区混放有二类医疗器械,一次性使用配药注射器(带针),注册证:
赣食药监械(准)字2014第********号,批号:
********;3、抽取烟台市康贝尔医疗器械有限公司生产的供氧器(型号:
KBR-10L型,出厂日期:
2015年7月15日)、青岛海诺生物工程有限公司生产的无菌敷贴(注册证:
鲁械注准********,批号:
********),现场不能提供供货商资质、产品资质等相关证明文件;4、抽取上海联辉医疗用品有限公司生产的手术刀片(塑柄刀和各种规格刀片),现场不能提供不能提供供货商资质、产品资质等相关证明文件。
限期整改
4
宁夏众康和医疗器械有限公司
督查飞检
冯琳、张晟、
沈明辉、
王凯
2018.9.14
1、库房内无分区,无色标标识管理;未对医疗器械分类摆放,部分医疗器械席地摆放,未离墙离地;2、对储存的医疗器械未进行定期检查,无记录;3、抽取上海医用缝合针厂有限公司生产的手术刀片(注册证:
沪食药监械(准)字2010第********号,批号:
********)现场不能提供供货商资质、产品资质等相关证明文件。
限期整改
5
宁夏陇济堂永盛合医药连锁有限公司庆丰店
督查飞检
张晟、
王凯
2018.9.18
1、未建立质量管理制度;2、未开展医疗器械法律法规和专业知识培训;3、未注册医疗器械不良事件监测用户名;4、抽取欧姆龙(大连)有限公司生产的电子血压计HEM-7300(上臂式)(批号:
********LF),现场不能提供供货商资质、产品资质、检验报告书等相关证明文件。
限期整改
6
宁夏康润达医疗科技有限公司
督查飞检
王松安、沈明辉
2018.9.19
1、冷藏室中医疗器械与食物(葡萄)混放;2、库房温湿度记录造假(提前记录),医疗器械未分类分区摆放,医疗器械与消字号产品混放;3、冷库测点终端超温到12度未报警;4、销售过期产品一次性20ul采血吸管3盒3桶(每盒5桶);5、质管检验员(霍宝清)不在岗,该同志原工作单位是宁夏康元泽润医院,现场不能提供医院离职证明,并且没有签订劳动合同;6、未注册医疗器械不良事件监测用户;7、对人员的医疗器械法律法规知识培训引用的是废止的旧条例,培训流于形式;8、现场未见当地监管部门检查记录。
1、限期整改;
2、对违法违规行为由**市市场监督管理局立案调查。
涉嫌销售过期失效医疗器械。
7
银川海迩斯科贸有限公司
督查飞检
王松安、王凯
2018.9.25
1、企业制定的质量管理文件没有进行起草人、审阅人和批准人签字确认,无制定日期;2、不能严格落实制定的近效期管理制度,库房贮存近效期医疗器械没有区分和登记;3、管理制度中出现废止、错误的法规文件表述,如《医疗器械经营监督管理条例》《医疗器械经营企业许可证》等。
限期整改
8
宁夏卓奥信达医疗器械有限公司
督查飞检
王松安、张晟、王凯
2018.9.26
1、上墙的法规制度都是已经废止的法规要求;2、医疗器械首营企业资质审批表签字为电脑打印,不是手签。
限期整改
9
宁夏涵予商贸有限公司
督查飞检
王松安、张晟、王凯
2018.9.26
1、培训内容中引用废止的法律法规,培训流于形式;2、库房面积小,与经营范围和经营规模不相适应;3、库房三色五区分区划分不合理,验收区设置不合理;4、库房贮存北京哈特凯尔医疗科技有限公司生产的心衰超滤脱水装置(注册证:
国械注准********,规格型号:
FQ-16)现场不能提供购销合同、检验报告和随货同行单;5、该公司经营场所和经营库房2018年3月变更,但未在同一地址,不符合自治区食品药品监督管理局实施《经营规范》要求;6、冷库、冷藏箱未做高温极值验证。
限期整改
10
宁夏百灵科技仪器有限公司
督查飞检
张晟、王凯
2018.9.27
1、抽取希森美康生物科技(无锡)有限公司生产的活化部分凝血活酶时间检测试剂盒(凝固法)(批号:
R8033),现场提供的产品检验报告不符合要求,没有检验依据和质管部的印章;2、冷链交接单时间内容不完整。
限期整改
11
宁夏祥瑞医疗用品有限公司
督查飞检
张晟、王凯
2018.9.27
1、现场不能提供相关质量管理文件;2、检查时质量负责人不在岗;3、现场不能提供医疗器械法律法规、专业知识培训记录;4、现场不能提供健康档案;5、冷库设施未进行验证;6、库房三色五区标识不符合要求,合格产品席地存放,库房内脏乱差;7、2-8℃冷藏器械,冷库温度设置超标,温度到17℃压缩机才开始工作;8、质量负责人不在岗,现场不能提供不良事件注册用户名;9、抽取罗氏总前列腺特异性抗原(PSA)测定试剂盒(电化学发光法)(规格:
100测试/盒,批号:
********)现场不能提供任何冷链相关票据,检验合格报告全部为英文;10、抽取威海威高富森医用材料有限公司生产的非吸收性外科缝线(聚丙烯线)(2-090cmP21262D,批号:
********),现场不能提供检验合格报告;11、罗氏总前列腺特异性抗原(PSA)测定试剂盒(电化学发光法)(规格:
100测试/盒,批号:
********)由联合快递用纸箱加冰块邮寄,到货后未验收产品在途温度便入库。
限期整改
12
宁夏康丰瑞通科技有限公司
督查飞检
王松安、沈明辉、王凯
2018.10.9
1、未在醒目位置悬挂证照,公司门头悬挂银川天恩食品招牌,名不符实;2、培训中使用废止的、编造的医疗器械法规文件,如《医疗器械监督管理办法》,培训流于形式;3、抽取江苏双羊医疗器械有限公司生产的钛质接骨板(解剖型接骨板),规格型号:
指掌骨型5孔90°L形右,批号:
********,生产日期(2009-01-10)和检验日期(2013-03-28)不相符,现场不能提供产品注册证;4、供货商北京爱康宜城医疗器材股份有限公司销售人员法人授权书授权范围显示甘肃地区,不是宁夏地区。
限期整改
13
宁夏弘生源医疗器械有限公司
督查飞检
王松安、沈明辉、王凯
2018.10.9
1、现场不能提供质量管理制度;2、检查时质量负责人不在岗;3、该公司销售大英太极医疗器械有限公司生产的小儿清肺止咳贴(备案号:
川遂宁械备********)、腰椎间盘突出型医用冷敷贴(备案号:
川遂宁械备********)、风湿关节型医用冷敷贴(备案号:
川遂宁械备********)等医疗器械产品,涉嫌非药品冒充药品;以上产品标签显示为太极,涉嫌侵权名牌商标;4、该公司销售山东新陆生物科技有限公司生产的太极咽爽活性银离子喷剂(注册号:
鲁宁食药监械(准)字2014第********号),涉嫌非药品冒充药品。
限期整改
14
银川朗道医疗器械有限公司
督查飞检
王松安、沈明辉、王凯
2018.10.9
1、上墙的质量管理制度引用废止的医疗器械法规;2、检查时企业负责人杜晓川、质量负责人王凤玲和检验员王月珍都不在岗;3、从业人员健康证已过期(发证时间:
2017年7月11日,有效期1年);4、该公司冷库没有使用,未进行验证;使用冷藏箱贮存体外诊断试剂,违反《医疗器械经营质量管理规范》相关要求。
限期整改
15
宁夏星辰医疗器械有限公司
督查飞检
王松安、沈明辉、王凯
2018.10.9
1、上墙的质量管理制度引用废止的医疗器械法规;2、未开展医疗器械专业知识培训;3、抽取浙江科惠医疗器械股份有限公司生产的股骨远端外侧接骨板(型号:
BC29型,生产批号:
********),现场不能提供销售人员法人授权书。
限期整改
16
宁夏六环科技有限公司
督查飞检
王松安、沈明辉、王凯
2018.10.9
1、现场不能提供质量管理制度;2、检查时质量负责人不在岗;3、现场不能提供培训档案;4、销售人员法人授权书过期(有效期至2018年8月31日)。
限期整改
17
宁夏美益康医疗器械有限公司
督查飞检
王松安、沈明辉、王凯、马莹珺
2018.10.10
1、质量管理制度不够规范完善;2、未主动收集不良事件监测报告。
限期整改
18
宁夏昊世盛源科贸有限公司
督查飞检
王松安、沈明辉、王凯、马莹珺
2018.10.10
1、质量管理制度不够完善;2、检查时质量负责人不在岗;3、医疗器械法规培训不够全面;4、未对从业人员进行健康体检;5、冷库制冷机组只有1个,不符合一用一备要求;6、冷藏车没有按要求做极值温度验证;7、未注册不良事件监测用户名。
限期整改
19
宁夏达美医药有限公司
督查飞检
王松安、沈明辉、曹志鹏
2018.10.12
1、现场检查发现,该公司经营体外诊断试剂,但没有聘任检验师;2、现场抽取交锁髓内钉,产品注册号:
国食药监械(准)字2014第********号(更),现场提供的产品标示规格型号与注册证附件上的规格型号标注不一致,注册证左下角栏未载明产品注册登记表,现场也未能提供产品注册登记表;3、质保协议供销双方都没有签字,也没有签署日期;4、现场不能提供一次性使用血液透析管路(批号:
********)随货同行单;5、该公司销售的一类医疗器械小儿清肺止咳贴(产品备案号:
川遂宁械备********号)等产品,产品名称涉及疾病的治疗和诊断,违反医疗器械法规命名要求。
限期整改
使用单位检查情况
序号
企业名称
检查类型
检查人员
检查日期
检查中存在问题
采取的措施
备注
1
银川军大皮肤病医院
督查飞检
王松安、张晟、
王凯
2018.9.17
1、未建立医疗器械相关管理制度,无质量管理体系;2、未开展医疗器械法律法规、专业知识培训;3、对质量管理体系运行情况无考核和评价;4、该院B超无安装调试、无验收报告;5、该院B超无校准、维修保养记录;6、大型医疗器械档案不完整;7、现场不能提供质量管理自查报告;8、该院检验室冷藏箱(现场检查温度7℃)内贮存中生北控生物科技股份有限公司生产的胆固醇校准品,注册号:
京食药监械(准)字2014第********号,批号:
********,贮存条件:
-25℃~-15℃。
贮存不符合要求,现场不能提供供货商资质、产品资质等其他证明文件;9、该院从武汉唯美尔科技有限公司采购的体外诊断试剂缺失冷链记录,在途监控温度涉嫌造假。
1、限期整改;
2、对违法违规行为由**市市场监督管理局立案调查。
涉嫌未按照产品标签标示温度要求储存医疗器械。
2
宁夏华夏中西医结合医院(华夏医院)
督查飞检
王松安、张晟、
王凯
2018.9.17
1、未建立医疗器械相关管理制度,无质量管理体系;2、未开展医疗器械法律法规、专业知识培训;3、对质量管理体系运行情况无考核和评价;4、未建立冷链验收记录;5、检查时库管不在岗;6、未建立大型医疗器械档案;7、未开展不良事件监测工作;8、现场不能提供质量管理工作自查报告;9、该院检验科冷冻箱内贮存康彻思坦生物生产的抗TP标准物质1瓶(批号:
********,有效期至2017年05月11日)、抗HIV-I标准物质1瓶(批号:
********,有效期至2017年02月03日)已过有效期,涉嫌使用过期产品。
1、限期整改;
2、对违法违规行为由**市市场监督管理局立案调查。
涉嫌使用过期失效医疗器械。
3
宁夏新协和医院
督查飞检
张晟、
王凯
2018.9.18
1、未建立医疗器械质量管理体系,无质量管理文件;2、未开展医疗器械法律法规、专业知识培训;3、库房内未划分医疗器械贮存专区,医疗器械和药品、不合格品混放;4、没有对医疗器械贮存冰柜温度、湿度进行监测记录;5、无效期管理制度,无记录;6、未建立大型医疗器械档案;7、未按要求进行维护、保养,无相关记录;8、使用过期、失效医疗器械;9、未开展不良事件监测工作;10、在该院检验科冰柜中发现贮存北京利德曼生化股份有限公司生产的单一液体60m2瓶(注册号:
京药监械(准)字2012第********号,生产批号:
********K,失效日期:
2017.05.24)、P校准品3ml1瓶(批号:
********K,失效日期:
2017.05.24)、肌酸激酶同工酶质控品1瓶(注册号:
京械注准********,批号:
********A,失效日期:
2018.07.11)、总胆红素及直接胆红素校准品1盒(注册号:
京械注准********,批号:
********K,失效日期:
2018.05.20)、;淀粉酶(AMY)测定试剂盒(EPS底物法)1盒(注册号:
京械注准********,批号:
********J,失效日期:
2018.04.13),以上产品全部过期,涉嫌使用过期医疗器械。
11、在该院检验科冰柜中发现贮存武汉明德生物科技股份有限公司生产的糖化血红蛋白(HbA1c)检测试剂盒5袋(批号;********,有效期至:
2018/08/25,标示:
仅供临床试验用),涉嫌使用未经注册产品。
12、抽取深圳市新产业生物医学工程股份有限公司生产的血清透明质酸(HA)测定试剂盒(化学发光法),生产批号:
********,现场提供的供货方兰州九州通医疗器械有限公司签订的《医疗器械质量保证协议书》无进货方盖章,无有效期,属无效协议书;现场不能提供检验报告等相关资质。
13、存放药品医疗器械的冷藏柜内放有食用肉制品。
1、限期整改;
2、对违法违规行为由**市市场监督管理局立案调查。
1、涉嫌使用过期失效医疗器械;2、涉嫌使用未经注册医疗器械。
4
银川维多利亚医疗器械美容有限公司
督查飞检
王松安、冯琳、沈明辉
2018.9.18
1、检查中发现近效期试剂未单独存放,如梅甲苯胺红不加热血清实验诊断试剂(生产批号********,有效期********);2、血液样本和其他人体采集样本与试剂混放;3、存放需冷藏试剂的冰箱内未设置任何温湿度监测装置;
4、该院质量管理体系不完善,未开展医疗器械法规知识培训;5、伊可颜医用自交联透明质酸钠凝胶(批号********)无随货同行单和批检验报告;6、需冷藏的体外诊断试剂未做温度验收记录;7、该院与西安高创生物科技有限公司签订的质量保证协议书未签字,并已过期;8、未进行医疗器械质量管理自查工作。
限期整改
5
银川中美宁大医院有限公司
督查飞检
王松安、冯琳、沈明辉
2018.9.18
1、声泰特(成都)科技有限公司生产的SASET超声彩色多普勒诊断仪(iMagoc21,规格1300Hx570wx760Dmm)现场不能提供相关资质,大型医疗设备未建档;2.现场抽取的郑州安图生物科技股份有限公司生产的支原体培养鉴定计数药敏试剂盒(********)不能提供相关资质,未建立并履行进货查验制度;
3.未建立质量管理体系,未开展医疗器械质量管理自查工作,未开展医疗器械专业法规知识培训,未见当地监管部门医疗器械检查记录。
限期整改
6
宁夏康元泽润医院
督查飞检
张晟、
王凯
2018.9.18
1、医疗器械质量管理文件建立不全;2、未开展医疗器械法律法规、专业知识培训;3、无采购验收管理制度;4、购进体外诊断试剂现场不能提供冷链验收记录;5、无效期管理制度,无相关记录;6、未建立大型医疗器械档案;7、未按要求进行维护、保养,无相关记录;8、未开展不良事件监测工作;9、在该院检验科冷藏柜中发现贮存潍坊三维生物工程集团有限公司生产的乙型肝炎病毒表面抗原诊断试剂盒(酶联免疫法)1盒(生产批号:
********,有效期至:
2018.09.01)、肌酸激酶同工酶(2ml)1瓶(有效期至********)、上海血液生物医药有限责任公司生产的抗A抗B血型定型试剂(单克隆抗体)1盒(生产批号:
********,有效期至********)、株洲康乐试剂有限公司生产的多功能染色液(BTR)1盒(生产批号:
********/05,有效期两年),以上产品全部过期,涉嫌使用过期、失效产品。
10、在该院检验科冷藏柜中发现贮存中山大学达安基因股份有限公司生产的人乳头瘤病毒(HPV)16,18型核酸扩增(PCR)荧光检测试剂盒1盒(生产批号;********,有效期至:
********,标示:
仅供研究,不用于临床诊断),涉嫌使用未经注册产品。
11、抽取北京万泰德瑞诊断技术有限公司生产的尿微量白蛋白测定试剂盒(免疫比浊法)(注册证:
京械注准********,生产批号:
SG8101A),现场不能提供供货商资质、产品资质、检验报告等相关资质。
1、限期整改;
2、对违法违规行为由**市市场监督管理局立案调查。
1、涉嫌使用过期失效医疗器械;2、涉嫌使用未经注册医疗器械。
7
银川爱康国宾综合门诊部(有限公司)
督查飞检
冯琳、
张晟、
王凯
2018.9.19
1、未建立医疗器械质量管理体系,质量管理文件不健全;2、未开展医疗器械法律法规、专业知识培训;3、质量管理体系无考核,无评价;4、现场未能提供抽取产品供货商资质、产品资质及其他证明文件;5、因人员不在岗,现场不能提供进货查验记录;6、冷藏柜温度计损坏,无法有效监测温度数据;7、无效期管理制度;8、现场不能提供大型设备档案;9、现场不能提供医疗器械维护维修相关记录;10、未开展不良事件监测工作;11、未对医疗器械质量管理工作进行自查;12、在该院检验科冷藏柜内贮存有华兰生物疫苗有限公司生产的重组乙型肝炎疫苗(汉逊酵母)2盒(产品批号:
********A005,有效期至:
2018.03.09)。
限期整改
8
**大学总医院心脑血管病医院
督查飞检
王松安、
王凯
2018.9.25
1、未建立质量管理体系;2、未开展医疗器械法律法规、专业知识培训;3、未严格履行进货查验制度;4、医疗器械库房面积太小,没有按规定进行三色五区划分,产品靠墙码放,产品堆放过高,库房温度(25℃)不符合产品标签标示温度要求(阴凉干燥),库房漏水;5、检验科医疗器械库房无温度、湿度数据记录;6、未开展不良事件监测工作;7、未进行质量管理工作自查,无自查报告;8、抽取华臣诊断试剂(批号:
01HBDH********)、水胶体敷料(规格型号:
3536,批号:
********)现场不能提供供货商资质、产品资质等证明文件。
限期整改
9
宁夏虹桥怡康妇产医院
督查飞检
王松安、
沈明辉
2018.9.28
1、未开展医疗器械法规专业知识培训;2、库房医疗器械与非医疗器械混放,靠墙码放;3、现场抽查美国GE公司生产的E8超声诊断仪(注册证号国械注进********),未能提供大型设备档案;4、现场未能提供医疗机构自查报告。
限期整改
10
宁夏慈安妇儿医院
督查飞检
王松安、
沈明辉
2018.9.28
1、该院质量管理制度引用废止的法规文件;2、未建立效期管理制度;3、未开展医疗器械法律法规专业知识培训;4、未对医疗器械质量管理工作进行自查,并未形成报告;5、现场检查飞利浦(彩色超声诊断系统)B超,注册证号:
CFDA
(1)********不能提供有关购销合同、注册证等资质,该机配套探头C5-1、S5-2与机身铭牌标签不一致。
限期整改
11
贺兰县人民医院
督查飞检
王松安、沈明辉、曹志鹏
2018.10.12
1、医疗器械质量管理制度不完善;2、未开展医疗器械专业知识法规培训;3、抽检善释.疝修补片(国械注准********,批号:
********)无购进企业法人授权委托书;4、现场检查发现,多项免疫类质控液(注册号:
京食药监械准字2014第********号,批号:
********C)、糖化血红蛋白校准品(注册号:
京械注准********,批号:
********)、Fer质控品(2水平×1支×0.6ml,批号:
********)三盒产品过期;5、医疗器械库房面积过小不符合存储要求,不能按照规范要求进行分类分区储存;6、未按要求进行冷链产品到货温度验收;7、现场抽查DR设备,不能提供大型设备档案及使用维护记录;8、未建立医疗器械不良事件监测工作制度,并开展相关工作。
1、限期整改;
2、对违法违规行为由贺兰县市场监督管理局立案调查。
涉嫌使用过期失效医疗器械。
附件2:
**市医疗器械经营使用环节飞行检查信息汇总表
经营企业检查情况
序号
企业名称
检查类型
检查人员
检查日期
检查中存在问题
采取的措施
备注
1
**市佰弘达商贸有限公司
督查飞检
王松安、张晟、
王凯、
何香莲
2018.8.30
1、检查时质量负责人雷艳丽、主管检验师周丽不在岗,现场不能提供周丽前任单位的离职证明文件;2、培训计划中出现了《医疗器械监管办法》《医疗器械经营许可证管理办法》等不符合实际的内容,培训针对性不强;3、培训记录不真实,专业法规知识培训欠缺,培训流于形式;4、对冷库冷藏柜未做极值温度验证;5、没有注册医疗器械不良事件监测用户名。
限期整改
2
**市宝康医疗器械有限公司
督查飞检
王松安、张晟、
王凯、
何香莲
2018.8.30
1、检查时质量负责人马晓超不在岗;2、没有注册医疗器械不良事件监测用户名。
限期整改
3
宁夏德融泽医药连锁有限公司隆湖店
督查飞检
王松安、张晟、
王凯
2018.8.31
1、抽取深圳市优瑞恩科技有限公司生产的臂式电子血压计(型号:
U80BH,生产批号:
BGL017)、北京健新医疗器械有限公司生产的医用固定带(规格型号:
YWP-M,生产批
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 银川市 医疗器械 经营 使用 环节 飞行 检查 信息 汇总表 模板
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《当代世界政治与经济》.docx
《当代世界政治与经济》.docx
