 专题检测卷十++32.docx
专题检测卷十++32.docx
- 文档编号:24328394
- 上传时间:2023-05-26
- 格式:DOCX
- 页数:14
- 大小:630.70KB
专题检测卷十++32.docx
《专题检测卷十++32.docx》由会员分享,可在线阅读,更多相关《专题检测卷十++32.docx(14页珍藏版)》请在冰豆网上搜索。
专题检测卷十++32
温馨提示:
此套题为Word版,请按住Ctrl,滑动鼠标滚轴,调节合适的观看比例,答案解析附后。
专题检测卷(十)
(45分钟100分)
一、单项选择题(本大题共6小题,每小题4分,共24分,在每小题给出的四个选项中只有一个选项符合题目要求,选对的得4分,选错或不答的得0分)
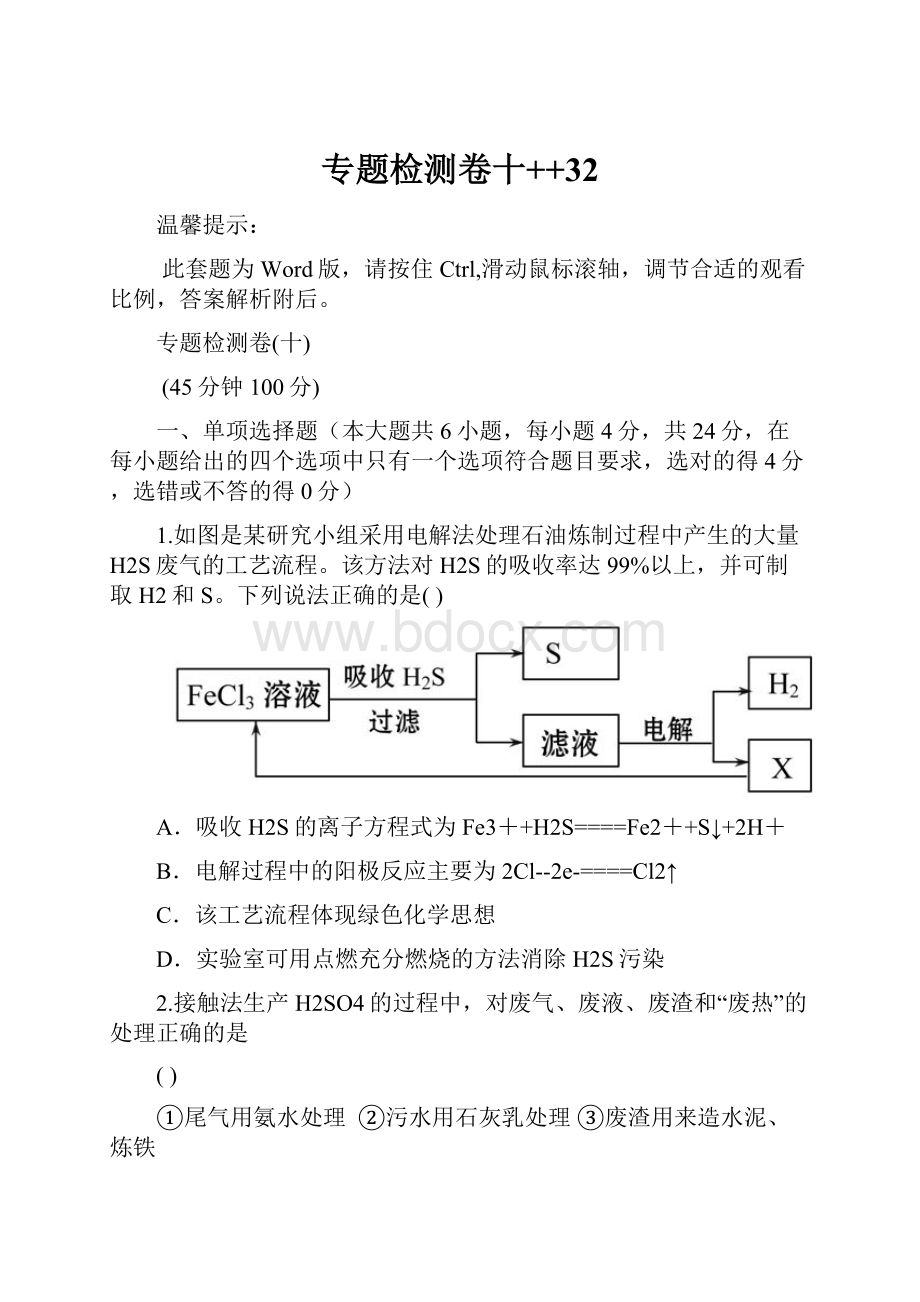
1.如图是某研究小组采用电解法处理石油炼制过程中产生的大量H2S废气的工艺流程。
该方法对H2S的吸收率达99%以上,并可制取H2和S。
下列说法正确的是()
A.吸收H2S的离子方程式为Fe3++H2S====Fe2++S↓+2H+
B.电解过程中的阳极反应主要为2Cl--2e-====Cl2↑
C.该工艺流程体现绿色化学思想
D.实验室可用点燃充分燃烧的方法消除H2S污染
2.接触法生产H2SO4的过程中,对废气、废液、废渣和“废热”的处理正确的是
()
①尾气用氨水处理②污水用石灰乳处理③废渣用来造水泥、炼铁
④设置“废热”锅炉产生蒸汽,供热或发电
A.只有①②B.只有①③④
C.只有①②③D.全部
3.(2012·中山一模)海洋约占地球表面积的71%,对其进行开发利用的部分流程如图所示。
下列说法不正确的是()
A.可用BaCl2溶液除去粗盐中的
B.从苦卤中提取Br2的反应的离子方程式为2Br-+Cl2====2Cl-+Br2
C.试剂1可以选用石灰乳
D.工业上,电解熔融Mg(OH)2冶炼金属镁
4.下列有关化工生产的说法中,不正确的是()
A.工业上用热还原法冶炼铁:
Fe2O3+3CO
3CO2+2Fe
B.适当提高合成氨原料气中N2的含量,可提高H2的转化率
C.在铁管上镀锌,用铁管作阳极,锌块作阴极
D.利用反应:
NaCl(饱和)+CO2+NH3+H2O====NaHCO3↓+NH4Cl制取NaHCO3时,应先通入过量的NH3,再通入过量的CO2
5.(2012·淮安二模)美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(工业流程如图所示)。
下列有关该工艺的说法中错误的是()
A.该过程能量转化的形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金与水的反应属于置换反应
D.总反应式为:
2H2O====2H2↑+O2↑
6.天然海水中主要含有Na+、K+、Ca2+、Mg2+、Cl-、
-、Br-、
、
等离子,火力发电燃煤排放的含SO2的烟气可利用海水脱硫,其工艺流程如图所示:
下列说法错误的是()
A.天然海水pH≈8的原因是海水中的
、
水解
B.“氧化”是利用氧气将
、
等氧化生成
C.“反应、稀释”时加天然海水的目的是中和、稀释经氧气氧化后海水中生成的酸
D.“排放”出来的海水中
的物质的量浓度与进入吸收塔的天然海水相同
二、双项选择题(本大题共2小题,每小题6分,共12分,在每小题给出的四个选项中有两个选项符合题目要求,全部选对的得6分,只选一个且正确的得3分,有选错或不答的得0分)
7.(2012·湛江二中模拟)某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下:
下列说法中,错误的是()
A.操作①发生的反应为氧化还原反应
B.若在实验室进行操作①只需要漏斗和烧杯两种玻璃仪器
C.操作②是蒸发、浓缩、结晶
D.在整个制备过程中,未发生置换反应
8.铜的冶炼过程大致可分为:
①富集,将硫化物矿进行浮选;
②焙烧,主要反应为2CuFeS2+4O2====Cu2S+3SO2+2FeO(炉渣);
③制粗铜,在1200℃发生的主要反应为2Cu2S+3O2====2Cu2O+2SO2;2Cu2O+Cu2S====6Cu+SO2↑;
④电解精炼铜。
下列说法正确的是()
A.冶炼过程中的尾气可用来制硫酸
B.上述过程中,由1molCuFeS2制取1molCu时共消耗2molO2
C.在反应2Cu2O+Cu2S====6Cu+SO2↑中,只有Cu2O作氧化剂
D.电解精炼铜的过程中,每转移1mol电子时,阳极溶解铜的质量小于32g
三、非选择题(本大题共4小题,共64分,按题目要求作答)
9.(18分)(2012·大纲版全国卷)
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。
为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。
回答下列问题:
(1)起始滤液的pH7(填“大于”“小于”或“等于”),其原因是
;
(2)试剂Ⅰ的化学式为,①中发生反应的离子方程式为
;
(3)试剂Ⅱ的化学式为,②中加入试剂Ⅱ的目的是
;
(4)试剂Ⅲ的名称是,③中发生反应的离子方程式为
;
(5)某同学称取提纯的产品0.7759g,溶解后定容在100mL容量瓶中,每次取25.00mL溶液,用0.1000mol·L-1的硝酸银标准溶液滴定,三次滴定消耗标准溶液的平均体积为25.62mL,该产品的纯度为
(列式并计算结果)。
10.(16分)(2012·广州二模)硫酸铅广泛应用于制造蓄电池、白色颜料等。
利用锌冶炼过程中的铅浮渣生产硫酸铅的流程如下:
已知铅浮渣的主要成分是PbO、Pb,还含有少量Ag、Zn、CaO和其他不溶于硝酸的杂质。
25℃时,Ksp(CaSO4)=4.9×10-5,Ksp(PbSO4)=1.6×10-8。
(1)已知步骤Ⅰ有NO产生,浸出液中含量最多的阳离子是Pb2+。
分别写出PbO、Pb参加反应的化学方程式、。
(2)步骤Ⅰ需控制硝酸的用量并使Pb稍有剩余,目的是
。
(3)母液可循环利用于步骤Ⅰ,其溶质主要是(填一种物质的化学式),若母液中残留的
过多,循环利用时可能出现的问题是。
(4)产品PbSO4还需用Pb(NO3)2溶液多次洗涤,目的是除去。
(5)铅蓄电池的电解液是硫酸,充电后两个电极上沉积的PbSO4分别转化为PbO2和Pb,充电时阴极的电极反应式为。
11.(18分)(2012·佛山二模)钯(Pd)的性质与铂相似。
工业上从废催化剂(主要成分是钯和活性炭,还含有少量铁、锌)中回收钯,采用如图流程:
请回答下列问题:
(1)酸溶Ⅰ的目的是。
(2)①酸溶Ⅱ时残渣与王水在加热条件发生的主要反应是:
3Pd+12HCl+2HNO3
3H2PdCl4+2NO↑+4H2O
写出催化剂中另一种主要成分与浓硝酸反应的化学方程式:
。
②酸溶Ⅱ需控制温度不宜过高,除了控制一定反应速率外,其原因可能还有
。
③若用足量的烧碱吸收气体,请写出吸收后溶液中含有的溶质的化学式:
NaOH、NaNO2、、。
(3)使用甲醛还原钯的化合物时,溶液须保持碱性,否则会造成甲醛的额外损耗,原因是。
(4)操作Ⅰ的名称是,溶液Ⅰ可能含有的有机离子为。
(5)有人提出,在进行酸溶前最好先将废催化剂在700℃下进行灼烧,同时不断通入空气,其目的是
。
12.(12分)(2012·山东高考改编)工业上由黄铜矿(主要成分为CuFeS2)冶炼铜的主要流程如下:
(1)气体A中的大气污染物可选用下列试剂中的吸收。
a.浓硫酸b.稀硝酸
c.NaOH溶液d.氨水
(2)用稀硝酸浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,说明溶液中存在(填离子符号),检验溶液中还存在Fe2+的方法是
(注明试剂、现象)。
(3)由泡铜冶炼粗铜的化学反应方程式为
。
答案解析
1.【解析】选C。
选项A不符合电荷守恒,正确的离子方程式为
2Fe3++H2S====2Fe2++S↓+2H+,所得滤液中含有Fe2+、H+和Cl-,由于还原性
Fe2+>Cl-(或根据图示循环),电解时阳极反应式为Fe2+-e-====Fe3+,故B错。
由于H2S充分燃烧的化学方程式为2H2S+3O2====2SO2+2H2O,生成的SO2也是一种有毒气体,故D也错。
2.【解析】选D。
3.【解析】选D。
Ba2++SO42-====BaSO4↓,可知A正确。
由流程图可知从苦卤中提取Br2发生了反应2Br-+Cl2====2Cl-+Br2,所以B正确。
试剂1的作用是沉淀Mg2+,所以C正确。
工业上用电解熔融MgCl2的方法冶炼金属镁,所以D错误。
4.【解析】选C。
在电镀过程中,一般用镀层金属作阳极,镀件金属作阴极,用含有镀层金属阳离子的溶液作电解液,因此在铁管上镀锌,应用锌块作阳极,铁管作阴极,C说法错误。
其余说法均符合工业生产实际,正确。
5.【解析】选A。
该过程能量转化的形式有3种,A错误。
由所给工业流程图可知B正确。
铝镓合金与水的反应的实质是铝把水中的H置换出来,属于置换反应,C正确。
由图可知该流程的总反应为2H2O====2H2↑+O2↑,D正确。
6.【解析】选D。
D项,排放出的海水中吸收了SO2气体,并通过氧化生成了
,故
的物质的量浓度大于进入吸收塔的天然海水,故不正确。
7.【解析】选A、B。
操作①发生的反应为MgCl2+Ca(OH)2====Mg(OH)2↓+CaCl2,为复分解反应,不是氧化还原反应,A项错误;操作①为过滤,实验室中除需要漏斗、烧杯外,还需要玻璃棒引流,B项错误;整个过程中发生的反应还有Mg(OH)2+2HCl====MgCl2+2H2O,
,C、D项正确。
8.【解析】选A、D。
1molCuFeS2反应,焙烧时需要氧气2mol,生成的Cu2S转化为Cu2O还需要氧气,B不正确;C项中作氧化剂的除Cu2O外还有Cu2S,C不正确;电解精炼铜时阳极除溶解铜外还溶解比较活泼的金属,当转移1mol电子时,溶解铜的量小于0.5mol,即小于32g。
9.【解析】
(1)起始滤液中含有碳酸钾,碳酸根水解呈碱性,故溶液的pH大于7。
(2)要除掉杂质离子硫酸根离子和碳酸根离子,应加入过量的钡离子,又不能引入其他离子,因此试剂Ⅰ选用BaCl2溶液,与
和
均能反应。
(3)要除掉多余的钡离子,所需试剂必须既能除去过量的Ba2+,又不能引入其他杂质且过量离子较易除去,因此选用K2CO3。
(4)要除掉多余的碳酸根离子,要滴加过量的盐酸。
(5)计算样品的纯度,注意0.7759g样品配成100mL溶液,每次只取
25.00mL;另外从本题所给数据来看需保留四位有效数字。
答案:
(1)大于强碱弱酸盐K2CO3发生水解使体系呈碱性
(2)BaCl2
-+Ba2+====BaSO4↓、
+Ba2+====BaCO3↓
(3)K2CO3除去A中的Ba2+
(4)盐酸
+2H+====CO2↑+H2O
(5)w=
10.【解析】
(1)因浸出液中含量多的阳离子为Pb2+,可知PbO、Pb与硝酸反应的生成物为Pb(NO3)2。
(2)因为Ag可与硝酸发生反应:
3Ag+4HNO3====3AgNO3+NO↑+2H2O,故应控制硝酸不宜过量并使Pb稍有剩余,防止Ag被溶解进入溶液导致所得PbSO4纯度降低。
(3)由流程图可知,浸出液中的阳离子除Pb2+外,还含有Zn2+和Ca2+,当加入40%硫酸时,因ZnSO4易溶,而Ksp(CaSO4)>Ksp(PbSO4),故步骤Ⅱ所得沉淀主要为PbSO4,发生反应为Pb(NO3)2+H2SO4====PbSO4↓+2HNO3,母液中溶质主要为HNO3及少量Zn(NO3)2、Ca(NO3)2等;若母液中残留
过多,则会在浸出时部分Pb2+生成PbSO4随浸出渣排出而降低PbSO4产率。
(4)在步骤Ⅱ所得滤渣中会含少量CaSO4杂质,因Ksp(CaSO4)>Ksp(PbSO4),当用Pb(NO3)2溶液洗涤沉淀时,CaSO4会转化为溶解度更小的PbSO4,从而除去CaSO4杂质。
(5)铅蓄电池充电时为电解池,电解池阴极发生还原反应,其电极反应式为PbSO4+2e-====Pb+
。
答案:
(1)PbO+2HNO3====Pb(NO3)2+H2O
3Pb+8HNO3====3Pb(NO3)2+2NO↑+4H2O
(2)防止Ag被溶解进入溶液(或使Ag留在浸出渣中)
(3)HNO3浸出时部分铅离子生成PbSO4随浸出渣排出,降低PbSO4的产率
(4)CaSO4杂质
(5)PbSO4+2e-====Pb+
11.【解析】
(1)酸溶Ⅰ使用了盐酸,它能溶解掉铁、锌等杂质。
(2)①废催化剂中含有活性炭,它在加热时可与王水中的硝酸发生下列反应:
C+4HNO3(浓)
CO2↑+4NO2↑+2H2O。
②酸溶Ⅱ需控制温度不宜过高,因为较高温度时硝酸会分解,且盐酸、硝酸会挥发。
③若用足量的烧碱吸收气体,则CO2经反应生成Na2CO3,NO2与烧碱反应生成NaNO2,N的化合价降低,所以同时会生成NaNO3。
(3)使用甲醛还原钯的化合物时,溶液须保持碱性,因为酸性时甲醛会被硝酸氧化。
(4)操作Ⅰ为过滤,经过滤可得到金属单质钯,甲醛碱性条件下被还原生成HCOO-。
(5)在进行酸溶前最好先将废催化剂在700℃下进行灼烧,同时不断通入空气,可以除去废催化剂中的活性炭,从而减少王水的消耗。
答案:
(1)除去铁、锌等杂质
(2)①C+4HNO3(浓)
CO2↑+4NO2↑+2H2O
②防止硝酸分解,防止盐酸、硝酸挥发
③NaNO3Na2CO3
(3)酸性条件下,甲醛会被硝酸氧化
(4)过滤HCOO-
(5)除去废催化剂中的活性炭,减少王水的消耗
【易错提醒】
(1)回答酸溶Ⅱ需控制温度不宜过高的原因时只考虑硝酸的不稳定性,忽略了硝酸、盐酸的挥发性。
(2)用足量的烧碱吸收气体,分析NO2与氢氧化钠的反应时不能从电子得失守恒判断反应的产物。
12.【解析】
(1)从冰铜的元素组成上看,其中含有硫元素,焙烧产物泡铜和熔渣中不再含有硫元素,故可推知A一定为SO2,一般选用碱性溶液,故答案为c、d。
(2)向溶液中滴加KSCN溶液,溶液呈红色,可推知溶液中一定含有Fe3+;要检验溶液中还含有Fe2+,可取适量酸性KMnO4溶液于一支试管中,滴入几滴该溶液,若酸性高锰酸钾溶液褪色或变浅,说明该溶液中含有Fe2+。
(3)泡铜制取粗铜,是Cu2O和铝发生氧化还原反应,根据氧化还原反应的配平方法进行配平可得,化学反应方程式为3Cu2O+2Al
Al2O3+6Cu。
答案:
(1)c、d
(2)Fe3+可取适量酸性KMnO4溶液于一支试管中,滴入几滴该溶液,若酸性高锰酸钾溶液褪色或变浅,说明该溶液中含有Fe2+
(3)3Cu2O+2Al
Al2O3+6Cu
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题 检测 32
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《当代世界政治与经济》.docx
《当代世界政治与经济》.docx
