 苏教版高中化学必修一专题2 检测试题.docx
苏教版高中化学必修一专题2 检测试题.docx
- 文档编号:2416207
- 上传时间:2022-10-29
- 格式:DOCX
- 页数:9
- 大小:67.29KB
苏教版高中化学必修一专题2 检测试题.docx
《苏教版高中化学必修一专题2 检测试题.docx》由会员分享,可在线阅读,更多相关《苏教版高中化学必修一专题2 检测试题.docx(9页珍藏版)》请在冰豆网上搜索。
苏教版高中化学必修一专题2检测试题
专题2 检测试题
(时间:
45分钟 满分:
100分)
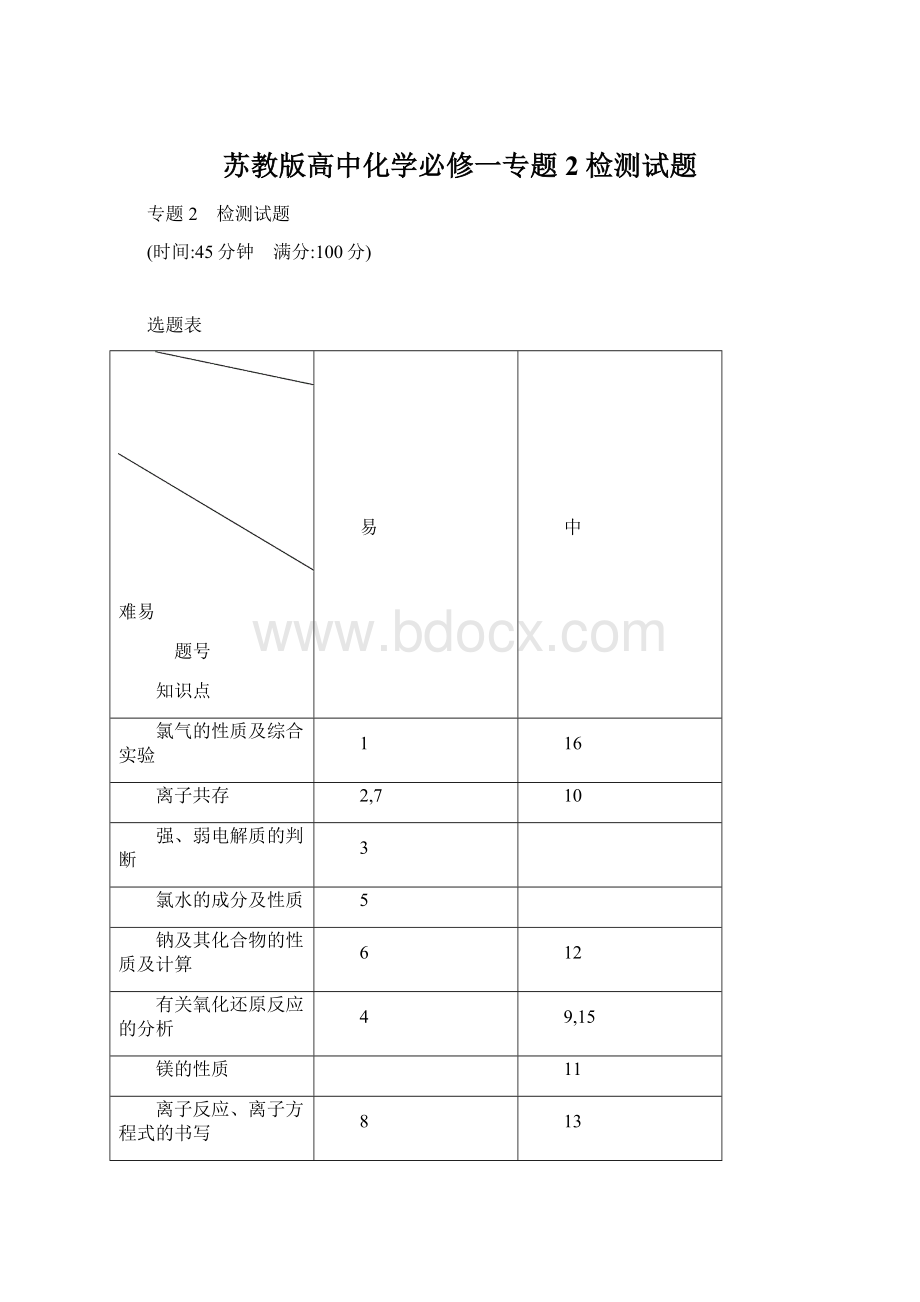
选题表
难易
题号
知识点
易
中
氯气的性质及综合实验
1
16
离子共存
2,7
10
强、弱电解质的判断
3
氯水的成分及性质
5
钠及其化合物的性质及计算
6
12
有关氧化还原反应的分析
4
9,15
镁的性质
11
离子反应、离子方程式的书写
8
13
海水的综合应用
14
一、选择题(共12小题,每小题4分,共48分)
1.(2012山东青岛质检)下列关于氯的说法中正确的是( C )
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.Cl2和NaCl中均含有氯元素,它们的化学性质相同
C.实验室制备Cl2可用排饱和食盐水集气法收集
D.氯气、液氯和氯水是一种物质
解析:
Cl2中氯元素的化合价为0价,既可升高也可降低,故在化学反应中Cl2既可作氧化剂也可作还原剂,A错;Cl2与NaCl的化学性质不同,B错;在饱和食盐水中Cl-浓度大,氯气在其中的溶解度小,收集Cl2可用排饱和食盐水法集气,C正确;Cl2和液氯是Cl2的不同状态,是纯净物,属于同一种物质,但氯水中除Cl2外,还有Cl-、ClO-、HClO、H2O等其他微粒,是混合物,故Cl2、液氯和氯水不是同一种物质,D错。
2.(2012雅安中学高一期中)下列能在溶液中大量共存的离子组是( C )
A.Cu2+、S、OH-、K+B.Na+、C、H+、Cl-
C.H+、Cl-、N、Ba2+D.Ca2+、H+、C、N
解析:
A项,Cu2+能和OH-反应生成Cu(OH)2沉淀;B项,C和H+反应可生成H2O和CO2;D项,Ca2+和C反应生成CaCO3沉淀,H+与C反应生成CO2和H2O。
3.下列各组物质中,前者为强电解质,后者为弱电解质的是( D )
A.硫酸,硫酸钡B.NH3,氢氧化钠
C.食盐,酒精D.碳酸钠,醋酸
解析:
A项,两者均为强电解质;B项,前者为非电解质,后者为强电解质;C项,前者为强电解质,后者为非电解质;D项,前者为强电解质,后者为弱电解质。
故应选D。
4.对于反应3Cl2+6NaOH5NaCl+NaClO3+3H2O,以下叙述中正确的是( C )
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的Cl原子和被还原的Cl原子的物质的量的比为5∶1
C.Cl2既是氧化剂又是还原剂
D.每生成1mol的NaClO3转移6mol的电子
解析:
该反应的电子转移情况为:
可得Cl2既是氧化剂又是还原剂,被氧化的Cl原子和被还原的Cl原子的物质的量的比为1∶5,每生成1mol的NaClO3转移5mol的电子。
故应选C。
5.(2013江阴期中)下列说法正确的是( B )
A.氯气是一种具有刺激性气味的无色气体
B.新制氯水可使蓝色石蕊试纸先变红后褪色
C.光照氯水有气泡逸出,该气体是Cl2
D.铁分别与氯气、盐酸反应时得到相同的氯化物
解析:
氯气是一种具有刺激性气味的黄绿色气体,A错;新制氯水中含有H+和HClO,且HClO具有漂白性,故B正确;氯水经光照后HClO分解产生氧气和氯化氢,C错;铁与氯气反应得到高价铁的化合物——FeCl3,铁与盐酸反应得到低价铁的化合物——FeCl2,D错。
6.下面有关Na2CO3与NaHCO3的性质比较中错误的是( C )
A.相同浓度溶液的碱性:
Na2CO3>NaHCO3
B.在水中的溶解度:
Na2CO3>NaHCO3
C.与同浓度的硫酸溶液反应放出气泡的速率:
NaHCO3 D.热稳定性: NaHCO3 解析: Na2CO3与NaHCO3与硫酸反应的离子方程式分别为: ①C+H+HC;②HC+H+H2O+CO2↑。 生成CO2等量的气体,所需的酸的量前者多。 与等浓度的硫酸溶液反应,前者需通过①②两步反应才能生成CO2,后者只需②一步就生成CO2,前者生成气体的速率比较慢。 故应选C。 7.下列有关氯水的叙述中正确的是( B ) A.新制氯水只含有氯分子和次氯酸分子 B.新制氯水可使紫色石蕊试液先变红后褪色 C.氯水光照时有气泡逸出,该气体的主要成分是氯气 D.氯水放置数天后,其酸性逐渐减弱 解析: A项,新制氯水中含有Cl2、H2O、HClO三种分子,错误;B项,含HCl和HClO,显酸性,HClO有强氧化性,能漂白,正确;C项,氯水光照时逸出的气泡为HClO分解生成的氧气,错误;D项,氯水放置数天后HClO分解生成HCl,溶液酸性逐渐增强,错误。 故应选B。 8.(2012北京海淀检测)某同学在实验室中进行如下实验: 编号 Ⅰ Ⅱ Ⅲ 实验 现象 没有明显变化, 溶液仍为无色 有沉淀生成, 溶液为蓝色 有无色 气体放出 以下结论中正确的是( C ) A.Ⅰ中无明显变化,说明两溶液不反应 B.Ⅱ中的白色沉淀为CuCl2 C.Ⅲ中的离子方程式为2H++ZnZn2++H2↑ D.Ⅲ中发生的反应不是离子反应 解析: Ⅰ中NaOH与H2SO4发生中和反应,无明显现象,A错;Ⅱ中产生的白色沉淀是BaSO4,B错;Ⅲ中发生锌与稀HCl发生置换反应: Zn+2HClZnCl2+H2↑,其离子方程式为: 2H++ZnZn2++H2↑,故C对,D错。 9.(2013哈尔滨高一模拟)已知: 2KMnO4+16HCl2KCl+2MnCl2+5Cl2↑+8H2O,K2Cr2O7+14HCl2KCl+2CrCl3+3Cl2↑+7H2O,MnO2+4HClMnCl2+Cl2↑+2H2O,其中,KMnO4和一般浓度的盐酸即可反应,K2Cr2O7需和较浓盐酸(>6mol/L)反应,MnO2需和浓盐酸(>8mol/L)反应。 根据以上信息,下列结论中不正确的是( D ) A.上述反应既属于氧化还原反应,又属于离子反应 B.生成1molCl2转移电子数均为2NA C.盐酸浓度越大,Cl-的还原性越强 D.氧化性: KMnO4>K2Cr2O7>Cl2>MnO2 解析: 审题时观察方程式,发现三个反应中均有盐酸参与,且都有氯气生成,再结合题给信息,氧化性的顺序为KMnO4>K2Cr2O7>MnO2>Cl2。 以上三个反应均为溶液中的离子反应且有化合价升降,A项正确;根据Cl-被氧化生成Cl2,B项正确;结合题给盐酸的浓度知,盐酸浓度越大,Cl-的还原性越强,C项正确。 10.(2012陕西师大附中期末)在碱性溶液中能大量共存且溶液为无色透明的离子组是( B ) A.K+、Mn、Na+、Cl-B.K+、Na+、N、C C.Na+、H+、N、SD.Fe3+、Na+、Cl-、S 解析: Mn、Fe3+均为有颜色的离子,A、D两项不符合题意;C项,H+在碱性溶液中不能大量共存;故应选B。 11.工业上制造镁粉是将镁蒸气在气体中冷却。 可作为冷却气体的是( C ) ①空气 ②CO2 ③Ar ④H2 ⑤N2 A.①②B.②③C.③④D.④⑤ 解析: Ar和H2难以与镁反应,可作镁蒸气的冷却气体,故应选C。 12.用1L1mol·L-1NaOH溶液吸收0.8molCO2,所得溶液中Na2CO3和NaHCO3的物质的量之比约为( A ) A.1∶3B.1∶2 C.2∶3D.3∶2 解析: 设生成Na2CO3和NaHCO3的物质的量分别为a、b, NaOH+0.8CO2aNa2CO3+bNaHCO3+H2O ⇒ 两者的物质的量之比为1∶3,故应选A。 二、非选择题(共52分) 13.(11分)现有一包白色粉末,其中可能含有CaCO3、Na2CO3、Na2SO4、NaCl、CuSO4,进行如下实验①溶于水得无色溶液;②向溶液中加入BaCl2溶液生成白色沉淀,再加盐酸时沉淀部分消失,据上述实验现象推断: 一定不存在 ,一定存在 ,可能存在 ,对于可能存在的物质应如何近一步检验? 写出简要的步骤和有关的离子方程式: 。 解析: CuSO4溶液呈蓝色,实验①说明无CuSO4;CaCO3不溶于水,实验①也说明无CaCO3;BaCl2溶液与Na2CO3、Na2SO4生成白色沉淀,且BaCO3溶于盐酸、BaSO4不溶于盐酸,实验②说明既有Na2CO3、又有Na2SO4。 答案: CaCO3、CuSO4 Na2SO4、Na2CO3 NaCl 取无色溶液少量放于试管中,滴加足量的稀HNO3,待气泡不再冒出后,滴加AgNO3溶液,看是否产生白色沉淀。 若有,则含有NaCl,反之则无 C+2H+CO2↑+H2O Ag++Cl-AgCl↓ 14.(13分)我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,如图是海水综合利用的一个方面。 请回答下列问题: (1)写出①步加入的试剂和有关的离子方程式: , 。 (2)写出②⑤反应的离子方程式: ② ; ⑤ 。 (3)写出④反应的化学方程式: 。 (4)海水制镁的中间产品氢氧化镁经两步反应可制得碳酸镁,用离子方程式表示其过程 ; 。 解析: 第①步将Br-转化为溴,需加入一种氧化剂,如Cl2。 ②为Mg2+与熟石灰的反应,⑤为电解氯化钠水溶液的反应,④为电解熔融的氯化镁制取镁的反应。 氢氧化镁能溶于酸,再与可溶性碳酸盐反应,即可制得碳酸镁。 答案: (1)Cl2 2Br-+Cl22Cl-+Br2 (2)②Mg2++2OH-Mg(OH)2↓ ⑤2Cl-+2H2O2OH-+H2↑+Cl2↑ (3)MgCl2Mg+Cl2↑ (4)Mg(OH)2+2H+Mg2++2H2O Mg2++CMgCO3↓ 15.(13分)将Cu投入足量的FeCl3的水溶液中,两者发生反应的化学方程式如下: 2FeCl3+Cu2FeCl2+CuCl2 (1)请用双线桥法标出电子转移的方向和数目。 (2)在该反应中,氧化剂是 ,氧化产物是 。 (3)当有0.3mol电子发生转移时,发生反应的Cu的质量为 。 (4)请将以上反应改写为离子方程式 。 解析: 该反应的电子转移情况为: 反应中FeCl3为氧化剂,CuCl2为氧化产物。 当有0.3mol电子发生转移时,反应的Cu为0.15mol,其质量为9.6g。 答案: (1) (2)FeCl3 CuCl2 (3)9.6g (4)2Fe3++Cu2Fe2++Cu2+ 16.(2012山东威海高一检测)(15分)氯气是一种很重要的工业原料,很多化学物质中均含有氯,如饮用水常用氯气作消毒剂。 一般情况下,实验室中常用较强的氧化剂[如MnO2、PbO2、KMnO4、KClO3、Ca(ClO)2等]氧化浓盐酸制氯气。 请回答下列问题: (1)写出PbO2和浓盐酸制取氯气的化学方程式,并标明电子转移的方向和数目: 。 (2)为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,小明设计了如图所示的实验装置,按要求填空。 ①请根据小明的意图,连接相应的装置,接口顺序: 接 , 接 , 接 ; ②U形管中所盛试剂的化学式为 ; ③装置C中CCl4的作用是 ; ④小红认为小明的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。 为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,小红同学提出在某两个装置之间再加装置F。 你认为装置F应加在 之间(填装置序号)。 瓶中可以放入 ; ⑤小强看到小明设计的装置后提出无需多加装置,只需将原来烧杯中
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 苏教版高中化学必修一专题2 检测试题 苏教版 高中化学 必修 专题 检测 试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
