 ICHQ3D元素杂质指南.docx
ICHQ3D元素杂质指南.docx
- 文档编号:24099225
- 上传时间:2023-05-24
- 格式:DOCX
- 页数:23
- 大小:48.21KB
ICHQ3D元素杂质指南.docx
《ICHQ3D元素杂质指南.docx》由会员分享,可在线阅读,更多相关《ICHQ3D元素杂质指南.docx(23页珍藏版)》请在冰豆网上搜索。
ICHQ3D元素杂质指南
5.4RecommendationsforElementstobeConsideredintheRiskAssessment 风险评估中要考虑的要素建议
Thefollowingtableprovidesrecommendationsforinclusionofelementalimpuritiesintheriskassessment.Thistablecanbeappliedtoallsourcesofelementalimpuritiesinthedrugproduct.
以下表格对于风险评估中需要包括的元素杂质做出了建议。
该表可以用于药品中所有来源的元素杂质。
Table5.1:
ElementstobeConsideredintheRiskAssessment
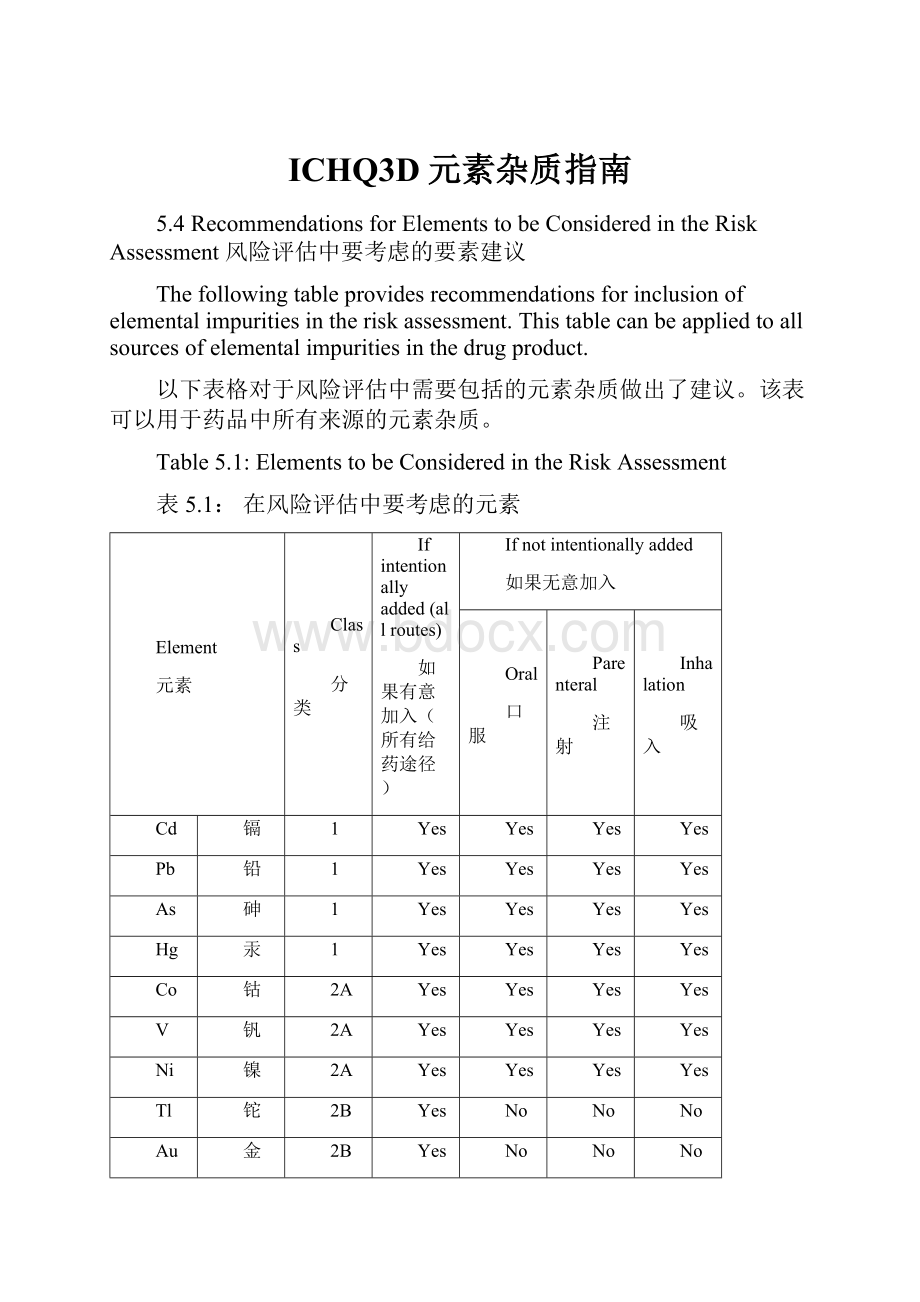
表5.1:
在风险评估中要考虑的元素
Element
元素
Class
分类
Ifintentionallyadded(allroutes)
如果有意加入(所有给药途径)
Ifnotintentionallyadded
如果无意加入
Oral
口服
Parenteral
注射
Inhalation
吸入
Cd
镉
1
Yes
Yes
Yes
Yes
Pb
铅
1
Yes
Yes
Yes
Yes
As
砷
1
Yes
Yes
Yes
Yes
Hg
汞
1
Yes
Yes
Yes
Yes
Co
钴
2A
Yes
Yes
Yes
Yes
V
钒
2A
Yes
Yes
Yes
Yes
Ni
镍
2A
Yes
Yes
Yes
Yes
Tl
铊
2B
Yes
No
No
No
Au
金
2B
Yes
No
No
No
Pd
钯
2B
Yes
No
No
No
Ir
铱
2B
Yes
No
No
No
Os
锇
2B
Yes
No
No
No
Rh
铑
2B
Yes
No
No
No
Ru
铷
2B
Yes
No
No
No
Se
硒
2B
Yes
No
No
No
Ag
银
2B
Yes
No
No
No
Pt
铂
2B
Yes
No
No
No
Li
锂
3
Yes
No
Yes
Yes
Sb
锑
3
Yes
No
Yes
Yes
Ba
钡
3
Yes
No
No
Yes
Mo
钼
3
Yes
No
No
Yes
Cu
铜
3
Yes
No
Yes
Yes
Sn
锡
3
Yes
No
No
Yes
Cr
铬
3
Yes
No
No
Yes
5.5Evaluation 评估
Asthepotentialelementalimpurityidentificationprocessisconcluded,therearetwopossibleoutcomes:
在对潜在元素杂质进行识别后,可能会有两种结论:
1) Theriskassessmentprocessdoesnotidentifyanypotentialelementalimpurities.Theconclusionoftheriskassessmentandsupportinginformationanddatashouldbedocumented.
1) 风险评估未能识别出任何潜在元素杂质。
风险评估的结论和支持性资料和数据要进行记录。
2) Theriskassessmentprocessidentifiesoneormorepotentialelementalimpurities.Foranyelementalimpuritiesidentifiedintheprocess,theriskassessmentshouldconsideriftherearemultiplesourcesoftheidentifiedelementalimpurityorimpuritiesanddocumenttheconclusionoftheassessmentandsupportinginformation.
2) 风险评估识别出了一个或多个潜在元素杂质。
对所有识别出的元素杂质,如果该元素杂质有多个来源,要考虑进行风险评估。
并记录评估的结论和支持性资料。
Theapplicant’sriskassessmentcanbefacilitatedwithinformationaboutthepotentialelementalimpuritiesprovidedbysuppliersofdrugsubstances,excipients,containerclosuresystems,andmanufacturingequipment.Thedatathatsupportthisriskassessmentcancomefromanumberofsourcesthatinclude,butarenotlimitedto:
申报人的风险评估可以利用原料药、辅料、容器密闭系统和生产设备供应商提供的关于潜在元素杂质的信息。
支持风险评估的数据可以来自于许多来源,包括但不仅限于:
- Priorknowledge;
- 之前的知识
- Publishedliterature;
- 出版的文献
- Datageneratedfromsimilarprocesses;
- 从类似工艺中产生的数据
- Supplierinformationordata;
- 供应商的信息或数据
- Testingofthecomponentsofthedrugproduct;
- 药品组分检测
- Testingofthedrugproduct.
- 药品检测
Duringtheriskassessment,anumberoffactorsthatcaninfluencethelevelofthepotentialimpurityinthedrugproductandshouldalsohavebeenconsideredintheriskassessment.Theseincludebutarenotlimitedto:
在风险评估中,很多因素会对药品中潜在杂质的水平造成影响,因此也需要在风险评估中进行考虑。
这包括但不仅限于:
- Efficiencyofremovalofelementalimpuritiesduringfurtherprocessing;
- 进一步加工中除去元素杂质的有效性
- Naturalabundanceofelements(especiallyimportantforthecategoriesofelementswhicharenotintentionallyadded);
- 自然富含的元素(特别重要的是没有添加单身的杂质类别)
- Priorknowledgeofelementalimpurityconcentrationrangesfromspecificsources;
- 特定来源的元素杂质浓度已有知识
- Thecompositionofthedrugproduct.
- 药品组分
5.6SummaryofRiskAssessmentProcess 风险评估过程的总结
Theriskassessmentissummarizedbyreviewingrelevantproductorcomponentspecificdatacombinedwithinformationandknowledgegainedacrossproductsorprocessestoidentifythesignificantprobableelementalimpuritiesthatmaybeobservedinthedrugproduct.
通过对相关产品或组成相关数据,结合在产品或工艺中获得的信息和知识进行审核,进行风险评估,以识别明显可能在药品中观察到的元素杂质。
ThesummaryshouldconsiderthesignificanceoftheobservedorpredictedleveloftheelementalimpurityrelativetothePDEoftheelementalimpurity.Asameasureofthesignificanceoftheobservedelementalimpuritylevel,acontrolthresholdisdefinedasalevelthatis30%oftheestablishedPDEinthedrugproduct.Thecontrolthresholdmaybeusedtodetermineifadditionalcontrolsmayberequired.
总结要考虑相对于元素杂质PDE值,已观察到的或预期的元素杂质水平的显著性。
这里,将药品中已建立的PDE值的30%定义为控制阈值,作为对已观察到的元素杂质水平的显著性的衡量方法,
Ifthetotalelementalimpuritylevelfromallsourcesinthedrugproductisexpectedtobeconsistentlylessthan30%ofthePDE,thenadditionalcontrolsarenotrequired,providedtheapplicanthasappropriatelyassessedthedataanddemonstratedadequatecontrolsonelementalimpurities.
如果药品中所有来源的总元素杂质水平预期会保持一致,且低于PDE值的30%水平,而申报人已对数据进行了适当的评估,证明对元素杂质的控制已经足够充分,则不需要采用更多的控制措施。
Iftheriskassessmentfailstodemonstratethatanelementalimpuritylevelisconsistentlylessthanthecontrolthreshold,controlsshouldbeestablishedtoensurethattheelementalimpurityleveldoesnotexceedthePDEinthedrugproduct.(SeeSection6)
如果风险评估未能证明一种元素杂质的水平具有一致性且低于控制阈值,则要建立控制措施来保证元素杂质水平不会超过药品的PDE值(参见第6部分)。
Thevariabilityofthelevelofanelementalimpurityshouldbefactoredintotheapplicationofthecontrolthresholdtodrugproducts.Sourcesofvariabilitymayinclude:
元素杂质水平的可变性应分解到药品阈值控制的应用中去。
可变性的来源可能包括:
- Variabilityoftheanalyticalmethod;
- 分析方法的可变性
- Variabilityoftheelementalimpuritylevelinthespecificsources;
- 特定来源中的元素杂质的可变性
- Variabilityoftheelementalimpuritylevelinthedrugproduct.
- 药品中元素杂质水平的可变性
Atthetimeofsubmission,intheabsenceofotherjustification,thelevelandvariabilityofanelementalimpuritycanbeestablishedbyprovidingthedatafromthree(3)representativeproductionscalelotsorsix(6)representativepilotscalelotsofthecomponentorcomponentsordrugproduct.Forsomecomponentsthathaveinherentvariability(e.g.,minedexcipients),additionaldatamaybeneededtoapplythecontrolthreshold.
在提交申报时,如果没有其它论证,一种元素杂质的水平和可变性可以通过提供成分或药品生产的3批生产规模或6批中试规模具代表性的批次数据来建立。
对于有些具有内在可变性的成分(例如,矿物质辅料),在应用控制阈值时可能需要额外的数据。
Therearemanyacceptableapproachestosummarizinganddocumentingtheriskassessmentthatmayinclude:
tables,writtensummariesofconsiderationsandconclusionsoftheassessment.Thesummaryshouldidentifytheelementalimpurities,theirsources,andthecontrolsandacceptancecriteriaasneeded.
许多总结和记录风险评估的方法都是可以接受的,包括:
表格、所有考虑因素的书面总结、评估的结论。
总结应识别出元素杂质、其来源、以及控制方式,需要时要制订可接受标准。
5.7SpecialConsiderationsforBiotechnologically-DerivedProducts 生物技术衍生药品的特殊考虑
Forbiotechnology-derivedproducts,therisksofelementalimpuritiesbeingpresentatlevelsthatraisesafetyconcernsatthedrugsubstancestageareconsideredlow.Thisislargelybecause:
a)elementsarenottypicallyusedascatalystsorreagentsinthemanufacturingofbiotechproducts;b)elementsareaddedattracelevelsinmediafeedsduringcellcultureprocesses,withoutaccumulationandwithsignificantdilution/removalduringfurtherprocessing;c)typicalpurificationschemesusedinbiotechmanufacturingsuchasextraction,chromatographystepsanddialysisorUltrafiltration-Diafiltration(UF/DF)havethecapacitytoclearelementsintroducedincellculture/fermentationstepsorfromcontactwithmanufacturingequipmenttonegligiblelevels.Assuch,specificcontrolsonelementalimpuritiesuptothebiotechdrugsubstancearegenerallynotneeded.Incaseswherethebiotechnology-deriveddrugsubstancecontainssyntheticstructures(suchasantibody-drugconjugates),appropriatecontrolsonthesmallmoleculecomponentforelementalimpuritiesshouldbeevaluated.
对于生物技术衍生药品,在原料药阶段引起安全关注的元素杂质的风险被认为是很低的。
这很大程度是因为1)元素不是在生物技术药品生产中典型用作催化剂或试剂,2)在细胞发酵过程中培养基补料时加入的元素为痕量水平,不会累积,在进一步加工时会被显著稀释/清除,3)在生物技术生产中使用的典型的纯化过程,如萃取、色谱分离和透析或超滤-渗滤(UF/DF),具备能力将细胞生长/发酵步骤或与生产设备接触过程中引入的元素清除至可忽略的水平。
在这种情况下,对生物技术原料药中元素杂质的特别控制通常并不需要。
如果生物技术衍生原料药含有合成结构(例如抗体药偶合物),需要评估是否需要对小分子成分中的元素杂质进行适当的控制。
However,potentialelementalimpuritysourcesincludedindrugproductmanufacturing(e.g.,excipients)andotherenvironmentalsourcesshouldbeconsideredforbiotechnologically-deriveddrugproducts.Thecontributionofthesesourcestothefinishedproductshouldbeassessedbecausetheyaretypicallyintroducedinthedrugproductmanufactureatastepintheprocesswheresubsequentelementalimpurityremovalisnotgenerallyperformed.Riskfactorsthatshouldbeconsideredinthisassessmentshouldincludethetypeofexcipientsused,theprocessingconditionsandtheirsusceptibilitytocontaminationbyenvironmentalfactors(e.g.,controlledareasforsterilemanufacturinganduseofpurifiedwater)andoveralldosingfrequency.
但是,生物技术衍生药品要考虑药品生产中所包括的(例如辅料),及其它环境来源的潜在元素杂质来源。
这些制剂中来源的影响应进行评估,因为它们会在制剂生产工艺某步骤中被引入,之后一般没有对元素杂质的清除。
在该评估中要考虑的风险因素应包括所用辅料的类型,加工条件及其被环境因素污染的难易程度(例如,无菌生产控制区域,纯化水的使用)以及总体给药频率。
6.CONTROLOFELEMENTALIMPURITIES 元素杂质的控制
ControlofelementalimpuritiesisonepartoftheoverallcontrolstrategyforadrugproductthatassuresthatelementalimpuritiesdonotexceedthePDEs.Whenthelevelofanelementalimpuritymayexceedthecontrolthreshold,additionalmeasuresshouldbeimplementedtoassurethattheleveldoesnotexceedthePDE.Approachesthatanapplicantcanpursueincludebutarenotlimitedto:
控制元素杂质是药品全面控制策略的一部分,它能保证元素杂质不超过PDE值。
当元素杂质有可能超过控制阈值时,需采取更多措施来保证其水平不会超过PDE值。
申报人可以采用的措施包括但不仅限于:
- Modificationofthestepsinthemanufacturingprocessthatresultinthereductionofelementalimpuritiesbelowthecontrolthresholdthroughspecificornon-specificpurificationsteps;
- 改进生产工艺步骤,通过特定或非特定的精制步骤将元素杂质降低至控制阈值以下
- Implementationofin-processorupstreamcontrols,designedtolimittheconcentrationoftheelementalimpuritybelowthecontrolthresholdinthedrugproduct;
- 实施中控或上游控制,用以将元素杂质的浓度限定在制剂的控制阈值以下
- Establishmentofspecificationlimitsforexci
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- ICHQ3D 元素 杂质 指南
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《当代世界政治与经济》.docx
《当代世界政治与经济》.docx
