 高考化学复习专题十三 化学实验基础知识.docx
高考化学复习专题十三 化学实验基础知识.docx
- 文档编号:23672881
- 上传时间:2023-05-19
- 格式:DOCX
- 页数:11
- 大小:175.12KB
高考化学复习专题十三 化学实验基础知识.docx
《高考化学复习专题十三 化学实验基础知识.docx》由会员分享,可在线阅读,更多相关《高考化学复习专题十三 化学实验基础知识.docx(11页珍藏版)》请在冰豆网上搜索。
高考化学复习专题十三化学实验基础知识
专题十三 化学实验基础知识
一、小题对点练
一、化学实验基本操作及物质的分离与提纯
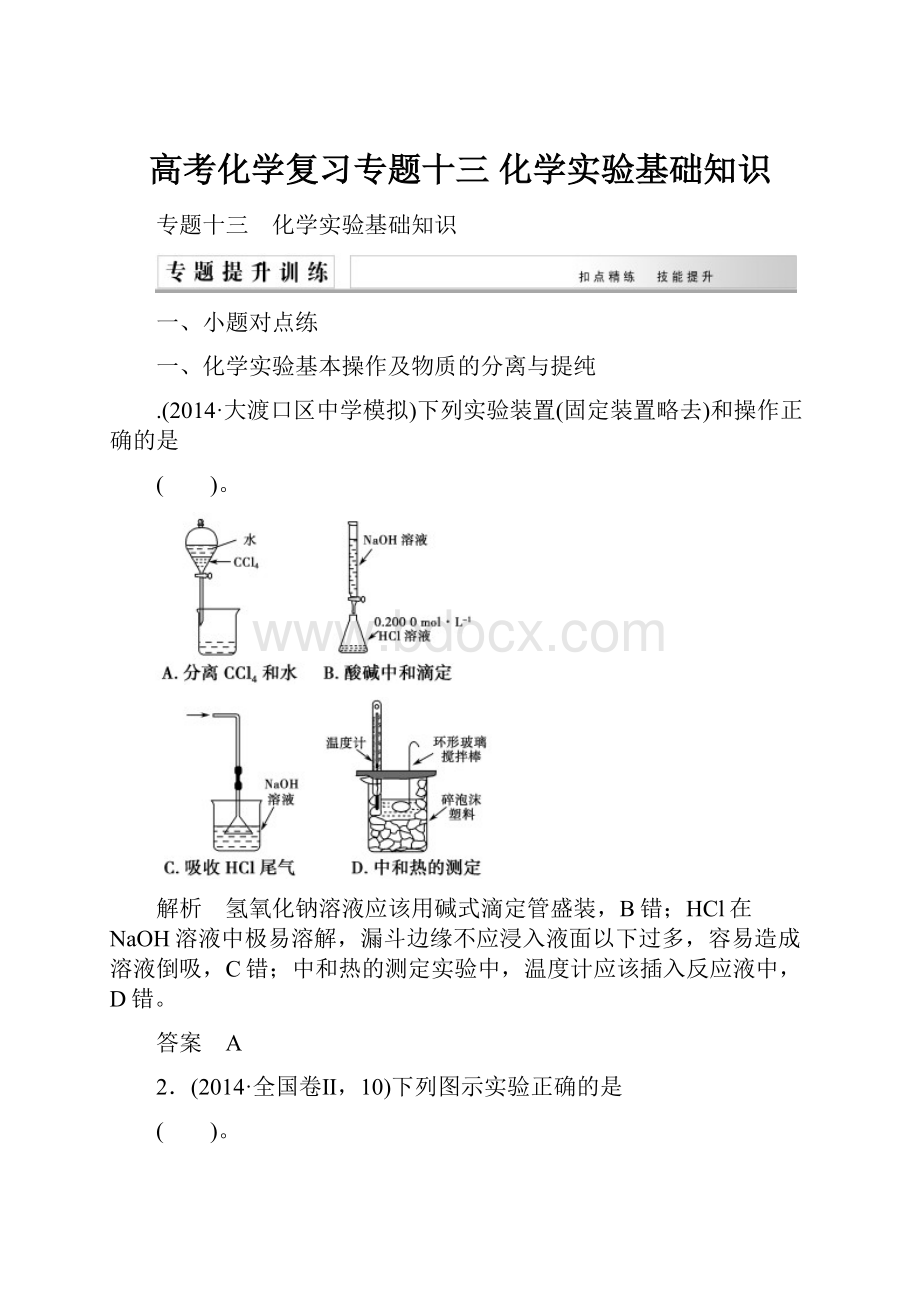
.(2014·大渡口区中学模拟)下列实验装置(固定装置略去)和操作正确的是
( )。
解析 氢氧化钠溶液应该用碱式滴定管盛装,B错;HCl在NaOH溶液中极易溶解,漏斗边缘不应浸入液面以下过多,容易造成溶液倒吸,C错;中和热的测定实验中,温度计应该插入反应液中,D错。
答案 A
2.(2014·全国卷Ⅱ,10)下列图示实验正确的是
( )。
解析 A项,过滤时要求“一贴、二低、三靠”,该实验中玻璃棒悬在漏斗上方,没有靠在三层滤纸上,且漏斗颈尖嘴一侧应紧贴烧杯内壁,错误;B项,加热分解碳酸氢钠时,因为有水生成,试管口应稍向下倾斜,错误;C项,混合气体应长进短出,错误。
答案 D
3.下列说法正确的是
( )。
A.久置的浓HNO3呈黄色,为除去黄色可通入O2
B.NH4Cl固体中混有I2,可用加热的方法除去
C.为除去FeSO4溶液中的Fe2(SO4)3,可加入Cu粉
D.为除去CO2中少量的SO2,可使其通过澄清石灰水
解析 该题主要考查了用化学方法分离、提纯物质的方法。
久置的浓HNO3呈黄色是由于硝酸分解生成的NO2溶解导致,通入O2发生反应:
4NO2+O2+2H2O===4HNO3,从而可以除去黄色,A正确;NH4Cl固体中混有I2,加热时,I2升华,NH4Cl也分解为NH3和HCl,B错误;FeSO4溶液中混有Fe2(SO4)3,加入Cu粉,发生反应:
Fe2(SO4)3+Cu===2FeSO4+CuSO4,虽然除去了Fe2(SO4)3,但引入了新杂质CuSO4,C错误;SO2、CO2均能与澄清石灰水反应,除去CO2中少量的SO2,应使其通过饱和NaHCO3溶液:
NaHCO3+SO2===NaHSO3+CO2,D错误。
答案 A
二、物质的检验
4.(2013·浙江,13)现有一瓶标签上注明为葡萄糖酸盐(钠、镁、钙、铁)的复合制剂,某同学为了确认其成分,取部分制剂作为试液,设计并完成了如下实验:
已知:
控制溶液pH=4时,Fe(OH)3沉淀完全,Ca2+、Mg2+不沉淀。
该同学得出的结论正确的是
( )。
A.根据现象1可推出该试液中含有Na+
B.根据现象2可推出该试液中并不含有葡萄糖酸根
C.根据现象3和4可推出该试液中含有Ca2+,但没有Mg2+
D.根据现象5可推出该试液中一定含有Fe2+
解析 由于试液中加入了Na2CO3溶液和NaOH溶液,所以不能确定原溶液中是否含有Na+,A项错误;葡萄糖酸中不存在醛基,所以无法用是否发生银镜反应来判断葡萄糖酸根的存在,B项错误;现象3说明无Mg2+,现象4说明存在Ca2+,C项正确;由于加H2O2之前,也没有进行过是否存在Fe2+的测定,最后检测得到存在Fe3+,可能是原来存在的,也可能是由Fe2+氧化得到的,D项错误。
答案 C
5.某钠盐溶液中可能含有NO、SO、SO、CO、Cl-、I-等阴离子。
某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液的pH大于7
②加入盐酸,产生有色、有刺激性气味气体
③加入硝酸酸化的AgNO3溶液,产生白色沉淀,且放出有色、有刺激性气味气体
④加入足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色
⑤加入足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)2溶液,再滴加KSCN溶液,显红色
该同学最终确定该钠盐溶液中仅含NO、CO、Cl-三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出结论( )。
A.①②④⑤B.③④
C.③④⑤D.②③⑤
解析 由①溶液的pH大于7,溶液呈碱性,知此溶液中至少有一种弱酸根离子;②加入盐酸,产生有色、有刺激性气味气体,可推知原溶液中有NO;③加入硝酸酸化的AgNO3溶液,产生白色沉淀,且放出有色、有刺激性气味气体,可确定原溶液中有Cl-、NO,无I-;④加入足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色,确定有CO,无SO,综合③和④即可得到实验结论。
答案 B
三、气体制备实验中仪器的组装与创新
6.(2014·北京理综,11)用下图装置(夹持、加热装置已略)进行实验,有②中现象,不能证实①中反应发生的是
( )。
①中实验
②中现象
A
铁粉与水蒸气加热
肥皂水冒泡
B
加热NH4Cl和Ca(OH)2混合物
酚酞溶液变红
C
NaHCO3固体受热分解
澄清石灰水变浑浊
D
石蜡油在碎瓷片上受热分解
Br2的CCl4溶液褪色
解析 A项,Fe与水蒸气高温反应产生H2,但加热时,反应装置中空气受热膨胀,以及水蒸气均会使②中肥皂水冒泡,错误;B项NH4Cl和Ca(OH)2加热产生NH3,NH3溶于水生成NH3·H2O,NH3·H2O
NH+OH-,使酚酞变红,正确;C项,2NaHCO3Na2CO3+H2O+CO2↑,CO2可使澄清石灰水变浑浊,正确;D项,石蜡油受热分解产生烯烃,烯烃可与Br2发生加成反应使Br2的CCl4溶液褪色,正确。
答案 A
7.利用如图所示的装置进行实验,将液体A逐滴加入烧瓶中与B发生反应,下列有关叙述中不正确的是
( )。
A.若A为硫酸,B为亚硫酸钠,C中盛品红溶液,则C中溶液褪色
B.若A为醋酸,B为贝壳,C中盛澄清石灰水,则C中溶液变浑浊
C.若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先产生沉淀后沉淀溶解
D.仪器D可以起到防止溶液倒吸的作用
解析 该题就同一装置考查了二氧化硫、二氧化碳和氨气这三种气体的制备方法。
A选项制备的是SO2,该气体可以使品红溶液褪色,A正确;B选项制备的是CO2,CO2能使澄清石灰水变浑浊,B正确;C选项制备的是NH3,但是Al(OH)3沉淀在氨水中不溶解,C错误;仪器D球形部分可以防止溶液倒吸,故D正确。
答案 C
8.下列实验装置图正确的是
( )。
解析 A项,MnO2和浓盐酸反应制Cl2需加热;B项,制乙烯,温度计应插入液面以下;D项,收集乙酸乙酯,导气管口应在饱和Na2CO3溶液液面上方。
答案 C
二、大题冲关练
9.某化学兴趣小组的同学利用如图所示实验装置进行实验(图中a、b、c表示止水夹)。
请按要求填空:
(1)利用B装置可制取的气体有________(任写两种即可)。
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。
若在丙中加入适量水,即可制得氯水。
将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象及结论如表所示:
实验序号
实验操作
现象
结论
Ⅰ
将氯水滴入品红溶液
溶液褪色
氯气与水反应的产物有漂白性
Ⅱ
向氯水中加入碳酸氢钠粉末
产生气泡
氯气与水反应的产物具有酸性
请你评价实验Ⅰ、Ⅱ的结论是否合理?
若不合理,请说明理由:
________________。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验。
①B中发生反应的化学方程式为____________。
②欲用D装置验证NO2与水的反应,其操作步骤为:
先关闭止水夹________,再打开止水夹________,使烧杯中的水进入试管丁的操作是______________。
解析
(1)B装置可用于块状不溶于水的固体与液体反应制取气体,故可用锌粒与稀H2SO4反应制取H2,也可用大理石与盐酸反应制取CO2等。
(2)A装置制取Cl2使用的浓盐酸具有挥发性,有一部分被氯水吸收,使氯水呈酸性,可与NaHCO3反应产生CO2,故实验Ⅱ的结论不合理。
(3)铜与浓HNO3反应放出NO2,收集于试管丁中然后用微热法使NO2与水接触从而使水倒流进入试管丁中。
答案
(1)H2、CO2(其他合理答案均可)
(2)实验Ⅰ结论合理,实验Ⅱ结论不合理,制取的氯气中含有HCl气体,HCl溶于水后能与NaHCO3粉末反应产生气泡,不能说明酸性是氯气与水的反应产物造成的
(3)①Cu+4HNO3(浓)===Cu(NO3)2+2NO2↑+2H2O
②a、b c 双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流进入试管丁中
10.(2014·重庆八中高三模拟)亚硝酸钠是重要的防腐剂。
某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利用一氧化氮与过氧化钠反应制备亚硝酸钠(夹持装置和A中加热装置已略,气密性已检查)。
HNO2为弱酸,室温下存在反应3HNO2===HNO3+2NO↑+H2O
NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸。
实验操作:
①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;
③从C中取少量固体,检验是否是亚硝酸钠。
(1)A中盛装浓硝酸的仪器名称是______________________。
(2)B中观察的主要现象是_____________________。
D装置的作用是___________________________。
(3)检验C中产物有亚硝酸钠的操作是__________________。
(4)经检验C产物中亚硝酸钠含量较少。
a.甲同学认为C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠。
生成碳酸钠的化学方程式是_________________。
为排除干扰,甲在B、C装置间增加装置E,E中盛放的试剂是________(写名称)。
b.乙同学认为除上述干扰因素外,还会有氧气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是_________________。
(5)实验经改进后可制得较纯亚硝酸钠,下列关于亚硝酸钠的说法正确的是________。
a.亚硝酸钠有咸味,可代替食盐食用
b.室温下,0.1mol/L亚硝酸钠溶液pH>7
c.0.1mol/L亚硝酸钠溶液中存在:
c(Na+)+c(H+)=c(NO)+c(OH-)
d.0.1mol/L亚硝酸钠溶液中存在:
c(NO)>c(Na+)>c(OH-)>c(H+)
解析 利用图示装置可知A中碳与浓硝酸反应得到CO2、NO2的混合气体,混合气体进入B中,NO2与H2O作用得到稀HNO3,稀HNO3会与Cu反应,生成Cu(NO3)2、NO和H2O,因此在B装置中可观察到:
溶液变蓝,铜片溶解,导管口有无色气体冒出;B中产生的NO以及进入B中的CO2和水蒸气等一起进入C装置,因此C装置中不仅有NaNO2生成,还会有Na2CO3、NaOH生成,为排除CO2、H2O对制备NaNO2的干扰,最好在B、C间添加除杂装置,试剂可选用碱石灰,可将CO2、H2O一并吸收,结合题中信息可知D中KMnO4溶液是为了吸收未反应的NO,防止污染空气。
利用信息“HNO2为弱酸,室温下存在反应3HNO2===HNO3+2NO↑+H2O”可知,检验固体中是否含NaNO2,可将固体溶于水,加入稀硫酸看有无无色气体放出,且无色气体能否在液面上方变为红棕色;NaNO2为强碱弱酸盐,NO水解导致溶液显碱性,故室温下NaNO2溶液pH>7,溶液中离子浓度的关系为:
c(Na+)>c(NO)>c(OH-)>c(H+),再利用电荷守恒知NaNO2溶液中:
c(Na+)+c(H+)=c(NO)+c(OH-)。
答案
(1)分液漏斗
(2)溶液变蓝,铜片溶解,导管口有无色气体冒出
除去未反应的NO,防止污染空气
(3)将生成物置于试管中,加入稀硫酸,若产生无色气体并在液面上方变为红棕色,则D中产物是亚硝酸钠。
反应的离子方程式是3NO+2H+===NO+2NO↑+H2O
(4)2CO2+2Na2O2===2Na2CO3+O2 碱石灰 打开弹簧夹,通入N2一段时间
(5)bc
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考化学复习专题十三 化学实验基础知识 高考 化学 复习 专题 十三 实验 基础知识
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《酒店人力资源管理》教案.docx
《酒店人力资源管理》教案.docx
