 中考化学专题复习 气体制备和除杂.docx
中考化学专题复习 气体制备和除杂.docx
- 文档编号:23513733
- 上传时间:2023-05-17
- 格式:DOCX
- 页数:16
- 大小:291.03KB
中考化学专题复习 气体制备和除杂.docx
《中考化学专题复习 气体制备和除杂.docx》由会员分享,可在线阅读,更多相关《中考化学专题复习 气体制备和除杂.docx(16页珍藏版)》请在冰豆网上搜索。
中考化学专题复习气体制备和除杂
2020年中考化学专题复习气体制备与除杂
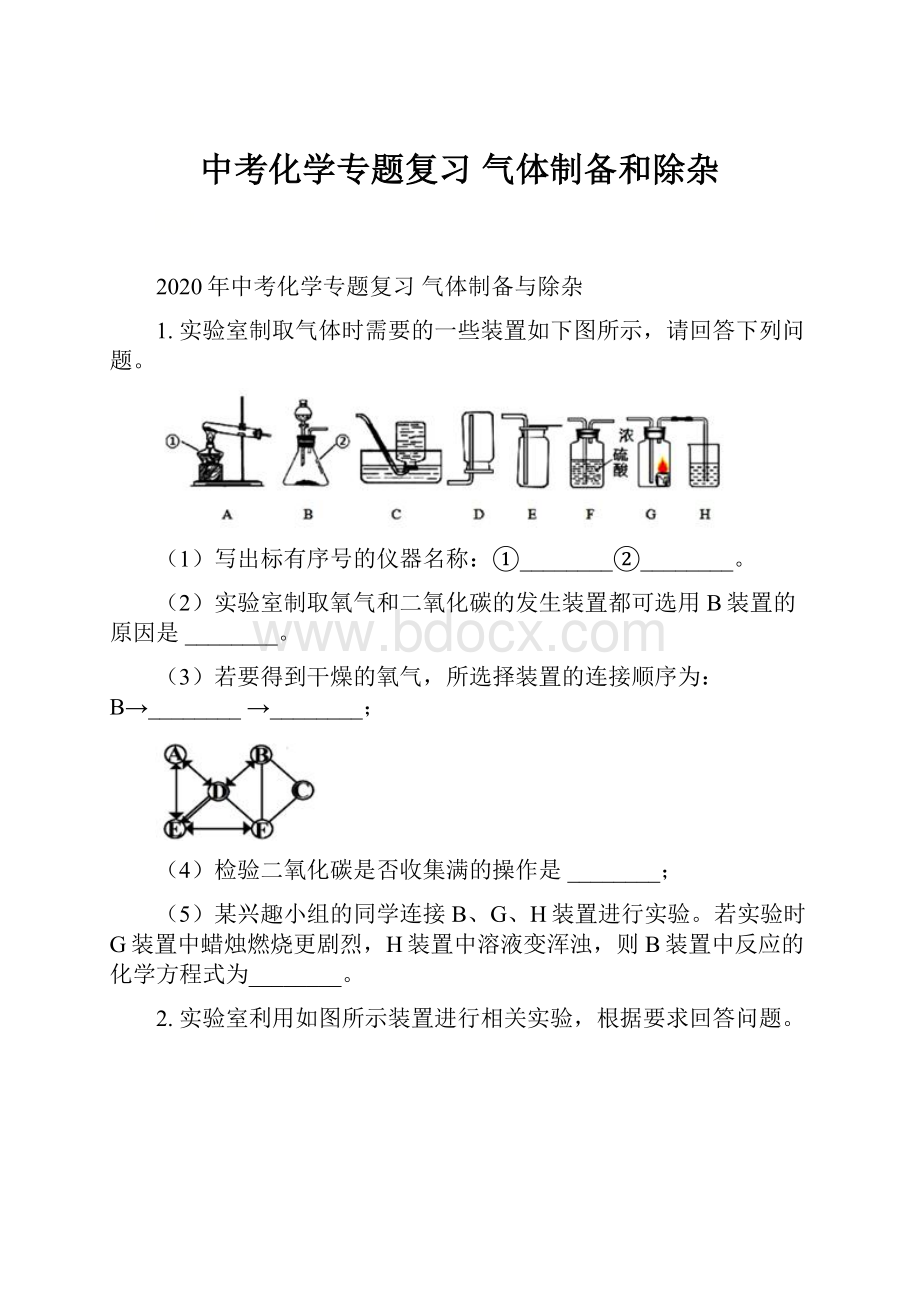
1.实验室制取气体时需要的一些装置如下图所示,请回答下列问题。
(1)写出标有序号的仪器名称:
①________②________。
(2)实验室制取氧气和二氧化碳的发生装置都可选用B装置的原因是________。
(3)若要得到干燥的氧气,所选择装置的连接顺序为:
B→________ →________;
(4)检验二氧化碳是否收集满的操作是________;
(5)某兴趣小组的同学连接B、G、H装置进行实验。
若实验时G装置中蜡烛燃烧更剧烈,H装置中溶液变浑浊,则B装置中反应的化学方程式为________。
2.实验室利用如图所示装置进行相关实验,根据要求回答问题。
(1)写出仪器名称:
a________用氯酸钾和二氧化锰制氧气的发生装置是________(填字母序号),化学方程式为________,不能用E装置收集氧气的原因________。
(2)发生装置可选装置C的是________。
I.石灰石和稀盐酸制二氧化碳II.双氧水和二氧化锰制氧气III.锌块和稀硫酸制氢气
(3)石灰石与稀盐酸制二氧化碳的化学方程式为________。
为测定产生二氧化碳的质量(假设二氧化碳已完全放出,忽略空气中物质的影响),设计如右图装置:
产生二氧化碳的质量________(填“大于”、“小于”或“等于”)氢氧化钠固体增加的质量。
(4)对锥形瓶中反应后的剩余溶液成分进行探究(杂质不溶于水且不参加反应),剩余溶液中一定有的溶质是________。
把剩余溶液分成两份,分别置于两个试管中进行实验。
实验I.往一个试管中滴加硝酸银溶液,产生白色沉淀,再加入稀硝酸,沉淀不溶解。
实验II.往另一个试管中逐滴滴入碳酸钠溶液,并用pH传感器连续监测试管内溶液的pH,得下图
根据实验________(填编号)可知,剩余溶液中还有盐酸。
(5)曲线上M点溶液的溶质成分是________。
3.
(1)同学们利用下图所示装置进行气体的制备实验(A~F为装置编号)
①写出上图D装置中甲仪器的名称________。
②用A装置加热氯酸钾和二氧化锰的混合物制取氧气,化学方程式为________,其中二氧化锰起________作用;收集氧气可选择________ (填装置编号)。
③实验室制备二氧化碳通常选择下列药品中的________(填药品序号)。
a.稀盐酸b.熟石灰c.块状石灰石d.稀硫酸
通常检验二氧化碳气体的反应可用化学方程式表示为________ 。
④常温下,可用固体硫化亚铁(FeS)和稀硫酸反应制取硫化氢(H2S)气体,若要控制滴加液体的速率,可选择的发生装置是________(填装置编号)。
⑤制取气体前应先检查装置的气密性,若按F图所示操作,结果在导管口未看到气泡,其可能原因与下列因素无关的是________ (填序号)。
a.将烧杯换成水槽b.导管伸入水中位置过深,气体无法逸出
c.将水换成冰水d.先用手捂住试管壁,再将导管另一端插入水中
(2)为什么汗水有咸味?
学习小组同学为此开展探究。
【提出问题】汗水中产生咸味的物质是什么?
【假设与猜想】根据生活经验推测,汗水中产生咸味的物质可能是________。
(3)【查阅资料】用铂丝醮取少许含有钠元素的溶液(或物质)在酒精灯火焰上灼烧,会呈现黄色火焰。
【制订计划】为了证明咸味物质是猜想中的物质,一是要证明汗水溶液中含有阴离子________(填写离子符号),二是要证明汗水溶液中有阳离子________(填写离子符号)。
(4)【进行实验】证明阴离子的实验:
向汗水溶液中滴加________溶液,再加入少量稀硝酸,振荡,仍有白色沉淀产生。
证明阳离子的实验:
________。
(5)【结论】经上述实验证明,汗水中的咸味物质就是猜想中的物质。
【分析与交流】上述实验中,证明阴离子存在的化学反应方程式为:
________,该化学反应属于________反应。
4.在实验室中,我们通常用块状大理石与稀盐酸反应来制取二氧化碳气体,供选用的装置如图甲所示。
(1)仪器a的名称为________。
(2)若要制取并收集一瓶CO2,不可以选择的装置是________ (填图甲中装置对应的字母序号)。
(3)CO2是一种酸性氧化物(能与碱反应生成盐和水的氧化物)。
为探究CO2确实能和NaOH发生化学反应,华雪同学选用了图乙中两种装置进行实验,都证明了CO2和NaOH确实发生了化学反应。
请回答下列问题。
①选择装置Ⅰ时,可观察到的实验现象为________。
②选择装置Ⅱ时,可观察到烧杯内的水沿着导管倒流入锥形瓶中,产生该实验现象的有关化学变化的原因是(用化学方程式说明):
________。
5.
(1)同学们用下图所示仪器和装置探究制取气体的方法,请回答下列问题:
①图中仪器B的名称为________。
②装配KClO3制备O2的发生装置,上图中还缺少的玻璃仪器是________(写名称),该反应的化学方程式是________。
③图中的微型装置F可用于实验室制备H2,反应化学方程式为________。
该装置在操作上的优点是________。
G是医用输液观察滴液快慢的滴壶,若用它作微型的O2干燥装置,则气体应从________(填选“a”或“b”)进入,滴壶中装的试剂是________。
(2)实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣。
(查阅资料)
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水;
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
(发现问题)
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:
碱式碳酸铜受热分解生成的黑色固体成分.
(猜想与假设)该黑色固体可能是①碳粉;②________;③碳和氧化铜的混合物。
(3)(设计方案)请帮助该同学完成下述实验报告:
实验操作与现象
实验结论
________
猜想②符合题意
(4)探究二:
碱式碳酸铜受热分解还会生成CO2和H2O.
(进行实验)选择如下图所示装置进行验证
步骤一:
连接A和B,打开活塞,通入一段时间的空气;
步骤二:
点燃酒精灯,依次连接装置A→B→________→________(填“C”,“D”);步骤三:
点燃酒精灯,观察到明显现象后,停止加热。
(5)(解释与结论)
①当观察到________,说明碱式碳酸铜受热分解生成了CO2和H2O,写出装置C中反应的化学方程式________;
②写出Cu2(OH)2CO3受热分解的化学方程式________。
(6)(反思与评价)
上述装置中A的作用是________。
6.今天又是化学实验室开放日,老师拿出两瓶无标签的固体,一种白色一种黑色,他各取少量试剂在试管中混合加热,很快产生一种无色气体,我们对此气体展开了一系列探究。
(1)①此气体是什么物质?
验证它的实验方案如下
猜想
实验步骤
现象
结论
此气体可能是________
生成该气体反应的文字表达式________,基本反应类型________
②我想制取该气体,采用的收集装置可以选用上图中的________(填序号),理由是________。
(2)该气体也可用一种固体一种液体混合制取,请你写出反应的文字表达式(或符号表达式)________
(3)有同学只用一种固体加热也制取了该气体,请你写出文字表达式(或符号表达式)________。
他在反应的过程中发现水槽内的水变紫色了,请你帮他分析原因________。
(写出一条即可)
(4)氨气是一种无色的气体,极易溶于水,在实验室可用氯化铵固体和氢氧化钙固体混合加热来制取,则采取的发生装置可选取上图中的________(填序号)
7.通过化学学习,应该知道有多种途径可以制取氧气。
如:
A分离空气 B加热高锰酸钾 C分解过氧化氢 D_______________
(1)相信你在D处还可以写出另一种制取氧气的方法;
(2)若用如图装置加热高锰酸钾制取氧气:
写出标号仪器的名称①________ ②________;实验结束,停止加热时要先把导管移出水面,其理由是________,
(3)若分解过氧化氢制取氧气,供选用的装置如下:
要得到平稳的氧气流,应选用的发生装置是________(选填“甲”或“乙”);
(4)用排水法收集氧气,当气泡________时,再开始收集;
(5)写出实验室加热高锰酸钾制氧气的文字表达式:
________
8.下面是实验室制取氧气的装置图,根据装置图回答下列问题:
(1)写出装置图中标有①②序号的仪器名称:
①________②________
(2)实验室用高锰酸钾制取氧气时的文字表达式________,若选用A为发生装置,则需要进行的改进方法是________;若要收集较纯净的氧气选用的收集装置是________(写出装置代号),如用D收集氧气,验满的方法是________。
(3)装置________(写出装置代号)是实验室用过氧化氢和二氧化锰制取氧气的发生装置。
写出实验室用过氧化氢和二氧化锰制取氧气的文字表达式________。
(4)加热氯酸钾制氧气时,如果不加二氧化锰做催化剂,其后果是:
(________)
A没有氧气放出 B放出氧气速度慢
C生成氧气总量少 D影响不大
(5)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法制备甲烷。
发生装置应选择________(填字母),可用装置C收集甲烷,是利用了甲烷________的物理性质;
9.实验室有如下气体制取的装置图:
(1)写出仪器的名称:
①________,②________。
(2)实验室用高锰酸钾制取氧气应选用的发生装置是________(填序号,下同),本装置还需进行的改进是________,该化学反应的化学方程式为________,实验结束后,先________,后________以防止试管破裂。
(3)若用B装置制取氧气,反应的化学方程式为________,收集氧气可以选C装置,理由是________,若收集较纯净的氧气可以选________装置。
10.如图是实验室常用的实验仪器与装置。
依据题目要求回答下列问题:
(1)制取氧气有很多种方法,如分解过氧化氢溶液、加热高锰酸钾、________等。
(2)采用分解过氧化氢溶液制取氧气有许多优点,如:
________(填序号)。
①产物无污染 ②不需加热 ③需加热 ④生成物只有氧气
(3)实验室用氯酸钾制氧气时,应选择的装置组合是________。
(4)甲同学用分解过氧化氢溶液的方法制取并收集氧气,应分别选择________(填字母)装置;除过氧化氢溶液外,通常还需要的一种药品是________,其作用是________;加入药品前应注意检查装置的________性。
(5)乙同学选择装置A以高锰酸钾为原料制取氧气,他在该装置试管内的导管口处添加了一团棉花,其目的是:
________。
(6)丙同学对乙同学的制氧装置产生了质疑。
他认为加热高锰酸钾时,在试管较小的空间内氧气浓度高、温度也较高,而棉花是易燃物质,实验时可能会发生危险,他建议采用不易燃烧的丝状物质代替棉花更安全。
丙同学的观点是否正确,你认为最科学的判断依据是________(填序号)。
①依据教科书的观点 ②依据老师的观点 ③依据实验事实
(7)用排空气法收集气体时导管伸到集气瓶底部的原因________。
11.化学是一门以实验为基础的科学,根据如图所示装置,回答相关问题。
(1)写出有标号仪器的名称:
①________②________。
(2)实验室用加热高锰酸钾制取氧气,发生装置可选择________(填字母),该反应的化学方程式是________,该装置有一处不足之处是________;
(3)用氯酸钾制取氧气的化学方程式为________,应选择的发生和收集装置是________,若用装置G收集氧气则气体应从________(填“a”或“b”)通入。
(4)装置C与D组合,可制取二氧化碳,反应的化学方程式为:
________;装置B和C对比,用分液漏斗代替长颈漏斗进行实验的优点是________。
(5)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷(CH4),甲烷密度比空气小,难溶于水,发生和收集装置可以选择________(填字母序号,一种即可);请写出甲烷完全燃烧的化学方程式________。
12.实验室制取氧气,提供了下列药品和常用装置,请按要求回答有关问题
药品:
①过氧化氢溶液②高锰酸钾③二氧化锰
装置:
(1)装置中仪器a的名称为________;
(2)若小明用A来制取氧气,则该装置中发生反应的文字表达式是________。
(3)若小明采用B作为发生装置来制取氧气,则他选择的药品应为________(填序号);若采用图2所示的方法对B装置进行气密性检查,采用向左推动右侧注射器活塞时,观察到________现象时,说明该装置气密性良好。
(4)F装置有多种用途:
若用排空气法收集氧气时,气体应从F装置的________(“左”或“右”)端通入。
参考答案
1.
(1)酒精灯;锥形瓶
(2)都是固体和液体在常温时反应
(3)F;E
(4)将燃着的小木条放到集气瓶口(观察,若木条熄灭,证明已满)
(5)2H2O2
2H2O+O2↑
2.
(1)试管;A;2KClO3
2KCl+3O2↑;氧气的密度比空气大
(2)I、III
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;小于
(4)CaCl2;II
(5)NaCl、Na2CO3
3.
(1)集气瓶;2KClO3
2KCl+3O2↑;催化;D或E;ac;Ca(OH)2+CO2=CaCO3↓+H2O;C;abc
(2)NaCl
(3)Cl-;Na+
(4)AgNO3;用铂丝醮取少许溶液(或物质)在酒精灯火焰上灼烧,火焰的颜色为黄色
(5)NaCl+AgNO3=AgCl↓+NaNO3;复分解
4.
(1)长颈漏斗
(2)B、E、F
(3)气球变大;CO2+2NaOH=Na2CO3+H2O
5.
(1)长颈漏斗;酒精灯;2KClO3
2KCl+3O2↑;Zn+H2SO4=ZnSO4+H2↑;可以控制液体加入的量(或控制反应速率);b;浓硫酸
(2)氧化铜
(3)取黑色粉末,加入足量稀硫酸,充分反应后,黑色固体全部溶解形成蓝色溶液
(4)D;C
(5)C中石灰水变浑浊,D中无水硫酸铜变蓝;CO2+Ca(OH)2=CaCO3↓+H2O;Cu2(OH)2CO3
2CuO+H2O+CO2↑
(6)除去空气中的水分和二氧化碳,防止对产物的检验造成干扰6.
(1)氧气;
;分解反应;C或E;氧气密度略大于空气且不易溶于水,因此可用排水法和向上排空气法收集
(2)
(3)
;试管口未塞棉花
(4)A
7.
(1)加热分解氯酸钾
(2)试管;集气瓶;为了防止先移走酒精灯,试管内的压强减小,水沿导管进入热的试管,使试管炸裂
(3)甲
(4)连续均匀冒出
(5)
8.
(1)试管;集气瓶
(2)高锰酸钾
锰酸钾+二氧化锰+氧气;试管口放一团棉花;E;将带火星的木条放到集气瓶口,木条复燃,说明氧气已满
(3)B;过氧化氢
水+氧气
(4)B
(5)A;密度比空气小
9.
(1)酒精灯;水槽
(2)A;在试管口放一棉花团;2KMnO4
K2MnO4+MnO2+O2↑;把导管移出水面;熄灭酒精灯
(3)2H2O2
2H2O+O2↑;密度比空气大;E
10.
(1)加热氯酸钾
(2)①②
(3)AD或AE
(4)C、D(或C、E);二氧化锰;加快化学反应速率(或催化作用);气密
(5)防止加热时高锰酸钾粉末进入导管
(6)③
(7)排净装置底部的空气
11.
(1)长颈漏斗;集气瓶
(2)A;
;试管口未放一团棉花
(3)
;AD或AE或AG;a
(4)CaCO3+2HCl=CaCl2+H2O+CO2↑;能够控制反应的速率
(5)AE(或AF或AG);
12.
(1)长颈漏斗
(2)高锰酸钾
锰酸钾+二氧化锰+氧气
(3)①③;长颈漏斗中液面上升的
(4)左
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 中考化学专题复习 气体制备和除杂 中考 化学 专题 复习 气体 制备
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《地质测量图绘制细则》.docx
《地质测量图绘制细则》.docx
