 体外诊断IVD行业分析报告.docx
体外诊断IVD行业分析报告.docx
- 文档编号:23479
- 上传时间:2022-10-01
- 格式:DOCX
- 页数:23
- 大小:885.02KB
体外诊断IVD行业分析报告.docx
《体外诊断IVD行业分析报告.docx》由会员分享,可在线阅读,更多相关《体外诊断IVD行业分析报告.docx(23页珍藏版)》请在冰豆网上搜索。
体外诊断IVD行业分析报告
2016年体外诊断IVD行业分析报告
2016年1月
体外诊断试剂在国家政策鼓励下将快速实现国产替代化。
科技部发布《“十二五”生物技术发展规划》,要求突破一批体外诊断仪器设备与试剂的重大关键技术,在一体化化学发光免疫诊断系统等高端产品方面实现重大突破,加速体外诊断产业的结构调整和优化升级。
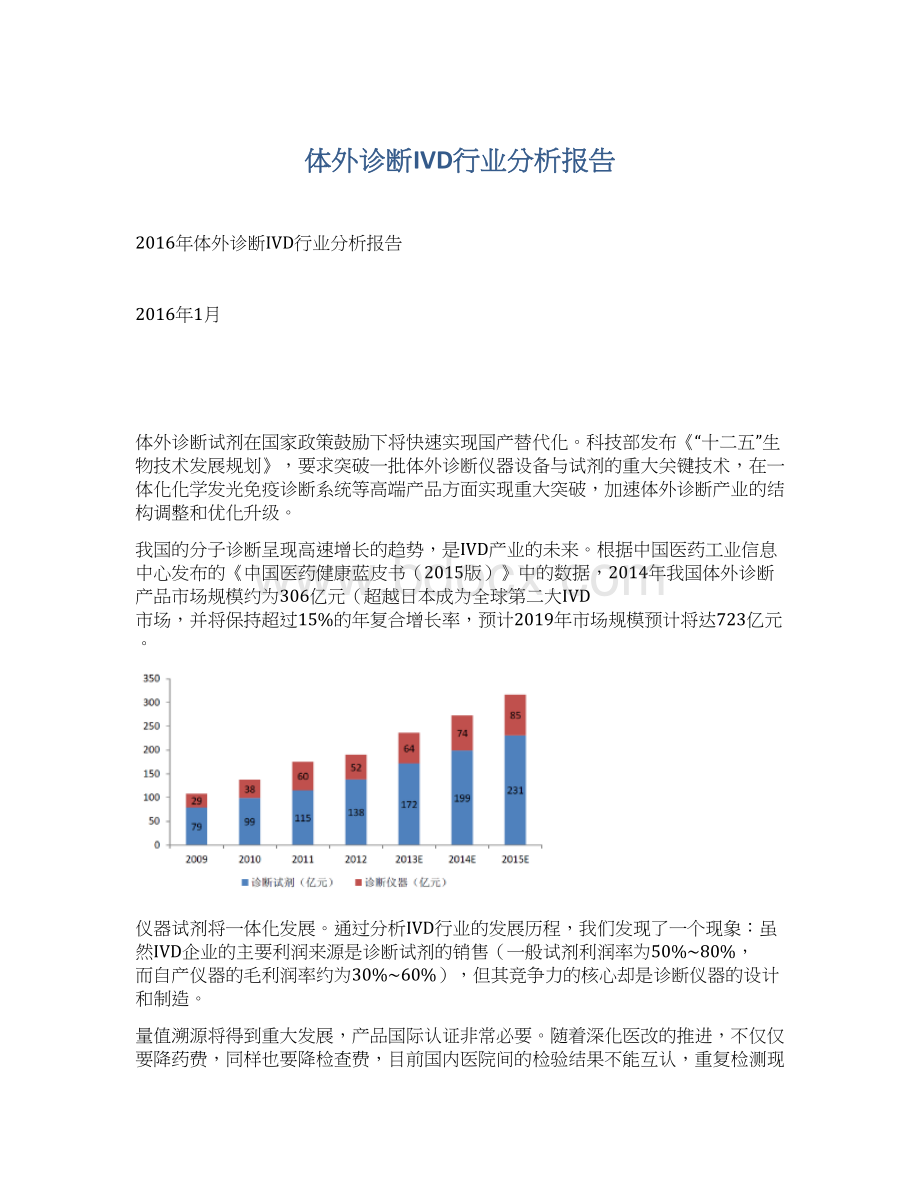
我国的分子诊断呈现高速增长的趋势,是IVD产业的未来。
根据中国医药工业信息中心发布的《中国医药健康蓝皮书(2015版)》中的数据,2014年我国体外诊断产品市场规模约为306亿元(超越日本成为全球第二大IVD市场,并将保持超过15%的年复合增长率,预计2019年市场规模预计将达723亿元。
仪器试剂将一体化发展。
通过分析IVD行业的发展历程,我们发现了一个现象:
虽然IVD企业的主要利润来源是诊断试剂的销售(一般试剂利润率为50%~80%,而自产仪器的毛利润率约为30%~60%),但其竞争力的核心却是诊断仪器的设计和制造。
量值溯源将得到重大发展,产品国际认证非常必要。
随着深化医改的推进,不仅仅要降药费,同样也要降检查费,目前国内医院间的检验结果不能互认,重复检测现象严重,加重了医保基金和患者自费的负担,促进医院检验科结果互认将成必然趋势,量值溯源将得到重大发展,产品国际认证非常必要。
一、IVD的定义
IVD(invitrodiagnosticproducts,体外诊断市场)从广义上讲,是指在人体之外,通过对人体的样品(血液、体液、组织等)进行检测而获取临床诊断信息的产品和服务。
从狭义上讲,体外诊断产业主要指体外诊断相关产品,包括体外诊断试剂及体外诊断仪器设备。
《体外诊断试剂注册管理办法(试行)》中所称我国体外诊断试剂是指:
可单独使用或与仪器、器具、设备或系统组合使用,在疾病的预防、诊断、治疗监测、预后观察、健康状态评价以及遗传性疾病的预测过程中,用于对人体样本(各种体液、细胞、组织样本等)进行体外检测的试剂、试剂盒、校准品(物)、质控品(物)等。
国家法定用于血源筛查的体外诊断试剂、采用放射性核素标记的体外诊断试剂不属于《体外诊断试剂注册管理办法(试行)》的管理范围,属于《药品注册管理办法》管理范围。
体外诊断试剂经营企业必须按照《药品经营质量管理规范》从事经营活动。
其中体外诊断仪器设备的技术难度较高,目前国内企业大多以试剂为主,占比80%左右。
二、IVD行业的分类
体外诊断仪器主要产品有生化分析仪、血液分析仪、霉标仪、化学发光免疫分析仪、实时荧光定量PCR仪,流式细胞仪等。
体外诊断试剂则不仅仅包括进行体外检测直接使用的试剂,还包括相应的校准物品、质控品、对照材料等。
体外诊断试剂与相应的体外诊断仪器组成整体体外诊断系统,两者一般应组合使用,但某些类别试剂亦可单独使用,比如胶体金快速诊断试剂。
体外诊断试剂按国家食品药品监督管理总局2014年7月30日发布(国家食品药品监督管理总局令第5号)《体外诊断试剂注册管理办法》,体外诊断试剂依次划分为第三类、第二类、第一类产品。
1、第三类产品:
1.与致病性病原体抗原、抗体以及核酸等检测相关的试剂。
2.与血型、组织配型相关的试剂。
3.与人类基因检测相关的试剂。
4.与遗传性疾病相关的试剂。
5.与麻醉药品、精神药品、医疗用毒性药品检测相关的试剂。
6.与治疗药物作用靶点检测相关的试剂。
7.与肿瘤标志物检测相关的试剂。
8.与变态反应(过敏原)相关的试剂。
2、第二类产品
1.用于蛋白质检测的试剂。
2.用于糖类检测的试剂。
3.用于激素检测的试剂。
4.用于酶类检测的试剂。
5.用于酯类检测的试剂。
6.用于维生素检测的试剂。
7.用于物资离子检测的试剂。
8.用于药物及药物代谢物检测的试剂。
9.用于自身抗体检测的试剂。
10.用于微生物鉴别或药敏试验的试剂。
11.用于其他生理、生化或免疫功能指标检测的试剂。
3、第一类产品
1.微生物培养基(不用于微生物鉴别和药敏试验)。
2.样本处理用产品,如溶血剂、稀释液、染色液等。
第一类体外诊断试剂实行备案管理,第二类、第三类体外诊断试剂实行注册管理。
境内第一类体外诊断试剂备案,备案人向设区的市级食品药品监督管理部门提交备案资料,进口第一类体外诊断试剂备案,备案人向国家食品药品监督管理总局提交备案资料。
境内第二类体外诊断试剂由省、自治区、直辖市食品药品监督管理部门审查,批准后发给医疗器械注册证。
境内第三类体外诊断试剂由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
进口第二类、第三类体外诊断试剂由国家食品药品监督管理总局审查,批准后发给医疗器械注册证。
按检验原理和方法的不同,体外诊断主要包括临床生化诊断、免疫诊断、分子生物学诊断、血液学诊断、微生物诊断、尿液诊断、凝血诊断。
其中生化诊断、免疫诊断、分子生物学诊断为临床体外诊断主要的三大领域。
三、我国IVD行业的发展历程
1、内资企业独享市场(2000前)
在2000年之前,我国的IVD行业堪称国内企业的乐园:
一方面,随着诊断产品迅速开始产业化生产,市场整体快速成长;另一方面,跨国公司作为日后强劲的竞争对手,此时还没有大规模参与中国市场。
市场规模的不断扩张催生了一大批国内体外诊断产品生产企业。
此时的国内企业并没有先进的技术,他们利用跨国公司没有大规模参与市场竞争的机会,依靠仿制国外产品和灵活的销售方式取得了大量的市场份额。
据统计,截止2000年,我国体外诊断产品市场规模约35亿,其中国内企业销售收入约30亿,占总体市场份额的85%左右。
反观跨国公司,除极少数几家企业已经在中国设立生产企业外(如DPC公司,已被西门子收购),很多企业甚至没有在中国内地设立办事处(他们在境外设立办事处,通过遥控国内代理商开发市场)。
跨国公司对中国市场的忽视直接导致其市场份额的萎靡不振(2000年销售收入约5亿,市场份额约15%)。
2000年我国IVD市场竞争格局:
2、外企高歌猛进(2000-2005年)
2000年后,随着中国IVD市场需求的日益扩大,外资企业逐渐察觉了国内市场的巨大商机,特别是2001年中国加入WTO之后,外资企业解除了后顾之忧,开始大规模进入中国市场,其市场份额也大幅提升,并逐步在三级医院等高端市场基本占据垄断地位。
3、国内龙头初具雏形(2005年后)
在跨国公司不断攻城略地的时候,一部分先知先觉的国内企业也开始了技术追赶的历程。
虽然目前外资企业依然占据着国内IVD市场的过半份额且整体增速依然高于国内企业,但随着内资企业的逐步成长,部分领军企业已经在某些细分领域取得了技术突破,如目前在血液分析仪(三分类、五分类仪)以及在全自动生化仪方面国产仪器已经能够与进口产品一争高下,龙头企业也已经完成了仪器-试剂的一体化,其中较为典型的就是目前内资IVD的领军者迈瑞和科华。
四、IVD行业监管情况、法规及产业政策
1、行业主管部门
目前,我国体外诊断试剂行业已经形成了政府部门监督与行业自律相结合的管理方式,将体外诊断试剂作为单独一类产品管理。
(1)国家食品药品监监督管理局(CFDA)
体外诊断试剂行业的主管部门为国家食品药品监督管理总局,其下属的医疗器械注册管理司、医疗器械监管司负责具体监管,主要履行有关医疗器械的产品标准、市场准入、生产企业资格、产品临床试验、产品注册等管理职能。
中国药品生物制品检定所是国家食品药品监督管理局的直属事业单位,是国家检验药品生物制品质量的法定机构和最高技术仲裁机构,其下设体外诊断试剂与培养基室,负责按医疗器械管理的诊断试剂及临床检验分析一起的检验及有关国家标准的技术审核、修订或起草等。
(2)卫生部临床检测中心(NCCL)
卫生部临床检测中心作为卫生部检验质量管理与控制中心,也履行部分行业监管职责,包括:
组织全国临床检验质量管理与控制活动,组织开展全国医疗机构实验室室间质量评价,协助制定临床检验质量管理与控制技术规范与标准,提供相关工作建议与咨询、论证意见,落实临床检验质量管理和控制措施。
(3)行业协会组织
中国医疗器械行业协会是体外诊断试剂行业的自律组织,主要工作为负责行业发展调查、监督执行行业政策、参与相关标准制定、组织行业交流合作、开展行业咨询等。
2、监管体制
我国将体外诊断行业作为单独一类产品并作为医疗器械进行分类管理,对医疗器械的生产经营采取生产许可、产品注册和备案经营许可制度。
对开办医疗器械生产的企业,应按分类获得相应级别的政府食品药品监督管理部门的同意,取得《医疗器械生产企业许可证》,在有效期(有效期5年)内开展生产活动。
产品注册制度对体外试剂试行分类注册管理,符合要求的产品可在通过相应级别的政府食品药品监督管理机构审查后取得《医疗器械注册证》,在有效期内(有效期4年)从事所注册产品的生产销售。
经营许可制度要求从事医疗器械经营的企业分类取得相应级别政府食品药品监督管理部门核发的《医疗器械经营企业许可证》,在有效期(有效期5年)内从事相关经营活动。
经营第一类医疗器械不需许可和备案,经营第二类医疗器械实行备案管理,经营第三类医疗器械实行许可管理。
3、IVD行业主要法律法规
4、IVD行业相关产业政策
我国的体外诊断试剂行业尚处于发展初期,近年来国家、地方有关部门相继出台了一系列政策措施,支持体外诊断试剂行业发展。
(1)2009年6月,国务院办公厅发布《促进生物产业加快发展的若干政策》(国办发【2009】45号),旨在通过加大投入、人才培养、财税支持和改善市场环境等方式,将生物产业培育成为高技术领域的支柱产业和国家战略性新兴产业。
其中,将严重威胁我国人民群众生命健康的重大传染病的新型疫苗和诊断试剂作为生物医药的重点发展领域。
(2)2010年10月,科技部发布《国家高技术研究发展计划(863计划)生物和医药技术领域体外诊断技术产品开发重大项目申请指南》,设立了“体外诊断技术产品开发”重大项目,指出要突破一批体外诊断仪器设备与试剂的重大关键技术,研制出一批具有自主知识产权的创新产品和具有国际竞争力的优质产品,在临床检验设备、试剂、原材料、检测、推广方面提升行业的技术创新能力和国际竞争力,提高体外诊断产品在高端市场的国产化率等。
(3)2011年3月27日,国家发改委发布《产业结构调整指导目录(2011年本)》,将“新型诊断试剂的开发和生产”、“新型医用诊断医疗仪器设备”、“诊断用酶等酶制剂”列为鼓励类项目
(4)2011年7月14日,科技部发布《国家“十二五”科学和技术发展规划》,在国家科技重大专项上,要求重点围绕艾滋病、病毒性肝炎、结核病等重大传染病,突破检测诊断、监测预警、疫苗研发和临床救治等关键技术,研制150种诊断试剂,其中20种以上获得注册证书。
(5)2011年11月28日,科技部发布《“十二五”生物技术发展规划》,要求突破一批体外诊断仪器设备与试剂的重大关键技术,在一体化化学发光免疫诊断系统等高端产品方面实现重大突破,加速体外诊断产业的结构调整和优化升级。
(6)2011年12月,科技部颁布《医疗器械科技产业“十二五”专项规划》(国科发计(2011)705号),指出到2015年,初步建立医疗器械研发创新链,医疗器械产业技术创新能力显著提升;突破一批共性关键技术和核心部件,重点开发一批具有自主知识产权的、高性能、高品质、低成本和主要依赖进口的基本医疗器械产品,提出产品上创制50-80项临床急需的新型预防、诊断、治疗、康复、急救医疗器械产品,重点开发需求量大、应用面广以及主要进口的基础装备和医用材料。
研发能力突出、产品线丰富、销售规模较大的医疗器械龙头企业有望得到国家的重点扶持。
(7)2012年7月,国务院出台《“十二五”国家战略性新兴产业发展规划》,提出加快培育和发展节能环保、新一代信息技术、生物、高端装备制造等七战略性新兴产业。
在生物产业中,提出:
研究开发
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 体外 诊断 IVD 行业 分析 报告
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 国企会计岗位笔试试题及答案解析(分享).docx
国企会计岗位笔试试题及答案解析(分享).docx
 行政事业单位内部审计流程图(按照新内部审计准则).xls
行政事业单位内部审计流程图(按照新内部审计准则).xls
