 初中化学方程式超级大全中考版.docx
初中化学方程式超级大全中考版.docx
- 文档编号:23457342
- 上传时间:2023-05-17
- 格式:DOCX
- 页数:19
- 大小:83.65KB
初中化学方程式超级大全中考版.docx
《初中化学方程式超级大全中考版.docx》由会员分享,可在线阅读,更多相关《初中化学方程式超级大全中考版.docx(19页珍藏版)》请在冰豆网上搜索。
初中化学方程式超级大全中考版
初中化学方程式超级大全(中考版)
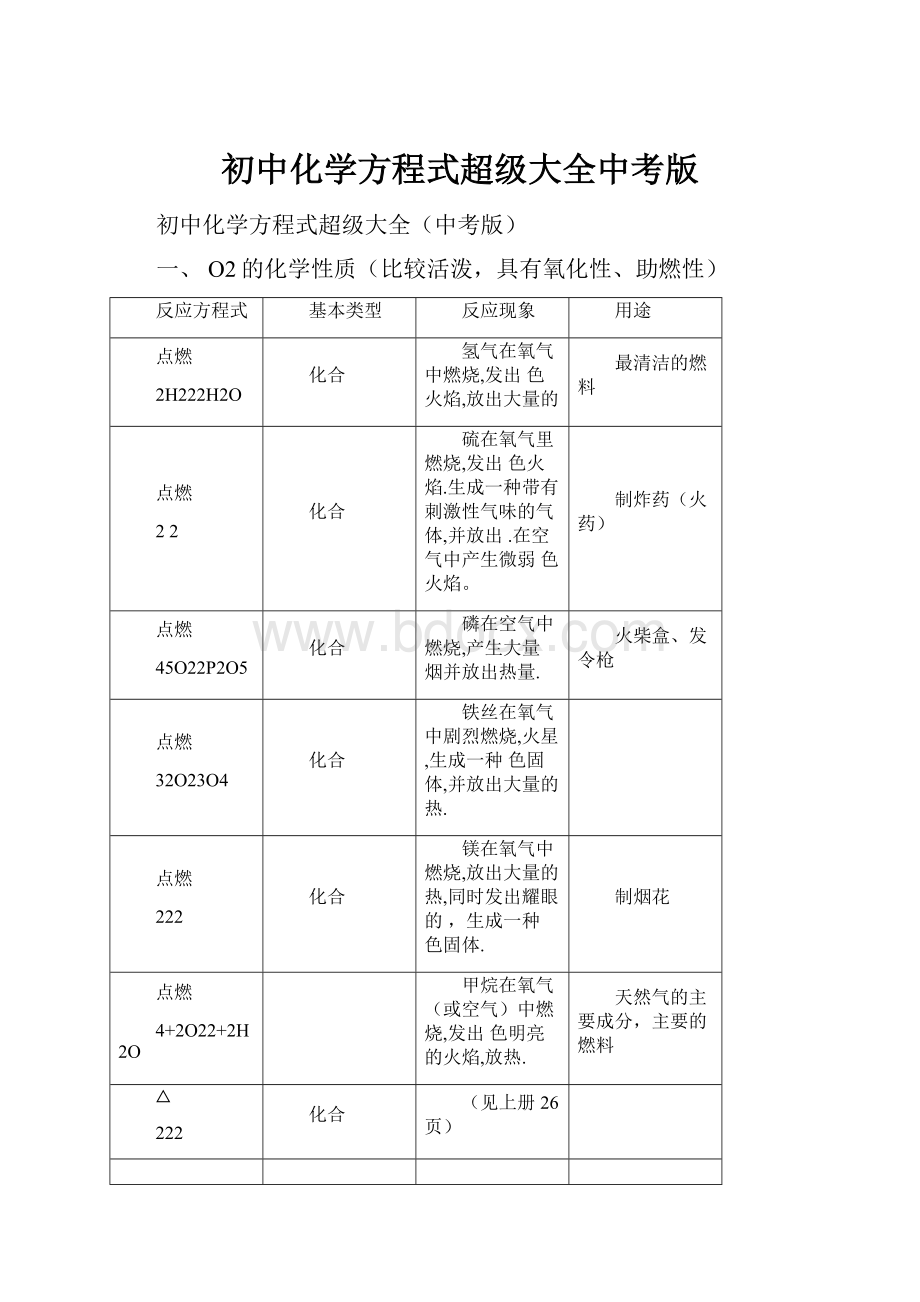
一、O2的化学性质(比较活泼,具有氧化性、助燃性)
反应方程式
基本类型
反应现象
用途
点燃
2H222H2O
化合
氢气在氧气中燃烧,发出色火焰,放出大量的
最清洁的燃料
点燃
22
化合
硫在氧气里燃烧,发出色火焰.生成一种带有刺激性气味的气体,并放出.在空气中产生微弱色火焰。
制炸药(火药)
点燃
45O22P2O5
化合
磷在空气中燃烧,产生大量烟并放出热量.
火柴盒、发令枪
点燃
32O23O4
化合
铁丝在氧气中剧烈燃烧,火星,生成一种色固体,并放出大量的热.
点燃
222
化合
镁在氧气中燃烧,放出大量的热,同时发出耀眼的,生成一种色固体.
制烟花
点燃
4+2O22+2H2O
甲烷在氧气(或空气)中燃烧,发出色明亮的火焰,放热.
天然气的主要成分,主要的燃料
△
222
化合
(见上册26页)
二.O2的制法
反应方程式
基本类型
反应现象
用途
△
242422↑
分解
实验室制取O2
2
2323O2↑
△
分解
2
2H2O22H22↑
分解
产生大量无色气泡
通电
2H22H2↑2↑
分解
正负电极上分别产生无色气泡,负极上产生的气体体积是正极上产生气体体积的两倍
△
222↑
分解
色固体渐消失,产生色液体
三.C的化学性质
1.可燃性
反应方程式
基本类型
反应现象
用途
(O2充足)点燃
22
化合
碳在氧气里燃烧,发出白光,并放出热量,燃烧后生成的无色气体能使澄清石灰水变浑浊
煤,木炭的主要成分,做燃料
(O2不充足)点燃
2C22
化合
碳在氧气里燃烧,发出白光,并放出热量,燃烧后生成的无色气体有毒
含碳燃料不充分的燃烧均生成
2.还原性
反应方程式
基本类型
反应现象
用途
高温
22
化合
该反应热
煤炉中的反应之一
高温
222↑
置换
黑色固体逐渐变成色,且生成一种能使澄清石灰水变浑浊的气体
还原
(冶炼金属)
高温
22O33C432↑
置换
还原2O3(炼铁)
四.的化学性质
1.可燃性
反应方程式
基本类型
反应现象
用途
点燃
2222
化合
一氧化碳在空气中燃烧,发出色火焰,并放出热量,燃烧后生成的无色气体能使澄清石灰水变浑浊
煤气主要成分,做燃料
2.还原性
反应方程式
基本类型
反应现象
用途
△
2
色的逐渐变成色的,且生成一种使澄清石灰水变浑浊的无色气体
还原(冶炼铜)
高温
2O3+3232
还原2O3(炼铁)
高温
3O4+4342
还原3O4(炼铁)
对比:
△
H22O
置换
黑色固体变红色,管壁有水珠
精练
五2的化学性质
1.与H2O反应
反应方程式
基本类型
反应现象
用途
2223
化合
将2通入紫色石蕊溶液,溶液变色
制碳酸饮料
△
H2322↑
分解
加热上述溶液产生气泡,且变回色
(H23不稳定)
2.与碱的反应
反应方程式
类型
反应现象
用途
()223↓2O
产生白色沉淀.(石灰水变浑浊)
用石灰浆粉刷墙壁;实验室检验2
22232O
无明显现象
工业上吸收废气
六、2的制取
反应方程式
类型
反应现象
用途
3+2222↑
复分解
产生无色气泡,大理石逐渐溶解
实验室制取2,在大理石上"刻字"
23+2222↑
复分解
反应剧烈,产生大量气泡,白色固体溶解
可治疗胃酸过多
324422↑
复分解
开始产生无色气泡,过一会儿,反应逐渐停止
大理石与硫酸在常温下反应,生成微溶于水的4、水和2,微溶的4会包住大理石,使反应停止(一般不用于制2)
高温
32↑
分解
工业上用石灰石制取生石灰、2
七.金属的化学性质
金属活动性顺序:
K(H)
反应方程式
类型
反应现象
用途
金属+O2→金属氧化物
43O222O3
化合
常温下铝表面形成致密氧化膜
△
222
化合
△
222
化合
红色固体变成色固体
金属+酸→盐+H2
2442↑
置换
铁钉表面有少量无色气泡生成,无色溶液逐渐变成浅色
2442↑
置换
反应较剧烈,产生无色气泡,锌粒逐渐溶解;
实验室制取H2
222↑
置换
反应剧烈,产生大量无色气泡,镁条溶解;
金属+盐→盐+金属
44
置换
铁钉表面有色物质生成,色溶液逐渐变成浅色
古代湿法制
2342(4)3+3
置换
铝片表面有红色物质生成,色溶液逐渐变成无色
23(3)2+2
置换
铜片表面有色物质生成,无色溶液逐渐变成浅色
八.酸、碱、盐的性质
1、酸在水中的解离方程式进行总结归纳:
=+H24=242-3=3-
2、几种碱在水中的解离方程式:
=+=+()2=2++2
3、几种盐在水中的解离方程式:
=+2(4)3=23++342-3+3-
4=+4-42++42-2=2++2–
酸碱盐概念的比较
化学组成
举例
溶液中的阴、阳离子
酸
氢离子和酸根离子
3
阳离子:
全部是,阴离子是酸根离子
碱
氢氧根离子和金属离子
阴离子:
金属离子,阴离子:
全部是—
盐
金属离子和酸根离子
3
阳离子:
金属离子阴离子:
酸根离子
附表1稀硫酸的化学性质(稀盐酸相似)
实验内容
实验现象
实验结论(或化学方程式,注明基本类型)
跟指示剂反应
1、紫色石蕊试液
2、无色酚酞试液
1、试液显色
试液显色
1、紫色石蕊遇酸溶液
2、无色酚酞遇酸溶液
跟金属反应
1、镁条
2、锌粒
3、铁钉
1、反应剧烈,产生,镁条溶解;
2、反应较剧烈,产生,锌粒逐渐溶解;
3、铁钉表面有少量,溶液逐渐变为色
2442↑
2442↑
2442↑
跟金属氧化物反应
1、铁锈(除铁锈)
2、氧化铜
1、铁钉表面的锈逐渐溶解,溶液显色
2、黑色固体溶解,溶液显色
2O3+3H242(4)3+3H2O
2442O
跟碱反应
()2
蓝色固体慢慢溶解,溶液显色
()2244+2H2O
跟盐反应
1、2溶液
2、23固体
1、生成
2、固体溶解,产生大量
1、2244↓+2
2、23242422↑
附表2盐酸与硫酸的性质比较表
项目
名称
盐酸
硫酸
化学式
H24
颜色,气味
浓无色、有性气味
浓H24无色无味
挥发性
浓易挥发(在空气中形成)
不挥发 。
有性、性
与指示剂作用
紫色石蕊变
无色酚酞
紫色石蕊变
无色酚酞
与活泼金属反应
(练习书写化学方程式,并注明基本类型,下同)
222↑
222↑
2442↑
23H242(4)3+3H2↑
与金属氧化物反应
222O
2O3+623+3H2O
2O3+3H242(4)3+3H2O
H2442O
与碱的反应
2O
()2+22+2H2O
()2244+2H2O
2()3+3H242(4)3+6H2O
与某些盐反应
3↓3
3+2222↑
322↑
(3)2244↓+23
K2324=K24+H22↑
鉴别试剂
3溶液和稀3
2溶液或(3)2溶液和稀3
附表3氢氧化钠的化学性质
实验步骤
实验现象
实验结论(或化学方程式)
1、与指示剂的反应
紫色石蕊试液变色
无色酚酞试液变色
氢氧化钠溶液使紫色石蕊试液变色,
氢氧化钠溶液使无色酚酞试液变色
2、与非金属氧化物反应
氢氧化钠与二氧化碳
氢氧化钙溶液与二氧化碳
1、
2、
1、
2、
3、与盐溶液的反应
氢氧化钠溶液与硫酸铜溶液
氢氧化钠溶液与氯化铁溶液
氢氧化钙溶液与碳酸钠溶液
氢氧化钡溶液与硫酸铜溶液
1、产生色沉淀
2、产生色沉淀
3、产生色沉淀
4、产生蓝、白色沉淀
1、4+2()2↓24
2、3+3()3↓+3
3、()2233↓+2
4、4()2()2↓4↓
附表4氢氧化钠与氢氧化钙的性质比较表
用途
性质
氢氧化钠
氢氧化钙
化学式
()2
俗名
烧碱火碱苛性钠
熟石灰消石灰
物理性质
1、白色固体
2、具有吸水性(易潮解)
3、极易溶于水,放热
4、具有强腐蚀性
1、白色固体
2、微溶于水
3、具有腐蚀性
工业制法
()2+23=3↓+2
(纯碱)
高温
3+、2↑
+H2O()2(剧烈反应,放出大量热,白色块状固体变成粉末)
化学性质
1、使紫色石蕊试液变蓝色,使无色酚酞试液变红色
2、与某些非金属氧化物反应
22232O
22232O
23242O
(工业上吸收废气)
3、与酸反应
2O
22424+2H2O
332O
4、与某些盐反应
24()2↓24
2+2()2↓+2
(3)2+2()2↓+23
1、使紫色石蕊试液变蓝色,使无色酚酞试液变红色
2、与某些非金属氧化物反应
()223↓2O
(用于鉴别2气体)
3、与酸反应(用于中和土壤酸性)
()2244+2H2O
()2+22+2H2O
()2244+2H2O
4、与某些盐反应
()2233↓+2
()24()2↓4(波尔多液的制取)
()2233↓+2
△盐的化学性质(1、2、3见上述内容)
1、盐溶液+金属→新盐+新金属
2、盐+酸→新盐+新酸
3、盐+碱→新盐+新碱
4、盐+盐→两种新盐
例:
424↓23↓+3
23+2=23↓K23+(3)2=23+3↓
初中化学全册方程式网络图
一、氧系网络
①
②
③
④
⑤
⑥
⑦
⑧
⑨
⑩
⑾
⑿
⒀
⒁
⒂
二、碳系网络
⑴可燃性
还原性
⑵可燃性
还原性
⑶可燃性
还原性
⑷
⑸
⑹
⑺
⑻实验室制二氧化碳
工业制二氧化碳
⑼
⑽
⑾
⑿
三、金属、酸、碱、盐系网络
(一)、复分解反应(有五类、见上图①②③④⑤)
①酸+金属氧化物→盐+水
②酸+碱→盐+水
③酸+盐→酸+盐
④盐+碱→盐+碱
⑤盐+盐→盐+盐
(二)金属和酸、盐溶液的置换反应(见上图⑥⑦)
⑥金属+酸→盐+氢气
⑦金属+盐→金属+盐
(三)金属氧化物制碱的反应(见上图⑧ 2O、K2O、、分别和水反应 )
⑧金属氧化物+水→碱
(四)非金属氧化物制取酸(见上图⑨ 2、2、3分别和水反应)
⑨非金属氧化物+水→酸
(五)碱溶液和金属氧化物反应( 见上图⑩ )
⑩碱溶液+非金属氧化物→盐+水
(六)还原剂还原金属氧化物(见上图⑾)
巧记初中化学全册方程式
反应类型
巧记内容
化合反应
单+单
P、S、H2、C、、、、的完全燃烧,C的不完全燃烧
单+化
的燃烧、高温2和木炭反应得
化+化
2、2、3或、K2O、2O、与水反应得对应酸碱
分解反应
氧化物
H2O、H2O2分解
酸
H23分解
碱
不溶性碱()2、()3分解
盐
4、3、3分解
置换反应
金属+酸
金属活动性在H前,酸一般用稀H24、稀
金属+盐
遵守金属活动性前置后,盐可溶
金属氧化物+还原性单质
常见、2O3和H2、C反应
复分解反应
酸+金属氧化物
酸+金属氧化物→盐+H2O
酸+碱
酸+碱→盐+H2O
盐+酸
盐+酸→盐+酸(盐不能用4、)
盐+碱
盐+碱→盐+碱(反应物必须全溶)
盐+盐
盐+盐→盐+盐(反应物必须全溶)
非四大
反应类型
一氧化碳做还原剂
常见、2O3和反应
二氧化碳和可溶性碱
常见2和()2、反应
有机物的燃烧
常见4的燃烧
写出以上反应的化学方程式
反应类型
记忆
化学方程式
化合反应
单+单
P +
S +
H2 +
C +
C +
+
+
+
+
单+化(全书共2个)
+
2 +
化+化
2 +
2 +
3+
+
K2O+
2O+
+
分解反应
氧化物分解
H2O ——
H2O2 ——
酸分解
H23 ——
不溶性碱分解
()2 ——
()3 ——
盐分解
4 ——
3 ——
3 ——
置换反应
(金属活动顺序表)
1、金属+酸
+
+
2、金属+盐(可溶)
+
+
3、金属氧化物+单质还原剂
+
2O3 +
复分解反应
(反应条件为生成物有H2O、↑、↓)
不参加复分解反应的四个物质分别为:
1、酸+金属氧化物
+
2O3 +
2、酸+碱
(中和反应)
+
()2 +
3、盐+酸
(盐必须溶于酸)
3 +
3 +
3 +
3 +
2+
4、盐+碱
(反应物全溶)
4+()2
5、盐+盐(反应物全溶)
非四大反应类型
一氧化碳做还原剂
+
2O3 +
二氧化碳+可溶性碱
2 +
2 +
2 +
2 +
有机物燃烧
4 +
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 初中 化学方程式 超级 大全 中考
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《地质测量图绘制细则》.docx
《地质测量图绘制细则》.docx
