 化学必修一氧化还原反应与离子反应知识点总结及练习题.docx
化学必修一氧化还原反应与离子反应知识点总结及练习题.docx
- 文档编号:2337943
- 上传时间:2022-10-28
- 格式:DOCX
- 页数:14
- 大小:162.05KB
化学必修一氧化还原反应与离子反应知识点总结及练习题.docx
《化学必修一氧化还原反应与离子反应知识点总结及练习题.docx》由会员分享,可在线阅读,更多相关《化学必修一氧化还原反应与离子反应知识点总结及练习题.docx(14页珍藏版)》请在冰豆网上搜索。
化学必修一氧化还原反应与离子反应知识点总结及练习题
氧化还原反应与离子反应知识点总结
一、氧化还原反应的有关概念
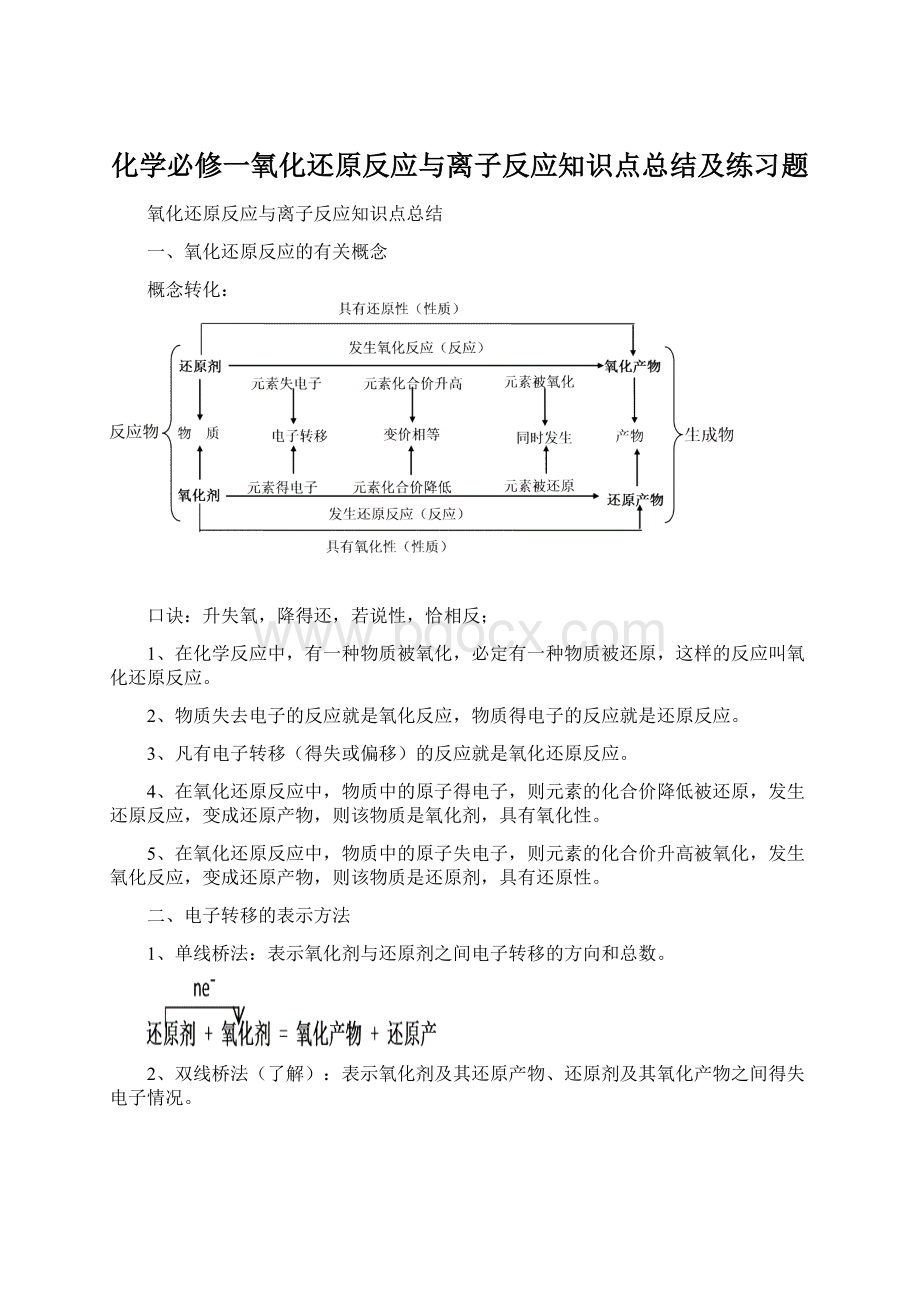
概念转化:
口诀:
升失氧,降得还,若说性,恰相反;
1、在化学反应中,有一种物质被氧化,必定有一种物质被还原,这样的反应叫氧化还原反应。
2、物质失去电子的反应就是氧化反应,物质得电子的反应就是还原反应。
3、凡有电子转移(得失或偏移)的反应就是氧化还原反应。
4、在氧化还原反应中,物质中的原子得电子,则元素的化合价降低被还原,发生还原反应,变成还原产物,则该物质是氧化剂,具有氧化性。
5、在氧化还原反应中,物质中的原子失电子,则元素的化合价升高被氧化,发生氧化反应,变成还原产物,则该物质是还原剂,具有还原性。
二、电子转移的表示方法
1、单线桥法:
表示氧化剂与还原剂之间电子转移的方向和总数。
2、双线桥法(了解):
表示氧化剂及其还原产物、还原剂及其氧化产物之间得失电子情况。
三、中学常见的氧化剂和还原剂及氧化性、还原性强弱的判断方法
(一)常见氧化剂与还原剂
1、氧化剂
(1)非金属性较强的单质:
(2)变价元素中高价态化合物:
(3)高价态金属阳离子:
(4)能电离出H+的物质:
(5)其他:
2、还原剂
(1)金属性较强的单质:
(2)某些非金属单质:
(3)变价金属中某些低价态化合物:
(4)其他:
单质S、Sn2+盐、浓盐酸、NH3等
(二)氧化性、还原性强弱的常用判断方法(两种题型考法)
1、根据金属活泼性判断
金属的金属性越强,单质的还原性越强,其对应离子的氧化性越弱。
(1)单质的还原性:
按金属活动性顺序依次减弱。
(强调顺序)
(2)离子的氧化性:
按金属活动性顺序依次增强(铁指Fe2+)
如氧化性:
2、根据非金属的活泼性判断
非金属性越强,单质的氧化性越强,其对应离子的还原性越弱。
(1)单质的氧化性:
(2)离子的还原性:
3、通过元素周期表判断
4、通过化学反应判断
氧化剂+还原剂氧化产物+还原产物
氧化性:
氧化剂>氧化产物;还原性:
还原剂>还原产物。
简记为:
左>右。
5、通过相近的反应判断
如由,可得出氧化性:
6、有反应条件的难易比较
不同氧化剂与同一还原剂反应时,反应条件越易,氧化性越强;不同还原剂与同一氧化剂反应时,反应条件越易,还原性越强。
如卤素单质按的顺序反应条件越来越难,反应条件要求越来越高,则可得出氧化性:
。
氧化还原反应专项练习
1.下列反应不属于四种基本反应类型,但属于氧化还原反应的是[]
A.2F2+2H2O==4HF+O2↑
C.2AgNO3+Na2CO3==2NaNO3+Ag2CO3↓
2.下列变化属于还原反应的是[]
A.Fe——→FeSO4 B.Cu(NO3)2——→Cu C.P——→P2O5 D.NaCl——→AgCl
3.下列说法中错误的是[]
A.化合反应不一定是氧化还原反应 B.分解反应不一定是氧化还原反应
C.置换反应一定是氧化还原反应 D.复分解反应一定是氧化还原反应
4.实现下列反应需加入氧化剂的是[]
A.HCl——→CaCl2 B.HCl——→H2 C.HCl——→Cl2 D.HCl——→CO2
5.下列对氧化还原反应的分析中合理的是[]
A.Mg变为MgO时化合价升高,因此Mg在该反应中应中作还原剂
B.KMnO4受热分解时,Mn元素化合价一方面升高一方面降低,因此反应中锰元素既被氧化又被还原
C.凡是氧化还原反应能能造福于人类
6.某元素在化学反应中由化合态变为游离态,则该元素[]
A.一定被氧化 B.一定被还原
C.既可能被氧化又可能被还原 D.以上都不是
7.在下列有关氧化还原反应的叙述中,正确的是[]
A.肯定有一种元素被氧化,另一种元素被还原
B.在反应中不一定所有元素的化合价都发生变化
C.置换反应一定属于氧化还原反应
D.氧化还原反应中的任一反应物,不是氧化剂,就一定是还原剂
8.下列粒子中,既具有氧化性,又具有还原性的是()
A.MgB.Zn2+C.Fe2+D.HCl
9.下列各反应中,水只做氧化剂的是()
A.C+H2O=CO+H2B.2H2O=2H2↑+O2↑
C.Na2O+H2O=2NaOHD.CuO+H2=Cu+H2O
10、对C+CO2===2CO的说法不正确的是
A、该反应是氧化还原反应B、该反应的氧化剂是CO2
C、氧化产物与还原产物的物质的量之比是1:
1
D、按照方程式该反应中转移的电子数是4
11、已知反应CL2+H2O===HCL+HCLO,对该反应的说法正确的是
A、CL2是氧化剂,H2O是还原剂B、氧化剂与还原剂的物质的量比是1:
2
C、按照方程式进行,氧化剂失电子1molD、CL2既是氧化剂又是还原剂
12.黑火药爆炸反应为:
S+2KNO3+3C=K2S+3CO2↑+N2↑。
在该反应中,氧化剂是()
①C②S③K2S④KNO3⑤N2
A、①③⑤B、②④C、②④⑤D、③④⑤
13.在H2SO3+2H2S=3H2O+3S反应中,被氧化与被还原元素的质量比为()
A.1:
1B.2:
1C.1:
2D.3:
2
14.M2O7x-离子和S2-在酸性溶液中发生如下反应:
M2O7x-+3S2-+14H+=2M3++3S↓+7H2O,则M2O7x-离子中M的化合价是()
A+2B+3C+4D+6
15.已知:
Ni+CuSO4=NiSO4+CuCu+2AgNO3=Cu(NO3)2+2Ag则下列判断正确的是()
A.还原性:
Ni>Cu>AgB.氧化性:
Ni2+>Cu2+>Ag+
C.还原性:
Ni Ni2+ 16.标出下列氧化还原反应中电子转移的方向和数目。 Cl2+2KBr=2KCl+Br2H2S+Cl2=S↓+2HCl 氧化剂: 还原剂: 氧化剂: 还原剂: MnO2+4HCl=MnCl2+Cl2↑+2H2O3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O 氧化剂: 还原剂: 氧化剂: 还原剂: 2H2S+SO2=3S+2H2OCl2+H2O=HCl+HClO 氧化剂: 还原剂: 氧化剂: 还原剂: 2FeCl3+2KI=2FeCl2+2KCl+I22Al+6H+=2Al3++3H2↑ 氧化剂: 还原剂: 氧化剂: 还原剂: 17.在2KClO3=2KCl+3O2↑的反应中,氯元素从__价变为__价,发生____反应;氧化剂是______,还原剂是______。 电子从___元素转移给__元素,转移的电子总数是_______。 18.氧化还原反应的实质是____________,其特征是____________。 物质中的某元素发生氧化反应时,反应结果该元素的化合价____,该物质在反应中所起的作用是________________;物质中某元素被还原时,它发生了______反应,______电子,结果化合价______,该物质在反应中所起的作用是____________。 19.在Cu2+、Fe2+、Al3+、Fe、Cl2、Cl-、S2-、S八种粒子中,只具有氧化性的是_________,只具有还原性的是_____________,既具有氧化性又具有还原性的是______________。 1.最外层具有8个电子(只有一个电子层的具有2个电子)的结构,属于相对稳定结构。 金属元素最外层电子一般少于4个,在反应中易失去电子;非金属元素最外层电子一般多于4个,在反应中易得到电子。 2.离子: 是带电的原子 原子 离子 定义 化学反应中的最小微粒 带电的原子(或原子团) 电性 不带电 带电荷 阳离子: 所带电荷数=+(质子数-核外电子数) 阴离子: 所带电荷数=-(核外电子数-质子数) 联系 都是构成物质的一种粒子,原子失去电子变成阳离子,原子得到电子变成阴离子 3、物质与其构成粒子之间的关系 4.物质的构成和物质组成的表示 5.相对原子质量: 是原子的相对质量,即以一种碳原子(原子核内有6个质子和6个中子的一种碳原子)质量的十二分之一作为标准,其他原子的实际质量跟它相比较,所得的数值,就是该种原子的相对原子质量 6.a.离子概念: 带电的原子或原子团 分类及形成: 阳离子(由于原子失去电子而形成)带正电;阴离子(由于原子得到电子而形成)带负电 b.注意: 原子在变为离子时,质子数、元素种类没有改变;电子数、最外层电子数、元素化学性质发生了改变。 c.表示方法: 在元素符号右上角标明电性和电荷数,数字在前,符号在后。 若数字为1时,可省略不写。 例如: 钠离子: Na+。 d.离子符号表示的意义: 表示一个某种离子;表示带n个单位某种电荷的离子。 例如: Fe3+: 带3个单位正电荷的铁离子 e.元素符号右上角的数字的含义: 表示一个离子所带的电荷数。 例如: Fe3+: 3表示一个铁离子带3个单位的正电荷 f.离子中质子数与电子数的关系: 阳离子: 质子数>电子数阴离子: 质子数<电子数 g.离子与原子的区别与联系 粒子的种类 原子 离子 阳离子 阴离子 区 别 粒子结构 质子数=电子数 质子数>电子数 质子数<电子数 粒子电性 不显电性 显正电 显负电 符号 用元素符号表示 用离子符号表示 用离子符号表示 相互转化 阳离子原子阴离子 相同点 都是构成物质的一种微粒;质量、体积都很小;在不停运动;有间隙 h.离子个数的表示方法: 在离子符号前面加系数。 例如: 2个钠离子: 2Na+ i.离子符号前面的数字: 表示离子的个数。 7.、离子间能发生复分解反应而不能大量共存: (1)离子间能生成难溶或微溶的物质,而不能大量共存。 如: ①SO42ˉ与Ba2+、Ca2+、Ag+等不能共存; ②CO32ˉ与Ba2+、Ca2+、Mg2+、Ag+、Cu2+、Zn2+等不能共存; ③S2ˉ与Cu2+、Pb2+、Fe2+、Hg2+、Ag+等不能共存; ④OHˉ与Mg2+、Al3+、Fe2+、Fe3+、Cu2+、Ag+、Zn2+等不能共存; ⑤AlO2ˉ与HCO3ˉ不能大量共存: AlO2ˉ+HCO3ˉ+H2O=Al(OH)3↓+CO32ˉ (2)离子间能生成气体或易挥发性物质而不能大量共存。 如: H+与CO32ˉ、HCO3ˉ、SO32ˉ、HSO3ˉ、S2ˉ、HSˉ等不能共存; (3)离子间能发生氧化还原反应而不能大量共存。 如: ①H+与OHˉ、AlO2ˉ、SiO32ˉ、ClOˉ、Fˉ、PO43ˉ、HPO42ˉ、H2PO4ˉ、CH3COOˉ、C6H5Oˉ等不能大量共存; ②OHˉ与H+、NH4+、HCO3ˉ、HSO3ˉ、HSˉ、H2PO4ˉ、HPO42ˉ等不能大量共存; 8.、离子间能发生氧化还原反应而不能大量共存: (1)在酸性条件下 ①NO3ˉ与Iˉ、Brˉ、Fe2+、S2ˉ、HSˉ、SO32ˉ、HSO3ˉ等不能共存; ②S2ˉ与SO32ˉ等不能共存;(碱性条件下可以共存) ③MnO4ˉ与Iˉ、Brˉ、Clˉ、S2ˉ、HSˉ
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 化学 必修 氧化 还原 反应 离子 知识点 总结 练习题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 (完整word版)信息论与编码期末考试题----学生复习用.doc
(完整word版)信息论与编码期末考试题----学生复习用.doc
 (完整版)固定资产盘点表.xls
(完整版)固定资产盘点表.xls
