 高中化学选修五141.docx
高中化学选修五141.docx
- 文档编号:23139207
- 上传时间:2023-05-08
- 格式:DOCX
- 页数:9
- 大小:101.95KB
高中化学选修五141.docx
《高中化学选修五141.docx》由会员分享,可在线阅读,更多相关《高中化学选修五141.docx(9页珍藏版)》请在冰豆网上搜索。
高中化学选修五141
课时作业(六)
(时间:
45分钟 满分:
60分)
一、选择题(每小题3分,共30分)
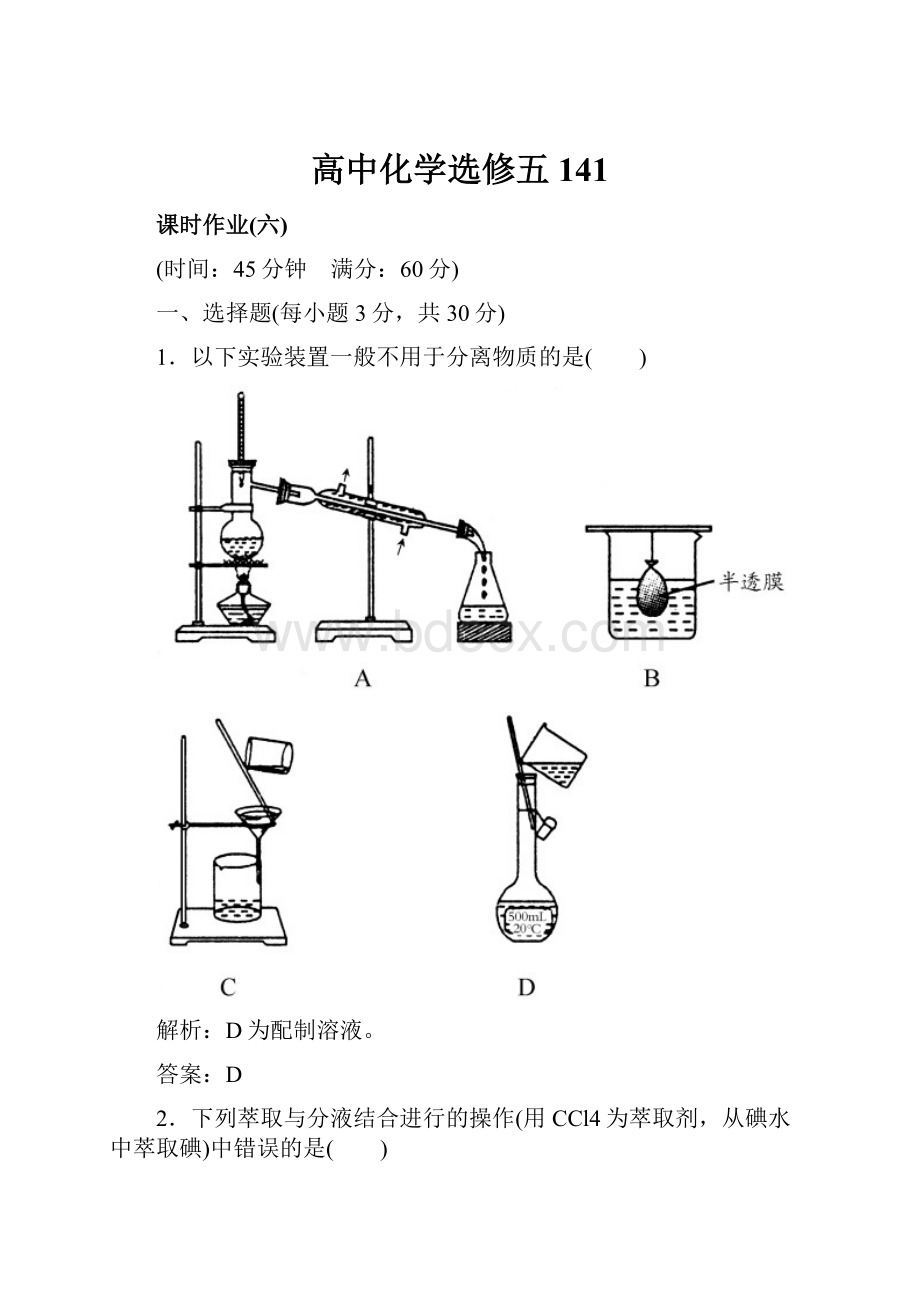
1.以下实验装置一般不用于分离物质的是( )
解析:
D为配制溶液。
答案:
D
2.下列萃取与分液结合进行的操作(用CCl4为萃取剂,从碘水中萃取碘)中错误的是( )
A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用一手压住分液漏斗上口部,一手握住活塞部分,把分液漏斗倒转过来振荡
B.静置,待分液漏斗中液体分层后,先使分液漏斗内外空气相通(准备放出液体)
C.打开分液漏斗的活塞,使全部下层液体沿盛接液体的烧杯内壁慢慢流出
D.最后继续打开活塞,另用容器盛接并保存上层液体
解析:
萃取后,分液漏斗中的下层液体从下端放出,上层液体应从上口倒出。
答案:
D
3.现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如下表。
据此,将乙二醇和丙三醇相互分离的最佳方法是( )
物质
熔点
沸点
密度
溶解性
乙二醇
-11.5℃
198℃
1.11g·cm-3
易溶于水和乙醇
丙三醇
17.9℃
290℃
1.26g·cm-3
能跟水、酒精任意比互溶
A.萃取法 B.结晶法 C.分液法 D.分馏法
解析:
混合物的分离方法,取决于组成混合物的各物质的性质差异。
萃取法适用于同一种溶质在两种互不相溶的溶剂中的溶解度差异,将混合物分离;结晶法适用于不同溶质在同一溶剂中,溶解度受温度影响的差异而实现物质分离;蒸馏(或分馏)法适用于沸点差异较大(一般大于30℃为好)的几种互溶液体混合物的分离;分液法适用于互不相溶的两种液体组成的混合物的分离。
由题中信息可知,乙二醇、丙三醇两种物质的性质差异主要表现在沸点上,所以应采用蒸馏法。
答案:
D
4.天然色素的提取往往应用到萃取操作,现在有用大量水提取的天然色素,下列溶剂不能用来萃取富集这些天然色素的是( )
A.四氯化碳B.苯
C.乙醇D.直馏汽油
解析:
乙醇极易溶于水。
答案:
C
5.用分液漏斗可以分离的一组液体混合物是( )
A.苯和CCl4B.溴和戊烷
C.溴苯和水D.汽油和煤油
解析:
溴苯和水互不相溶,分层析出。
答案:
C
6.下列关于物质的分离、提纯实验中的一些操作或做法,正确的是( )
A.在组装蒸馏装置时,温度计的水银球应伸入液面下
B.用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏
C.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量NaOH溶液
D.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到常温才过滤
解析:
用生石灰吸水,利用乙醇沸点低加热蒸出。
答案:
B
7.下列说法不正确的是( )
A.蒸馏是分离,提纯液态有机物的常用方法
B.重结晶的首要工作是选择适当的溶剂
C.萃取包括液—液萃取和固——液萃取
D.研究有机化合物可首先进行元素定量分析,再分离、提纯
解析:
研究有机化合物的基本步骤首先应该是分离、提纯然后再进行元素定量分析,所以D不正确。
答案:
D
8.下列各组混合物的分离或提纯方法不正确的是( )
A.用过滤法分离Fe(OH)3胶体和FeCl3溶液的混合物
B.用重结晶法提纯NaCl和KNO3混合物中的KNO3
C.用蒸馏法分离乙醇和甲醇的混合物
D.用萃取和分液的方法分离碘和水的混合物
解析:
胶体和溶液的分散质粒子都可以透过滤纸,故选A;KNO3的溶解度随温度变化大而NaCl的溶解度受温度影响很小,可利用重结晶法提纯KNO3;甲醇和乙醇的沸点相差较大,可用蒸馏法分离;碘易溶于有机溶剂而在水中的溶解度很小,可以利用萃取和分液的方法分离碘和水的混合物。
答案:
A
9.在一定条件下,萘可以与浓硝酸和浓硫酸的混合酸硝化生成二硝基物,它是1,5二硝基萘
和1,8二硝基萘
的混合物,后者可溶于质量分数大于98%的硫酸,而前者不能。
利用这一性质可将这两种异构体分离。
将上述硝化产物加入适量98%的硫酸,充分搅拦,用耐酸漏斗过滤,欲从滤液中得到固体1,8二硝基萘,应采用的方法是( )
A.蒸发浓缩结晶
B.向混合液中加水过滤
C.用Na2CO3溶液处理滤液
D.将滤液缓缓加入水中
解析:
由题给信息可知:
1,8二硝基萘应不溶于质量分数小于98%的浓H2SO4中,因此只要将浓H2SO4稀释后过滤即可,但要注意浓H2SO4的稀释方法是“酸入水”,否则易发生酸液沸腾溅出。
答案:
D
10.下列关于苯甲酸的重结晶实验的说法中正确的是( )
A.该实验中四次用到玻璃棒
B.该实验中第二次用到玻璃棒的作用是引流
C.该实验中结晶的温度越低越好
D.苯甲酸是常用的仪器防腐剂,因此可任意量添加
解析:
该实验中三次用到玻璃棒,即溶解时搅拌,过滤时引流(两次)。
答案:
B
二、非选择题(共30分)
11.(6分)选择下列实验方法分离提纯物质,将分离提纯方法的序号填在横线上。
A.萃取分液 B.升华 C.重结晶 D.分液 E.蒸馏 F.过滤 G.洗气
(1)________分离食盐水与沙子的混合物。
(2)________从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
(3)________分离水和汽油的混合物。
(4)________分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
(5)________除去混在乙烷中的乙烯。
(6)________提取碘水中的碘。
解析:
沙子不溶于食盐水,采用过滤的方法即可分离;硝酸钾在水中的溶解度随温度升高明显增大而NaCl在水中的溶解度受温度影响不大,采用重结晶法和过滤可将其分离;水和汽油互不相溶,分层,可用分液法进行分离;CCl4和甲苯两种互溶的液体,沸点差大于30℃,可用蒸馏法分离;乙烯中含双键,可被溴水吸收,可用洗气的方法除去;碘在有机溶剂中溶解度大,可用萃取分液方法提取。
答案:
(1)F
(2)C、F (3)D (4)E (5)G (6)A
12.(8分)化学上常用燃烧法确定有机物组成,这种方法是在电炉加热时用纯氧气氧化管内样品,根据产物的质量确定有机物的组成,下图中所列装置是用燃烧法确定有机物分子式常用的装置。
回答下列问题:
(1)产生的氧气按从左到右流向,所选择的装置各导管的连接顺序是________。
(2)C装置中浓硫酸的作用是____________________。
(3)燃烧管中氧化铜的作用是____________________。
(4)若准确称取0.9g样品(只含C、H、O三种元素中的两种或三种),经充分燃烧后,A管质量增加1.32g,B管质量增加0.54g,则该有机物的实验式为________________,要确定该有机物分子式,还要____________________。
解析:
(4)由A管质量增加可求CO2的量:
=0.03mol,由B管质量增加可求H2O的量:
=0.03mol,最后由质量守恒求氧原子的量:
=0.03mol。
所以有机物由C∶H∶O=0.03∶(0.03×2)∶0.03=1∶2∶1。
实验式:
CH2O。
答案:
(1)g、f、e、h、i、c(或d)、d(或c)、a(或b)、b(或a)
(2)吸收水蒸气,得到干燥的氧气
(3)使有机物充分氧化成CO2和H2O
(4)CH2O 测出有机物相对分子质量
13.(8分)将下图中所列仪器组装为一套实验室蒸馏石油的装置,并进行蒸馏,得到汽油和煤油。
(三)
(一)
(五)
(二)
(六)
(四)
(1)图中A、B、C三种仪器的名称是_________________________
__________________________________________________________________________________________________________________。
(2)将以下
(一)~(六)中的仪器,用字母a、b、c……表示连接顺序:
e接( );( )接( );( )接
( );( )接( );( )接( )。
(3)A仪器中c口用于________,d口用于________。
(4)蒸馏时,温度计水银球应处在________位置。
(5)在B中注入原油后,加几片碎瓷片的目的是________________________________________。
(6)在B加热,收集到沸点为60℃~150℃间的馏分是________,收集到沸点为150℃~300℃间的馏分是________。
解析:
冷凝管中冷凝水的流向应是“下进上出”,因为这样可使冷凝水充满整个冷凝管,达到最佳的冷凝效果。
由于测定的温度是蒸气的温度,故温度计的水银球应位于支管口处。
加热蒸馏时液体会暴沸,为了防止出现这种现象,我们通常在反应容器中加入几片碎瓷片。
答案:
(1)冷凝管、蒸馏烧瓶、锥形瓶
(2)i;h;a;k;l;b;f;g;m (3)进水 出水 (4)蒸馏烧瓶支管口处 (5)防止液体暴沸 (6)汽油 煤油
14.(8分)可用于分离或提纯的方法有:
A.分液 B.盐析 C.过滤 D.重结晶 E.升华 F.渗析 G.萃取 H.加热分解 I.蒸馏或分馏
下列各组混合物的分离或提纯选用上述哪一种方法最合适(把选用的方法的标号填在横线上):
(1)除去Ca(OH)2溶液中悬浮的CaCO3颗粒______;
(2)除去Fe(OH)3胶体中混有的Cl-离子________;
(3)除去乙醇中溶解的少量食盐________;
(4)分离石油中各种沸点不同的成分________;
(5)除去固体碘中混有的少量碘化钠________;
(6)除去CaO中的CaCO3________;
(7)分离苯和乙醚的混合物________;
(8)从溴苯和水中分离出溴苯________。
解析:
(1)不溶性固体和液体的分离通常用过滤的方法;
(2)因Cl-可以透过半透膜,而胶体粒子不能透过半透膜,故可用渗析法提纯胶体;(3)乙醇的沸点较低,可用蒸馏法除去溶于其中的NaCl;(4)利用沸点的不同可采用分馏的方法分离石油中的成分;(5)受热时碘易升华,可以实现碘和碘化钠的分离;(6)CaCO3受热时分解,生成CaO和CO2;(7)苯和乙醚互溶且沸点相差较大,可用蒸馏的方法分离;(8)溴苯和水互不相溶,且溴苯的密度比水大,可用分液法分离。
答案:
(1)C
(2)F (3)I (4)I (5)E (6)H (7)I (8)A
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高中化学 选修 141
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 #全自动电容电感测试仪.docx
#全自动电容电感测试仪.docx
