 第35课时 常见的化学反应.docx
第35课时 常见的化学反应.docx
- 文档编号:23133486
- 上传时间:2023-05-08
- 格式:DOCX
- 页数:21
- 大小:248.43KB
第35课时 常见的化学反应.docx
《第35课时 常见的化学反应.docx》由会员分享,可在线阅读,更多相关《第35课时 常见的化学反应.docx(21页珍藏版)》请在冰豆网上搜索。
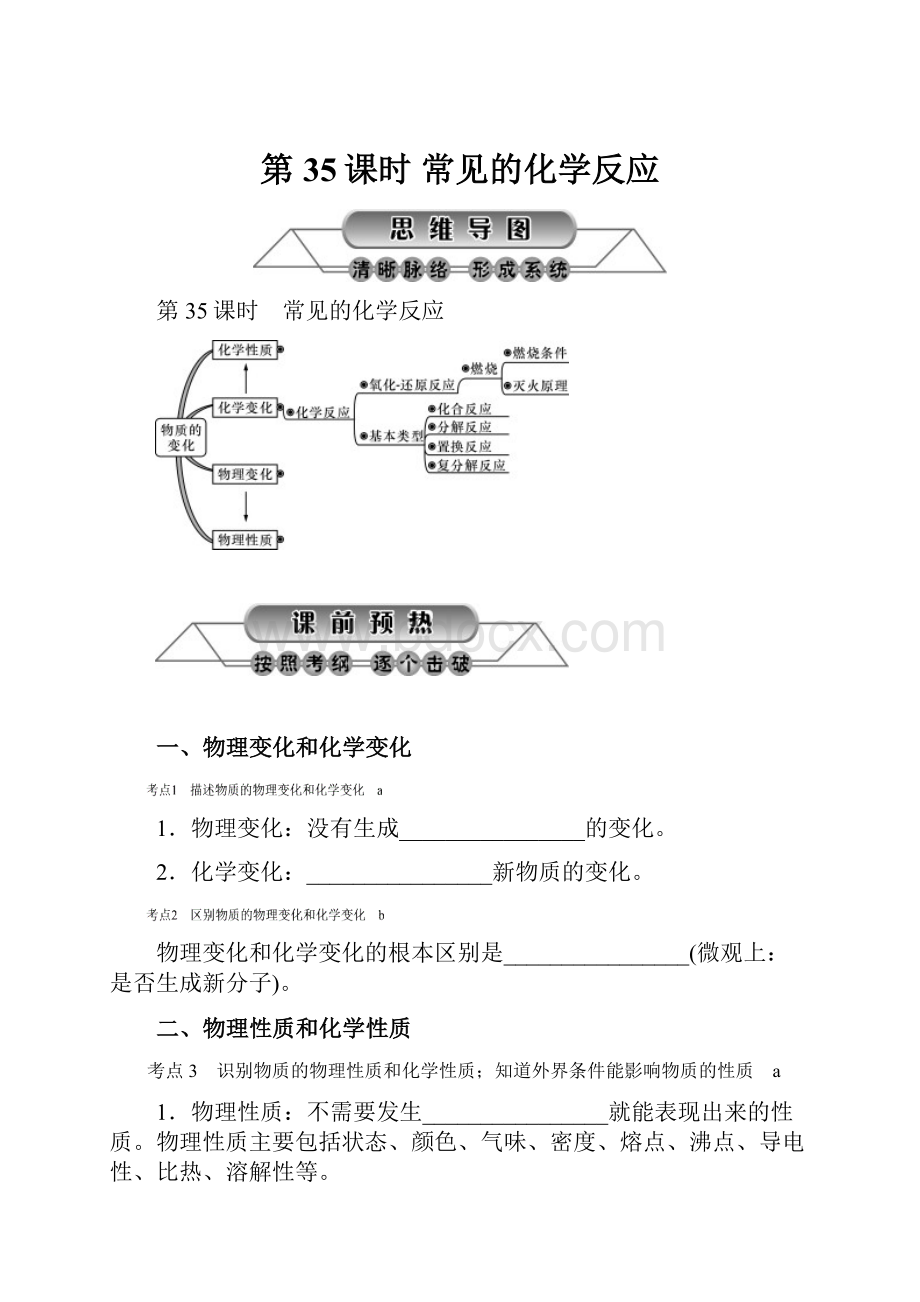
第35课时常见的化学反应
第35课时 常见的化学反应
一、物理变化和化学变化
1.物理变化:
没有生成________________的变化。
2.化学变化:
________________新物质的变化。
物理变化和化学变化的根本区别是________________(微观上:
是否生成新分子)。
二、物理性质和化学性质
考点3 识别物质的物理性质和化学性质;知道外界条件能影响物质的性质 a
1.物理性质:
不需要发生________________就能表现出来的性质。
物理性质主要包括状态、颜色、气味、密度、熔点、沸点、导电性、比热、溶解性等。
2.化学性质:
物质在________________中表现出来的性质。
化学性质主要包括:
可燃性、助燃性、毒性、氧化性、还原性等等。
三、氧化性和还原性
物质________________的反应叫氧化反应,物质________________的反应叫还原反应。
例 H2+CuO
H2O+Cu
在这个反应中,氢气得到氧化铜中的氧,________________,具有________________;氧化铜失去氧,________________,具有________________。
氧化反应中________________、具有氧化性的物质叫做________________。
氧气、氧化铜等是在氧化反应中提供氧的物质,具有________________,是常见的________________。
1.氢气和一氧化碳
氢气
一氧化碳
可
燃
性
反应
2H2+O2
2H2O
2CO+O2
2CO2
现象
淡蓝色火焰,放热,火焰上所罩干冷烧杯壁上有水雾生成
蓝色火焰,放热,生成能使澄清的石灰水变浑浊的气体
还
原
性
反应
H2+CuO
Cu+H2O
CO+CuO
Cu+CO2
装置
现象
黑色固体变红色;试管壁上有水珠生成
黑色固体变红色;生成能使澄清的石灰水变浑浊的气体。
注意:
尾气燃烧或收集起来,防止污染。
2.H2、CO等可燃性气体在使用前必须先________________,防止与空气混合受热时发生
________________。
H2的燃烧产物只有水,可用无水硫酸铜鉴别;CO的燃烧产物只有二氧化碳,可用澄清石灰水鉴别。
错误!
超链接引用无效。
1.(2017·安徽)化学在生产、生活中应用广泛,下列过程属于化学变化的是( )
2.进行如图实验,加热一段时间后,可观察到有红色物质出现,说明氢气具有( )
A.还原性
B.可燃性
C.氧化性
D.助燃性
3.某气体由氢气、一氧化碳、水蒸气中的一种或几种组成。
把该气体依次通过下列装置后,测得装有浓硫酸的装置质量增加,装有氢氧化钠溶液的装置质量不变。
(1)该气体中一定不存在________________。
(2)若实验中观察到________________现象,就可以证明原气体中存在氢气。
四、化学反应的基本类型
考点7 知道化合反应、分解反应、置换反应和复分解反应的特点;辨认具体化学反应的基本类型 a
反应类型
概念
表达式
化合反应
由________________的物质生成另________________物质的反应
A+B===AB
多变一
分解反应
由一种物质生成________________其他物质的反应
AB===A+B
一变多
置换反应
由一种单质跟一种________________反应,生成________________和另一种化合物的反应
A+BC===B+AC
一换一
复分解
反应
由两种化合物________________,生成另外两种化合物的反应
AB+CD===AD+CB
相互交换
五、化学反应中的能量变化
1.化学反应中往往伴随着________________的变化。
有热量放出的化学反应叫________________,吸收热量的化学反应叫________________。
2.物质的燃烧、生石灰与水反应可放出大量的热量,这两个反应是化学能转化为________________;反应条件为高温或需要加热的反应中,内能转化为________________。
光合作用太阳能转化为化学能;呼吸作用________________转化为其他形式的能;中和反应化学能转化为________________。
4.(2016·宁波)如图所示是某化学反应的微观示意图。
下列关于该化学反应的说法错误的是( )
A.反应类型是分解反应
B.反应前后各元素化合价不变
C.反应前后两种原子的数目不变
D.反应物是由两种元素组成的化合物
5.(2017·绍兴、义乌)下列属于置换反应的是( )
A.H2+CuO
Cu+H2O
B.2KMnO4
K2MnO4+MnO2+O2↑
C.HCl+NaOH===NaCl+H2O
D.2Mg+O2
2MgO
6.(2015·台州)下列事例中,不是通过化学反应提供能量的是( )
六、质量守恒定律
质量守恒定律:
化学反应中,参加化学反应的各物质的质量总和________________反应后生成的各物质的质量总和。
考点10 从分子、原子的角度解释质量守恒定律 b
在化学反应前后,原子的________________没有改变,原子的________________也没有增减,每个原子的质量也没有变化,所以化学反应前后各物质的质量总和相等。
七、化学方程式
以C+O2
CO2为例:
1.宏观意义:
表示什么物质参加了反应,结果生成了什么物质;反应是在什么条件下进行。
即在点燃的条件下,氧气和碳反应,生成二氧化碳。
2.质量意义:
表示了各物质之间的质量关系,即反应物和生成物之间的质量比:
如12份质量的碳与32份质量的氧气完全反应生成44份质量的二氧化碳。
3.微观意义:
表示各物质间原子和分子的________________。
1个碳原子和一个氧分子反应得到1个二氧化碳分子。
考点12 根据化学方程式进行生成物和反应物之间的计算 c
1.一般步骤:
设未知数→写出配平的化学方程式→写出有关物质的质量比和已知量→列方程、求解→写出简明的答案。
2.注意点:
①方程式必须配平;②计算有关物质的质量比时式量要乘以前面的系数;③单位必须统一;④如是不纯物必须换算成纯物质的质量代入计算。
错误!
超链接引用无效。
7.(2017·衢州)质量守恒定律是自然界最基本的规律之一。
下列装置及实验(天平未画出)能用来验证质量守恒定律的是( )
8.(2016·湖州)某Na2CO3样品中混有一定量的Na2SO4,小明想测定样品中Na2CO3的质量分数,取该样品20克放入烧杯,加入100克水使样品全部溶解,再向烧杯中滴加稀硫酸,当滴加的稀硫酸质量为50克时,恰好完全反应,称得烧杯中溶液的质量是165.6克。
请通过计算回答:
(1)滴加的稀硫酸中溶质的质量分数。
(2)该样品中Na2CO3的质量分数。
(2017·北京)用”W”型玻璃管进行微型实验,如图所示,下列说法不正确的是
( )
A.a处红棕色粉末变为黑色
B.a处的反应为CO+Fe2O3===2Fe+CO2
C.b处澄清石灰水变浑浊证明有CO2生成
D.可利用点燃的方法进行尾气处理
错误!
超链接引用无效。
1.(2017·金华)已知某混合气体由H2、CO和CO2三种气体组成。
为验证该混合气体成分,科学研究小组的同学经过讨论,设计了如图1所示的实验方案。
根据方案回答下列问题:
(1)装置C在实验中的作用是____________________。
(2)仅根据D装置中黑色粉末变红这一现象,能否证明混合气体中一定存在CO?
请判断并说明理由:
____________________。
(3)小丁根据装置E中出现白色硫酸铜粉末变成蓝色的实验现象,得出该混合气体中有氢气存在的结论。
你认为结论是否可靠?
若可靠,请说明理由;若不可靠,请对图1实验装置提出改进意见。
________________________________________________________________________
________________________________________________________________________。
(4)图1方案中B装置可用来吸收CO2但没有现象。
为证明CO2和NaOH能发生反应,小丁又设计了图2所示的方案。
则图2方案中所加试剂X应该是____________________。
(2016·潍坊)元素化合价发生改变的反应都是氧化还原反应。
例如:
2Fe0+3Cl20
2Fe+3Cl3-1,反应前后,Fe和Cl元素的化合价发生了改变,该反应是氧化还原反应。
下列判断错误的是( )
A.分解反应都属于氧化还原反应
B.置换反应都属于氧化还原反应
C.复分解反应都不属于氧化还原反应
D.有单质参加的化合反应属于氧化还原反应
2.(2015·黄石)下表所列的各基本反应类型对应的化学方程式实例正确的是( )
基本反应类型
化学方程式实例
A.
化合反应
CO2+H2O===HCO3
B.
分解反应
2KClO3
2KCl+3O2↑
C.
复分解反应
KOH+NaCl===KCl+NaOH
D.
置换反应
Zn+H2SO4===ZnSO4+2H2↑
(2017·滨州)在密闭容器中加入甲、乙、丙、丁四种物质,使之充分反应,反应前后测得有关数据如表:
物质
甲
乙
丙
丁
反应前质量/g
18
1
2
32
反应后质量/g
X
26
2
12
下列说法中,不正确的是( )
A.反应后物质甲的质量为13g
B.乙是反应物
C.反应中乙、丁的质量比为5∶4
D.物质丙可能是该反应的催化剂
错误!
超链接引用无效。
3.(2017·娄底)甲、乙、丙、丁四种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
A.x的值是15
B.丙可能是该反应的催化剂
C.该反应是分解反应
D.反应中甲和乙的质量比为4∶1
(2016·包头)将19.45克碳酸钠和氯化钠的固体混合物放置于烧杯(重50克)中,加入一定量的水,固体全部溶解,然后向烧杯中滴加一定溶质质量分数的稀盐酸,实验测得烧杯及杯中物质的总质量与加入稀盐酸的质量关系如图所示。
计算:
(1)所加稀盐酸的溶质质量分数。
(2)恰好完全反应时所得溶液的溶质质量分数。
(2016·绥化)氯化钙钾石的化学式为KCl·xCaCl2(x是CaCl2的系数),它是一种天然的钾肥,溶于水后得到KCl和CaCl2的混合溶液。
某化学兴趣小组为了测定氯化钙钾石中钾元素的质量分数,称取样品18.55g加水完全溶解,得到KCl和CaCl2的混合溶液。
向该溶液中逐滴加入Na2CO3溶液,发生反应的化学方程式为:
Na2CO3+CaCl2===CaCO3↓+2NaCl,产生的沉淀与加入Na2CO3溶液的质量关系如图所示。
请回答下列问题:
(1)图中AB段表示的意义是____________________。
(2)①样品中CaCl2的质量是多少?
②所用Na2CO3溶液中溶质的质量分数是多少?
(3)①样品中钾元素的质量分数是多少?
(精确到0.1%)
②氯化钙钾石化学式中的x值是多少?
错误!
超链接引用无效。
错误!
超链接引用无效。
错误!
超链接引用无效。
错误!
超链接引用无效。
错误!
超链接引用无效。
错误!
超链接引用无效。
【提醒】对混合气体进行除杂和干燥操作时,因除杂时需要把混合气体通过溶液,除杂后的气体中会含有一定量水分,所以干燥操作应放在除杂操作之后,但本题水分对实验无干扰,所以不用除水分。
(2015·河池)某化学小组利用混有少量CO2的CO气体还原CuO,并验证反应后的气体产物。
实验装置如图所示(可重复使用)。
按气体从左到右的方向,装置连接顺序正确的是( )
A.丙→甲→乙→丁 B.甲→丙→乙→丁
C.丙→乙→甲→乙→丁 D.乙→甲→丙→乙→丁
【提醒】由金属元素和硫酸根组成的硫酸盐中,减去金属的质量即为硫酸根的质量。
(2015·莱芜)60g镁、铁、锌混合物与足量的稀硫酸反应得到混合溶液,蒸发得到252g硫酸盐固体。
则反应产生的氢气质量为( )
A.4.0gB.3.9gC.3.0gD.2.5g
(2017·杭州)小金进行如图所示实验来验证质量守恒定律。
在实验中用电子天平和量筒准确测量出表中m1、m2、m3、m4和V(实验中操作正确,O2的密度为ρg/cm3)。
实验序号
1
2
…
m1(MnO2)/g
m2(KClO3)/g
m3(试管)/g
m4(试管+加热后剩余固体)/g
量筒内收集气体的体积V/cm3
(1)
装置中试管口略向下倾斜的原因是
__________________________________________________
_________________________________________________。
(2)根据质量守恒定律,m1、m2、m3、m4、V和ρ之间应存在的等量关系为
_______________________________________________________________________
________________________________________________________________________。
(3)每次实验结束后,小金在拆卸装置时总能闻到刺激性气味。
他将加热后剩余固体中的MnO2分离并测量其质量,发现总小于加热前MnO2的质量。
查阅资料后发现,一般认为加热KClO3和MnO2混合物的反应过程如下:
第1步:
2MnO2+2KClO3
2KMnO4+Cl2↑+O2↑(其中Cl2有刺激性气味)
第2步:
2KMnO4
K2MnO4+MnO2+O2↑
第3步:
K2MnO4+Cl2
2KCl+MnO2+O2↑
写出加热后剩余固体中MnO2质量小于加热前MnO2质量的原因:
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(友情提示:
本栏目建议午休时间完成))
1.(2017·鄂州)煤油中含有噻吩(用X表示),噻吩有令人不愉快的气味,其燃烧时发生反应的化学方程式表示为:
X+6O2
4CO2+SO2+2H2O,则噻吩的化学式为( )
A.C4H6SB.C4H4S
C.C4H4S2D.C8H8S
2.(2017·扬州)某实验过程如下:
取ag锡粉置于密闭容器中,称得容器和固体的总质量为bg,煅烧使锡粉与O2充分反应;冷却后打开容器时发现有空气冲入,待容器内气体组成恢复到反应前,称得容器和固体的总质量为cg;取出所有固体,称得固体为dg,则c等于( )
A.d+b+aB.d-b-a
C.d-b+aD.d+b-a
3.(2017·嘉兴、舟山)以下四个化学反应都有气体产生,其反应类型和产生的气体性质均正确的是( )
选项
化学反应方程式
反应类型
气体性质
A.
Fe+H2SO4===FeSO4+H2↑
置换反应
还原性
B.
2H2O2
2H2O+O2↑
分解反应
可燃性
C.
2KClO3
2KCl+3O2↑
化合反应
氧化性
D.
CaCO3+2HCl===CaCl2+
H2O+CO2↑
复分解反应
酸性
4.(2016·齐齐哈尔)在催化剂并加热的条件下,氨气和氧气能发生化学反应,其反应的化学方程式为4NH3+5O2
4X+6H2O,则X的化学式是( )
A.N2B.N2OC.NOD.NO2
(2017·河北)一定条件下,密闭容器内发生的某化学反应,测得t1和t2时各物质的质量见表,下列说法正确的是( )
物质
M
N
P
Q
t1时的质量/g
51
9
3
17
t2时的质量/g
23
3
x
51
A.x的值小于3
B.Q可能是单质
C.该反应一定是分解反应
D.M与N的质量变化比为14∶3
(2017·德阳)向盛有10g某Cu-Al合金样品的烧杯中加入100g稀硫酸,恰好完全反应,反应结束后,测得烧杯内物质的总质量为109.4g。
则该合金样品中铜的质量分数是( )
A.73%B.54%C.46%D.27%
7.(2017·温州)据报道,我国已在南海某海域试采可燃冰获得成功。
可燃冰分布于深海沉积物或陆域的永久冻土中,主要是由甲烷(CH4)与水在高压低温条件下形成的类冰状结晶物质,可燃烧,所以被称为”可燃冰”。
(1)CH4中C、H元素的质量比为____________________。
(2)已知在相同条件下,1米3CO和1米3CH4所含的分子数目相同。
CO、CH4燃烧的化学方程式分别为2CO+O2
2CO2,CH4+2O2
CO2+2H2O。
据此分析,在相同条件下,分别燃烧1米3的CO与CH4,消耗氧气较多的是____________________。
8.(2017·台州)某兴趣小组设计如下实验探究质量守恒定律。
第8题图
(1)如图甲,小柯将烧杯放在天平左盘,使天平重新平衡。
然后取下烧杯把铁钉放入试管中,一段时间后,再把烧杯放回天平左盘,最后天平是否平衡?
____________________,反应后试管内溶液的质量____________________(填”增加”、”减少”或”不变”)。
(2)如图乙,小妍将烧杯放在天平左盘,使天平重新平衡。
然后倾斜烧杯使盐酸与石灰石粉末混合,一段时间后再把烧杯放回天平左盘,发现天平不再平衡。
其原因是____________________。
小柯对该实验装置进行改进,把烧杯换成锥形瓶(如图丙,装置气密性良好),你认为能否验证质量守恒定律并阐述理由:
____________________。
(3)小妍想测定实验所用石灰石中碳酸钙的质量分数,取6克石灰石粉末与足量的稀盐酸充分反应,反应后总质量减少2.2克。
求石灰石中碳酸钙的质量分数(杂质与稀盐酸不反应)。
(结果精确到0.1%)
9.(2016·北京)为测定21.2g某变质氢氧化钠固体中碳酸钠的含量,将其配制成500mL溶液,分别取出50mL用两种方法进行测定,已知:
Na2CO3+BaCl2===BaCO3↓+2NaCl。
加入的试剂
测得数据
方法1
足量BaCl2溶液
BaCO3沉淀1.97g
方法2
足量稀硫酸
CO2气体0.44g
请任选1种方法的数据,计算该固体中碳酸钠的质量分数(写出计算过程及结果)。
参考答案
第35课时 常见的化学反应
课前预热
考点1 1.新物质 2.生成
考点2 有无新物质生成
考点3 1.化学变化 2.化学变化
考点4 得到氧 失去氧 被氧化 还原性 被还原 氧化性
考点5 提供氧 氧化剂 氧化性 氧化剂
考点6 2.检验纯度 爆炸
【考点真题】1.C 2.A 3.
(1)CO
(2)有红色物质生成或氧化铜变成红色物质
考点7 两种或两种以上 一种 两种或两种以上
化合物 另一种单质 相互交换成分
考点8 1.能量 放热反应 吸热反应 2.内能 化学能 化学能 内能
【考点真题】4.B 5.A 6.B
考点9 等于
考点10 种类 数目
考点11 3.个数比
【考点真题】7.A 8.
(1)滴加的稀硫酸中溶质的质量分数为19.6%
(2)该样品中Na2CO3的质量分数为53%
课堂突破
例1 B 例2 A 例3 B 例4
(1)由烧杯及杯中物质的总质量与加入稀盐酸的质量关系图可知,生成的二氧化碳的质量为:
202.2g+50g-250g=2.2g
设参加反应的盐酸中溶质的质量为x,碳酸钠的质量为y,生成的氯化钠的质量为z
Na2CO3+2HCl===2NaCl+H2O+CO2↑
106 73 11744
y x z2.2g
=
=
=
解得:
x=3.65g,y=5.3g,z=5.85g。
所加稀盐酸的溶质质量分数为:
×100%=7.3%
(2)恰好完全反应时所得溶液的溶质质量分数为:
×100%=10%
例5 C 例6 A 例7
(1)防止冷凝水倒流引起试管炸裂
(2)m1+m2+m3-m4=ρV (3)部分Cl2散失,未参加后续反应,导致部分锰元素以K2MnO4或KMnO4形式存在,故剩余固体中MnO2质量小于加热前MnO2质量(合理即可)
【变式拓展】
1.
(1)检验CO2是否除尽
(2)不能,因为氢气也能还原氧化铜(合理即可) (3)不可靠,应在CD之间加一个“先干燥后验无”的装置(合理即可)
(4)BaCl2和NaOH 2.B 3.C 4.
(1)CaCl2已完全反应,且Na2CO3溶液过量
(2)①11.1g ②10% (3)①21.0% ②1
校内作业
1.B 2.D 3.A 4.C 5.D 6.C
7.
(1)3∶1
(2)CH4(或甲烷)
8.
(1)平衡 减少
(2)产生的二氧化碳从烧杯中逸出 不能,气球体积变大,受到空气对它的浮力增大,天平不再平衡 (3)设石灰石中含CaCO3的质量为x
CaCO3+2HCl===CaCl2+H2O+CO2↑
10044
x2.2克
100/x=44/2.2克 x=5克
CaCO3%=5g/6g×100%=83.3%
9.设碳酸钠的质量为x
Na2CO3+BaCl2===BaCO3↓+2NaCl
106197
x1.97g
=
x=1.06g
该固体中碳酸钠的质量分数:
×100%=50%
答:
该固体中碳酸钠的质量分数为50%。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 第35课时 常见的化学反应 35 课时 常见 化学反应
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《地质测量图绘制细则》.docx
《地质测量图绘制细则》.docx
