 燃烧及其利用.docx
燃烧及其利用.docx
- 文档编号:22999381
- 上传时间:2023-04-30
- 格式:DOCX
- 页数:38
- 大小:49.36KB
燃烧及其利用.docx
《燃烧及其利用.docx》由会员分享,可在线阅读,更多相关《燃烧及其利用.docx(38页珍藏版)》请在冰豆网上搜索。
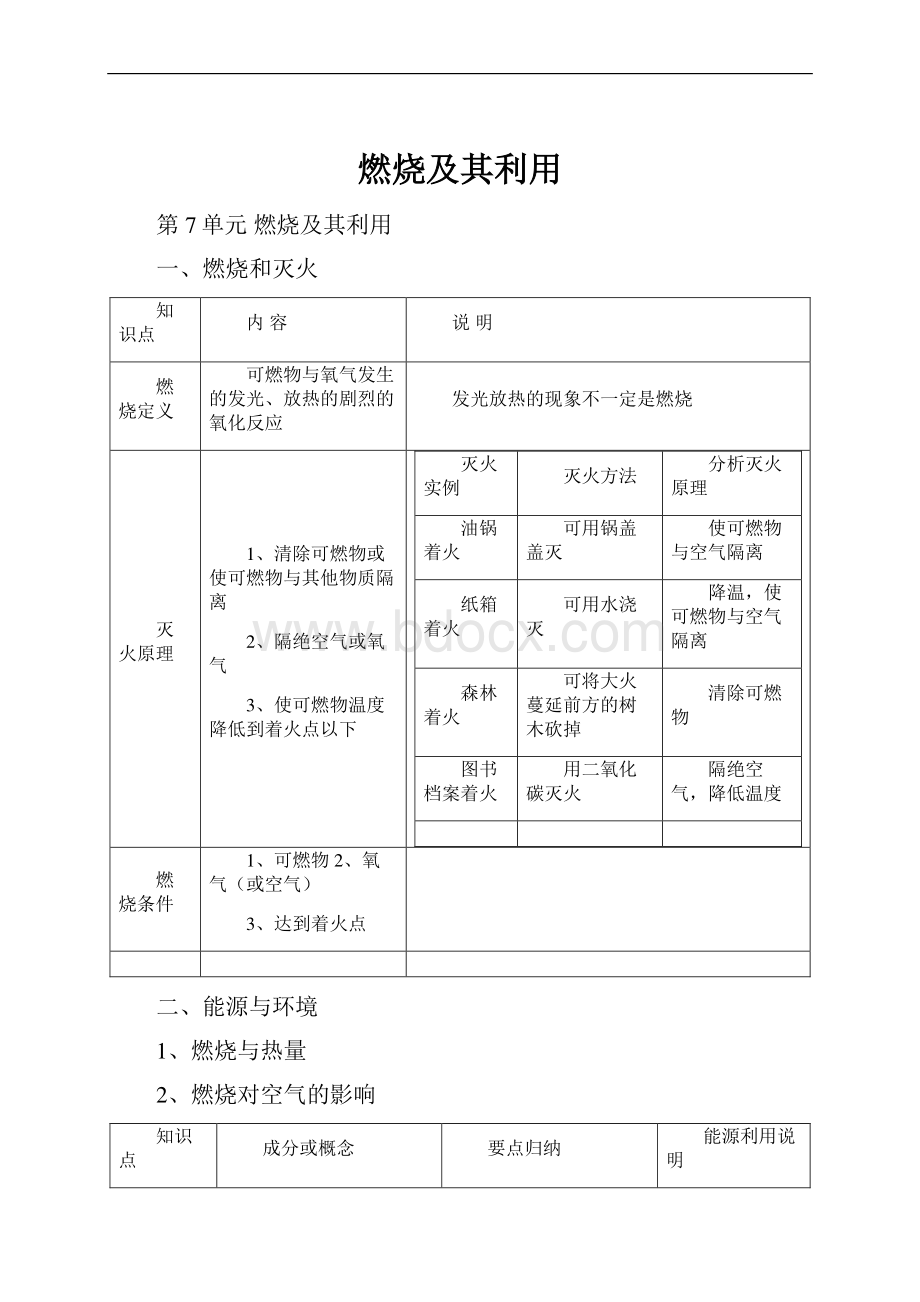
燃烧及其利用燃烧及其利用第7单元燃烧及其利用一、燃烧和灭火知识点内容说明燃烧定义可燃物与氧气发生的发光、放热的剧烈的氧化反应发光放热的现象不一定是燃烧灭火原理1、清除可燃物或使可燃物与其他物质隔离2、隔绝空气或氧气3、使可燃物温度降低到着火点以下灭火实例灭火方法分析灭火原理油锅着火可用锅盖盖灭使可燃物与空气隔离纸箱着火可用水浇灭降温,使可燃物与空气隔离森林着火可将大火蔓延前方的树木砍掉清除可燃物图书档案着火用二氧化碳灭火隔绝空气,降低温度燃烧条件1、可燃物2、氧气(或空气)3、达到着火点二、能源与环境1、燃烧与热量2、燃烧对空气的影响知识点成分或概念要点归纳能源利用说明化石燃料煤复杂的混合物,主要含碳元素将煤隔绝空气加热分解成许多产物,属于化学变化分解的产物有焦炭、煤焦油和煤气石油混合物,主要含碳、氢元素利用石油中各成分沸点不同来分离,属于物理变化产品为汽油、煤油等天然气主要由碳氢元素组成沼气燃料的充分燃烧节约能源,减少对环境污染充分燃烧的条件:
有适当过量的空气;有足够大的接触面积(3)、开发新燃料、新能源乙醇、氢气;新能源:
太阳能、风能、核能、地热能和潮汐能3、影响燃烧现象的因素:
可燃物的性质、氧气的浓度、与氧气的接触面积使燃料充分燃烧的两个条件:
(1)要有足够多的空气
(2)燃料与空气有足够大的接触面积。
4、爆炸:
可燃物在有限的空间内急速燃烧,气体体积迅速膨胀而引起爆炸。
一切可燃性气体、可燃性液体的蒸气、可燃性粉尘与空气(或氧气)的混合物遇火种均有可能发生爆炸。
二、燃料和能量1、三大化石燃料:
煤、石油、天然气(混合物、均为不可再生能源)
(1)煤:
“工业的粮食”(主要含碳元素);煤燃烧排放的污染物:
SO2、NO2(引起酸雨)、CO、烟尘等
(2)石油:
“工业的血液”(主要含碳、氢元素);汽车尾气中污染物:
CO、未燃烧的碳氢化合物、氮的氧化物、含铅化合物和烟尘(3)天然气是气体矿物燃料(主要成分:
甲烷),是较清洁的能源。
2、两种绿色能源:
沼气、乙醇
(1)沼气的主要成分:
甲烷甲烷的化学式:
CH4(最简单的有机物,相对分子质量最小的有机物)物理性质:
无色,无味的气体,密度比空气小,极难溶于水。
化学性质:
可燃性CH4+2O2点燃CO2+2H2O(发出蓝色火焰)
(2)乙醇(俗称:
酒精,化学式:
C2H5OH)化学性质:
可燃性C2H5OH+3O2点燃2CO2+3H2O工业酒精中常含有有毒的甲醇CH3OH,故不能用工业酒精配制酒!
乙醇汽油:
优点
(1)节约石油资源
(2)减少汽车尾气(3)促进农业发展(4)乙醇可以再生3、化学反应中的能量变化
(1)放热反应:
如所有的燃烧
(2)吸热反应:
如C+CO2高温2CO4、新能源:
氢能源、太阳能、核能、风能、地热能、潮汐能氢气是最理想的燃料:
(1)优点:
资源丰富,放热量多,无污染。
(2)需解决问题:
如何大量廉价的制取氢气?
如何安全地运输、贮存氢气?
第八单元知识点一、金属材料纯金属(90多种)合金(几千种)2、金属的物理性质:
(1)常温下一般为固态(汞为液态),有金属光泽。
(2)大多数呈银白色(铜为紫红色,金为黄色)(3)有良好的导热性、导电性、延展性3、金属之最:
(1)铝:
地壳中含量最多的金属元素
(2)钙:
人体中含量最多的金属元素(3)铁:
目前世界年产量最多的金属(铁铝铜)(4)银:
导电、导热性最好的金属(银铜金铝)(5)铬:
硬度最高的金属(6)钨:
熔点最高的金属(7)汞:
熔点最低的金属(8)锇:
密度最大的金属(9)锂:
密度最小的金属4、金属分类:
黑色金属:
通常指铁、锰、铬及它们的合金。
重金属:
如铜、锌、铅等有色金属轻金属:
如钠、镁、铝等;有色金属:
通常是指除黑色金属以外的其他金属。
5、合金:
由一种金属跟其他一种或几种金属(或金属与非金属)一起熔合而成的具有金属特性的物质。
:
一般说来,合金的熔点比各成分低,硬度比各成分大,抗腐蚀性能更好燃料对空气的影响防止污染的措施煤可吸入颗粒;SO2、NO2、CO酸雨形成充分燃烧、减少污染物排放(除尘脱硫)汽油和柴油尾气中含有一氧化碳、含铅化合物和烟尘使用催化净化装置,使用无铅汽油,改进发动机机构注:
钛和钛合金:
被认为是21世纪的重要金属材料,钛合金与人体有很好的“相容性”,因此可用来制造人造骨等。
(1)熔点高、密度小优点
(2)可塑性好、易于加工、机械性能好(3)抗腐蚀性能好二、金属的化学性质1、大多数金属可与氧气的反应合金铁的合金铜合金焊锡钛和钛合金形状记忆金属生铁钢黄铜青铜:
成分含碳量2%4.3%含碳量0.03%2%铜锌合金铜锡合金铅锡合金钛镍合金备注不锈钢:
含铬、镍的钢紫铜为纯铜熔点低具有抗腐蚀性能2、金属+酸盐+H2锌和稀硫酸Zn+H2SO4=ZnSO4+H2铁和稀硫酸Fe+H2SO4=FeSO4+H2镁和稀硫酸Mg+H2SO4=MgSO4+H2铝和稀硫酸2Al+3H2SO4=Al2(SO4)3+3H2锌和稀盐酸Zn+2HCl=ZnCl2+H2铁和稀盐酸Fe+2HCl=FeCl2+H2镁和稀盐酸Mg+2HCl=MgCl2+H2铝和稀盐酸2Al+6HCl=2AlCl3+3H23、金属+盐另一金属+另一盐(条件:
“前换后,盐可溶”)铁与硫酸铜反应:
Fe+CuSO4=Cu+FeSO4现象:
铁条表面覆盖一层红色的物质,溶液由蓝色变成浅绿色。
(古代湿法制铜及“曾青得铁则化铜”指的是此反应)40、铝片放入硫酸铜溶液中:
3CuSO4+2Al=Al2(SO4)3+3Cu现象:
铝片表面覆盖一层红色的物质,溶液由蓝色变成无色。
41、铜片放入硝酸银溶液中:
2AgNO3+Cu=Cu(NO3)2+2Ag现象:
铜片表面覆盖一层银白色的物质,溶液由无色变成蓝色。
铜和硝酸汞溶液反应:
Cu+Hg(NO3)2=Cu(NO3)2+Hg现象:
铜片表面覆盖一层银白色的物质,溶液由无色变成蓝色。
三、常见金属活动性顺序:
KCaNaMgAlZnFeSnPb(H)CuHgAgPtAu金属活动性由强逐渐减弱在金属活动性顺序里:
()金属的位置越靠前,它的活动性就越强()位于氢前面的金属能置换出盐酸、稀硫酸中的氢(不可用浓硫酸、硝酸)()位于前面的金属能把位于后面的金属从它们的盐溶液中置换出来。
(除K、Ca、Na)四、金属资源的保护和利用1、铁的冶炼
(1)原理:
在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
3CO+Fe2O3高温2Fe+3CO2
(2)原料:
铁矿石、焦炭、石灰石、空气常见的铁矿石有磁铁矿(主要成分是Fe3O4)、赤铁矿(主要成分是Fe2O3)2、铁的锈蚀
(1)铁生锈的条件是:
铁与O2、水接触。
铁锈的主要成分是氧化铁Fe2O3(红棕色)(铜生铜绿的条件:
铜与O2、水、CO2接触。
铜绿的化学式:
Cu2(OH)2CO3)
(2)防止铁制品生锈的措施:
保持铁制品表面的清洁、干燥表面涂保护膜:
如涂油、刷漆、电镀、烤蓝等制成不锈钢(3)铁锈很疏松,不能阻碍里层的铁继续与氧气、水蒸气反应,因此铁制品可以全部被锈蚀。
因而铁锈应及时除去。
(4)而铝与氧气反应生成致密的氧化铝薄膜,从而阻止铝进一步氧化,因此,铝具有很好的抗腐蚀性能。
3、金属资源的保护和利用:
防止金属腐蚀保护金属资源的途径:
回收利用废旧金属合理开采矿物寻找金属的代用意义:
节约金属资源,减少环境污染第九单元溶液知识点一、溶液的形成1、溶液
(1)溶液的概念:
一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物,叫做溶液
(2)溶液的基本特征:
均一性、稳定性的混合物注意:
a、溶液不一定无色,如CuSO4为蓝色FeSO4为浅绿色Fe2(SO4)3为黄色b、溶质可以是固体、液体或气体;水是最常用的溶剂c、溶液的质量=溶质的质量+溶剂的质量溶液的体积溶质的体积+溶剂的体积d、溶液的名称:
溶质的溶剂溶液(如:
碘酒碘的酒精溶液)碘酒中溶质是碘,溶剂是酒精。
盐酸溶质是HCl,石灰水溶质为Ca(OH)2,食盐水溶质为NaCl,氧化钙溶于水溶质为Ca(OH)2,三氧化硫溶于水溶质为H2SO4,胆矾CuSO45H2O溶于水溶质为CuSO4,医用酒精中溶质为C2H5OH。
固体、气体溶于液体,液体为溶剂2、溶质和溶剂的判断有水,水为溶剂液体溶于液体,3、饱和溶液、不饱和溶液无水,量多的为溶剂
(1)概念:
(2)判断方法:
看有无不溶物或继续加入该溶质,看能否溶解(3)饱和溶液和不饱和溶液之间的转化加水升温饱和溶液不饱和溶液熟石灰对温度例外增加溶质降温蒸发溶剂饱和石灰水变成不饱和的石灰水的方法是:
加水降温对于同一种溶质的溶液来说,在同一温度下,饱和溶液一定比不饱和溶液要浓。
注:
Ca(OH)2和气体等除外,它的溶解度随温度升高而降低最可靠的方法是:
加溶质、蒸发溶剂(4)浓、稀溶液与饱和不饱和溶液之间的关系饱和溶液不一定是浓溶液不饱和溶液不一定是稀溶液,如饱和的石灰水溶液就是稀溶液在一定温度时,同一种溶质的饱和溶液一定要比它的不饱和溶液浓(5)溶解时放热、吸热现象溶解吸热:
如NH4NO3溶解溶解放热:
如NaOH溶解、浓H2SO4溶解溶解没有明显热现象:
如NaCl二、溶解度1、固体的溶解度
(1)溶解度定义:
在一定温度下,某固态物质在100g溶剂里达到饱和状态时所溶解的质量四要素:
条件:
一定温度标准:
100g溶剂状态:
达到饱和质量:
单位:
克
(2)溶解度的含义:
20时NaCl的溶液度为36g含义:
在20时,在100克水中最多能溶解36克NaCl或在20时,NaCl在100克水中达到饱和状态时所溶解的质量为36克20时,易溶物质的溶解度为10g,可溶物质的溶解度1g10g,微溶物质的溶解度为0.01g1g,难溶物质的溶解度为0.01g。
(3)影响固体溶解度的因素:
溶质、溶剂的性质(种类)温度大多数固体物的溶解度随温度升高而升高;如KNO3少数固体物质的溶解度受温度的影响很小;如NaCl极少数物质溶解度随温度升高而降低。
如Ca(OH)2(4)溶解度曲线例:
(1)t3时A的溶解度为80g
(2)P点的的含义在该温度时,A和C的溶解度相同(3)N点为t3时A的不饱和溶液,可通过加入A物质,降温,蒸发溶剂的方法使它变为饱和(4)t1时A、B、C、溶解度由大到小的顺序CBA(5)从A溶液中获取A晶体可用降温结晶的方法获取晶体。
(6)从A溶解度是80g。
(7)t2时A、B、C的饱和溶液各W克,降温到t1会析出晶体的有A和B无晶体析出的有C,所得溶液中溶质的质量分数由小到大依次为ACB(8)除去A中的泥沙用过滤法;分离A与B(含量少)的混合物,用结晶法2、气体的溶解度
(1)气体溶解度的定义:
在压强为101kPa和一定温度时,气体溶解在1体积水里达到饱和状态时的气体体积。
(2)影响因素:
气体的性质温度(温度越高,气体溶解度越小)压强(压强越大,气体溶解度越大)3、混合物的分离
(1)过滤法:
分离可溶物+难溶物
(2)结晶法:
分离几种可溶性物质分离:
KCl和MnO2方法为过滤,步骤:
溶解、过滤、蒸发,NaCl和KNO3方法为结晶,步骤:
溶解、冷却结晶。
(冷却热饱和溶液法)对溶解度受温度变化不大的物质采用蒸发溶剂的方法来得到晶体(如NaCl)。
对溶解度受温度变化比较大的物质采用冷却热的饱和溶液的方法来得到晶体(如KNO3、CuSO4)冷却饱和CuSO4溶液析出晶体的化学式为CuSO45H2O。
结晶的两种方法蒸发溶剂,如NaCl(海水晒盐)降低温度(冷却热的饱和溶液,如KNO3)三、溶质的质量分数1、公式:
溶质质量分数=100%2、配制一定溶质质量分数的溶液
(1)用固体配制:
步骤:
计算、称量、溶解仪器:
天平、药匙、量筒、滴管、烧杯、玻璃棒
(2)用浓溶液稀释(稀释前后,溶质的质量不变)步骤:
计算、量取、稀释仪器:
量筒、滴管、烧杯、玻璃棒酸和碱知识点一、酸、碱、盐的组成酸是由氢元素和酸根组成的化合物如:
硫酸(H2SO4)、盐酸(HCl)、硝酸(HNO3)碱是由金属元素和氢氧根组成的化合物如:
氢氧化钠、氢氧化钙、氨水(NH3H2O)盐是由金属元素元素(或铵根)和酸根组成的化合物如:
氯化钠、碳酸钠酸、碱、盐的水溶液可以导电(原因:
溶于水时离解形成自由移动的阴、阳离子)二、酸1、浓盐酸、浓硫酸的物理性质、特性、用途金属在空气中在氧气中镁常温下逐渐变暗。
点燃,剧烈燃烧,发出耀眼的白光,生成白色的固体点燃,剧烈燃烧,发出耀眼的白光,生成白色的固体2Mg+O2点燃2MgO铝常温下表面变暗,生成一种致密的氧化膜点燃,剧烈燃烧,发出耀眼的白光,生成白色的固体4Al+3O2点燃2Al2O3铁持续加热变红点燃,剧烈燃烧,火星四射,生成黑色的固体3Fe+2O2点燃Fe3O4铜加热,生成黑色物质;在潮湿的空气中,生成铜绿而被腐蚀加热生成黑色物质2Cu+O2加热2CuO银金即使在高温时也不与氧气发生反应2、酸的通性(具有通性的原因:
酸离解时所生成的阳离子全部是H+)
(二)、酸的通性1、使紫色的石蕊试液变红的溶液不一定是酸溶液,但一定是酸性溶液;(如NaHSO4溶液是盐溶液,但溶液显酸性)使紫色的石蕊试液变蓝的溶液不一定是碱溶液,但一定是碱性溶液。
(如Na2CO3溶液是盐溶液,但溶液显碱性)2、酸的通性
(1)与酸碱指示剂作用,紫色石蕊遇酸变红色,无色酚酞不变色。
(2)与金属反应生成盐和氢气(条件:
在活动性顺序表中,只有排在H前面的金属才能置换出酸中的氢;酸除了HNO3和浓H2SO4,氧化性强,与金属反应时,不生成氢气而生成水,H2CO3酸性太弱)(3)与金属氧化物反应生成盐和水(一定反应)(4)与碱反应生成盐和水(一定反应)(5)与某些盐反应生成另一种酸和另一种盐(条件:
生成物有沉淀或气体)3、三种离子的检验三、碱1、氢氧化钠、氢氧化钙的物理性质、用途浓盐酸浓硫酸颜色、状态“纯净”:
无色液体无色粘稠、油状液体工业用盐酸:
黄色(含Fe3+)气味有刺激性气味无特性挥发性(敞口置于空气中,瓶口有白雾)吸水性脱水性强氧化性腐蚀性用途金属除锈制造药物人体中含有少量盐酸,助消化金属除锈浓硫酸作干燥剂生产化肥、精炼石油2、碱的通性(具有通性的原因:
离解时所生成的阴离子全部是OH-)
(1)碱溶液与酸碱指示剂的反应:
使紫色石蕊试液变蓝色,使无色酚酞试液变红色
(2)非金属氧化物+碱盐+水(3)酸+碱盐+水(4)盐+碱另一种盐+另一种碱(反应物均可溶,产物符合复分解条件)四、非金属氧化物与金属氧化物试剂Cl-AgNO3及HNO3SO42-Ba(NO3)2及HNO3HCl及BaCl2CO32-HCl及石灰水注:
难溶性碱受热易分解(不属于碱的通性)如Cu(OH)2加热CuO+H2O2Fe(OH)3加热Fe2O3+3H2O五、中和反应溶液酸碱度的表示法pH1、定义:
酸与碱作用生成盐和水的反应2、实质:
OH+H+=H2O3、应用:
(1)改变土壤的酸碱性。
(2)处理工厂的废水。
(3)用于医药。
4、溶液酸碱度的表示法pH
(1)014酸性增强中性碱性增强
(2)pH的测定:
最简单的方法是使用pH试纸用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读出溶液的pH(读数为整数)(3)酸碱性与酸碱度关系:
氢氧化钠氢氧化钙颜色、状态白色固体,极易溶于水(溶解放热)白色粉末,微溶于水俗名烧碱、火碱、苛性钠(具有强腐蚀性)熟石灰、消石灰制法Ca(OH)2+Na2CO3=CaCO3+2NaOHCaO+H2O=Ca(OH)2用途氢氧化钠固体作干燥剂化工原料:
制肥皂、造纸去除油污:
炉具清洁剂中含氢氧化钠工业:
制漂白粉农业:
改良酸性土壤、配波尔多液建筑:
(4)酸雨:
正常雨水的pH约为5.6(因为溶有CO2);pH5.6的雨水为酸雨说明:
1、溶液的酸碱度常用pH表示,pH=7时溶液呈中性,pH7时呈酸性,pH7时呈碱性。
PH=0时呈酸性,pH越小,酸性越强,pH越大,碱性越强。
蒸馏水的pH=7(雨水pH7显弱酸性),SO3溶于水,溶液pH7,CO2溶于水,溶液2、pH7;pH升高可加碱(可溶性碱)或水,pH降低可加酸或水。
PH=3和pH=4混合溶液pH7,测定pH的最简单的方法是使用pH试纸,测定时,用玻璃棒把待测溶液滴在pH试纸上,然后把试纸显示的颜色跟标准比色卡对照,便可知溶液的pH。
pH数值是整数。
3、指示剂的使用使用指示剂只能说明溶液呈酸性或碱性,不能确定溶液一定是酸或碱。
操作方法:
用玻璃棒沾取少量被测溶液滴在试纸上,绝不能将试纸伸入待测试液中,更不能将试纸投入到待测溶液中去。
紫色石蕊遇酸性溶液显红色,遇碱性溶液显蓝色;无色酚酞遇酸性溶液不变色,遇碱性溶液显红色。
4、溶液的酸碱度常用pH表示,测定pH最简单的方法是使用pH试纸。
PH的范围在014之间,pH7溶液呈碱性,pH=7溶液呈中性,pH7溶液呈酸性。
PH越大碱性越强,pH越小酸性越强;pH升高加碱(或水),pH降低加酸(或水)。
第十一单元盐化肥知识点一、常见的盐定义:
能解离出金属离子(或NH4+)和酸根离子的化合物非金属氧化物金属氧化物化学性质
(1)大多数可与水反应生成酸CO2+H2O=H2CO3SO2+H2O=H2SO3SO3+H2O=H2SO4
(1)少数可与水反应生成碱Na2O+H2O=2NaOHK2O+H2O=2KOH可溶BaO+H2O=Ba(OH)2性碱CaO+H2O=Ca(OH)2
(2)酸性氧化物+碱盐+水CO2+Ca(OH)2=CaCO3+H2O(不是复分解反应)
(2)碱性氧化物+酸盐+水Fe2O3+6HCl=2FeCl3+3H2O指示剂pH值石蕊酚酞酸性0.01%OCHNCaPKSNaClMg微量元素在人体中含量0.01%Fe、Zn、Se、I、F等二、人体中的常量元素1、钙99%在于骨骼和牙齿中
(1)成人体内约含钙1.26g,主要以Ca10(PO4)6(OH)2晶体的形式存在
(2)来源:
奶类、绿色蔬菜、水产品、肉类、豆类(3)钙过多:
结石、骨骼变粗过少:
青少年佝偻病、发育不良老年人骨质疏松(4)补钙产品:
钙中钙;葡萄糖酸钙;2、钠和钾
(1)Na+存在于细胞外液人体内含钠80g120gK+存在于细胞内液成人每千克含钾约2g
(2)作用:
维持人体内的水分和维持体液恒定的pH(如血液的pH7.35-7.45)三、人体中的微量元素必需元素(20多种)Fe、Zn、Se、I、F等对人体有害的元素Hg、Cr、Pb、Ag、Ba、Al、Cu等含N量使用注意事项NH4HCO317.7%易分解,施用时深埋铵态氮肥防晒防潮,且均不能与碱性物质(如草木灰、熟石灰等)混合施用NH4NO335%易爆,结块不可用铁锤砸(NH4)2SO421.2%长期使用会使土壤酸化、板结NH4Cl26.2%长期使用会使土壤酸化、板结CO(NH2)246.7%含氮量最高的氮肥(有机物)NH3.H2O加水稀释后施用不稳定,易放出NH3NaNO3课题3有机合成材料一、有机化合物是否含有碳元素无机化合物有机化合物(不包括CO、CO2和Na2CO3、CaCO3等碳酸盐)1、生活中常见的有机物CH4(最简单的有机物、相对分子质量最小的有机物)、C2H5OH(乙醇,俗名:
酒精)、CH3COOH(乙酸,俗名:
醋酸)、C6H12O6(葡萄糖)、蔗糖、蛋白质、淀粉等2、有机物数目庞大的原因:
原子的排列方式不同3、有机物有机小分子如:
CH4、C2H5OH、CH3COOH、C6H12O6等(根据相对分子质量大小)有机高分子化合物(有机高分子)如:
蛋白质、淀粉等二、有机合成材料1、有机高分子材料
(1)分类天然有机高分子材料如:
棉花、羊毛、蚕丝、天然橡胶等合成有机高分子材料塑料(三大合成材料)合成纤维:
涤纶(的确良)、锦纶(尼龙)、晴纶合成橡胶
(2)高分子材料的结构和性质链状结构热塑性如:
聚乙烯塑料(聚合物)网状结构热固性如:
电木(3)鉴别聚乙烯塑料和聚氯烯塑料(聚氯烯塑料袋有毒,不能装食品):
点燃后闻气味,有刺激性气味的为聚氯烯塑料。
(4)鉴别羊毛线和合成纤维线:
物理方法:
用力拉,易断的为羊毛线,不易断的为合成纤维线;化学方法:
点燃,产生焦羽毛气味,不易结球的为羊毛线;无气味,易结球的为合成纤维线。
2、“白色污染”及环境保护
(1)危害:
破坏土壤,污染地下水危害海洋生物的生存;如果焚烧含氯塑料会产生有毒的氯化氢气体,从而对空气造成污染
(2)解决途径减少使用不必要的塑料制品;重复使用某些塑料制品,如塑料袋、塑料盒等;使用一些新型的、可降解的塑料,如微生物降解塑料和光降解塑料等;回收各种废弃塑料(3)塑料的分类是回收和再利用的一大障碍化学方程式汇总一物质与氧气的反应:
(1)单质与氧气的反应:
1.镁在空气中燃烧:
2Mg+O2点燃2MgO2.铁在氧气中燃烧:
3Fe+2O2点燃Fe3O43.铜在空气中受热:
2Cu+O2加热2CuO4.铝在空气中燃烧:
4Al+3O2点燃2Al2O35.氢气中空气中燃烧:
2H2+O2点燃2H2O6.红磷在空气中燃烧:
4P+5O2点燃2P2O57.硫粉在空气中燃烧:
S+O2点燃SO28.碳在氧气中充分燃烧:
C+O2点燃CO29.碳在氧气中不充分燃烧:
2C+O2点燃2CO
(2)化合物与氧气的反应:
10.一氧化碳在氧气中燃烧:
2CO+O2点燃2CO211.甲烷在空气中燃烧:
CH4+2O2点燃CO2+2H2O12.酒精在空气中燃烧:
C2H5OH+3O2点燃2CO2+3H2O二几个分解反应:
13.水在直流电的作用下分解:
2H2O通电2H2+O214.加热碱式碳酸铜:
Cu2(OH)2CO3加热2CuO+H2O+CO215.加热氯酸钾(有少量的二氧化锰):
2KClO3=2KCl+3O216.加热高锰酸钾:
2KMnO4加热K2MnO4+MnO2+O217.碳酸不稳定而分解:
H2CO3=H2O+CO218.高温煅烧石灰石:
CaCO3高温CaO+CO2三几个氧化还原反应:
19.氢气还原氧化铜:
H2+CuO加热Cu+H2O20.木炭还原氧化铜:
C+2CuO高温2Cu+CO221.焦炭还原氧化铁:
3C+2Fe2O3高温4Fe+3CO222.焦炭还原四氧化三铁:
2C+Fe3O4高温3Fe+2CO223.一氧化碳还原氧化铜:
CO+CuO加热Cu+CO224.一氧化碳还原氧化铁:
3CO+Fe2O3高温2Fe+3CO225.一氧化碳还原四氧化三铁:
4CO+Fe3O4高温3Fe+4CO2四单质、氧化物、酸、碱、盐的相互关系
(1)金属单质+酸-盐+氢气(置换反应)26.锌和稀硫酸Zn+H2SO4=ZnSO4+H227.铁和稀硫酸Fe+H2SO4=FeSO4+H228.镁和稀硫酸Mg+H2SO4=MgSO4+H229.铝和稀硫酸2Al+3H2SO4=Al2(SO4)3+3H230.锌和稀盐酸Zn+
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 燃烧 及其 利用
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《地质测量图绘制细则》.docx
《地质测量图绘制细则》.docx
 企业员工培训PPT优质PPT.ppt
企业员工培训PPT优质PPT.ppt
