 必修一第一单元测试Word文档下载推荐.docx
必修一第一单元测试Word文档下载推荐.docx
- 文档编号:22940133
- 上传时间:2023-02-06
- 格式:DOCX
- 页数:41
- 大小:223.66KB
必修一第一单元测试Word文档下载推荐.docx
《必修一第一单元测试Word文档下载推荐.docx》由会员分享,可在线阅读,更多相关《必修一第一单元测试Word文档下载推荐.docx(41页珍藏版)》请在冰豆网上搜索。
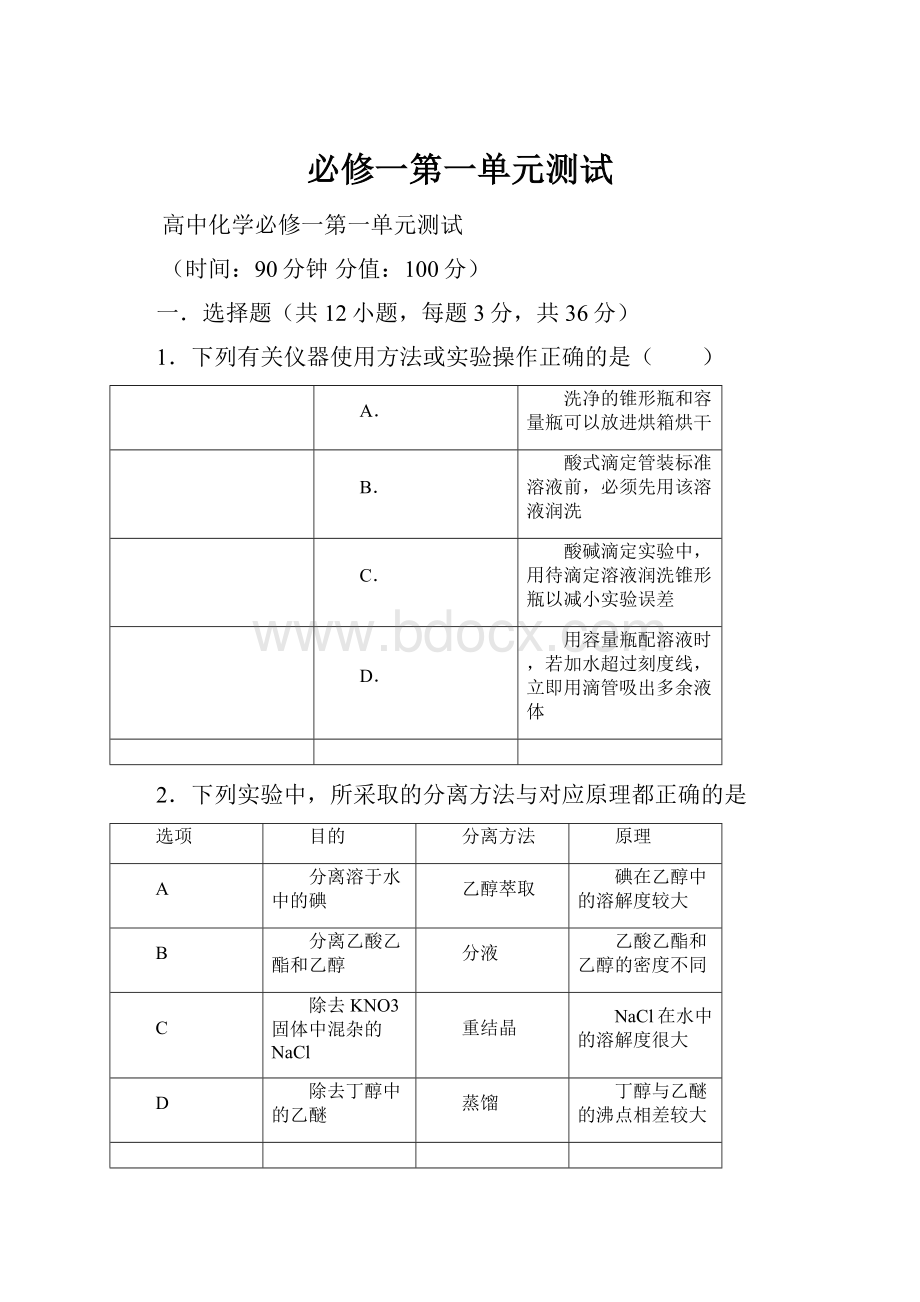
乙酸乙酯和乙醇的密度不同
C
除去KNO3固体中混杂的NaCl
重结晶
NaCl在水中的溶解度很大
D
除去丁醇中的乙醚
蒸馏
丁醇与乙醚的沸点相差较大
3.检验用硫酸亚铁制的硫酸铁中是否含有硫酸亚铁,可选用的试剂是( )
NaOH
KMnO4
KSCN
苯酚
4.下列仪器中,能在酒精灯上直接加热的是( )
试管
烧杯
量筒
集气瓶
5.用NaOH固体配制一定物质的量浓度的NaOH溶液时,不需要使用的玻璃仪器是( )
玻璃棒
容量瓶
圆底烧瓶
胶头滴管
6.在用海带提取碘的实验中,进行萃取和分液操作时要用到的仪器是( )
烧瓶
普通漏斗
分液漏斗
蒸发皿
7.溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )
溴酸银的溶解是放热过程
温度升高时溴酸银溶解速度加快
60℃时溴酸银的Ksp约等于6×
10﹣4
若硝酸钾中含有少量溴酸银,可用重结晶方法提纯
8.下列有关物质的量的说法中,正确的是( )
Mg的摩尔质量为24g
物质的量的单位是摩尔
1molO2在任何条件下的体积都为22.4L
将1molNaCl晶体加入到1L水中,得到NaCl溶液的浓度就是1mol•L﹣1
9.设NA为阿伏加德罗常数的值,下列判断正确的是( )
2gH2中含氢原子数为NA
1L1mol/LBaCl2溶液中含有的氯离子数为NA
标准状况下,22.4LH2O所含的原子数为3NA
0.1mol铁粉在足量氯气中充分燃烧,转移的电子数为0.3NA
10.用NA表示阿伏加德罗常数的值.下列判断正确的是( )
常温常压下,18g2H2O含有的原子总数目为3NA
标准状况下,22.4L水含有的分子数目为NA
1molNa在O2中完全燃烧转移的电子数目为NA
1mol•L﹣1KHSO4溶液中含有的钾离子数目为NA
11.科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是( )
原子数
分子数
体积
物质的量
12.只给出下列甲和乙中对应的物理量,不能求出物质的量的是( )
甲
物质中的粒子数
标准状况下的气体摩尔体积
固体的体积
溶液中溶质的物质的量浓度
乙
阿伏加德罗常数
标准状况下的气体的体积
固体的密度
溶液体积
二.填空题(共10小题,每空2分,共56分)
13.在0.2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,回答下列问题:
(1)该混合液中含溶质MgCl2的物质的量为 ,
(2)将该混合液加水稀释至体积为1L,稀释后溶液中Ca2+的物质的量浓度为 .
14.如图是配制50mL酸性KMnO4标准溶液的过程示意图.
(1)请你观察图示判断其中不正确的操作有 (填序号).
(2)其中确定50mL溶液体积的容器是 (填名称).
(3)如果按照图示的操作所配制的溶液进行实验,在其他操作均正确的情况下,所测得的实验结果将 (填“偏大”或“偏小”).
15.如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是 .
A.溶液中HCl的物质的量B.溶液的浓度C.溶液中Cl﹣的数目D.溶液的密度
(2)某学生欲用上述浓盐酸和蒸馏水配制500mL物质的量浓度为0.400mol•L﹣1的稀盐酸.
①该学生需要量取 mL上述浓盐酸进行配制.
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?
(“偏大”、“偏小)”或“无影响”)(a.用量筒量取浓盐酸时俯视观察凹液面
b.容量瓶使用前未干燥,有少量的蒸馏水
(3)①假设该同学用配制的0.400mol•L﹣1的盐酸,中和含0.4gNaOH的NaOH溶液,计算应消耗盐酸的体积为 ml.
②该同学用新配制的盐酸恰好中和含0.4gNaOH的NaOH溶液,发现实验实际消耗的盐酸比①中所求体积偏小,则可能的原因是 .
A.浓盐酸挥发,浓度不足
B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线
D.加水时超过刻度线,用胶头滴管吸出.
16.用98%的浓硫酸(其密度为1.84g/cm3)配制100mL1.0mol/L稀硫酸,若实验仪器有:
A.100mL量筒B.托盘天平C.玻璃棒D.50mL容量瓶
E.10mL量筒F.胶头滴管G.50mL烧杯H.100mL容量瓶
(1)需量取浓硫酸的体积为 mL.
(2)实验时选用的仪器有(填序号)
(3)配制过程中,下列情况会使配制结果偏高的是(填序号)
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线
(4)在容量瓶使用方法中,下列操作不正确的是(填序号)
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解,立即注入容量瓶中
D.将准确量取的18.4mol•L﹣1的硫酸,注入已盛有30mL水的100mL的容量瓶中,加水至刻度线
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
(5)在实验过程中出现如下情况应如何处理?
①加蒸馏水到离刻度线约1﹣﹣2厘米时,应
②加蒸馏水时不慎超过了刻度线,应 .
17.用浓硫酸吸收SO3可得发烟硫酸(H2SO4•SO3).某化工厂用1.5m398.3%的浓硫酸(密度为1.84g/mL)吸收SO3形成发烟硫酸,再与水混合,可得到95%的硫酸(密度为1.79g/mL) m3(保留2位小数).
18.0.01mol某物质的质量为1.08g,则此物质的摩尔质量为 .完全中和66mLHCl的质量分数为20%的稀盐酸(密度为1.10g/cm3),需要氢氧化钠 g, mol.
19.将4gNaOH溶于 g水中,可使溶液中H2O与Na+的物质的量之比为20:
1,此溶液中溶质的质量分数为 .
20.0.6mol的氧气与0.4mol臭氧,分子个数之比为 ,质量之比为 .
21.0.5molNa2CO3的质量为 g,其中含有 个Na+.
22.0.6molNH3分子中所含氢原子数与 molH2O分子中所含氢原子数相等.
三.解答题(共1小题,8分)
23.(2015•滕州市校级学业考试)
(1)如图信息,瓶中溶液长期放置后溶质质量分数变小,是因为该物质具有 性.
(2)某探究小组的同学对某工业废水(含有H2SO4、HNO3)中H2SO4的含量进行测定.取50g废水于烧杯中,加入足量BaCl2溶液、过滤、洗涤、干燥,得BaSO4固体11.65g.请解答下列问题:
①计算50g废水中H2SO4的溶质质量分数.(要求写出计算过程)
②若改用KOH溶液(利用消耗的KOH的质量)测定50g废水中H2SO4的含量,结果可能会 (选填“偏低”、“偏高”或“不变”),原因是 .
2015年07月03日lclzd0128的高中化学组卷
参考答案与试题解析
一.选择题(共12小题)
1.(2015春•澄城县校级月考)下列有关仪器使用方法或实验操作正确的是( )
考点:
计量仪器及使用方法.菁优网版权所有
专题:
实验评价题;
化学实验常用仪器.
分析:
A.锥形瓶和容量瓶在使用时不需要烘干,对实验结果没有影响;
B.滴定管在量取或者盛装溶液时必须润洗,否则会导致原溶液被蒸馏水稀释;
C.锥形瓶不能润洗,否则导致待测液中溶质的物质的量偏大,滴定过程中消耗的标准液体积偏大;
D.容量瓶中加水超过刻度线,导致配制的溶液体积偏大,溶液浓度偏小,此次配制失败.
解答:
解:
A.锥形瓶、容量瓶中有少量的蒸馏水,不影响滴定结果或配制溶液的浓度,所以不需要烘干锥形瓶或容量瓶,故A错误;
B.酸式滴定管在盛放标准液之前,为了避免滴定管中的少量蒸馏水将标准液稀释,应该先用标准液润洗,再盛放标准液,故B正确;
C.滴定过程中,锥形瓶不能润洗,否则会导致锥形瓶中待测液的溶质的物质的量偏大,测定结果偏高,故C错误;
D.用容量瓶配溶液时,若加水超过刻度线,此次配制失败,即使立即用滴管吸出多余液体,也不会使配制的溶液浓度恢复正常,故D错误;
故选B.
点评:
本题考查了常见计量仪器的构造及使用方法偏大,题目难度不大,注意掌握常见仪器的构造及正确的使用方法,明确容量瓶、锥形瓶、滴定管的使用方法.
2.(2015•衡水模拟)下列实验中,所采取的分离方法与对应原理都正确的是
物质的分离、提纯的基本方法选择与应用.菁优网版权所有
实验评价题.
A.乙醇和水混溶,不能用作萃取剂;
B.乙酸乙酯和乙醇混溶,不能用分液的方法分离;
C.应利用二者溶解度随温度的变化不同分离;
D.丁醇和乙醚的沸点不同,可用蒸馏的方法分离.
A.乙醇和水混溶,不能用作萃取剂,应用四氯化碳或苯萃取,故A错误;
B.乙酸乙酯和乙醇混溶,不能用分液的方法分离,应用蒸馏的方法分离,故B错误;
C.根据二者在水中随温度升高而溶解度不同,利用重结晶法.NaCl随温度升高溶解度变化不大,KNO3随温度升高溶解度变化大,经冷却过滤,故C错误;
D.丁醇和乙醚混溶,但二者的沸点不同,且相差较大,可用蒸馏的方法分离,故D正确.
故选D.
本题考查物质的分离提纯的实验方案的设计,题目难度不大,注意相关物质的性质的异同,把握常见物质的分离方法和操作原理.
3.(2015•上海)检验用硫酸亚铁制得的硫酸铁中是否含有硫酸亚铁,可选用的试剂是( )
物质的检验和鉴别的基本方法选择及应用.菁优网版权所有
亚铁离子具有还原性,可与氯水、高锰酸钾等氧化剂反应,以此解答该题.
A.加入氢氧化钠,因含有铁离子,可生成红褐色沉淀,不能检验是否含有亚铁离子,故A错误;
B.亚铁离子具有还原性,可与高锰酸钾等发生氧化还原反应,高锰酸钾溶液褪色,可鉴别,故B正确;
C.亚铁离子与KSCN不反应,不能鉴别,只能鉴别铁离子,故C错误;
D.亚铁离子与苯酚不反应,不能鉴别,只能鉴别铁离子,故D错误.
本题考查物质的检验,为高频考点,题目难度不大,本题注意亚铁离子与铁离子性质的区别,检验时必须有明显不同的现象.
4.(2015•枣庄校级模拟)下列仪器中,能在酒精灯上直接加热的是( )
直接加热的仪器及使用方法.菁优网版权所有
化学实验基本操作.
可直接加热的仪器有:
试管、燃烧匙、蒸发皿、坩埚.
A.试管属于玻璃仪器,并能在酒精灯火焰上直接加热,故A正确;
B.烧杯属于玻璃仪器,在酒精灯上加热时必须垫石棉网,不能直接加热,故B错误;
C.量筒只能用来量取液体,不能加热,故C错误;
D.集气瓶不能加热,故D错误.
故选A.
本题考查能直接加热的仪器,难度不大,能在酒精灯火焰上直接加热的仪器有:
试管、坩埚、蒸发皿、燃烧匙等,必须垫石棉网的仪器是:
烧杯、烧瓶、锥形瓶.
5.(2015•扬州模拟)用NaOH固体配制一定物质的量浓度的NaOH溶液时,不需要使用的玻璃仪器是( )
不能加热的仪器及使用方法.菁优网版权所有
用NaOH固体配制一定物质的量浓度的溶液的步骤为:
计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,根据配制的步骤选择使用的仪器.
根据配制一定物质的量浓度的氢氧化钠溶液的步骤可知,配制过程中使用的仪器有:
托盘天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管等,所以选项中必须使用的仪器为容量瓶、玻璃棒、胶头滴管,而圆底烧瓶在配制中不会用到,故选C.
本题考查了配制一定物质的量浓度的溶液中使用仪器选择方法,题目难度不大,注意掌握配制一定物质的量浓度的溶液步骤,能够根据配制步骤选用使用的仪器.
6.(2015•姜堰市)在用海带提取碘的实验中,进行萃取和分液操作时要用到的仪器是( )
利用物质的互不相溶的溶剂里溶解度的不同,用一种溶剂把物质从它与另一种溶剂所组成的溶液里提取出来,这种方法叫做萃取;
将萃取后两种互不相溶的液体分开的操作叫做分液.
萃取、分液必须用到的仪器名称叫分液漏斗,分液时,下层液体从下口倒出,上层液体从上口倒出,
故选C.
本题考查了萃取和分液实验的仪器确定,难度不大,注意分液时,下层液体从下口倒出,上层液体从上口倒出.
7.(2015•高安市校级模拟)溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( )
溶解度、饱和溶液的概念;
难溶电解质的溶解平衡及沉淀转化的本质.菁优网版权所有
物质的量浓度和溶解度专题.
A.根据图象中温度对溴酸银的溶解度影响可知溴酸银的溶解过程为吸热过程;
B.温度升高,可以加快物质的溶解速率;
C.根据溶度积表达式及溶液中银离子和溴酸根离子的浓度计算;
D.溴酸银的溶解度受温度的影响较小,可以通过重结晶法分离硝酸钾与溴酸银的混合物.
A.根据图象可知,升高温度,溴酸银的溶解度增大,说明溴酸银的溶解过程为吸热过程,故A错误;
B.升高温度,溴酸银的溶解度增大,所以温度升高时溴酸银溶解速度加快,故B正确;
C.60℃时溴酸银的溶解度为0.6g,溴酸银的物质的量为:
≈2.5×
10﹣3mol,100.6g溴酸银溶液的体积约为100.6mL,溶液中银离子、溴离子浓度约为2.5×
10﹣2mol/L,所以60℃时溴酸银的Ksp=2.5×
10﹣2×
2.5×
10﹣2≈6×
10﹣4,故C正确;
D.根据图象可知,溴酸银的溶解度受温度的影响不大,而硝酸钾的溶解度受温度影响较大,所以硝酸钾中含有少量溴酸银,可用重结晶方法提纯,故D正确;
本题考查了难溶物的溶解平衡、溶度积的表达式及计算、物质的分离与提纯,题目难度中等,注意掌握难溶物的溶解平衡及其影响因素,明确溶度积的概念及计算方法.
8.(2015•娄星区模拟)下列有关物质的量的说法中,正确的是( )
摩尔质量;
物质的量的单位--摩尔;
气体摩尔体积;
物质的量浓度的相关计算.菁优网版权所有
A、摩尔质量的单位是g/mol;
B、物质的量是七个基本物理量之一;
C、摩尔体积只与温度和压强有关;
D、溶液的体积不等于溶剂的体积.
A、Mg的摩尔质量是24g/mol,故A错误;
B、物质的量是七个基本物理量之一,其单位为摩尔,故B正确;
C、只有在标准状况下,1molO2的体积才为22.4L,故C错误;
D、将1molNaCl晶体加入到1L水中,溶液的体积不等于1L,所以溶液中NaOH的物质的量浓度不等于1mol/L,故D错误;
本题主要考查了概念,掌握概念的内涵是解题的关键,难度中等.
9.(2015•南京校级模拟)设NA为阿伏加德罗常数的值,下列判断正确的是( )
阿伏加德罗常数.菁优网版权所有
A.2gH2的物质的量是1mol;
B.1molBaCl2电离生成2mol氯离子;
C.标准状况下水不是气体;
D.铁粉在足量氯气中充分燃烧生成氯化铁.
A.2gH2的物质的量是1mol,含氢原子数为2NA,故A错误;
B.1molBaCl2电离生成2mol氯离子,含有的氯离子数为2NA,故B错误;
C.标况下水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故C错误;
D.0.1mol铁粉在足量氯气中充分燃烧生成氯化铁,转移的电子数为0.3NA,故D正确.
本题考查阿伏加德罗常数的相关计算,题目难度不大,注意物质的组成、结构、性质以及物质存在的外界条件和聚集状态等问题.
10.(2015•扬州模拟)用NA表示阿伏加德罗常数的值.下列判断正确的是( )
A、2H2O的摩尔质量为20g/mol;
B、标况下,水为液态;
C、根据反应后钠元素的价态为+1价来分析;
D、溶液体积不明确.
A、2H2O的摩尔质量为20g/mol,故18g2H2O的物质的量n=
=0.9mol,而1mol2H2O中含3mol原子,故0.9mol2H2O中含2.7mol原子,故A错误;
B、标况下,水为液态,故B错误;
C、反应后钠元素的价态为+1价,故1mol钠转移1mol电子,故C正确;
D、溶液体积不明确,溶液中钾离子的个数无法计算.
本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.
11.(2015•沈阳校级模拟)科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是( )
物质的量的相关计算.菁优网版权所有
计算题.
A.H3和H2都由H原子构成,二者质量相等,含有H原子数目相等;
B.H3和H2的摩尔质量不相等,二者质量相等,则二者物质的量不相等;
C.H3和H2的摩尔质量不相等,二者质量相等,则二者物质的量不相等,相同条件下,气体体积之比等于其物质的量之比;
D.H3和H2的摩尔质量不相等,二者质量相等,根据n=
可知二者物质的量不相等.
A.H3和H2都由H原子构成,二者质量相等,含有H原子数目相等,故A正确;
B.H3和H2的摩尔质量不相等,二者质量相等,则二者物质的量不相等,故含有分子数目不相等,故B错误;
C.H3和H2的摩尔质量不相等,二者质量相等,根据n=
可知二者物质的量之比=2:
3,相同条件下,气体体积之比等于其物质的量之比,故等质量H3和H2的体积之比=2:
3,故C错误;
可知二者物质的量不相等,故D错误,
本题考查物质的量有关计算,比较基础,注意对基础知识的理解掌握.
12.(2015•普兰店市)只给出下列甲和乙中对应的物理量,不能求出物质的量的是(
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 必修 第一 单元测试
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
