 高考满分之路搞定化学压轴题化工工艺流程综合题2Word下载.docx
高考满分之路搞定化学压轴题化工工艺流程综合题2Word下载.docx
- 文档编号:22864633
- 上传时间:2023-02-05
- 格式:DOCX
- 页数:14
- 大小:206.89KB
高考满分之路搞定化学压轴题化工工艺流程综合题2Word下载.docx
《高考满分之路搞定化学压轴题化工工艺流程综合题2Word下载.docx》由会员分享,可在线阅读,更多相关《高考满分之路搞定化学压轴题化工工艺流程综合题2Word下载.docx(14页珍藏版)》请在冰豆网上搜索。
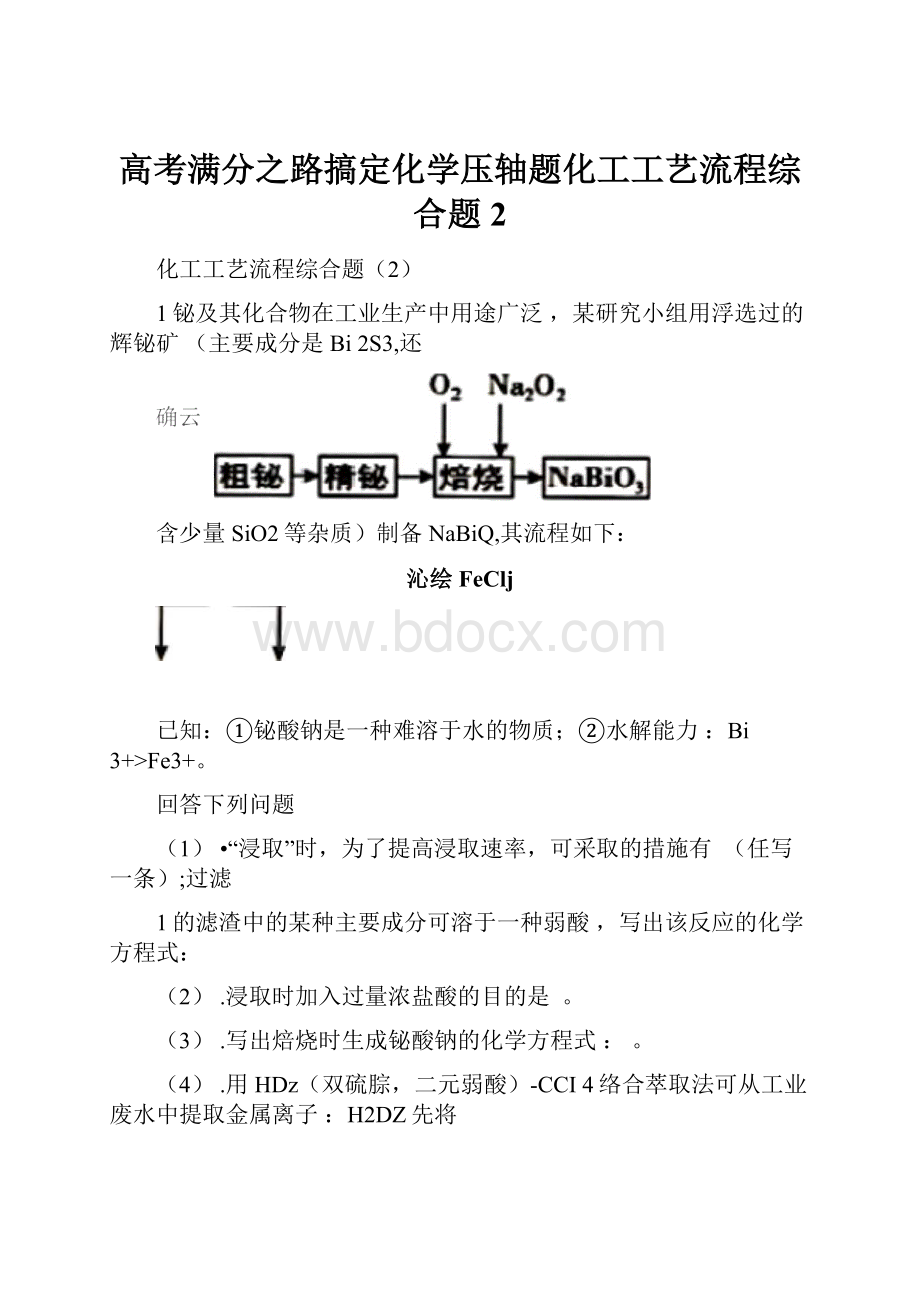
已知NaBiQ被还原
为Bi3+,Mn2+被氧化成•■•■■「'
:
;
=,试写出该反应的离子方程式:
2工业以软锰矿(主要成分是MnO,含有SiO2、Fe2Q等少量杂质)为主要原料制备高性能的磁
性材料碳酸锰(MnCO)。
其工业流程如下:
(1).浸锰过程中FaQ与SQ反应的离子方程式
为Fe2Q+SQ2+2H=2Fe2++J.
+H2Q,该反应是经历以下两步反应实现的。
i:
Fe203+6H+=2Fe3++3H2Q
ii:
写出ii的离子方程式:
(2).过滤I所得滤液中主要存在的两种金属阳离子为(填离子符号)。
(3).氧化过程中被MnQ氧化的物质有(写化学式):
(4)
Ir--uIfJ1u-1-I-I-
I(M5HCnw5(-k;
l(現Ii
LH介*$
仁•代融度对銭甩出率的涉响
•“浸锰”反应中往往有副产物MnSQ生成,温度对“浸锰”反应的影响如图所示,为减
少MnSQ6的生成,“浸锰”的适宜温度是;
向过滤H所得的滤液中加入NHHCQ溶液
时温度不宜太高的原因是
(5).加入NH4HCO溶液后,生成MnC沉淀,同时还有气体生成,写出反应的离子万程
式:
(6).生成的MnCO沉淀需经充分洗涤,检验洗涤是否完全的方法是
3、钛(22Ti)由于其特殊的性能被誉为“未来世纪的金属”。
钛铁矿主要成分为FeTiQ(含有
少量MgOSiO2等杂质),Li4Ti5O2和LiFePO4都是锂离子电池的电极材料,可利用钛铁矿来制
备,工艺流程如下
(1).Ti位于元素周期表中的位置为。
钛铁矿在预处理时需要进行粉碎,其原因
(2)
.过程①中,铁的浸出率结果如下图所示。
由图可知,当铁的浸出率为80%寸,所采用的
氨水反应转化成(NH4)2Ti5^5溶液时,Ti元素的浸出率与
反应温度的关系如下图所示,反应温度过高时,Ti元素浸出率下降的原因是
(4).写出由滤液D生成FePQ的离子方程式。
(5).由流程图可知FePQ制备LiFePQ4的化学方程式是
4、工业上用含三价钒(V2Q)为主的某石煤为原料(含有AI2Q、CaQ等杂质),钙化法焙烧制备
V2O5,其流程如下
丽芈作科輕[浸出菠V心|
【资料】:
+5价钒在溶液中的主要存在形式与溶液pH的关系:
pH
4~6
6~8
8~10
10~12
lAlJ
V02
VO3
vo3
(1).焙烧:
向石煤中加生石灰焙烧,将V2Q转化为Ca(VQ)2的化学方程式是
(2).酸浸:
1Ca(VQ)2难溶于水,可溶于盐酸。
若焙砂酸浸时溶液的pH=4,Ca(VQ)2溶于盐酸的离子方程
式是
2酸度对钒和铝的溶解量的影响如下图所示:
酸浸时溶液的酸度控制在大约3.2%,根据右
图推测,酸浸时不选择更高酸度的原因是
瘦出液沉淀ItWH乌泸灌也呗¥
0斗溶液常咛“腳①囿休
1浸出液中加入石灰乳的作用是。
2已知CaCO的溶解度小于Csb(VO4)2。
向Csb(VO4)2沉淀中加入(NH)2CO溶液,可使钒从沉淀
中溶出。
结合化学用语,用平衡移动原理解释其原
因:
3向(NH4)sVC4溶液中加入NHCI溶液,控制溶液的pH=7.5。
当pH>
8时,NH4VO的产量明显降
低,原因是。
(4).测定产品中V2O5的纯度:
称取ag产品,先用硫酸溶解,得到(VC2)2SC4溶液。
再加入bimLcimol・L-1(NH"
2Fe(SO"
2溶
液(VO2++2l4+Fe+^=vO++Fe3++H2O)。
最后用C2mol•L-1KMnO溶液滴定过量的(NH4)2Fe(SO4)2
至终点,消耗KMnO溶液的体积为b2mL。
已知MnO4被还原为MrT,假设杂质不参与反应。
则
产品中V2O5的质量分数是。
(V2O5的摩尔质量:
182g•mol-1)
5、工业从废铅酸蓄电池的渣泥(主要成分为PbSQ、PbO)回收铅。
RSR工艺的主要流程如下:
塑嚴丽科嗣体世瞇埜
(1).铅酸蓄电池放电时总反应为:
Pb(s)+PbO2(s)+2H2SQ(aq)=2PbSO4(s)+2H2OQ)
正极反应:
PbQ(s)+SQ2(aq)+4H+(aq)+2e-=PbSQ(s)+2H2O(I)
负极反应:
(2).向渣泥中加入Na^CO溶液将PbSO转化为更难溶的PbCO。
1用化学平衡移动原理解释其原因:
2工业上常用NaHCQ溶液代替NqCO溶液,将PbSO转化为PbCQPbSQ与NaHC3溶液或NqCO溶液不同物质的量比时,PbSO的转化率见下表。
I
n(PbSO):
n(NaHCQ)
1:
1.5
2
3
PbSQ转化率/%
95.5
96.9
97.8
n
n(PbSQ):
n(Na2CQ)
98
依据上表数据,物质的量比相同时,n中PbSQ的转化率比I中的略大,原因
3上述反应除生成PbCO外,还可能生成碱式碳酸铅[2PbCQ・Pb(OH)2],二者受热都易分解生
成PbO通过实验确定产物中含有2PbCO・Pb(OH)2,则该实验操作及现象
是;
通过定量实验确定产物中
2PbCO・Pb(OH)2的含量,则需测定的数据是。
(3).渣泥中加入NatSO溶液,利用其性质是。
(4).H2SiF4溶液溶解PbCO的化学方程式
6、三氯化铬是化学合成中的常见物质,三氯化铬易升华,在高温下能被氧气氧化,碱性条件下
能被H2Q氧化为Cr(W)。
制三氯化铬的流程如下
CCk(K>
Nr
•鮭代处理
(1).重铬酸铵分解产生的三氧化二铬(Cr2O>难溶于水)需用蒸馏水洗涤的原因
如何判断其已洗涤干净
(2).已知CC14沸点为57.6C,为保证稳定的CC14气流,适宜的加热方式是
(3).用下图装置制备CrCl3时,主要步骤包括:
1将产物收集到蒸发皿中
2加热反应管至400C,开始向三颈烧瓶中通入氮气,使CC14蒸气经氮气载入反应室进行反
应,继续升温到650C;
3三颈烧瓶中装入150mLCC4,并加热CCb,温度控制在50~60C之间;
4反应管出口端出现了CrCl3升华物时,切断加热管式炉的电源;
5停止加热CCl4,继续通入氮气
6检查装置气密性。
正确的顺序为:
⑥t③t
反应恃
(4).已知反应管中发生的主要反应有:
Cr2Q+3CCl4i2CrCI3+3COC2,因光气剧毒,实验需在
通风橱中进行,并用乙醇处理COC2,生成一种含氧酸酯(C5H0Q),用乙醇处理尾气的化学方程
式为
(5).样品中三氯化铬质量分数的测定
称取样品0.3300g,加水溶解并定容于250mL容量瓶中。
移取25.00mL于碘量瓶(一种带塞的
锥形瓶)中,加热至沸后加入1gNa2O2,充分加热煮沸,适当稀释,然后加入过量的2mol/LHSQ
至溶液呈强酸性,此时铬以CdQ;
-存在,再加入1.1gKI,密塞,摇匀,于暗处静置5分钟后,
加入1mL指示剂,用0.0250moI/L硫代硫酸钠溶液滴定至终点,平行测定三次,平均消耗标准硫代硫酸钠溶液24.00mL。
已知:
Cr2O2-+6I-+14H+=2Cr3++3I2+7H2O,2Na2S,O3+I2=Na2S4O6+2NaI。
1该实验可选用的指示剂名称为
2移入碘量瓶的CrCl3溶液需加热煮沸,加入NatQ后也要加热煮沸,其主要原因是
3样品中无水三氯化铬的质量分数为
答案以及解析
1答案及解析:
答案:
1.粉碎矿石、适当提高浸取时温度、适当提高FeCIs溶液浓度、浸取时不断搅拌(任
选其一);
SiO2+4HF—SF4f+2H2O
2.溶解Bi2S3,同时防止FeCIs和BiCI3水解生成不溶性沉淀,提高原料的浸出率。
3.2Bi+2O2+Na2Q'
2NaBiQ
4.①2.5
5.二池凶0卄么订护++14"
卜=处3十十他〃十十恥巾。
1十苗血
解析:
1.一般提高浸取速率的方法有搅拌、加热、将固体粉碎、增大浸取酸或碱的浓度等。
本题要注意:
盐酸具有挥发性,所以温度不能太高;
因加入的已经是浓盐酸了,故提高盐酸的
浓度意义不大。
第一步浸取后的滤渣主要是SiO2,该物质可溶于氢氟酸,化学方程式为
SQ2+4HF一SiF4?
+2H2O
2.加入过量的浓盐酸主要是为了将原料中的Bi元素溶解,同时也能抑制铁离子和铋离子的
水解。
3.焙烧和原料是单质铋,加入了氧气和过氧化钠,生成铋酸钠,结合的是电子守恒和原子守恒
w遍
写出化学方程式:
2Bi+2O2+N@Q“2NaBiQ。
4.①当n(Bi3+):
n[Bi(HDz)习=1:
4时,代表Bi3+的萃取率是80%,由图示得到此时废水的
pH=2.5。
2向萃取后的CCl4中加入足量的NaOH溶液可将Bi(HDz)3中铋元素以氧氧化物[Bi(OH)3]的形式沉淀出来,又H2Dz为二元弱酸,所以相应的离子方程式为
。
5.取培烧得到的NaBiQ;
样品加入稀硫酸和MnSO溶液使其完全溶解。
已知NaBiQ被还原为
Bi3+,Mn2+被氧化成'
'
根据守恒规律写出反应的离子方程
一」'
■--1'
"
o
2答案及解析:
1.2Fe3++SO2+2H2O=2Fe2++'
一+4H+
2+2+
2.Mn;
Fe
3.SO2;
(H2SO);
FeSO4
4.90C;
防止NHHCO受热分解,提高原料利用率
5.Mn2++2"
G°
3=MnCOX+COf+H2O
6.取1-2mL最后一次洗液于试管,滴加盐酸酸化BaCb溶液,若无白沉淀产生,则洗涤干净
3答案及解析:
1.第四周期IVB;
增大反应物接触面积,加快反应速率
2.100C3小时;
3.温度过高,双氧水分解与氨气逸出导致Ti元素浸出率下降
2++
4.2Fe+H2Q+2H3PQ=2FePO+4H+2H2O
5.2FePO4+Li2CO+HC2Q2LiFePO4+3COf+H2O
1.Ti的原子序数为22,处于第四周期第IVB族。
钛铁矿在预处理时进行粉碎,增大了
与盐酸的接触面积,可以加快反应速率。
2.由图中三条曲线可得,当铁的漫出率为80%寸,应为100°
C约浸取3小时。
3.由于二氧化钛与氨水、双氧水反应生成(NH4)2Ti5O5时,温度过高,双氧水和氨水都容易分解
(双氧水分解与氨气逸出),所以反应温度过高时,Ti元素浸出率下降。
4.由流程图可得,滤液D含有Fe2+,与H2Q、HPQ反应,生成FePQ,离子方程式
»
2++
为:
2Fe+HQ+2HPQ=2FePO+4H+2H2O。
5.由流程图可知FePQ与HC2Q、Li2CO高温锻烧发生反应生成LiFePO4,铁的化合价降
低,FePO4应为氧化剂,所以H2C2C4应为还原剂,故化学方程式
2FePO4+Li2CO+HOO2LiFePO4+3COf+H2O。
【点睛】
本题是一道工业流程题,是近年高考中必考的题型之一,关键是掌握工业流程题的解题技巧,
明确常考的知识点。
工业流程题目在流程上一般分为3个过程:
(1)原料预处理阶段,经常考查加快反应速率、溶解等方法,如本题就考查了通过粉碎来加快反应速率;
⑵分离提纯阶段,经常考到调节pH、加氧化剂(还原剂)、改变温度等方法涉及的反应,以及
混合物分离的常见操作;
⑶获得产品阶段,常考到蒸发、结晶、洗涤等操作。
4答案及解析:
1.CaO+O+V2QCa(VO)2
2.①Ca(VQ)2+4lH^=2vO++Ca++2HbO
②酸度大于3.2%时,钒的溶解量增大不明显,而铝的溶解量增大程度更大
3.①调节溶液的pH,并提供Ca2+,形成Ccb(VO4)2沉淀(富集钒元素)
2Ca3(VO4)2的浊液中存在平衡Ca3(VQ)2(s)=^3Ca(aq)+2VO4-(aq),(NH4)2CO溶液中
的CO3与Ca2+结合生成更难溶的CaCO沉淀,c(Ca2+)降低,平衡正向移动,使钒从沉淀中溶出
3pH>
8时,钒的主要存在形式不是VO3
4.91(cb-5c2b2)/(1000a)
5答案及解析:
1.Pb(s)+SO4-(aq)-2e-=PbSO(s)
2.①PbSQ浊液中存在平衡PbSO(s)=Pb2+(aq)+SO42-(aq),Na2CO溶液中的CO2-与Pb2+
结合生成更难溶的PbCQc(Pb)降低,平衡正向移动,即发生反应PbSO(s)+CO3-(aq)
2-
PbCQs)+SO4(aq)
2与PbSQ物质的量比相同时,Na2CO溶液中c(CQ2-)比NaHC晞液中的大
3取一定量样品充分干燥后加热,将产生的气体通过盛有无水硫酸铜的干燥管,无水硫酸铜
变蓝色,说明样品含有2PbCO・Pb(OH)2干燥后样品的质量m,充分加热、冷却后固体的质量m
3.还原性;
4.PbCO3+HSiF4=PbSiF4+COf+HO
6答案及解析:
1.除去其中可溶性杂质(或除去固体表面的重铬酸铵溶液);
取最后一次洗涤液适量于以试管中,向其中加入适量浓的氢氧化钠溶液,加热,取一片红色石蕊试纸润湿,粘在玻璃棒上,接近试管口,观察试纸是否变蓝,若不变蓝,则洗涤干净
2.水浴加热(并用温度计指示温度);
3.②④⑤①;
4.C0CI2+2C2H5OHtC2气OCOQ05+2HCI
5•①淀粉溶液;
2除去其中溶解的氧气,防止Q将I-氧化,产生偏高的误差。
396.1%(数值在95%~97不扣分)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 满分 搞定 化学 压轴 化工 工艺流程 综合
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《城市规划基本知识》深刻复习要点.docx
《城市规划基本知识》深刻复习要点.docx
