 江西铜鼓届高三化学选修五第二章烃和卤代烃能力提升检测试题Word文档格式.docx
江西铜鼓届高三化学选修五第二章烃和卤代烃能力提升检测试题Word文档格式.docx
- 文档编号:22827524
- 上传时间:2023-02-05
- 格式:DOCX
- 页数:21
- 大小:218.58KB
江西铜鼓届高三化学选修五第二章烃和卤代烃能力提升检测试题Word文档格式.docx
《江西铜鼓届高三化学选修五第二章烃和卤代烃能力提升检测试题Word文档格式.docx》由会员分享,可在线阅读,更多相关《江西铜鼓届高三化学选修五第二章烃和卤代烃能力提升检测试题Word文档格式.docx(21页珍藏版)》请在冰豆网上搜索。
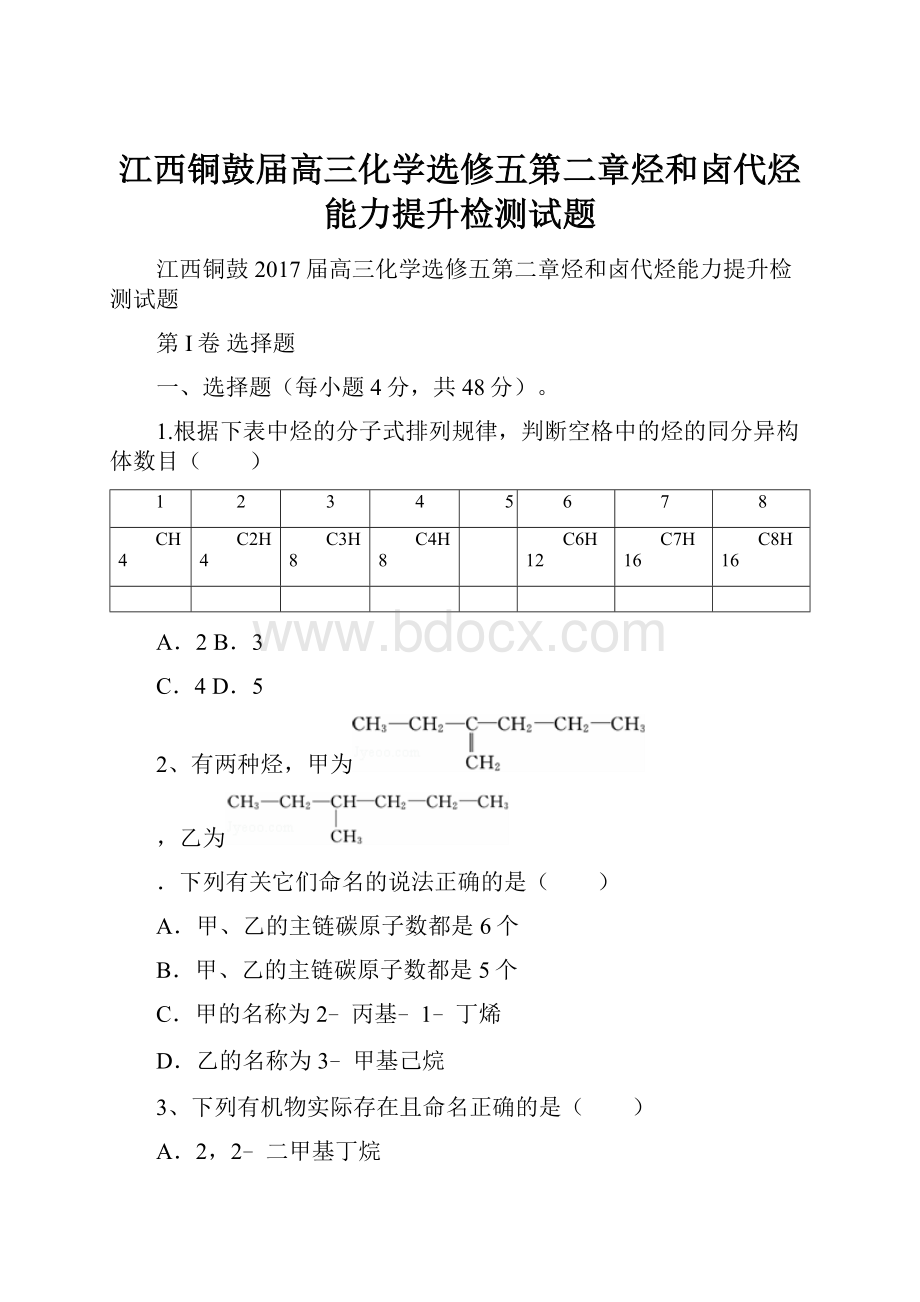
A.分子式为C7H16的烷烃,含有3个甲基的同分异构体有2种
B.丙烯能发生取代反应、加成反应,还能使酸性KMnO4溶液褪色
C.甲苯中所有原子都处于同一平面
D.相同质量的甲烷和乙烷完全燃烧乙烷耗氧量多
5、苯的同系物C12H18有多种同分异构体,其中二取代苯的同分异构体(不考虑立体异构)有( )
A.48种B.45种C.42种D.以上都不是
6、有人认为CH2=CH2与Br2的加成反应,实质是Br2先断裂为Br+和Br﹣,然后Br+首先与CH2=CH一端碳原子结合,第二步才是Br﹣与另一端碳原子结合.根据该观点如果让CH2=CH2与Br2在盛有NaCl和NaI的水溶液中反应,则得到的有机物不可能是( )
A.BrCH2CH2BrB.ClCH2CH2Cl
C.BrCH2CH2ID.BrCH2CH2Cl
7、下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是( )
A.甲烷与氯气发生取代反应
B.丙烯与水在催化剂的作用下发生加成反应
C.异戊二烯[CH2═C(CH3)﹣CH═CH2]与等物质的量的Br2发生加成反应
D.2﹣氯丁烷(CH3CH2CHClCH3)与NaOH乙醇溶液共热
8、烯烃、一氧化碳、氢气在催化剂的作用下生成醛的反应称为羰基合成,也叫烯烃的醛化反应,由乙烯到丙醛的反应为:
CH2═CH2+CO+H2→CH3CH2CHO.由分子式为C4H8的烯烃进行醛化反应得到的醛的同分异构体可能有( )
A.2种B.3种
C.4种D.5种
9、1mol某烃在氧气中充分燃烧,需要消耗氧气246.4L(标准状况下).它在光照的条件下与氯气反应能生成四种不同的一氯取代物.该烃的结构简式是( )
A.
B.CH3CH2CH2CH2CH3
C.
D.
10、用图所示装置检验乙烯时不需要除杂的是( )
选项
乙烯的制备
试剂X
试剂Y
A
CH3CH2Br与NaOH乙醇溶液共热
H2O
KMnO4酸性溶液
B
Br2的CCl4溶液
C
C2H5OH与浓H2SO4加热至170℃
NaOH溶液
D
溴水
11、下列命称的有机物实际上不可能存在的是( )
B.2﹣甲基﹣4﹣乙基﹣1﹣己烯
C.3﹣甲基﹣2﹣戊烯
12、下列说法正确的是(NA表示阿伏加德罗常数的值)( )
A.30g乙烷含有的共价键数目为8NA
B.2.8g乙烯和丙烯的混合气体中所含碳原子数为0.2NA
C.1mol甲基含10NA个电子
D.标况下,22.4L己烷完全燃烧后恢复至原状态,生成气态物质分子数为6NA
第II卷非选择题
二、非选择题(共52分)
13、对溴甲苯是合成农药溴螨酯的重要原料。
工业用液溴、甲苯与1-丙醇共热合成对溴甲苯和1-溴丙烷,其原子利用率很高。
实验室模拟的合成流程和相关数据如下:
已知:
甲苯与溴在有水存在时能反应。
物质
甲苯
1-丙醇
1-溴丙烷
沸点℃
110.8
97.2
71
对溴甲苯
邻溴甲苯
184.3
181.7
(1)液溴的颜色是______,实验室存放液溴时应密闭保存,同时需要在试剂瓶中加_____,以减少挥发。
(2)25℃恒温搅拌至溴的颜色完全褪去时完成甲苯的溴代反应。
搅拌的目的是__________。
加入水的作用是:
易于控制温度;
____________________。
(3)加热搅拌操作中加入浓硫酸,搅拌,完成1-丙醇的取代反应,加入浓硫酸的作用是______,加热微沸2小时的目的是____________。
(4)操作Ⅰ的名称是___________,洗涤操作应在_________(填写仪器名称)中进行。
(5)经以上分离操作后,粗对溴甲苯中还含有的最主要杂质为________(填写名称),使用操作Ⅱ分离出1-溴丙烷的原理是____________________________。
(6)分离出的水溶液中含HBr、H2SO4和Fe3+离子,将水溶液稀释定容至1000mL,取20.00mL,加入几滴甲基橙作指示剂,用一定浓度的NaOH溶液滴定,测定出HBr的物质的量明显低于理论值,原因是_____________________;
有同学认为无需加入指示剂,也能完成滴定,提出这一观点的理由是_______________________________。
14、某兴趣小组同学在实验室用加热1-丁醇、浓H2SO4和溴化钠混合物的方法来制备1-溴丁烷,并检验反应的部分副产物,设计了如图所示装置,其中夹持仪器、加热仪器及冷却水管没有画出。
请根据实验步骤,回答下列问题:
(1)关闭a和b、接通竖直冷凝管的冷凝水,给A加热30分钟,制备1-溴丁烷。
竖直冷凝管接通冷凝水,进水口是_____(填“I”或“Ⅱ”);
竖直冷凝管的主要作用是________。
(2)理论上,上述反应的副产物可能有:
丁醚(CH3CH2CH2CH2-O-CH2CH2CH2CH3)、1-丁烯、溴化氢、硫酸氢钠、水等。
熄灭酒精灯,在竖直冷凝管上方塞上塞子并打开a,利用余热继续反应直至冷却,通过B、C装置检验部分副产物,已知B、C装置中为常见物质的水溶液。
B装置检验的物质是_________,写出C装置中主要的化学方程式:
_______________。
(3)为了进一步分离提纯1-溴丁烷,该兴趣小组同学查得相关有机物的数据如表所示:
熔点/℃
沸点/℃
1-丁醇
-89.5
117.3
1-溴丁烷
-112.4
101.6
丁醚
-95.3
142.4
1-丁烯
-185.3
-6.5
请你补充下列实验步骤,直到分离出1-溴丁烷。
①待烧瓶冷却后,拔去竖直的冷凝管;
②插上带橡皮塞的温度计;
③关闭_______,打开_______;
④接通冷凝管的冷凝水,使冷水从______处流入;
⑤迅速升高温度至_______℃,收集所得馏分。
(4)若实验中所取1-丁醇、NaBr分别为7.4g、13.0g,蒸出的粗产物经洗涤、干燥后再次蒸馏得到9.6g1-溴丁烷,则1-溴丁烷的产率是_____。
(保留2位有效数字)
15、一溴乙烷为无色液体,熔点﹣119.1℃,沸点38.4℃,常用于汽油的乙基化、冷冻剂和麻醉剂.制备一溴乙烷的反应原理为:
NaBr+H2SO4═HBr↑+NaHSO4,CH3CH2OH+HBr→CH3CH2Br+H2O.实验室可用如图装置制备一溴乙烷
某学生的实验过程和具体操作可简述如下:
查阅资料可知:
①可能产生的副产物有:
CH3CH2OCH2CH3、CH2BrCH2Br、CH2=CH2、Br2、SO2,其中1,2﹣二溴乙烷为无色液体,熔点9.3℃,沸点131.4℃.
②油层a用浓硫酸处理可以除掉乙醚、乙醇和水等杂质.
请结合以上信息回答下列问题:
(1)实验过程中锥形瓶置于冰水混合物中的目的是 .
(2)水层a中的离子除Na+、H+、OH﹣和Br﹣外,还一定含有 ,检验该离子的方法是 .
(3)油层a、b均呈微黄色.该学生猜测油层b除一溴乙烷外还可能含有其它一种或多种副产物,为验证其成分设计了如下的实验操作.
实验步骤
预期现象和结论
步骤1:
将油层b转移至 中,再加入足量稀Na2SO3溶液充分振荡,静置.
步骤2:
取步骤1的水层少量于试管中,加入稀硫酸酸化,再加入适量新制氯水及少量CCl4,充分振荡,静置.
溶液分层,下层呈橙红色,证明 .
步骤3:
将步骤1的油层充分洗涤、干燥后装入蒸馏装置中, 至温度计升高至450C左右.
馏出蒸汽的温度稳定在38℃左右,不再有蒸汽馏出时,将蒸馏烧瓶中残留液体置于冰水浴中冷却,凝结成白色固体,则证明油层b中含有1,2﹣二溴乙烷.
(4)该同学在实验过程中加入了10mL乙醇(0.17mol),足量浓硫酸,适量水,以及0.15mol溴化钠,最后蒸馏获得了10.9g一溴乙烷产品.请计算产率 (用小数表示,保留二位小数).
16、已知乙醇在加热的条件下可与HBr反应得到溴乙烷(CH3CH2Br),二者某些物理性质如下表所示:
溶解性
沸点
密度(g/mL)
乙醇
与水互溶
78.5
0.8
溴乙烷
难溶于水
38.4
1.4
某研究性学习小组的同学将乙醇、80%的硫酸、NaBr固体按一定比例混合后(总体积约为140mL)置于图1的反应容器B中后进行加热(两个装置中的加热、固定装置及沸石均省略)。
(1)①仪器A的名称是
②容器B的容积是。
a.150mLb.200mLc.250mL
(2)两个水槽中的液体均是冰水,使用冰水的目的是。
(3)HBr与乙醇反应生成目标产物的化学方程式。
(4)图1中收集到的产品中含有一定量的杂质Br2,为除去该杂质,可先向混合液中加入适量的(从下面所给试剂中选取),然后再进行操作即可。
a.四氯化碳b.碳酸钠稀溶液c.无水CaCl2d.无水MgSO4
(5)经过(4)处理后的目标产物中还含有少量的水等杂质,可通过向产品中加入一定量的
(从上面的a~d中选取),充分作用后,过滤,将滤液使用图2中的装置进行提纯,冷却水应从口(填a或b)进入。
(6)若试验中使用的无水乙醇的体积是46mL,蒸馏后得到纯溴乙烷的体积是50mL,则溴乙烷的产率为%。
17、石蜡油(17个碳原子以上的液态烷烃混合物)的分解实验装置如图所示(部分仪器已省略)。
在试管①中加入石蜡油和氧化铝(催化石蜡分解);
试管②放在冷水中,试管③中加入溴水。
实验现象:
试管①中加热一段时间后,可以看到试管内液体沸腾;
试管②中有少量液体凝结,闻到汽油的气味,往液体中滴加几滴高锰酸钾酸性溶液颜色褪去。
根据实验现象回答下列问题:
(1)装置A的作用是______________________________
(2)试管①中发生的主要反应有:
C17H36
C8H18+C9H18C8H18
C4H10+C4H8
丁烷可进一步裂解,除得到甲烷和乙烷外,还可以得到另两种有机物,它们的结构简式为_____________和________________,这两种有机物混合后在一定条件下可聚合成高分子化合物,其反应类型属于________反应。
其可能结构为()(答案可能不止一个,下同)
(3)写出试管③中反应的一个化学方程式_____________________________,该反应的类型为__________反应。
(4)试管②中的少量液体的组成是____________(填序号)
①甲烷②乙烯③液态烷烃④液态烯烃
参考答案
1.【答案】B
【解析】解:
从1到8,物质的分子中C原子个数递增,因此物质5的分子中应含有5个碳原子,故A、C不符合规律;
各物质的分子构成中H原子符合1与2、3与4、7与8的H原子个数相等,则可推断5与6的分子构成中H原子个数相等,即物质5的分子中含有12个H原子;
综合以上分析,物质5的化学式为C5H12,同分异构体有3种.
故选B.
2.【答案】D
A.甲应含双键的最长碳链为主链,最长为5个碳,故A错误;
B.乙最长碳链为6个碳,故B错误;
C.甲的名称为2﹣乙基﹣1﹣丁烯,故C错误;
D.乙的名称为3﹣甲基己烷,符合命名规则,故D正确.
故选D.
3.【答案】A
A.符合命名规则,故A正确;
B.最长碳链为7个碳,命名为:
2,5﹣二甲基﹣庚烷,故B错误;
C.取代基的位次和最小,应为2﹣甲基﹣2﹣丁烯,故C错误;
D.3号碳上接了5个键,碳原子最多接4个键,故D错误.
故选A.
4.【答案】B
A.分子式为C7H16的烷烃,含有3个甲基的同分异构体有3种,故A错误;
B.丙烯中含有甲基和双键,所以丙烯有烷烃和烯烃的性质,既能发生取代反应又能发生加成反应还能使酸性KMnO4溶液褪色,故B正确;
C.甲苯含有﹣CH3,苯环相当于CH4中的一个H原子,CH4中各原子均不共面,因此甲苯中各原子不共面,故C错误;
D.甲烷和乙烷的燃烧方程式分别为:
假设分别燃烧1g燃料,需要的氧气分别为
CH4+2O2
CO2+2H2O
162mol
1gXmol
=
解得x=
2C2H6+7O2
4CO2+6H2O
607mol
1gXmol
所以燃烧相同质量的甲烷和乙烷,甲烷烷需要的氧气多,故D错误.
5.【答案】B
【解析】6个碳原子,可以形成1和5、2和4、3和3,
甲基只有1种,戊基有8种:
C﹣C﹣C﹣C﹣C,正戊烷形成的戊基有3种;
C﹣C﹣C(﹣C)2,异戊烷形成的戊基有4种
C(﹣C)4,新戊烷形成的戊基有1种,苯的2个取代基可以的邻位、间位和对位,此时共有1×
8×
3=24种;
乙基只有1种,丁基有4种:
C﹣C﹣C﹣C,正丁烷形成的戊基有2种;
C﹣C(﹣C)2,异丁烷形成的丁基有2种
C(﹣C)4,苯的2个取代基可以的邻位、间位和对位,此时共有1×
4×
3=12种;
丙基有2种:
C﹣C﹣C,丙烷形成的丙基有2种,苯的2个取代基可以的邻位、间位和对位,此时共有9种;
所以二取代苯的同分异构体共45种.
6.【答案】B
按照题意,第一步肯定要上Br+,即一定会出现BrCH2CH2﹣的结构,第二步才能上阴离子,NaCl和NaI的水溶液中含有氯离子和碘离子还有溴水中的溴离子,可以分别加在碳原子上,ACD均可以,故B错误.
7.【答案】A
A、甲烷与氯气发生取代反应可以生成一氯甲烷、二氯甲烷、三氯甲烷、三氯甲烷,含有的氯原子数目不同,不存在同分异构体,故A正确;
B、丙烯不是对称结构,与水发生加成反应,羟基有2种位置连接,可以生成OHCH2CH2CH3、CH3CHOHCH3,存在同分异构体,故B错误;
C、异戊二烯与溴可发生1,2﹣加成或1,4﹣加成两种物质,则存在同分异构体,故C错误;
D、2﹣氯丁烷(CH3CH2CHClCH3)与NaOH乙醇溶液共热发生消去反应可生成1﹣丁烯和2﹣丁烯,则存在同分异构体,故D错误;
8.【答案】C
丁烯进行醛化反应也可得到醛为戊醛,可以看作﹣CHO取代丁烷中1个H原子形成,
丁烷有正丁烷、异丁烷两种,正丁烷分子中有2种H原子,﹣CHO取代正丁烷中1个H原子形成的醛有2种,
异丁烷分子中有2种H原子,﹣CHO取代异丁烷中1个H原子形成的醛有2种,
故戊醛共有4种结构,
故选C.
9.【答案】A
该饱和烷烃在光照的条件下与氯气反应能生成4种不同的一氯取代物,说明该饱和烷烃中含有4种类型的氢原子;
氧气的物质的量=
=11mol,设该饱和烷烃的通式为CxH2x+2,1mol某饱和烷烃在氧气中充分燃烧,需要消耗氧气的物质的量=(x+
)mol=11mol,x=7,所以该饱和烷烃是庚烷且含有4种类型的氢原子,
10.【答案】B
A.发生消去反应生成乙烯,水吸收乙醇,乙醇能被高锰酸钾氧化,则需要加水除杂,否则干扰乙烯的检验,故A不选;
B.发生消去反应生成乙烯,乙醇与Br2的CCl4溶液不反应,乙烯与Br2的CCl4溶液反应,则不需要除杂,不影响乙烯检验,故B选;
C.发生消去反应生成乙烯,NaOH溶液吸收乙醇,乙醇能被高锰酸钾氧化,则需要NaOH溶液除杂,否则干扰乙烯的检验,故C不选;
D.发生消去反应生成乙烯,乙醇与溴水不反应,但可能混有二氧化硫,二氧化硫、乙烯均与溴水发生反应,则需要除杂,否则可干扰乙烯检验,故D不选;
11.【答案】D
A.2,2﹣二甲基丁烷结构为CH3C(CH3)2CH2CH3,名称符合系统命名,故A错误;
B.2﹣甲基﹣4﹣乙基﹣1﹣己烯结构为CH2═C(CH3)CH2CH(CH2CH3)2,名称符合系统命名,故B错误;
C.3﹣甲基﹣2﹣戊烯结构为CH3CH═C(CH3)CH2CH3,名称符合系统命名,故C错误;
D.3,3﹣二甲基﹣2﹣戊烯结构为CH3CH═C(CH3)2CH2CH3,2号碳原子呈5个共价键单键,碳原子为四价结构,故不可能存在,故D正确.
12.【答案】B
A、30g乙烷的物质的量为1mol,而1mol乙烷中含6molC﹣H键和1molC﹣C键即共7mol共价键即7NA条,故A错误;
B、乙烯和丙烯的最简式均为CH2,故2.8g混合物中含有的CH2的物质的量n=
=0.2mol,含0.2mol碳原子即0.2NA个,故B正确;
C、甲基不显电性,故1mol甲基含9mol电子即9NA个,故C错误;
D、标况下己烷为液体,故22.4L己烷的物质的量不是1mol,则生成的气体物质分子个数不是6NA个,故D错误.
13.【答案】
(1)深红棕色水
(2)使互不相溶的液体充分混合吸收反应生成的溴化氢气体
(3)催化剂提高氢溴酸和1-丙醇的利用(转化)率
(4)分液分液漏斗
(5)邻溴甲苯利用物质的沸点差异,用加热冷凝(蒸馏或分馏)的方法分离
(6)溴(溴化氢)挥发没有参加反应(溴与铁反应生成溴化铁)(答一点给分。
其他合理给分)滴定终点时,有Fe(OH)3红褐色沉淀生成,可以指示滴定终点
【解析】
(1)液溴的颜色是深红棕色,液溴易挥发,水的密度比液溴的小,所以实验室存放液溴时应密闭保存,同时需要在试剂瓶中加水,以减少其挥发;
(2)搅拌的目的是使互不相溶的反应物充分混合,有利于反应充分进行;
加入水的作用除易于控制温度外,还有就是吸收反应中产生的HBr气体;
(3)浓硫酸起到催化剂的作用,为提高氢溴酸和1-丙醇的利用(转化)率,加热微沸2小时,使之充分反应;
(4)将水溶液与互不相溶的有机物分离,可用分液漏斗进行分液操作,达到分离的目的;
(5)粗对溴甲苯中还含有的最主要杂质为邻溴甲苯,可利用物质的沸点差异,用加热冷凝(蒸馏或分馏)的方法分离;
(6)测定出HBr的物质的量明显低于理论值,可能原因为溴(溴化氢)挥发没有参加反应(溴与铁反应生成溴化铁),滴定终点时,有Fe(OH)3红褐色沉淀生成,可以指示滴定终点,所以无需加入指示剂,也能完成滴定。
14.【答案】
(1)Ⅱ冷凝回流
(2)溴化氢CH3CH2CH=CH2+Br2→BrCH2CHBrCH2CH3
(3)③关闭a,打开b④d处⑤101.6℃(4)70%
(1)冷凝管进水口与液体的充满方式有关,应是下口进水,即II口。
竖直冷凝管的主要作用是回流有机物,使其充分反应。
(2)溴化氢极易溶于水,而1-丁烯难溶于水,故先检验HBr;
C用于检验1-丁烯,溶液溶质可以是Br2,也可以是KMnO4,但Br2的加成反应更容易写出反应方程式。
(3)蒸馏出来1-溴丁烷,需要将a活塞关闭,将b活塞打开;
冷凝水还是由下口d处进入;
得到产品时蒸汽的温度应控制为1-溴丁烷的沸点(101.6℃)。
(4)1-丁醇、NaBr分别为7.4g、13.0g,即0.1mol、0.13mol,最多得到1-溴丁烷0.1mol,即13.7g
则1-溴丁烷的产率是
=70%。
15.【答案】
(1)防止产品挥发损失;
(2)SO42﹣;
取少量水层a的溶液于试管中,加入足量稀盐酸化,再滴加少量的BaCl2溶液,若产生浑浊,有SO42﹣,否则无SO42﹣;
(3)
分液漏斗
液体分层,下层液体逐渐褪为无色
油层b中含有Br2
水浴加热
(4)0.67。
95%乙醇、水和浓硫酸,冰水冷却,边搅拌边缓慢加入NaBr粉末,反应生成的HBr和乙醇发生取代反应得到一溴乙烷,分液小火加热得到馏出液,在分液漏斗中分层得到油层a,再边用冰水冷却,边加入适量浓硫酸,通过分液得到水层b和油层b得到一溴乙烷;
(1)一溴乙烷的沸点较低,易挥发,所以锥形瓶置于冰水混合物中的目的是防止产品挥发损失,减少损耗;
故答案为:
防止产品挥发损失;
(2)制备一溴乙烷所用试剂有浓硫酸,所以水层a中的离子除Na+、H+、OH﹣和Br﹣外,一定还有SO42﹣;
SO42﹣的检验方法是:
取少量水层a的溶液于试管中,加入足量稀盐酸化,再滴加少量的BaCl2溶液,若产生浑浊,有SO42﹣,否则无SO42﹣;
SO42﹣,取少量水层a的溶液于试管中,加入足量稀盐酸化,再滴加少量的BaCl2溶液,若产生浑浊,有SO42﹣,否则无SO42﹣;
(3)步骤2中溶液出现分层现象,所以将油层b转移至分液漏斗中,便于分离溶液;
一溴乙烷中可能含有CH3CH2OCH2CH3、CH2BrCH2Br、CH2=CH2、Br2、SO2等杂质,而使溶液显黄色.一溴乙烷的密度比水大,Na2SO3溶液可以吸收Br2、SO2在溶液的上层,一溴乙烷等油层在溶液的下层,所以出现的现象是液体分层,下层液体逐渐褪为无色;
步骤2中用新制氯气和四氯化碳溶液萃取,溶液分层,下层呈橙红色,证明原油层中b中含有Br2;
步骤1的油层中含有一溴乙烷、CH2BrCH2Br等,一溴乙烷的沸点较低,所以控制温度在38℃左右时溜出的馏分是一溴乙烷,常用水浴加热的方法,控制温度;
(4)乙醇的物质的量大于溴化钠的物质的量,所以理论上生成0.15mol的一溴乙烷,实际得到
mol=的一溴乙烷,所以产率=
=0.67.故答案为0.67。
16.【答案】
(1)①直形冷凝管②c
(2)降温,减少溴乙烷的挥发;
(3)HBr+C2H5OH
C2H5Br+H2O(4)b分液(5)cda(6)80%
(1)①根据仪器特征,仪器A的名称是直形冷凝管,②总体积约为140mL,烧瓶中溶液体积约占1/3,则容器B的容积是250mL,选c;
(2)两个水槽中的液体均是冰水,使用冰水的目的是降温,减少溴乙烷的挥发
(3)HBr与乙醇反应生成目标产物的化学方程式为HBr+C2H5OH
C2
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 江西 铜鼓 届高三 化学 选修 第二 卤代烃 能力 提升 检测 试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《JAVA编程基础》课程标准软件16级.docx
《JAVA编程基础》课程标准软件16级.docx
