 无机化学文档格式.docx
无机化学文档格式.docx
- 文档编号:22776999
- 上传时间:2023-02-05
- 格式:DOCX
- 页数:23
- 大小:146.19KB
无机化学文档格式.docx
《无机化学文档格式.docx》由会员分享,可在线阅读,更多相关《无机化学文档格式.docx(23页珍藏版)》请在冰豆网上搜索。
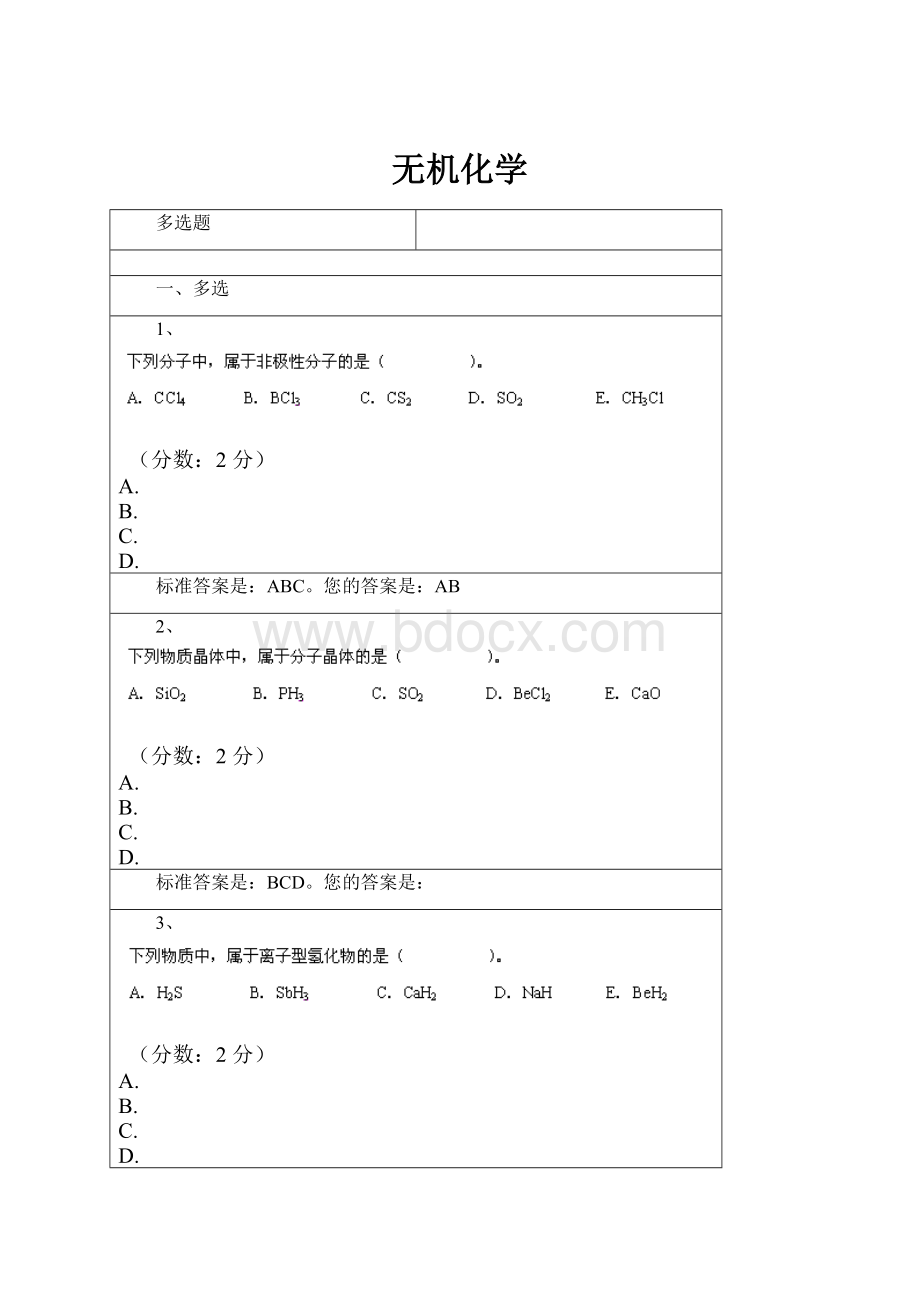
4、
AB。
5、
ACD。
6、
7、
8、
9、
10、
11、
再次测验
1、
渗透压
问题反馈
【显示答案】
正确答案:
【
为阻止渗透作用发生,必须在溶液表面施加的压力,称为溶液的渗透压。
】
2、
质量摩尔浓度
用单位质量(1kg)溶剂中所含溶质的物质的量表示的溶液浓度。
3、
标准生成焓
在标准状态下,由稳定单质生成1mol化合物或转变成其它形式单质时的焓变,称为该化合物或其它形式单质的标准生成焓。
4、
标准生成自由能
标准状态下,由稳定单质生成1mol某物质时的自由能变化,称为该物质的标准生成自由能。
标准熵
【在标准状态,1mol纯物质的熵值称为该物质的标准摩尔熵,简称标准熵。
6、
多重平衡规则
相同条件下,一体系中若有多个组分相关平衡,若干反应方程式相加(或相减)所得到的总反应的平衡常数等于这些反应的平衡常数之积(或商)。
7、
质子酸
凡能给出质子的物质(分子或离子)称为质子酸。
质子碱
【凡能接受质子的物质(分子或离子)称为质子碱。
缓冲溶液
【加入少量酸、碱或在一定范围内稀释,pH值基本保持不变的溶液称为缓冲溶液。
10、
同离子效应(电离平衡体系)
向已达平衡的弱电解质溶液中,加入与该弱电解质具有相同离子的强电解质,使弱电解质电离度减小的现象称为同离子效应。
同离子效应(沉淀−溶解平衡体系)
向难溶电解质平衡体系中,加入与其具有相同离子的强电解质,使难溶电解质溶解度减小的效应称为同离子效应。
12、
原子轨道
原子中一个电子可能的空间运动状态称为原子轨道。
13、
分子轨道
分子中电子的空间运动状态称为分子轨道。
14、
钻穿效应
离核较远的电子钻到离核较近的空间,受到的引力增强,导致其能量降低的现象。
15、
屏蔽效应
【多电子原子中,其它电子抵消部分核电荷对指定电子的吸引作用,称为屏蔽效应
16、
第一电离能
【基态的气态原子失去1个电子形成+1价气态阳离子所需要的能量。
17、电负性
元素的原子在分子中吸引电子的能力称为元素的电负性。
18、
元素周期律
【随着原子序数(核电荷数)的递增,元素性质呈现周期性变化的规律称为元素周期律。
19、配位单元
【具有价电子空轨道的离子或原子与具有孤对电子或π键电子的离子或分子以配位键相结合形成的复杂结构单元。
20、配位数
【配位单元中直接与中心原子键合的配位原子的总数称为配位数。
21、
螯合物
多齿配体与一个中心原子形成的具有环状结构的配合物。
22、
多核配合物
配位单元中含有两个或两个以上中心原子的配合物称为多核配合物
24、
晶体场稳定化能
【d电子从分裂前的d轨道进入分裂后的d轨道所降低的总能量称为晶体场稳定化能。
25、
歧化反应
【同一物质中同一元素,一部分氧化数升高,另一部分氧化数降低的氧化还原反应
23、
晶体场分裂能
d轨道分裂后,最高能量d轨道与最低能量d轨道的能级差称为晶体场分裂能,简称分裂能。
用反应速率理论说明,增大反应物浓度可以加快反应速率。
【温度一定时,活化分子百分数一定。
当增大反应物浓度时,单位体积内活化分子总数增加,导致有效碰撞频率增大,故反应速率加快。
写出基元反应2NO(g)+O2(g)=2NO2(g)的速率方程式。
当NO和O2的浓度均增大1倍或2倍时,初始反应速率将如何变化?
【答:
速率方程式:
v=k[NO]2[O2];
浓度均增大1倍时:
增大到原来的8倍,即增大7倍;
浓度均增大2倍时:
增大到原来的27倍,即增大26倍。
写出基元反应A(g)+2B(g)=2C(g)的速率方程式。
当反应容器的体积增大或减小1倍时,初始反应速率将如何变化?
反应速率方程为v=k[A][B]2;
当反应容器的体积增大1倍时,初始反应速率将减小到原来的1/8。
当反应容器的体积减小1倍时,初始反应速率将增大到原来的8倍。
用反应速率理论说明,升高反应温度可以加快反应速率。
温度升高时,分子运动速率加快,碰撞频率增大;
更重要的是温度升高时,活化分子的百分数增加,导致有效碰撞频率增大,故反应速率加快。
5、
用反应速率理论说明使用催化剂可以加快反应速率。
答:
因为催化剂参加了化学反应过程,改变了反应途径,降低了反应的活化能,活化分子百分数增加,导致有效碰撞频率增大,故反应速率加快。
6、写出最外层5s轨道上有1个电子,次外层d轨道半充满的元素的名称、符号和核外电子排布式,并指出其在周期表中的周期数和族数。
钼;
Mo;
1s22s22p63s23p63d104s24p64d55s1;
第五周期;
VIB族。
8、
第四周期的某元素,其原子失去3个电子后,在角量子数为2的轨道上恰好半充满。
写出该元素原子的核外电子排布式、原子序数、名称,并指出其在周期表中的周期数和族数。
失去3个电子后的核外电子排布为:
1s22s22p63s23p63d5;
原子的核外电子排布式为:
1s22s22p63s23p63d64s2;
其原子序数Z=26,铁,Fe,第四周期;
VIII族。
7、写出最外层4s轨道上有2个电子,次外层d轨道全充满的元素的名称、符号和核外电子排布式,并指出其在周期表中的周期数和族数。
锌;
Zn;
1s22s22p63s23p63d104s2;
第四周期;
IIB族。
第四周期的某元素,其原子失去3个电子后,在角量子数为2的轨道上恰好全充满。
写出该元素原子的核外电子排布式、原子序数、名称、符号,并指出其在周期表中的族数。
1s22s22p63s23p63d10;
1s22s22p63s23p63d104s24p1;
其原子序数Z=31,镓,Ga,IIIA族。
某元素的最高氧化数为+6,最外层有1个电子,原子半径在同族元素中最小。
写出该元素的名称、符号和核外电子排布式,并指出其在周期表中的周期数和族数。
铬,Cr,1s22s22p63s23p63d54s1,第四周期,VIB族
H2O和H2S的沸点何者高?
NH3与PH3的沸点何者高?
说明原因。
H2O的沸点比H2S高;
NH3的沸点比PH3高;
因H2O分子间和NH3分子间存在氢键,使水和液氨气化时需消耗额外热量破坏氢键,使缔合分子解离。
12、
SbH3和AsH3的沸点何者高?
HI与HBr的沸点何者高?
SbH3的沸点比AsH3高;
HI的沸点比HBr高;
因为分子量:
SbH3
>
AsH3、HI>
HBr,分子间色散力:
HBr。
改答案是否正确?
【正确
C和Si是IVA族相邻元素,但SiO2和CO2的熔点差别很大。
问SiO2和CO2的熔点何者高?
为什么?
SiO2的熔点高。
因为SiO2为原子晶体,固态CO2为分子晶体,原子晶体的熔点高于分子晶体。
14、
【d2sp3,内轨型,顺磁性,八面体
15、
【sp3d2,外轨型,顺磁性,八面体
16、
【d2sp3,内轨型,顺磁性,八面体
17、
【sp3d2,外轨型,反磁性,八面体
18、
19、
正确
、
9、
13、
20、
21、
22、
23、
24、
25、
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 无机化学
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
