 中考化学考点总动员系列 专题08 常见酸Word格式.docx
中考化学考点总动员系列 专题08 常见酸Word格式.docx
- 文档编号:22708141
- 上传时间:2023-02-05
- 格式:DOCX
- 页数:16
- 大小:371.09KB
中考化学考点总动员系列 专题08 常见酸Word格式.docx
《中考化学考点总动员系列 专题08 常见酸Word格式.docx》由会员分享,可在线阅读,更多相关《中考化学考点总动员系列 专题08 常见酸Word格式.docx(16页珍藏版)》请在冰豆网上搜索。
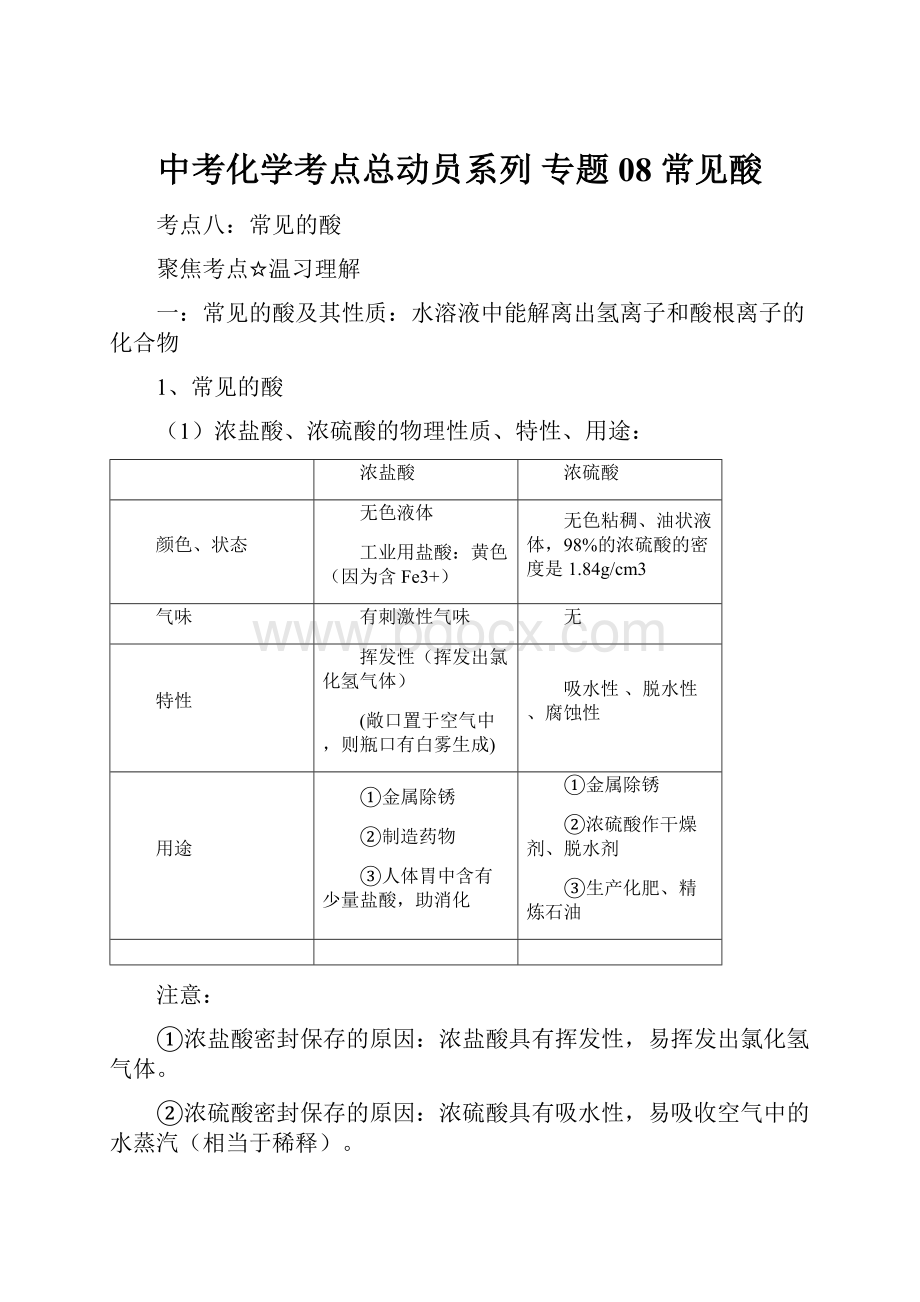
浓硫酸具有吸水性,易吸收空气中的水蒸汽(相当于稀释)。
③浓盐酸敞口放置在空气中一段时间后,溶质、溶液质量减少,溶剂质量不变,所以溶质质量分数减小。
④浓硫酸敞口放置在空气中一段时间后,溶质质量不变,溶剂、溶液质量增加,所以溶质质量分数减小。
⑤稀释浓硫酸时:
应把浓硫酸沿烧杯壁慢慢注入水里,并不断搅动。
切不可把水直接倒入浓硫酸中。
用玻璃棒搅拌的作用:
①加速溶解②散热。
⑥如果不慎将浓硫酸
沾到皮肤或衣服上,应先用布拭去,再用水冲洗,最后涂上3%—5%的碳酸氢钠溶液。
2、浓硫酸具有以下特性:
吸水性:
浓硫酸能吸收空气中的水分,可用来做干燥剂。
碱性气体不宜用浓硫酸干燥,如氨气。
脱水性:
浓硫酸能将纸张、木材、布料、皮肤里的氢、氧元素按水的组成比脱去,生成黑色的炭。
强氧化性(腐蚀性):
活泼金属与浓硫酸在一定条件下发生反应时,没有氢气生成。
3、酸的化学性质(具有相似性质的原因:
酸离解时所生成的阳离子全部是H+):
①与酸碱指示剂的反应:
使紫色石蕊试液变红色,不能使无色酚酞试液变色。
②金属+酸==盐+氢气置换反应(条件:
活动性:
金属>H)
H2SO4+Fe==FeSO4+H2↑2HCl+Fe==FeCl2+H2↑
③金属氧化物+酸==盐+水
Fe2O3+6HCl==2FeCl3+3H2O(注FeCl3溶液:
黄色)
现象:
铁锈溶解,溶液由无色变为黄色。
CuO+2HCl==CuCl2+2H2O(注CuCl2溶液:
蓝色)
黑色固体溶解,溶液由无色变为蓝色。
④碱+酸==盐+水
HCl+NaOH==NaCl+H2OH2SO4+2NaOH==Na2SO4+2H2O
⑤盐+酸→另一种盐+另一种酸(产物符合复分解条件)
二:
溶液的酸碱度(溶液酸碱度的表示法——pH)
1、PH值的范围:
0----14
0714
酸性增强中性碱性增强
在酸性溶液中,酸性越强,PH值越小,溶液中氢离子浓度越大;
在碱性溶液中,碱性越强,PH值越大,溶液中氢氧根离子浓度越大。
2、PH值与溶液酸碱性的
关系:
PH=7溶液呈中性例如:
H2ONaCl溶液Na2SO4溶液
PH<7溶液呈酸性,PH越小酸性越强例如:
酸溶液
PH>
7溶液呈碱性,PH越大碱性越强例如:
碱溶液
酸溶液一定是酸性溶液,但酸性溶液不一定是酸溶液
碱溶液一定是碱性溶液,但碱性溶液不一定是碱溶液
3、改变溶液PH值的方法:
(1)向酸性溶液中:
加水,溶液PH值不断增大,最终将接近于7(但不能达到7);
加碱性溶液,溶液PH值不断增大,最终PH值大于7。
(2)向碱性溶液中:
加水,溶液PH值不断减小,最终将接近于7(但不能达到7);
加酸性溶液,溶液PH值不断减小,最终PH值小于7。
4、pH的测定:
最简单的方法是使用pH试纸。
用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读出溶液的pH(读数为整数)。
(1)用PH试纸测得的PH值只能为正整数,不能为小数及零。
(2)用PH试纸测PH值时,不能先用蒸馏水润湿PH试纸。
若先用蒸馏水润湿后再测会影响结果:
使酸性溶液的PH值增大;
使碱性溶液的PH值减小;
中性溶液的PH值不变。
5、酸雨:
正常雨水的pH约为5.6(因为溶有CO2);
pH<
5.6的雨水为酸雨。
名师点睛☆典例分类
类型一、酸的物理性质
【例1】【2015年辽宁省丹东市】下列物质敞口放置在空气中一段时间后,质量会减少的是()
A.浓硫酸B.氯化钠C.浓盐酸D.烧碱
【答案】C
【解析】
试题分析:
浓硫酸和烧碱都会吸收空气中水分而质量变大,氯化钠质量基本不变,浓盐酸具有挥发性,所以其质量会减少。
故选C.
考点:
物质的性质
【点睛】常见的酸为盐酸、硫酸、硝酸、醋酸等浓盐酸具有挥发性,敞口放置挥发出氯化氢气体溶液的质量减少,而浓硫酸具有吸水性能吸收空气中的水分,溶液质量增加.
类型二、酸的化学性质
【例2】
【2015年四川省眉山市】下列物质与对应的用途错误的是()
A.Na2CO3治疗胃
酸过多B.熟石灰:
改良酸性土壤
C.稀盐酸:
除铁锈D.pH试纸:
测定溶液的酸碱度
【答案】B
常见物质的性质及用途
【点睛】稀酸的化学性质有与指示剂的反应、与活泼金属反应、与金属氧化物反应、与碱反应、与部分盐的反应;
而碱的化学性质为与酸碱指示剂反应、与酸反应、与非金属氧化物反应、与盐反应,根据性质选择试剂,只要出现不同的现象就是正确的答案。
.
类型三、浓硫酸的特性及稀释
【例3】【2015年湖南省株洲市】下列有关说法中不正确的是
A.酸溶液中都含有H+,所以有相似的化学性质B.酸、碱在水溶液中都可解离出带电的粒子
C.在实验室,常用浓硫酸来干燥某些气体D.医疗上的生理盐水是0.9%的纯碱溶液
【答案】D
A、酸溶液中都含有H+,所以有相似的化学性质,正确,B、酸、碱在水溶液中都可解离出带电的粒子,即离子,正确,C、浓硫酸具有吸水性,故在实验室,常用浓硫酸来干燥某些气体,正确,D、医疗上的生理盐水是0.9%的氯化钠溶液,错误,故选D
酸的特性及通性,常见物质的用途
【点睛】浓硫酸具有吸水性、脱水性及强氧化性浓硫酸吸收空气中的水分质量增加,在稀释浓硫酸时,要把浓硫酸沿玻璃棒倒入水中且不断的搅拌,不能把水倒入浓硫酸中,在实验操作时量筒只能作为量器使用,不能做任何反应容器.
类型四、酸的化学性质与PH
【例4】【2015年浙江省丽水市】科学实验方案是根据特定实验目的而设计的。
在学习了“酸能使紫色石蕊试液变色”的知识后,进一步了解到“盐酸能电离产生H+和Cl-,氯化钠能电离产生Na+和Cl-”。
为深入研究某一问题,小科同学设计了如图所示的实验方案。
请回答:
(1)往三支试管中分别滴入2滴紫色石蕊试液后,乙试管中的溶液将变为色;
(2)小科设计的实验方案研究的主要问题是。
【答案】
(1)红;
(2)稀盐酸中哪种微粒使石蕊试液变红?
【解析】
酸的性质、实验目的的确定
【点睛】解题的关键时熟记酸、碱的性质,酚酞试液在碱性情况下变为红色,而在酸性溶液中不变色,,反应后整个装置内都变色,说明碱溶液过量,剩余碱性溶液。
课时作业☆能力提升
一、选择题
1.【2015年辽宁省丹东市】下列物质敞口放置在空气中一段时间后,质量会减少的是()
2.【2015年湖南省张家界市】对物质进行分类,是化学研究上的一种基本方法。
例如,我们可将无机化合物根据其组成的不同,把它们分为氧化物、酸、碱、盐四类物质。
请你据此判断:
在下面的四种化合物中
,其中一种与另外三种不属于同一类别的物质是()
A.HClB.FeSO4C.CuSO4D.Na2CO3
【答案】A
从物质的分类看FeSO4;
CuSO4;
Na2CO3属于盐类,而HCl属于酸。
故选A.
物质的分类
3.【2015年江苏省连云港市】下列实验中利用提供的方案不能达到目的的是(
)
选项
实验目的
实验方案
A
稀释浓硫酸
将浓硫酸沿器壁慢慢注入水里,并不断搅拌
B
鉴别氮气和氧气
将带火星的木条插入集气瓶中,看是否复燃
C
测某溶液的酸碱度
滴入酚酞试液,观察溶液颜色的变化
D
除去固体氯化钾中少量的二氧化锰
加水溶解后,过滤,蒸发
浓硫酸的稀释,物质的鉴别
4.【2015年贵州省遵义市】酸溶液中都含有大量H+,因此不同酸表现出一些共同性质,下列关于盐酸性质的描述中,不属于酸的共同性质的是( )
A.能使紫色石蕊试液变为红色 B.能与氢氧化钠溶液反应生成水
C.能与硝酸银溶液反应生成白色沉淀 D.能与锌反应生成氢气
A、酸能使紫色石蕊试液变为红色,正确,B、能与碱发生中和反应生成盐和水,故能与氢氧化钠溶液反应生成水,正确,C、能与硝酸银溶液反应生成白色沉淀,是由于盐酸中含有氯离子,并不是含有H+,故这不属于酸的共同性质,错误,D、酸能与锌反应生成氢气,正确,故选C
酸的化学性质
5.【2015年广西省桂林市】区分稀硫酸和稀盐酸,不能使用的试剂是()
A.硝酸钡B.氯化钡C.氢氧化钡D.氯化钠
根据复分解反应的条件,硝酸钡、氯化
钡、氢氧化钡都能与稀硫酸反应生成硫酸钡沉淀,与稀盐酸不反应,故选D
物质的鉴别,复分解反应的条件
6.【2015年广西省桂林市】下列所用试剂能达到实验目的的是()
试剂
鉴别浓硫酸与稀硫酸
木条
鉴别氯化钡溶液与氯化钙溶液
碳酸钾溶液
除去氮气中的氧气
水
除去二氧化碳中的一氧化碳
氢氧化钠溶液
物质的鉴别和除杂
7.【2015年福建省莆田市】进行下列对比实验,不需要控制变量的是()
A.用酚酞溶液鉴别稀硫酸和氢氧化钠溶液B.用红磷和白磷探究可燃物燃烧的条件
C.用二氧化锰、氧化铜和过氧化氢溶液比较二氧化锰、氧化铜的催化效果
D.用镁、锌和稀盐酸比较镁、锌的金属活动性强弱
实验方案的选择和评价
8.【2015年广东省佛山市】只用石蕊试液就能将下列各组溶液区分开来的是()
A.NaClNaOHNaNO3B.NaOHH2SO4KNO3
C.HClNaClNa2SO4D.Na2SO4H2SO4CuSO4
【答案】BD
B中H2SO4KNO3不能用石蕊试液区分;
D.Na2SO4和CuSO4都是中性的溶液,所以石蕊无法区分。
故选BD。
物质的鉴别 物质的性质
二、非选择题
9.【2015年广西省南宁市】
(4分)盐酸、硫酸、氢氧化钠是重要的化工原料。
(1)浓硫酸是实验室常用的气体干燥剂,说明浓硫酸具有性;
(2)稀盐酸和稀硫酸都可以用于金属除锈,是因为它们的溶液中都含有;
(3)氢氧化钠暴露在空气中
,容易潮解,同时吸收空气中的而变质,所以氢氧化钠固体必须保存。
(1)吸水性
(2)H+(3)二氧化碳密封
(1)浓硫酸是实验室常用的气体干燥剂,说明浓硫酸具
有吸水性
(2)稀盐酸和稀硫酸具有相似的化学性质
,都可以用于金属除锈,是因为它们的溶液中都含有H+
(3)氢氧化钠暴露在空气中,容易潮解,同时吸收空气中的二氧化碳而变质,所以氢氧化钠固体必须密封保存
常见酸、碱的通性及特性
10、【2015年广东省揭阳市】
(9分)操作和保存药品不当,标签常常易损毁。
现有四瓶溶液①②③④的试剂标签已破损(如下图),但是已经知道这四瓶试剂是NaOH、Ca(OH)2、Na2CO3、KCl溶液中的一种,某兴趣小组同学决定对四瓶破损标签溶液成分进行实验探究(实验另外药品只提供盐酸和酚酞溶液):
【提出问题】标签已经破损的①②③④四瓶溶液分别是什么溶液?
【实验探究1】第④瓶试剂肯定是:
(写化学式)。
【实验探究2】兴趣小组对①②③④瓶溶液进行了如下的实验探究:
序号
实验步骤
实验现象
实验结论
1
取①②③瓶溶液少量
于三支试管中,分别
加入酚酞试液
酚酞试液不能将其中
的一种溶液鉴别出来
2
再取①②③瓶溶液少
量于另外三支试管中
分别加入溶液
加入了①溶液的试管
中;
其余两支试管中无明显现象
①瓶溶液为Na2CO3
3
取②③瓶溶液少量于
两支试管中,分别加
入溶液
加入了②溶液的试管
加入了③溶液的试管
②瓶溶液为
③瓶溶液为
Ca(OH)2
【反思与交流】为了防止标签发生破损,我们在倾倒溶液时应注意:
。
【答案】【实验探究1】KCl【实验探究2】序号1:
三瓶溶液都使无色酚酞变红色;
序号2:
稀盐酸产生大量气泡;
序号3:
Na2CO3无明显现象产生白色沉淀NaOH
【反思与交流】倾倒药品时,标签应向手心
【实验探究1】根据瓶塞来判断,因为NaOH、Ca(OH)2、Na2CO3这三种溶液都显碱性,能与玻璃里的主要成分二氧化硅反应,故它们应用橡皮塞,所以第④瓶试剂肯定是:
KCl
碱的化学性质,碳酸盐的化学性质
11.【2015年广东省佛山市】
(7分)A~N
是初中学过的物质。
D是相对分子质量为40的氧化物,A是不溶于稀硝酸的白色沉淀,E是难溶于水的白色沉淀,实验室通常用N制取CO2。
右下图是这些物质的转化关系,部分反应物、生成物及反应条件已省略。
(注:
难溶性碱加热分解生成对应的氧化物)
(1)写出化学式:
A,N。
(2)写出E→B的化学反应方程式。
(3)由F生成E需加入的物质是。
(4)C在空气中燃烧生成D的实验现象是。
C在空气中燃烧除了生成D之外,也可能与空气中的氮气生成氮化物(氮元素化合价为-3),该氮化物的化学式是。
(1)BaSO4HCl
(2)Mg(OH)2+H2SO4=MgSO4+2H2O(3)NaOH或KOH等(4)发出耀
眼的白光,产生白烟,生成白色固体Mg3N2
酸碱盐的性质及转化
12.【2015年福建省漳州市】复习课上,老师要求学生用不同的方法鉴别稀硫酸和氢氧化钠溶液。
小东
、小南两位同学取同一溶液分别进行如下实验:
【实验方案】
用玻璃棒蘸取溶液滴到pH试纸上,对照比色卡并读出pH
pH试纸变色
pH7(填“>
”或“<
”)
该溶液是氢氧化钠溶液
小南
取适量溶液于试管中,加入经打磨过的铝条
有气泡产生
该溶液是稀硫酸
【提出问题】为什么我们取相同溶液而实验结论却不同
呢?
【解决问题】
小东、小南讨论后决定再用硫酸铜溶液进一步验证,结果观察到的现象是,于是一致认为该溶液是氢氧化钠溶液。
为什么小南加入铝条会有气泡产生呢?
通过查阅资料,他们发现初中常见金属中只有铝能与酸、碱反应,铝与氢氧化钠溶液反应的化学方程式是:
2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
【拓展延伸】利用老师要求鉴别
的那两种溶液,测定镁铝铜
合金中各成分的含量。
实验设计如下:
【回答问题】
(1)写出操作I中玻璃棒的作用:
(2)a溶液是,选择该溶液的理由是。
(3)金属铜的质量为g,固体A含有的物质是,溶液A中所含溶质是。
【答案】【实验方案】>
【解决问题】有蓝色沉淀产生【回答问题】
(1)引流
(2)氢氧化钠溶液;
只有金属铝能与氢氧化钠溶液反应产生氢气,通过生成氢气质量方可求出铝质量(3)0.5Mg、CuNaOH、NaAlO2
NaOH的化学性质,金属的化学性质,反应后溶液中溶质的判断
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 中考化学考点总动员系列 专题08 常见酸 中考 化学 考点 总动员 系列 专题 08 常见
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《JAVA编程基础》课程标准软件16级.docx
《JAVA编程基础》课程标准软件16级.docx
