 北京顺义 高三化学一轮复习 氯元素及其化合物学案答案不全Word格式.docx
北京顺义 高三化学一轮复习 氯元素及其化合物学案答案不全Word格式.docx
- 文档编号:22673119
- 上传时间:2023-02-05
- 格式:DOCX
- 页数:21
- 大小:322.29KB
北京顺义 高三化学一轮复习 氯元素及其化合物学案答案不全Word格式.docx
《北京顺义 高三化学一轮复习 氯元素及其化合物学案答案不全Word格式.docx》由会员分享,可在线阅读,更多相关《北京顺义 高三化学一轮复习 氯元素及其化合物学案答案不全Word格式.docx(21页珍藏版)》请在冰豆网上搜索。
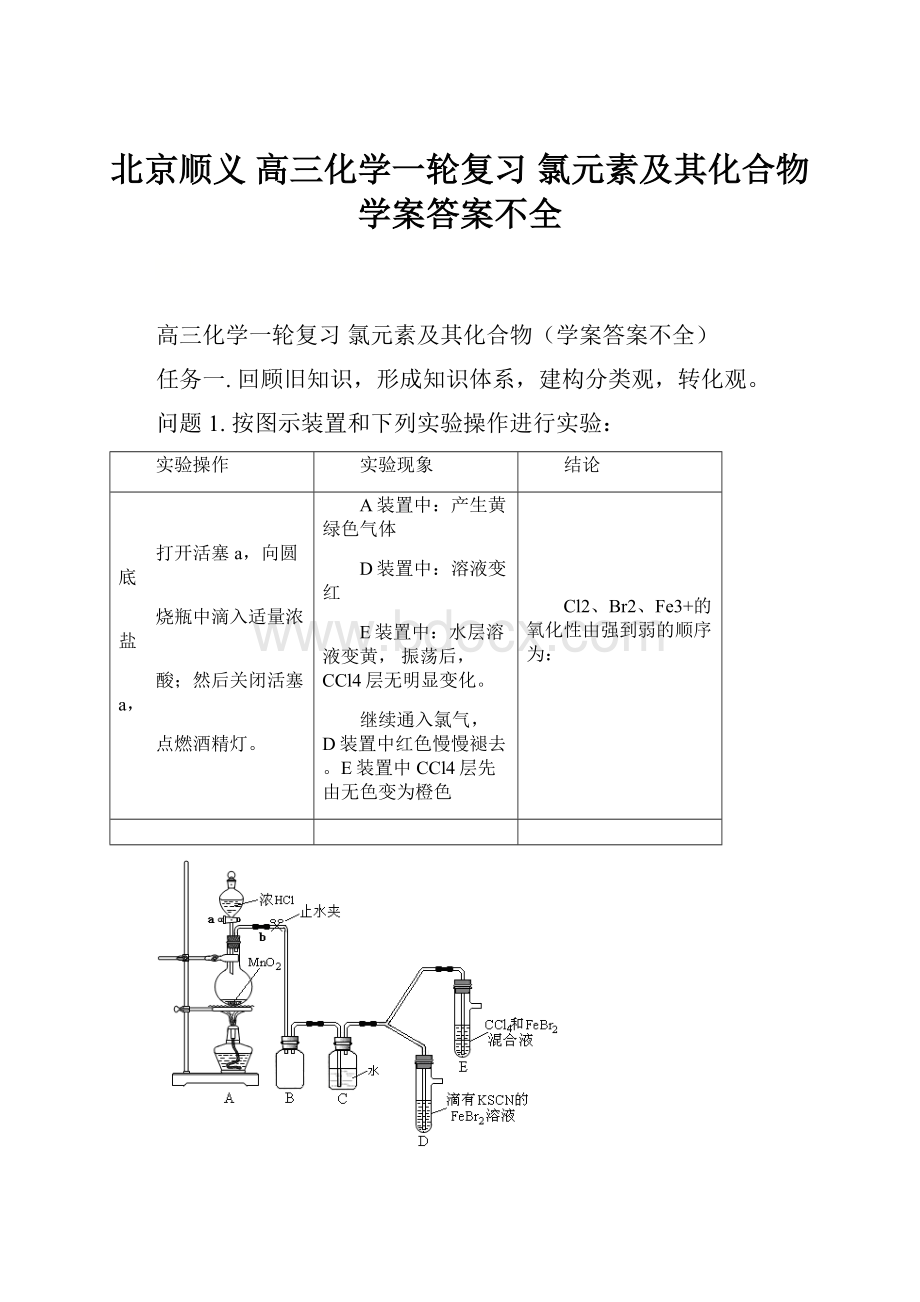
任务二.从实验入手认识重要物质的性质和制备等
(一)Cl2的检验方法:
用惰性电极电解pH=1的0.2mol/LNaCl溶液做对照实验,记录如下:
序号
电压
/
V
阳极现象
检验阳极产物
Ⅰ
x>
a
有气泡产生
有Cl2
Ⅱ
a>x≥c
无明显变化
Ⅲ
c>x≥b
无Cl2
Ⅰ中检验Cl2的实验方法:
。
Ⅱ中检验Cl2的实验方法:
(二)认识氯气、ClO-的氧化性
思考:
在一定条件下,氯气能氧化哪些物质?
ClO-能氧化哪些物质?
1、已知:
(SCN)2性质与卤素单质类似。
氧化性:
Cl2>
(SCN)2
向右图示试管中通入足量的氯气,先变红的溶液,慢慢褪去。
请结合化学用语和适当的文字解释溶液红色褪去的原因:
2、某学生对SO2与漂粉精的反应进行实验探究:
操作
现象
取4g漂粉精固体,加入100mL水
部分固体溶解,溶液略有颜色
过滤,测漂粉精溶液的pH
pH试纸先变蓝(约为12),后褪色
ⅰ.液面上方出现白雾;
ⅱ.稍后,出现浑浊,溶液变为黄绿色;
ⅲ.稍后,产生大量白色沉淀,黄绿色褪去
(1)Cl2和
制取漂粉精的化学方程式是。
(2)pH试纸颜色的变化说明漂粉精溶液具有的性质是。
(3)向水中持续通入SO2,未观察到白雾。
推测现象ⅰ的白雾由HCl小液滴形成,进行如下实验:
a.用湿润的碘化钾淀粉试纸检验白雾,无变化;
b.用酸化的AgNO3溶液检验白雾,产生白色沉淀。
①实验a的目的是。
②由实验a、b不能判断白雾中含有HCl,理由是。
(4)现象ⅱ中溶液变为黄绿色的可能原因:
随溶液酸性的增强,漂粉精的有效成分和
发生反应。
通过进一步实验确认了这种可能性,其实验方案是
(5)将A瓶中混合物过滤、洗涤,得到沉淀X。
①向沉淀X中加入稀HCl,无明显变化。
取上层清液,加入BaCl2溶液,产生白色沉淀。
则沉淀X中含有的物质是。
②用离子方程式解释现象ⅲ中黄绿色褪去的原因:
任务三、问题解决:
若某化工厂发生了大量贮氯罐泄露事件,为了厂区和周围地区群众的安全,你作为现场事故处理的总指挥,打算采取哪些应急措施?
任务四、海水的综合利用:
海水淡化、氯碱工业、冶炼金属钠、提取镁、提取溴、提取碘
注意:
生产或实验中所用原料(或试剂)、实验操作、反应方程式?
生产或实验中应注意的问题?
海水提溴:
海带提碘:
【巩固练习】
1、下列说法不正确的有
(1)可以用饱和食盐水洗气,除去氯气中混有的少量HCl气体
(2)泳池常用漂白粉或漂粉精杀菌消毒,不直接使用氯气或次氯酸。
(3)向氯水中加入适量的碳酸钙粉末、NaHCO3或Na2SO3固体,可使溶液中HClO浓度增大
(4)84消毒液(主要成分为NaClO)与洁厕灵(主要成分为HCl)混用,产生有毒Cl2:
2、小组同学制得了较高浓度的NaClO溶液。
他们把漂白液和滴有酚酞的红色Na2SO3溶液混合后,得到无色溶液。
提出猜想:
ⅰ.NaClO把Na2SO3氧化了
ⅱ.NaClO把酚酞氧化了
ⅲ.NaClO把Na2SO3和酚酞均氧化了
①下列实验方案中可以证明NaClO氧化了Na2SO3的是。
a.向混合后的溶液中加入过量盐酸
b.向混合后的溶液中加入过量盐酸,再加入氯化钡溶液
c.向混合后的溶液中加入过量硝酸,再加入硝酸银溶液
d.向混合后的溶液中加入氢氧化钡溶液,再加入过量盐酸
②为证明NaClO氧化了酚酞,可进行的实验是。
3、84消毒液不能用于消毒钢铁(含Fe、C)制品,易发生电化学腐蚀,钢铁制品表面生成红褐色沉淀。
正极反应为。
4、碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在。
几种粒子之间有如下转化关系:
①如以途径I制取I2,通入的Cl2要适量.如过量就会发生途径Ⅲ的副反应。
写出途径对应的离子方程式Ⅲ
②如以途径Ⅱ在溶液中制取I2,反应后的溶液显酸性,则反应的离子方程式是:
5.某化学兴趣小组在探究次氯酸钠溶液的性质时发现:
往过量FeSO4溶液中滴入几滴NaClO溶液,并加入适量硫酸,溶液立即变黄。
请你协助他们完成该反应还原产物的探究。
(1)甲同学推测该反应的还原产物为Cl2;
乙同学推测该反应的还原产物为。
(2)你认为甲同学的推测是否正确?
(填“正确”或“不正确”)。
请用简要的文字或离子方程式说明理由。
根据乙同学的推测,上述反应的离子方程式为。
(3)请你设计一个实验方案,验证乙同学的推测(还原产物)是否正确。
要求在答题卡上按下表格式写出实验步骤、预期现象和结论:
预期现象和结论
步骤1:
步骤2:
6、(14分)某校兴趣小组用如图Ⅰ装置制取漂白液(气密性已检验,试剂已添加),并研究其相关性质。
实验操作和现象:
打开分液漏斗的活塞,缓缓滴加一定量浓盐酸,点燃酒精灯;
一段时间后,关闭分液漏斗的活塞,熄灭酒精灯。
(1)烧瓶中反应的化学方程式是。
(2)饱和食盐水的作用是。
(3)若用图Ⅱ装置收集多余的氯气,请在虚线框内画出该装置简图。
(4)该小组同学用上述装置制得的漂白液中NaClO的浓度偏低。
查阅资料:
在溶液中发生反应:
(a)Cl2(g)+2NaOH(aq)═NaCl(aq)+NaClO(aq)+H2O(l)H1=-101.1kJ/mol
(b)3NaClO(aq)═2NaCl(aq)+NaClO3(aq)H2=-112.2kJ/mol
反应(a)的反应速率很快,反应(b)在室温下较慢
根据资料,请对图Ⅰ装置提出改进建议:
(5)修改方案后,该小组同学制得了较高浓度的NaClO溶液。
(6)氯气与氢氧化钠溶液反应,若所得溶液恰好为中性,则溶液中离子浓度关系正确的是。
A.c(Na+)+c(H+)=c(OH-)+c(Cl-)
B.c(Na+)=c(ClO-)+c(Cl-)
C.c(Na+)=2c(ClO-)+c(HClO)
(7)氢氧化铁在氢氧化钠溶液中可与氯酸钠反应生成高铁酸钠,写出反应的离子方程式
7.氯化铝极易吸水,在177.8℃时升华,某同学利用氧化铝和炭粉在加热条件下与氯气反应制取无水氯化铝,并把它收集起来。
他设计的装置如下(夹持仪器已略去,已知在制取氯化铝的反应过程中,氧化剂和还原剂的物质的量之比为1∶1):
(1)仪器A的名称是______________。
(2)设置C和E装置的目的有相似之处,它是______________________________________,
E比C还多一个用途,它是___________________________________________________
(3)D中发生反应的化学方程式是______________________________________________。
(4)该同学设计的实验遗漏两个重要的装置,从左到右它们依次是(要说清遗漏装置所处位置):
①______________________;
②__________________。
针对②的缺陷,提出改进意见
________________________________________________________________________。
(5)如果把D中的氧化铝和炭粉的混合物换成纯净的铝粉,则为了提高铝粉的利用率,装
入药品后,应该进行的操作是_______________________________________。
(6)用无水氯化铝配制氯化铝溶液时的实验操作是
★(7)另一同学欲利用上述装置和反应2CuO+2Cl2
2CuCl2+O2测定铜的相对原子质量。
①你认为他要测定的物理量有________________________,按你设计测定的物理量,
写出铜的近似相对原子质量的表达式:
____________________________________。
②如果要通过测定反应物CuO的质量m(CuO)和产物O2的体积V(O2)来测定铜的近似相对原子质量,可在装置E后添加右图示装置。
装置F是由干燥管和碱式滴定管改造而成的测量气体体积的装置,实验前滴定管液面初读数为V1L,实验后恢复到室温,调节装置两侧液面相平后得到末读数为V2L,则铜的近似相对原子质量的表达式为(设室温时气体摩尔体积为VmL·
mol-1)[用含m(CuO)、V1、V2的代数式表示:
F
若氧化铜中混有铜,则测定结果_____(填“偏大”“偏小”或“无影响”)。
8.(2016-新课标I卷-28)NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
回答下列问题:
(1)NaClO2中
的化合价为__________。
(2)写出“反应”步骤中生成ClO2的化学方程式。
(3)“电解”所用食盐水由粗盐水精制而成,精制时,为除去Mg2+和Ca2+,要加入的试剂分别为__________、__________。
“电解”中阴极反应的主要产物是。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应中,氧化剂与还原剂的物质的量之比为__________,该反应中氧化产物是。
(5)“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:
每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力。
NaClO2的有效氯含量为。
(计算结果保留两位小数)。
8(2015朝阳1).(14分)
、漂白液(有效成分为
)在生产、生活中广泛用于杀菌、消毒。
(1)电解
溶液生成
的化学方程式是。
(2)
即获得氯水、漂白液。
①干燥的氯气不能漂白物质,但氯水却有漂白作用,说明起漂白作用的物质是。
②
的反应如下:
反应Ⅰ
K1=4.5×
10-4
反应Ⅱ
K2=7.5×
1015
解释不直接使用氯水而使用漂白液做消毒剂的原因。
(3)家庭使用漂白液时,不宜直接接触铁制品,漂白液腐蚀铁的电极反应为:
发生的电极反应式为。
(4)研究漂白液的稳定性对其生产和保存有实际意义。
30℃时,pH=11的漂白液中
的质量百分含量随时间变化如下:
①比较分解速率v(Ⅰ)、v(Ⅱ)的大小关系,原因是_______。
②
分解的化学方程式是。
③4d~8d,Ⅰ中v(NaClO)=mol/(L·
d)(常温下漂白液的密度约为1g/cm3,且变化忽略不计)。
9(2016石景山1)28.(15分)某兴趣小组利用文献资料设计方案对氯及其化合物进行探究。
Ⅰ.用高锰酸钾和浓盐酸反应制取氯气
(1)该小组利用右图装置及试剂制备并收集适
量Cl2,装置B、C的作用分别是
___________、_______________。
(2)制得的氯气中加入适量水,得到饱和氯水,
饱和氯水中含氯元素的微粒有_____________
(写出全部微粒)。
(3)饱和氯水与石灰石的反应是制取较浓HC1O溶液的方法之一。
在过量的石灰石中加入饱和氯水充分反应,有少量气泡产生,溶液浅黄绿色褪去,过滤,得到的滤液其漂白性比饱和氯水更强。
①滤液漂白性增强的原因是_________________________________________(用化学平衡移动原理解释)。
②饱和氯水与石灰石反应生成HC1O的方程式是_______________________________。
Ⅱ.ClO3—、Cl—和H+反应的探究
(4)KClO3、KCl与硫酸可以反应。
该小组设计了系列实验研究反应条件对反应的影响,实验记录如下(实验在室温下进行):
烧杯编号
1
2
3
4
氯酸钾饱和溶液
1mL
氯化钾固体
1g
水
8mL
6mL
3mL
0mL
硫酸(6mol/L)
2mL
(____)mL
现象
无现象
溶液呈浅黄色
溶液呈黄绿色,生成浅黄绿色气体
溶液呈黄绿色,
生成黄绿色气体
①该系列实验的目的_________________________。
②烧杯3取用硫酸的体积应为______________mL。
(5)该小组同学查资料得知:
将氯酸钾固体和浓盐酸混合也能生成氯气,同时有大量ClO2生成;
ClO2沸点为10℃,熔点为-59℃,液体为红色;
Cl2沸点为-34℃,液态为黄绿色。
设计最简单的实验验证Cl2中含有ClO2____________________________________。
10、某小组设计不同实验方案比较Cu2+、Ag+的氧化性。
(1)方案1:
通过置换反应比较
向酸化的AgNO3溶液插入铜丝,析出黑色固体,溶液变蓝。
反应的离子方程式是,说明氧化性Ag+>Cu2+。
(2)方案2:
通过Cu2+、Ag+分别与同一物质反应进行比较
实验
试剂
编号及现象
试管
滴管
1.0mol·
L-1
KI溶液
L-1
AgNO3溶液
Ⅰ.产生黄色沉淀,溶液无色
CuSO4溶液
Ⅱ.产生白色沉淀A,溶液变黄
①经检验,Ⅰ中溶液不含I2,黄色沉淀是。
②经检验,Ⅱ中溶液含I2。
推测Cu2+做氧化剂,白色沉淀A是CuI。
确认A的实验如下:
a.检验滤液无I2。
溶液呈蓝色说明溶液含有(填离子符号)。
b.白色沉淀B是。
c.白色沉淀A与AgNO3溶液反应的离子方程式是,说明氧化性Ag+>Cu2+。
(3)分析方案2中Ag+未能氧化I-,但Cu2+氧化了I-的原因,设计实验如下:
编号
实验1
实验2
实验3
a中溶液较快变棕黄色,b中电上析出银;
电流计指针偏转
c中溶液较慢变浅黄色;
电流计指针偏转
(电极均为石墨,溶液浓度均为1mol/L,b、d中溶液pH≈4)
①a中溶液呈棕黄色的原因是(用电极反应式表示)。
②“实验3”不能说明Cu2+氧化了I-。
依据是空气中的氧气也有氧化作用,设计实验证实了该依据,实验方案及现象是。
③方案2中,Cu2+能氧化I-,而Ag+未能氧化I-的原因:
(资料:
Ag++I-=AgI↓K1=1.2×
1016;
2Ag++2I-=2Ag↓+I2K2=8.7×
108)
答案:
(1)
(2)①AgI②a.
b.AgClc.
(3)①
②将d烧杯内的溶液换为pH≈4的1mol/L
溶液,c中溶液较慢变浅黄,电流计指针偏转
(4)K1>K2,故
更易与
发生复分解反应,生成AgI。
2Cu2++4I-=2CuI+I2,生成了CuI沉淀,使得
的氧化性增强。
11、某小组以4H++4I–+O2=2I2+2H2O为研究对象,探究影响氧化还原反应的因素。
气体a
HCl
Ⅰ.溶液迅速呈黄色
SO2
Ⅱ.溶液较快呈亮黄色
CO2
Ⅲ.长时间后,溶液呈很浅的黄色
空气
Ⅳ.长时间后,溶液无明显变化
(1)实验Ⅳ的作用是。
用CCl4萃取Ⅰ、Ⅱ、Ⅲ、Ⅳ的溶液,萃取后下层CCl4的颜色均无明显变化。
(2)取萃取后上层溶液,用淀粉检验:
Ⅰ、Ⅲ的溶液变蓝;
Ⅱ、Ⅳ的溶液未变蓝。
溶液
变蓝说明Ⅰ、Ⅲ中生成了。
(3)查阅资料:
I2易溶于KI溶液。
下列实验证实了该结论并解释Ⅰ、Ⅲ的萃取现象。
现象x是。
(4)针对Ⅱ中溶液未检出I2的原因,提出三种假设:
假设1:
溶液中c(H+)较小。
小组同学认为此假设不成立,依据是_____
、
假设2:
O2只氧化了SO2,化学方程式是_____
假设3:
I2不能在此溶液中存在。
(5)设计下列实验,验证了假设3,并继续探究影响氧化还原反应的因素。
ⅰ.取Ⅱ中亮黄色溶液,滴入品红,红色褪去。
ⅱ.取Ⅱ中亮黄色溶液,加热,黄色褪去,经品红检验无SO2。
加入酸化的AgNO3
溶液,产生大量AgI沉淀,长时间静置,沉淀无明显变化。
加热检验无SO2可能的原因是:
ⅲ.取Ⅱ中亮黄色溶液,控制一定电压和时间进行电解,结果如下。
电解时间/min
阳极
阴极
t1
黄色变浅、有少量SO42-
检出I2,振荡后消失
H2
t2(t2>
t1)
溶液无色、有大量SO42-
结合化学反应,解释上表中的现象:
(6)综合实验证据说明影响I–被氧化的因素及对应关系________。
(1)对照组,证明只有
时很难氧化
(2)
(3)上层黄色,下层无色
(4)假设1:
在水中的溶解度比
大,且
的酸性强于
,因此溶液
酸性更强
(5)加热加快了SO2和I2的反应
阳极发生
,生成的
与溶液中的
发生反应:
,以上过程循环进行,
减少,
增多。
(6)通过Ⅰ、Ⅲ、Ⅳ,说明c(H+)越大,I-越易被氧化;
在酸性条件下,KI比AgI易氧化,说明
越大越易被氧化;
与反应条件有关,相同条件下,电解时检出I2,未电解时未检出I2。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 北京顺义 高三化学一轮复习 氯元素及其化合物学案答案不全 北京 顺义 化学 一轮 复习 元素 及其 化合物 答案 不全
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《城市规划基本知识》深刻复习要点.docx
《城市规划基本知识》深刻复习要点.docx
