 届北京市海淀区北大附中高三化学阶段性测试化学试题Word格式文档下载.docx
届北京市海淀区北大附中高三化学阶段性测试化学试题Word格式文档下载.docx
- 文档编号:22612422
- 上传时间:2023-02-04
- 格式:DOCX
- 页数:15
- 大小:272.84KB
届北京市海淀区北大附中高三化学阶段性测试化学试题Word格式文档下载.docx
《届北京市海淀区北大附中高三化学阶段性测试化学试题Word格式文档下载.docx》由会员分享,可在线阅读,更多相关《届北京市海淀区北大附中高三化学阶段性测试化学试题Word格式文档下载.docx(15页珍藏版)》请在冰豆网上搜索。
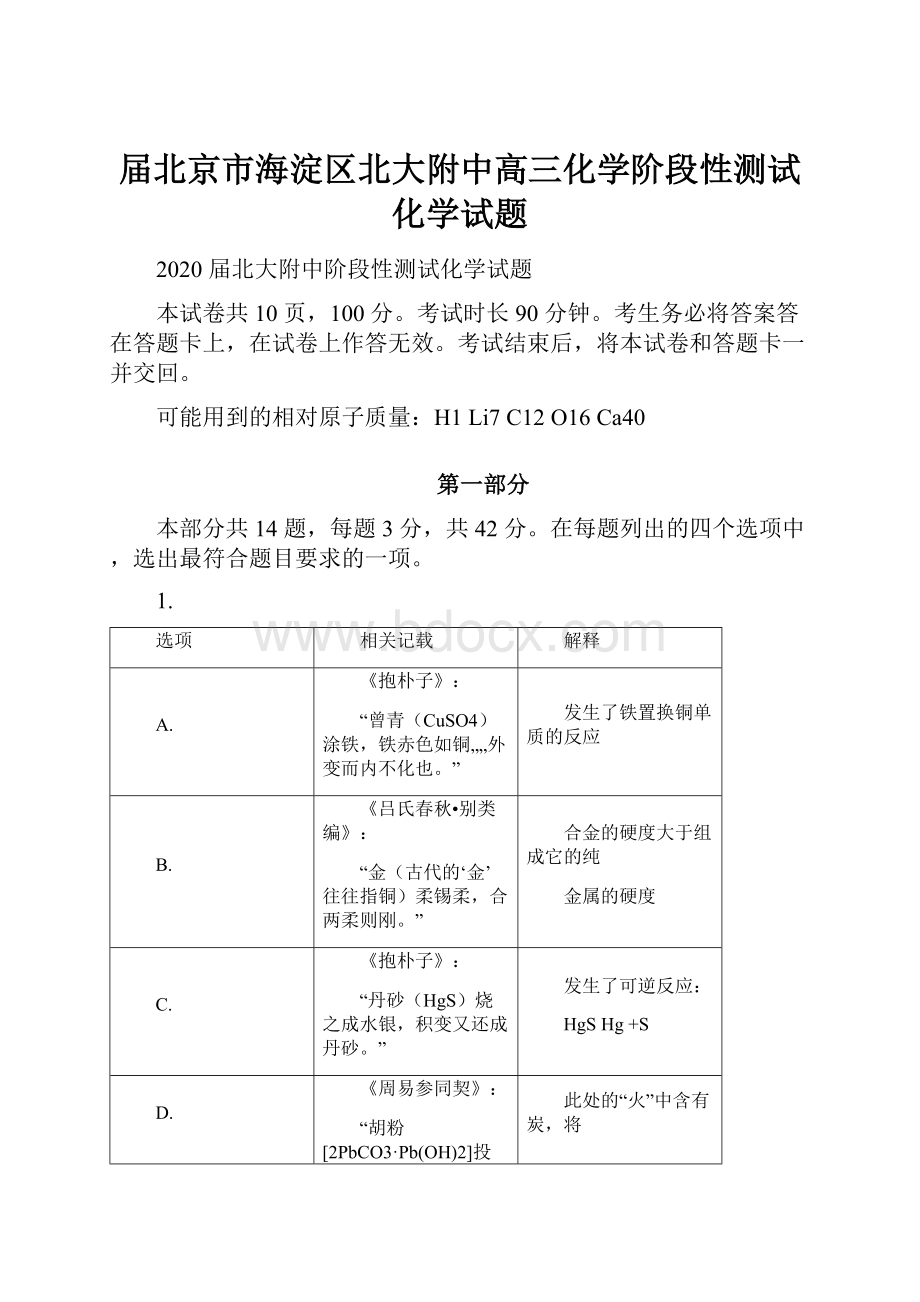
D.
《周易参同契》:
“胡粉[2PbCO3·
Pb(OH)2]投火中,色坏还为铅(Pb)。
此处的“火”中含有炭,将
胡粉发生分解反应生成的铅的氧化物还原为单质铅。
中国古代炼丹术中蕴含了丰富的化学知识,相关记载不绝于书。
下列对炼丹术中相关记载的原理解释不.正.确.的是
2.下列化学用语不.正.确.的是
A.氯化铵的电子式:
B.乙醛的比例模型:
8
C.中子数为8的氧原子是16OC.氯离子的结构示意图是
3.下列说法不.正.确.的是
A.葡萄糖作为人类重要能量来源,是由于它在人体的酶催化下发生氧化反应,放出能量
B.油脂在一定条件下能发生水解,是由于它属于天然有机高分子
C.生石灰、草木灰等可用于腌制松花蛋,是由于碱性物质能使鸡蛋中蛋白质变性
D.植物油能使酸性高锰酸钾溶液褪色,是由于植物油是含较多不饱和脂肪酸成分的甘油酯
4.下列各项比较中,一定相等的是
A.相同质量的Fe完全转化为FeCl2和FeCl3时转移的电子数
B.相同质量的苯和乙炔所含的碳原子的数目
C.标准状况下的2.24LHCl气体和1L0.1mol·
L−1盐酸中所含Cl−的数目
D.
+
相同物质的量浓度的NH4Cl和(NH4)2FeSO4溶液中NH4的浓度
5.
相对能量
一氧化碳甲烷化反应为:
CO(g)+3H2(g)===CH4(g)+H2O(g)。
下图是使用某种催化剂时转化过程中的能量变化(部分物质省略)。
下列说法不.正.确.的是
A.步骤①只有非极性键断裂
B.步骤②的原子利用率为100%
C.过渡态Ⅱ能量最高,因此其对应的步骤③反应速率最慢
D.该方法可以清除剧毒气体CO,从而保护环境
6.下列解释事实的方程式不.正.确.的是
A.84消毒液(有效成分为NaClO)中加入少量白醋可增强消毒效果:
ClO−+CH3COOH===HClO+CH3COO−
B.用Na2CO3将水垢中的CaSO4转化为易于除去的CaCO3:
CaSO4+CO32−===CaCO3+SO42−
C.稀硫酸酸化的淀粉−KI溶液在空气中放置一段时间后变蓝:
2I−+SO42−+4H+===I2+SO2+2H2O
D.用Na2S2O3做碘量法实验时,溶液pH不可太低:
S2O32−+2H+===SO2+S↓+H2O
7.
实验目的
实验方法
A
证明甲苯中的甲基活化了苯环
分别取甲苯和苯与酸性高锰酸钾反应,观察使酸性高锰酸钾溶液褪色的情况
B
除去CuSO4溶液中的少量Fe2+、Fe3+
先加入少量H2O2,再加入CuO调节溶液pH≈4,过滤
C
证明Ag+能将Fe2+氧化为Fe3+
取少量Fe(NO3)2溶液,加入几滴KSCN;
再加入几滴
AgNO3溶液(pH=5),观察加入AgNO3溶液前后的颜色变化
D
检验CH3CH2Br消去反应的产物乙烯
将产物气体直接通入酸性KMnO4溶液
下列实验能达到目的的是
8.四种短周期元素X、Y、Z和W在周期表中的位置如图所示,原子序数之和为48。
A.原子半径(r)大小比较r(X)>r(Y)
B.Z的最低价单核阴离子的还原性比Y的强
C.X和W可形成共价化合物XW3
D.含氧酸的酸性强弱关系一定是:
W>Z
9.某小组同学自酿米酒,具体步骤如下:
10.
定时监测获得的实验数据图如下:
A.糯米中淀粉在酒曲中糖化酶作用下水解为葡萄糖,葡萄糖在酒化酶作用下转化为乙醇
B.酿造过程中米酒pH逐渐下降,可能是因为部分乙醇被空气氧化为乙酸
C.从第7天开始米酒的酒精度近乎不变,说明溶液中的葡萄糖已经完全反应
D.该小组最终酿出的米酒酒精度不高,可采用蒸馏法提高酒精度
11.由N−乙烯基吡咯烷酮(NVP)和甲基丙烯酸β−羟乙基(HEMA)合成水凝胶材料高聚物
A具有较高的含水量,其路线如下图所示:
A.HEMA的水解产物均可用作聚合反应的单体
B.高聚物A因含有多个—OH而具有良好的亲水性
C.HEMA和NVP通过缩聚反应生成高聚物A
D.若将高聚物A与足量HOOC(CH2)4COOH反应,可能通过形成新的酯基,进而交联形成网状结构
12.
一种锂离子电池的反应式为LixC6+Li1−xCoO2
6C+LiCoO2(x<1)。
其工作原理如图所示。
A.放电时,A极电极式为:
LixC6−xe−===6C+xLi+
B.放电时,若转移0.3mol电子,石墨电极将减重2.1g
C.充电时,Li+从左向右移动
D.若要从废旧该型锂电池的正极材料中回收锂元素,先进行放电处理,有利于Li+尽可能从负极脱出,在正极富集
13.用0.1000mol·
L−1NaOH溶液分别滴定20.00mL0.1000mol·
L−1的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是
A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.V(NaOH)=10.00mL时,醋酸溶液中
c(CH3COOH)<c(CH3COO−)
C.pH=7时,滴定盐酸消耗的NaOH溶液体积小于滴定醋酸消耗的NaOH溶液体积
D.V(NaOH)=20.00mL时,两溶液中c(CH3COO−)=c(Cl−)
14.反应2SiHCl3(g)SiH2Cl2(g)+SiCl4(g)在催化剂作用下,于323K和343K时充分反应,
SiHCl3的转化率随时间变化的结果如图所示:
A.343K时反应物的平衡转化率为22%
B.a、b处反应速率大小:
va>vb
C.要提高SiHCl3转化率,可采取的措施是降温和及时移去反应产物
为物质的量分数,则343K时
15.水浴加热滴加酚酞的NaHCO3溶液,颜色及pH随温度变化如下(忽略水的挥发):
时间
①
②
③
④
⑤
温度/℃
20
30
40
从40℃冷却到20℃
沸水浴后冷却到20℃
颜色变化
红色略加深
红色接近①
红色比③加深较多
pH
8.31
8.29
8.26
9.20
A.NaHCO3溶液显碱性的原因:
HCO3−+H2OH2CO3+OH−
B.①→③的过程中,颜色加深的原因可能是HCO3−水解程度增大
C.①→③的过程中,pH略微下降说明升温过程中c(OH−)减小
D.⑤比①pH增大,推测是由于NaHCO3分解生成的Na2CO3的缘故
第二部分(本部分共5题,共58分)
16.(10分)《我在故宫修文物》这部纪录片里关于古代青铜器的修复引起了某个研学小组的兴趣。
“修旧如旧”是文物保护的主旨。
(1)查阅高中教材得知铜锈的主要成分为Cu2(OH)2CO3,俗称铜绿,可溶于酸。
铜绿在一定程度上可以提升青铜器的艺术价值。
参与形成铜绿的物质有Cu和。
(2)继续查阅资料,了解到铜锈的成分非常复杂,主要成分有Cu2(OH)2CO3和Cu2(OH)3Cl。
考古学家将铜锈分为无害锈和有害锈,结构如下图所示:
Cu2(OH)2CO3和Cu2(OH)3Cl分别属于无害锈和有害锈,请解释原因
。
(3)文献显示有害锈的形成过程会产生CuCl(白色不溶于水的固体),请结合下图回答:
①过程Ⅰ的正极反应物是。
②过程Ⅰ负极的电极反应式是。
(4)青铜器的修复有以下三种方法
ⅰ.柠檬酸浸法:
将腐蚀文物直接放在2%~3%的柠檬酸溶液中浸泡除锈;
ⅱ.碳酸钠法:
将腐蚀文物置于含Na2CO3的缓冲溶液中浸泡,使CuCl转化为难溶的Cu2(OH)2CO3;
ⅲ.BTA保护法请回答下列问题:
①写出碳酸钠法的离子方程式。
②三种方法中,BTA保护法应用最为普遍,分析其可能的原因有。
A.在青铜器表面形成一层致密的透明保护膜
B.替换出锈层的Cl−,能够高效的除去有害锈
C.和酸浸法相比,不破坏无害锈,可以保护青铜器的艺术价值,做到“修旧如旧”
17.(13分)天然石灰石是工业生产中重要的原材料之一,它的主要成分是CaCO3,一般以
CaO的质量分数表示钙含量,常采用高锰酸钾法测定。
步骤如下:
Ⅰ.称取ag研细的石灰石样品于250mL烧杯中,加过量稀盐酸溶解,水浴加热10分钟;
Ⅱ.稍冷后逐滴加入氨水至溶液pH≈4,再缓慢加入适量(NH4)2C2O4溶液,继续水浴加热
30分钟;
Ⅲ.冷却至室温后过滤出沉淀,用另外配制的稀(NH4)2C2O4溶液洗涤沉淀三次,再用蒸馏水洗涤至洗涤液中无法检出Cl−;
Ⅳ.加入适量热的稀硫酸至沉淀中,获得的溶液用cmol·
L−1KMnO4标准溶液滴定至终点。
Ⅴ.平行测定三次,消耗KMnO4溶液的体积平均为VmL。
已知:
H2C2O4是弱酸;
CaC2O4是难溶于水的白色沉淀。
(1)Ⅰ中为了加快反应速率而采取的操作有。
(2)Ⅱ中加入氨水调节溶液pH的作用是。
(3)Ⅲ中洗涤得到干净的沉淀。
①结合平衡移动原理,解释用稀(NH4)2C2O4溶液洗涤沉淀的目的
②检测洗涤液中无Cl−的试剂和现象是。
③若沉淀中的Cl−未洗涤干净,则最终测量结果(填“偏大”、“偏小”或
“不变”)。
(4)Ⅳ中用KMnO4标准溶液滴定。
①滴定时发生反应的离子方程式为。
②滴定至终点的现象为。
③样品中以CaO质量分数表示的钙含量为(列出表达式)。
18.(12分)CO2的资源化利用能有效减少CO2排放,充分利用碳资源。
(1)在海洋碳循环中,通过右图所示的途径固碳。
①写出钙化作用的离子方程式。
②同位素示踪法证实光合作用释放出的O2只来自于H2O。
用18O标记物质的光合作用的化学方程式如下,将其补充完整:
CaCO3(CH2O)x
(2)电解法转化CO2可实现CO2资源化利用。
电解CO2制HCOOK的原理示意图如下。
①阴极的电极反应式为。
②电解一段时间后,阳极区KHCO3浓度下降,原因是。
(3)CO2催化加氢合成二甲醚是一种CO2转化方法,其过程中主要发生下列反应:
反应Ⅰ:
CO2(g)+H2(g)===CO(g)+H2O(g)ΔH=+41.2kJ·
mol−1
反应Ⅱ:
2CO2(g)+6H2(g)===CH3OCH3(g)+3H2O(g)ΔH=−122.5kJ·
在恒压、CO2和H2的起始量一定的条件下,CO2平衡转化率和平衡时CH3OCH3的选择性随温度的变化如图。
CH3OCH3的选择性=
2⨯CH3OCH3的物质的量
反应的CO2的物质的量×
100%
①温度高于300℃时,CO2平衡转化率随温度升高而上升的原因是。
②220℃时,在催化剂作用下CO2与H2反应一段时间后,测得CH3OCH3的选择性为
48%(图中A点)。
反应时间和温度不变,提高CH3OCH3选择性的措施有。
A.增大压强B.使用对反应Ⅱ催化活性更高的催化剂C.及时移走产物
19.(12分)化合物M是桥环化合物二环[2.2.2]辛烷的衍生物,其合成路线如下:
20.
ⅰ.
ⅱ.
(ⅰ、ⅱ中R1、R2、R4均代表烃基,R3代表烃基或氢原子)
(1)A可与NaHCO3溶液反应,其名称为。
B中所含官能团的结构简式为。
(2)B→C的化学方程式为。
(3)试剂a的分子式为C5H8O2,能使Br2的CCl4溶液褪色,则C→D的反应类型为。
(4)F→G的化学反应方程式为。
(5)已知E→F和J→K都发生了相同的反应,则带六元环结构的K的结构简式为。
(6)HOCH2CH2OH的作用是保护G中的酮羰基,若不加以保护,则G直接在C2H5ONa作用下可能得到I之外的副产物,请写出一个带六元环结构的副产物的结构简式。
(7)
已知。
由K在NaOH作用下反应得
到化合物M,该物质具有如下图所示的二环[2.2.2]辛烷的立体结构,请在图中补充必要的官能团得到完整的M的结构简式。
21.(11分)某小组探究Na2SO3溶液和KIO3溶液的反应。
实验Ⅰ:
向某浓度的KIO3酸性溶液(过量)中加入Na2SO3溶液(含淀粉),一段时间(t
秒)后,溶液突然变蓝。
−−−−+
资料:
IO3在酸性溶液中氧化I,反应为IO3+5I+6H===3I2+3H2O
(1)溶液变蓝,说明Na2SO3具有性。
(2)针对t秒前溶液未变蓝,小组做出如下假设:
ⅰ.t秒前未生成I2,是由于反应的活化能(填“大”或“小”),反应速率慢导致的。
ⅱ.t秒前生成了I2,但由于存在Na2SO3,(用离子方程式表示),
I2被消耗。
(3)下述实验证实了假设ⅱ合理。
实验Ⅱ:
向实验Ⅰ的蓝色溶液中加入,蓝色迅速消失,后再次变蓝。
(4)
表盘
时间/min
0~t1
t2~t3
t4
偏转位置
右偏至Y
指针回到“0”处,又返至“X”处;
如此周期性往复多次……
指针归零
进一步研究Na2SO3溶液和KIO3溶液反应的过程,装置如下。
实验Ⅲ:
K闭合后,电流表的指针偏转情况记录如下表:
①K闭合后,取b极区溶液加入盐酸酸化的BaCl2溶液,现象是。
②0~t1时,从a极区取溶液于试管中,滴加淀粉溶液,溶液变蓝;
直接向a极区滴加淀粉溶液,溶液未变蓝。
判断IO3−在a极放电的产物是。
③结合反应解释t2~t3时指针回到“0”处的原因。
(5)综合实验Ⅰ、Ⅱ、Ⅲ,下列说法正确的是。
A.对比实验Ⅰ、Ⅱ,t秒后溶液变蓝,Ⅰ中SO32−被完全氧化
B.对比实验Ⅰ、Ⅲ,t秒前IO3−未发生反应
实验Ⅲ中指针返回X处的原因,可能是I2氧化SO32−
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 北京市 海淀区 北大附中 化学 阶段性 测试 化学试题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《城市规划基本知识》深刻复习要点.docx
《城市规划基本知识》深刻复习要点.docx
