 质量管理SOP大全Word文档格式.docx
质量管理SOP大全Word文档格式.docx
- 文档编号:22525572
- 上传时间:2023-02-04
- 格式:DOCX
- 页数:90
- 大小:101.81KB
质量管理SOP大全Word文档格式.docx
《质量管理SOP大全Word文档格式.docx》由会员分享,可在线阅读,更多相关《质量管理SOP大全Word文档格式.docx(90页珍藏版)》请在冰豆网上搜索。
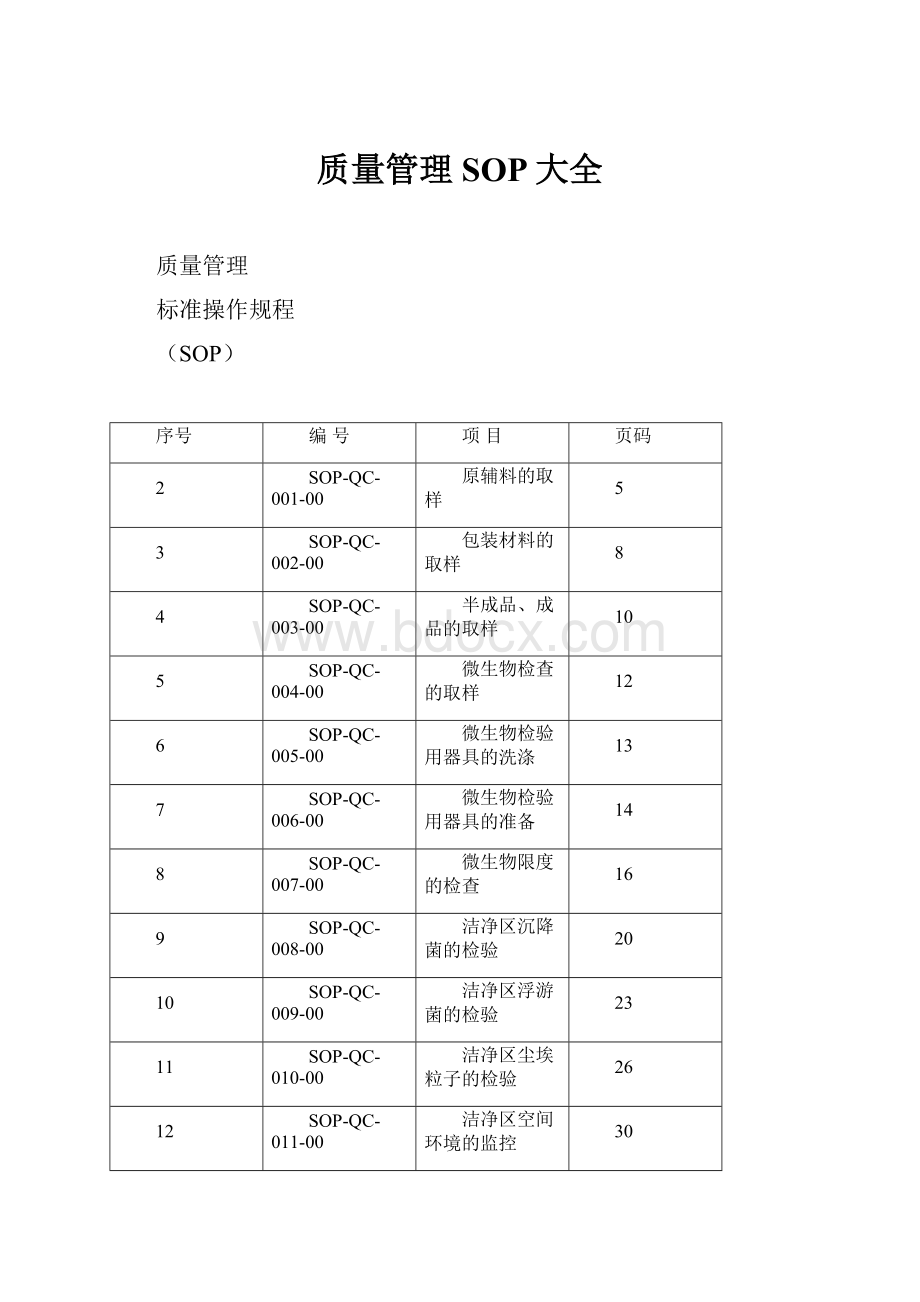
SOP-QC-011-00
洁净区空间环境的监控
30
SOP-QC-012-00
工艺用水的理化监测
31
SOP-QC-013-00
说明书的检验
38
15
SOP-QC-014-00
药用铝箔的检验
40
SOP-QC-015-00
药用聚氯乙烯的检验
42
17
药用塑料袋的检验
45
18
SOP-QC-016-00
设备清洁的微生物检查
46
19
SOP-QC-017-00
小包装盒的检验
48
SOP-QC-018-00
中包装盒的检验
51
21
SOP-QC-019-00
大包装盒的检验
53
22
SOP-QC-020-00
医用净化工作台的使用
55
SOP-QC-022-00
LB-2B型崩解时限测定仪的使用
57
24
SOP-QC-023-00
片剂硬度仪的使用
59
25
SOP-QC-024-00
隔水式电热培养箱的使用
61
SOP-QC-025-00
酸度计的操作
63
27
SOP-QC-026-00
玻璃仪器的校正
65
28
SOP-QC-027-00
微生物检验用培养基的准备
67
29
SOP-QC-028-00
UV-754型紫外可见分光光度计的使用
69
SOP-QC-029-00
电热鼓风干燥箱(101A型)操作规程
72
SOP-QC-030-00
电子天平的使用
74
32
SMP-QC-031-00
仓库取样车的使用
33
SMP-QC-032-00
工艺用水的质量标准
34
SMP-QC-033-00
工艺用水的检测时间的确定
35
SMP-QC-034-00
实验室安全技术操作规程
36
SMP-QC-035-00
洁净室(区)的空间消毒与维护
37
SMP-QC-036-00
Waters515高效液相色谱仪
操作规程
SMP-QC-037-00
2487紫外检测器及高效液相
色谱仪数据处理系统操作规程
39
SMP-QC-038-00
.机动门真空灭菌器的使用.
SMP-QC-039-00
机动门真空灭菌器的清洁.
。
文件编号
颁发部门
总页数
执行日期
编制者
审核者
批准者
编制日期
审核日期
批准日期
1.目的:
明确原辅料取样的标准操作规程。
2.范围:
原辅料的取样。
3.责任:
QA检查员、仓库管理员。
4.内容:
4.1取样程序:
4.1.1QA检查员在接到仓库管理员的检验通知报告单后的两个工作日内,到仓库待验区,在仓库管理员的协助下进行取样操作。
4.1.2取样前,QA检查员先根据检验通知报告单内容核对待验品的品名、批号、容器数,来源及原辅料供应商所提供的出厂检验报告单是否符合、一致。
4.1.3QA检查员应先对待验的外包装进行检查是否无污染、水渍、虫蛀、霉变、混杂等情况,如不符合要求,应拒绝抽样,待原因调查清楚,经主管负责人批准后才可抽样。
4.1.4取样应用取样器具
固体:
不锈钢探子、不锈钢勺、不锈钢铲、不锈钢镊子
液体:
玻璃采样管、玻璃油提
样品应置于标准容器中
具有封口装置的无毒塑料袋
具盖玻璃瓶,无毒塑料袋
需取无菌样品时,以上相应器具均应无菌
4.1.5由仓库管理员打开物料内外包装(注意:
应穿清洁服、戴口罩、手套),由QA检查员检查外观(色泽、嗅味等)。
4.1.6取完一种物料的样品后,应先由仓库管理员将包装封好,再取下一种物料。
取不同种物料时,应更换一次性手套及取样工具以避免污染物料。
4.1.7确认所取样品的均一性,取样应具有代表性,并符合各有关测试标准的要求,所取样品应放在带盖瓶(或有色瓶或塑料袋)中。
4.1.8取样时QA检查员与仓库管理员均必须换清洁服,并戴一次性口罩、手套。
避免交叉污染。
而且必要时应更换,以避免发生混药。
4.1.9取样工具必须洁净,使用前,用75%的酒精棉消毒;
使用后,用清水反复冲洗数次,再用去离子水冲洗二遍,自然晾干后,保存在干燥、洁净、无污染的柜中,或包于无纤维脱落、无毒的塑料袋中。
4.1.10取样后:
在容器外标签上注明取样量、取样日期及取样人签字。
4.1.11取样时,如发现不同容器中所取样品外观有异常,或者某个包装有损坏,则应单独取样,以证实是否一致,并在标签的备注栏内清楚注明。
4.1.12取样后,取样员在货物标签上签名,并在样品瓶上贴以标签。
然后将样品和检验通知报告单以及供应商的出厂报告,送交QC主管。
4.1.13取样后物控部门仓库管理员恢复所取样品的原包装并在取样证标签上签字表明已取样,由仓库管理员将已取过样的物料运回待验区。
4.2取样量规定:
4.2.1固体物料:
除测试标准中另有规定外,从一个批号容器中随机抽取一定量的样品(至少为检量的3倍)。
4.2.2液体物料:
除测试标准中另有规定外,用适当干燥工具从一个批号容器中随机抽取一定容量的样品(至少为检量的3倍)。
4.2.3具有粘性和不均匀的物料:
按照测试标准规定,将容器充分振摇后,从一个批号容器中随机抽取一定量的样品(至少为检量的3倍)。
4.2.4当批件数n≤3时,每件全取。
4≤n≤300时,取
+1件,
n≥300时,取样件数为√n/2+1
5.培训:
5.1培训对象:
5.2培训时间:
二小时。
明确包装材料取样的标准操作规程。
包装材料的取样。
QA主管、QA检查员、仓库保管员对此程序负责。
4.1.1QA检查员接到仓库保管员的包装材料检验通知报告单后两个工作日内,到仓库待验区取样。
4.1.2取样前,QA检查员应先核对品名、来源及包装材料供应商所提供的出厂检验报告单是否符合我厂质量标准,并检查包装外观,核对包装有无破损、混杂、污染。
4.1.3取样时,由仓库管理员首先对容器外包装做简单清洁,再打开容器外包装,由QA检查员取样,取样应戴洁净的手套。
4.1.4取样后应在容器外黄色待验标签上注名取样量、取样日期及取样人签字。
仓库管理员将外包装复原,并放回原处。
4.2取样原则及取样量:
取样应具有代表性,随机抽样,以包装为单位。
4.2.1铝箔、PVC:
按其检测标准操作程序,以一个批号包装总数的N1/2个包装中随机抽取一定量的样品。
4.2.2说明书:
≤5万张时,应逐包检查
4.2.3小盒、中盒:
>
5万张时,应按总件数的n1/2中随机抽样。
4.2.4大箱:
按总件数的n1/2个包装中随机抽取。
4.2.5当检品数≥300时,取样件数n为:
√n/2+1
4.2.6取样结束后,由仓库保管员封口,取样员贴好取样标签,库管填写取样记录。
QA主管、QA检查员、仓库保管员;
一小时。
明确半成品、成品取样的标准操作规程。
各品种的半成品、成品的取样。
QA主管,QA检查员对本程序的实施负责。
4.1半成品的取样:
4.1.1待验品应尽可能按B、M、E(开始、中间、结束)原则存放。
4.1.2QA检查员接到制造部请验单后,到中间站取样。
取样人员应穿洁净工作服,戴口罩手套。
取样时应严格按照取样规程进行,避免对药品的污染。
4.1.3样品容器及取样工具由QC检测员准备.
4.1.4取样前应先核对样品与请验单内容是否相符,容器外观是否清洁,是否有混药现象。
4.1.5取样应按B、M、E原则抽取,使样品具有代表性。
取样时,若发现外观异常,应单独取样,在取样记录上如实记录,并向QA主管报告。
4.1.6取样后,将样品及请验单送QC主管。
4.2成品的取样:
4.2.1成品包装进行到一半以上时,生产部开具请验单给A检查员,已包装完成品应先放入仓库待验区。
QA检查员接到生产部请验单后,在仓库管理员协助下取样。
4.2.2取样时,由仓库管理员打开封条,QA检查员按取样规程取样。
4.2.3取样后,由仓库管理员与QA检查员共同用零头箱内药品补足取样量。
并实行二人核对,保证每批产品只能有一个零头箱存在。
4.2.4取样后,二个共同在取样记录上签字,并由仓库管理员重新封箱,贴上仓库封签。
4.2.5取样记录夹入批文件。
QA主管,QA检查员。
1
明确无菌取样的标准操作规程。
需做微生物检查的检品。
QA检查员对本程序的实施负责,QA主管负责监督。
4.1抽样时,凡发现异常可疑样品,应抽取有疑问的样品,但因机械损伤明显破裂的包装不得做为样品。
4.2凡从外观看出长螨、发霉、虫蛀及变质的药品,可直接判为不合格,无需再抽样检验。
4.3供试样品在检验之前,应保持原包装状态,严禁开启。
包装已开启的样品不得做为供试品。
4.4供试品稀释成供试液后,应在均匀下取样。
凡含抑菌成份或防腐剂等的供试品应做特殊处理后进行检验。
4.5抽样量应为检验用量(2个以上最小包装单位)的3倍量。
所有剂型的检验均需取自2个以上包装单位。
4.6采取随机方法取样。
4.7取样器具应按微生物检验用器皿的准备标准操作程序进行准备好。
二小时
微生物检验用器具的洗涤
SOP-QC-O05-OO
1.目的:
明确微生物检验用器具洗涤的标准操作规程
2.范围:
微生物检验用各种玻璃、不锈钢器具
3.责任:
QC检查员负责实施、QC主管监督执行
4.内容:
4.1培养后的培养皿、三角瓶、试管、置121℃20分钟高压蒸汽灭菌后,将内容物用多量水清洗并晾干
4.2衣物被污染后应立即高压蒸汽灭菌后再清洗
4.3带菌的实验用品应浸泡在5%的甲酚溶液内,24小时后取出冲洗
4.4凡带有活菌的物品必须消毒后才能在水龙头下冲洗,严禁污染下水道
4.5不锈钢筒、研钵、三角瓶、试管、吸管等作完实验后,尽量用刷子,把器具内的残渣去除,用洗涤剂洗涤,然后用水冲洗干净后晾干。
微生物检验用器皿的准备
明确微生物检验用器皿准备的标准操作规程
微生物检验用各种器材、稀释剂
检测负责实施、主管监督执行
5.1灭菌器材的准备工作
4.1.1灭菌器材的包装:
平皿分10个作一个包装包好,各种试管用合适的塞子按需要包好;
吸管上塞进少许棉花,;
松紧适度以防污染,然后按其容量大小分别包好;
三角瓶量筒用合适的塞子塞好,分别包好;
不锈钢筒、药匙、剪子、镊子、无菌衣、口罩称量等分别包好
4.1.2稀释剂的配制:
生理盐水,取氯化钠9克加蒸馏水1000ml溶解,分装后包扎好。
4.2灭菌
4.2.1将包装好的待灭菌器材、稀释剂置121℃高压灭菌20分钟
4.2.2高压灭菌应严格按操作规程进行,必须逐渐加热,彻底排除灭菌器内的冷空气,使灭菌物品同灭菌器的温度一致,逐渐升压保持预定的压力和时间后令其自然降压
4.3玻璃器皿应按玻璃器皿洗涤干燥规程准备好
4.4灭菌器材的保存
4.4.1环境条件:
灭菌后的各种器材应置于烘箱内保持干燥,不得潮湿。
生理盐水应置于洁净水箱内保存5℃为宜不得冻结
4.4.2保存时间:
各种灭菌器材应在三日内用完,生理盐水应在七日内用完
4.5管理
4.5.1储藏灭菌器材的烘箱不得随意打开,不得存放其他未灭菌的物品
4.5.2实验人员用前应检查包装是否有破损,塞子松动或脱落等异常情况,发现问题及时处理或停止使用
4.5.3超过保存期限未用完的器材应重新灭菌,不得继续使用
QA主管,QA检测员。
SOP-QC-O07-00
明确微生物限度检查的标准操作规程,以保障产品质量得到有效的控制。
成品、半成品。
QC检测员负责执行,QC主管负责监督。
4.1总则
4.1.1抽样用具的清洁与贮存见微生物检验用器皿准备标准操作程序。
4.1.2抽样方法见微生物检查取样标准操作程序。
4.1.3供试品在检查前不得开启,检查前和检查中应防止供试中的污染受损、致死或繁殖。
4.1.4检查全过程均应严格遵守无菌操作规程,严防再污染。
4.1.5控制菌的污染检查应做相应的已知菌对照试验,对照菌为大肠杆菌[CMCC(B)44102],每批试验已知菌加入量为50--100。
4.1.6染菌量的检查或控制菌的检查均应做空白对照试验。
4.1.7供试品稀释成稀释液后应在均匀状态下取样,凡有抑菌成份或防腐剂的供试品应做特殊处理后进行检验。
4.1.8供试品稀释后应在1小时内操作完毕。
4.1.9细菌、霉菌检验结果的报告以g、ml为单位的菌落数表示。
控制菌检验报告以g或ml为单位报告“检出”或“未检出”。
4.2检查法
4.2.1细菌、霉菌的染菌量,采用培养皿菌落计数法。
4.2.1.1供试液的制备:
固体供试品以无菌操作称取10g,置含0.9%氯化钠的生理盐水100ml中,振摇溶解,使成1:
10稀释度的供试液。
然后依次稀释成1:
10、1:
100、1:
1000的供试液。
4.2.1.2吸样
分别吸取1:
1000的供试液分别注入2-3个平皿中。
4.2.1.3注皿
事先将细菌培养基融化,置于45℃水浴中备用。
当供试液注入平皿后,用培养基倾注入平皿,每皿约15ml,随即转动平面,使供试液与培养基混匀后置水平台上待凝。
4.2.1.4培养
将平皿倒置于培养箱中培养。
细菌培养30-35℃、48小时;
霉菌培养25-28℃、72小时。
4.2.1.5菌落计数法
细菌先用肉眼观察,点数菌量(霉菌除外),然后持5-10倍放大镜检查有无遗漏。
如有片状菌落或花斑样菌落蔓延生长的以及平板受到污染的情况,则该平板计数无效。
若平板上有2个或者个以上的菌落重叠,如可分辩,仍以2个或是个以上菌落计数。
当一个稀释级用2个平板时,应采用2个平板菌落数的均值为平均平板菌落数。
若2个平板菌落数相差1倍以上时,该当稀释级不宜采用(不包括2个平板菌落数均在15个以下的情况)点计后,计算各稀释级的平均平板菌落数按菌数报告规则报告。
4.2.2控制菌的检查
4.2.2.1检查步骤:
按增菌、分离、纯化培养、革兰氏镜检检与生化鉴别等项试验进行。
4.2.2.2大肠杆菌检查法
取供试液10ml(供试品1g、1ml)于100ml胆盐乳糖,增菌培养液内,置36±
1℃、18-24小时培养,如增菌注呈现混浊、表面可见或未见气泡都表明有菌生长,如混浊不明显,可延长培养时间至48小时。
取其增菌培养物划线,接种于伊红美兰琼脂培养皿中,置36±
1℃、18-24小时培养,如无菌落生长,可判为:
未检出大肠杆菌。
若有菌生长或疑似者,应挑选2-3个菌落,继续做染色镜检和乳糖发酵试验。
4.3细菌检查:
4.3.1细菌菌落形态
细菌菌落是一个菌细胞或菌细胞团在局限位置上,经一定条件下繁殖成肉眼可见的细菌群体,外观湿润或干燥,表面光滑或折皱,外缘整齐或缺陷。
4.3.2霉菌菌落形态
具有放射或树枝样分枝的菌丝是霉菌菌落的特征。
初形成时多无色透明,成熟的霉菌菌落有各种颜色的孢子形成。
4.3.3大肠杆菌菌落形态
在EBM琼脂平板上的典型菌落呈紫黑色或中心深紫色,圆形,稍凸起,边缘整齐,表面光滑,带有金属光泽。
非典型形态,在EBM琼脂平板上呈浅紫、粉紫、粉色,无明显的暗色中心,应做为疑似菌进行鉴定。
4.4对照试验
4.4.1阴性对照试验:
检验试验全过程无菌技术的可靠性。
4.4.1.1菌数测定阴性对照试验
分别吸取生理盐水1ml置于无菌平皿中,分别按细菌、霉菌测定方法注皿、培养,不得长菌。
4.4.1.2控制菌检查阴性对照试验
吸取生理盐水1ml于增菌液中,按控制菌检查方法检查不得长菌。
4.4.2阳性对照试验:
检查供试品是否对控制菌生长产生干扰作用及检查培养条件是否适宜。
4.4.2.1方法:
于供试液中加入一定量的相应对照菌,做平行试验。
4.4.2.2规定阳性对照菌株为大肠杆菌[CMCC(B)44102]。
对照菌的加入量为50-100个,可事先预试确定。
4.4.2.3用计数方法,取37℃培养费8-20小时的新鲜肉汤培养物10倍递增稀释至10-6,取其0.1ml于普通肉汤琼脂板表面涂抹或取10-7稀释液1ml以少于皿法进行测定。
4.4.2.4当供试品未检出菌时,而阳性对照试验也未能检出,则不能做出供试品未检出控制菌的结论。
4.4.2.5阳性对照试验操作必须与供试品检验操作严格分开,避免交叉污染。
4.5复试
4.5.1菌数测定不合格者应复试,控制菌检验以一次检验为准,不再复试,但应保留检出菌株一个月备查。
4.5.2复试项目以不合格项目为准,做单项复试。
4.5.3复试需取同批样品测定2次。
4.5.4复试报告以3次测定结果的算术增均值报告。
4.6检验报告
4.6.1测定菌数报告:
以各次测定结果的全部平均值报告。
4.6.2控制菌按全部复试检验结果报告:
如全部复试均未检出控制菌时,报告为“按规定抽样检验未检出×
×
菌”如全部抽样中任一样品检出控制菌时,报告为“按规定抽样检验,检出×
菌,不符合药品微生物限度规定”。
QC主管,QC检测员。
明确洁净室(区)沉降菌检验的标准操作规程。
洁净区(室)。
QC检测员负责执行,QA检查员负责监督。
4.1采样点数目:
洁净区域
面积m2
取样点(个)
脱包
磨样室
备料室
配料室
筛粉室
湿混制粒室
制软材室
空桶室
前室
(1)
干燥整粒混合室
中间站
压片室
(1)
压片室
(2)
前室
(2)
冲模室
水泡眼包装室
袋包装室
胶囊填充室
内包材室
中间站
(2)
质控室
包衣室
溶媒存放室
缓冲间
男二更
女二更
洗衣室
衣物存放室
卫生洁具室
器具存放室
清洗器具室
办公室
取样室
通道
仓库取样室
超净工作台
无菌室
备注
4.2取样点布置,如图示:
○○
4.2.1采样点布置在离地0.8米高的水平面上均匀布置。
4.2.2采样点多于5点时,可在离地面0.8-1.5m高度的区域内分层布置,但每层不少于5个点。
4.2.3布置采样点时,应避开回风口。
4.3测试时间:
净化空调系统正常运行不少于30分钟后开始。
4.4测试方法
4.4.1将已准备好的培养皿置于采样点,打开培养皿盖,使培养基表面暴露0.5h,再将培养器盖盖上。
4.4.2全部采样结束后,将培养器倒置于30-35℃恒温培养箱中培养48小时。
4.4.3菌落计数:
方法见《微生物限度检验程序》中菌落计数法
4.4.4结果计算:
4.4.5结果判定:
100级:
平均菌落数≤1个/皿为合格
10000级:
平均菌落数≤3个/皿为合格
100000级:
平均菌落数≤10个/皿为合格
300000级:
平均菌落数≤15个/皿为合格
若测定结果不符和上述标准,则必须对此区域进行消毒,然后重新采样2次,测试结果均须合格。
QC检查员,QA检查员。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 质量管理 SOP 大全
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《Java程序设计》考试大纲及样题试行.docx
《Java程序设计》考试大纲及样题试行.docx
