 中考化学复习专题2Word文件下载.docx
中考化学复习专题2Word文件下载.docx
- 文档编号:22443095
- 上传时间:2023-02-04
- 格式:DOCX
- 页数:23
- 大小:170.38KB
中考化学复习专题2Word文件下载.docx
《中考化学复习专题2Word文件下载.docx》由会员分享,可在线阅读,更多相关《中考化学复习专题2Word文件下载.docx(23页珍藏版)》请在冰豆网上搜索。
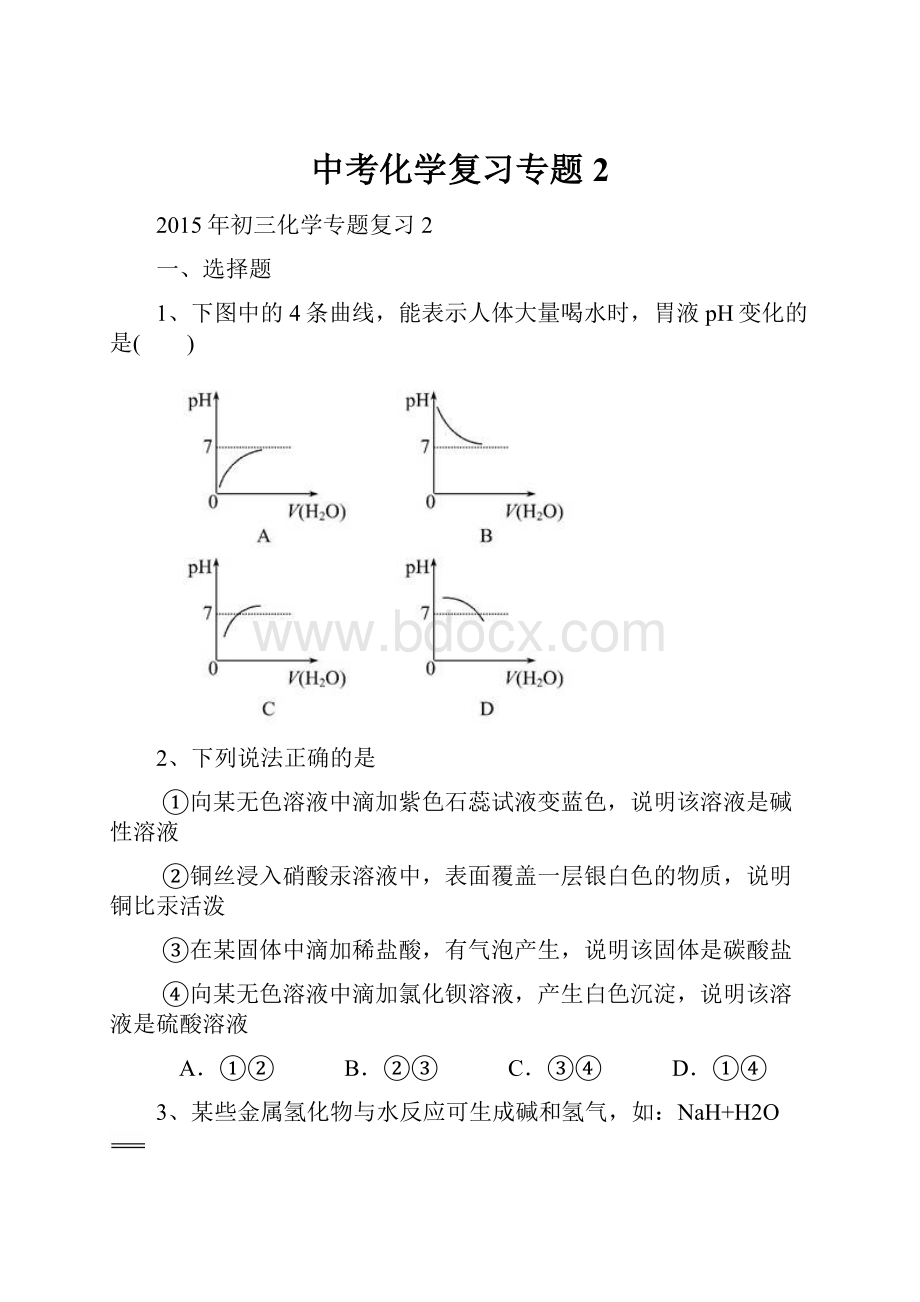
7、X可以发生如下反应:
(1)X+酸
盐+水;
(2)X+非金属氧化物
盐+水。
X可能是(
A.氧化铜
B.盐酸
C.氢氧化钠
D.碳酸钠
8、滴有酚酞的Ca(OH)2溶液分别与下列各物质恰好完全反应后,溶液仍显红色的是( )
A.CO2
B.H2SO4溶液
C.稀盐酸
D.K2CO3溶液
9、某NaOH固体样品已部分变质。
常温下,取61.2g该样品溶于水得到1000g溶液,取出500g溶液进行测定,其中含Na元素16.1g,碳元素1.2g,则原NaOH固体样品中NaOH的质量分数为
A.65.4%
B.34.6%
C.82.3%
D.64.5%
10、将17.1克10%的Ba(OH)2溶液跟10克10%的H2SO4溶液均匀混合后过滤,得到的滤液
是(
A.水
B.含少量H2SO4的水溶液
C.含少量B
a(OH)2的水溶液
D.BaSO4的不饱和溶液
11、向一定量的氢氧化钡溶液中逐滴滴加稀硫酸至过量,下列图像与该反应事实相符合的是(
12、除去下列物质中所含的少量杂质,所用方法错误的是(
选项
物质
杂质
除杂质的方法
A
铁粉
氧化铁
加过量稀盐酸充分反应后过滤
B
硫酸亚铁溶液
硫酸铜溶液
加过量铁粉充分反应后过滤
C
氯化钙溶液
盐酸
加过量碳酸钙粉末充分反应后过滤
D
氯化钠溶液
碳酸钠
加稀盐酸至溶液呈中性
13、某实验室废水含有较多的盐酸,排放前应加入某种试剂将废水调至中性,下列试剂中最合适的是( )
A.AgNO3溶液
B.NaOH溶液
C.稀醋酸
D.KNO3溶液
14、下列除去杂质的试剂和方法可行的是(
物质(括号内为杂质)
除杂试剂和方法
Mg(NO3)2溶液(AgNO3)
加入过量铁粉,过滤
NaCl溶液(Na2SO4)
加入适量BaCl2溶液,过滤
CO2(CO)
通过足量澄清石灰水
N2(O2)
通过灼热的氧化铜
15、下列对某一主题知识归纳,正确的一组是(
)
A.生活常识
B.物质鉴别
硬水与软水——观察颜色区别
人体缺钙元素——甲状腺肿大
食盐与蔗糖——品尝味道
硝酸铵与氢氧化钠——加水溶解
C.化学与生产
D.“一定”与“不一定”
硫酸铵不能与草木灰混合使用——会产生氨气
CO用于冶炼金属——CO有可燃性
原子中一定含有质子、中子、电子三种粒子
浓溶液一定是饱和溶液,稀溶液一定是不饱和溶液
16、将一定质量的铁粉和铜粉的混合物加入AgNO3溶液中,反应结束后过滤,分别向滤液和滤渣中加入稀盐酸,均无明显现象,下列对滤渣和滤液的说明中,不正确的是( )
A.
滤渣中一定含有银
B.
滤液中一定含有Fe2+
C.
滤渣中可能含有铜
D.
滤液中一定含有Cu2+
二、填空题
17、根据下列反应事实写出相应的化学方程式。
(1)常温下,铝和氧气发生反应,在铝表面形成致密的氧化铝膜:
______________________________。
(2)稀盐酸与氧化铁反应,生成水和氯化铁溶液:
(3)炼铁高炉内焦炭与二氧化碳反应生成一氧化碳:
_
_____________________________。
(4)铁粉浸入硫酸铜溶液中,置换出单质铜,生成硫酸亚铁溶液:
(5)碳酸氢铵晶体受热后生成氨气、水和二氧化碳气体:
18、2012年一辆载有近30吨苯酚的槽罐车途经某市时发生侧翻,约有10吨的苯酚泄漏,空气中弥漫着浓烈的酸臭气味,对该市居民生活造成很大诚胁。
苯酚是一种有毒的物质,对
皮肤、黏膜有强烈的腐蚀作用。
(1)苯酚化学式为(C6H6O)属于________。
(填“有机物”或“无机物”)
(2)现场救护人员应佩戴呼吸器,穿好防化服的原因是_____________________
(3)你认为下列对事故的处理方法合理的是_________。
①用水进行冲洗或用泥土填埋②挖隔离沟、铺薄膜防止扩散并回收泄漏的苯酚
③随时监测附近水源、土壤中的苯酚
(4)用木屑吸附残余的苯酚,然后燃烧处理。
写出苯酚完全燃烧的化学方程式。
_______________________________________
19、如图,A是黑色氧化物,C溶液呈蓝色(部分生成物略去)。
D的化学式为 ;
B的类别属于 (填“单质”、“酸”、“碱”或“盐”);
A和B反应的基本反应类型是 ;
写出C和氢氧化钠溶液反应的化学方程式为 。
20、某工业园区新拟建一硫酸厂,在生产硫酸的过程中会产生SO2,如SO2直接向大气排放,则易形成酸雨,酸雨的pH<
________;
为防止SO2污染大气,有以下方案你认为可行的是________(填序号)。
①建造高烟囱,将废气向高空排放
②用废NaOH溶液吸收SO2
③用熟石灰吸收SO2
④用废硫酸溶液吸收SO2
请任意写出可能发生的一个化学方程式:
_______________________________
_______________________________________。
21、有一包固体混合物可能由CaCO3
,KMnO4,BaCl2,KCl,Na2CO3
中的一种或几种组成,现取该混合物进行如下实验:
(1)将固体混合物投入水中,搅拌后完全溶解,得到无色溶液。
(2)往上述溶液中滴加盐酸,产生一种能使石灰水变浑浊的无色气体,由
上述实验现象可知:
该固体混合物中一定存在的是_______一定不存在的是
________不能确定是否存在的是_______。
22、从化学的视角认识生活中的有关问题。
(1)我们所用的下列物品中,主要材料属于有机合成材料的是
。
(填序号)
A.塑料保鲜膜
B.棉布围裙
C.合成橡胶手套
(2)洗涤剂可用来洗碗,是因为它对油污具有
功能。
(3)紫薯营养丰富,富含淀粉、蛋白质、维生素、锌、铁、钙、硒等。
其中能给人体提供能量的是
;
“锌、钙、硒”是指
(填“单质”、“元素”或“分子”)
(4)吸烟有害健康。
在公共场所,非吸烟者会因少数吸烟者吸烟
造成被动吸烟,从分子的性质解释原因_______________________________________________________。
(5)奶制品、豆类和虾皮等含有丰富的钙,是常见的补钙食物。
青少年缺钙会导致
(6)自来水厂净水过程中常用活性炭,活性炭的作用是
23、氨气(NH3)是一种无色、有刺激性气味的气体,极易溶于水,它的水溶液称为氨水,显碱性,氨在化学工业中用途很广泛,例如制化肥、制纯碱等;
近年来,氨还用于环境治理。
⑴实验室收集氨气可采用的方法为
,干燥氨气可选用试剂为
⑵工业上在细菌作用下用氨处理含甲醇的废水,使其变为毒的N2和CO2,从而消除对环境的污染,有关的反应为:
6NH3+5CH3OH+12
3N2+5CO2+19H2O,上述反应中B的化学式是
⑶在400℃、催化剂存在的条件下,用氨气可将有毒气体NO还原,生成N2和H2O。
试写出该反应的化学方程式:
。
三、实验,探究题
24、某化学实验小组为了除去混在N2中的O2,将混合气体通过红热的铜丝网后,发现铜丝网变黑。
在研究如何除去黑色物质,回收再利用铜丝网的讨论中,制定了下列方案。
甲方案图示
乙方案图示
请根据以上方案回答:
(1)乙方案的烧杯中发生反应的化学方程式是(其中B物质自行确定)__________________。
两种方案相比较,甲方案明显的不足之处是________________________。
(2)若采用甲、乙两种方案处理此黑色铜丝网,则回收的铜丝网a的质量______(填“<
”“>
”或“=”)铜丝网b的质量。
(3)实验小组的同学发现,反
应后烧杯中的液体有腐蚀性,应加以适当的处理。
他们采取加入铁粉的方案处理废液。
加入足量的铁粉充分搅拌,最后得到的溶液中溶质为______。
25、兴趣小组同学向盛有生石灰的烧杯中加入碳酸钠溶液,搅拌、过滤、洗涤、干燥后得到固体A和溶液B,并对固体A和溶液B进行探究。
上述实验中发生的反应有:
①CaO+H2O=Ca(OH)2;
②
(写化学方程式)。
Ⅰ.固体A成分的探究及测定
[猜想]
①固体A中只有CaCO3;
②固体A中含有CaCO3和Ca(OH)2;
含有Ca(OH)2的理由是
[实验]
取少量固体A于试管中加足量水,振荡、静置,向上层清液中滴加硫酸铜溶液,出现
,猜想②成立。
[组成测定]
取8.7g固体A于试管中,加足量稀盐酸至固体完全溶解,收集到纯净CO22.2g,则固体A中CaCO3和Ca(OH)2的质量比为
Ⅱ.溶液B的成分探究
①溶液B中的溶质是NaOH;
②溶液B中的溶质是NaOH和Na2CO3;
③溶液B中的溶质是NaOH和Ca(OH)2。
根据对固体A成分的探究,小组同学认为猜想③正确,其理由是
取少量溶液B于试管中,滴加
溶液,产生白色沉淀,证明猜想③正确。
26、将一定量的碳酸钠溶液与氯化钡溶液混合后,过滤反应的混合物。
某研究小组的同学们欲探究滤液中溶质的组成。
请你一同参与探究并回答有关问题:
【查阅资料】碳酸钠溶液显碱性;
氯化钠、氯化钡溶液
显中性。
请你写出碳酸钠溶液与氯化钡溶液反应的化学方程式________________________________。
【提出猜想】
猜想1:
滤液中溶质是NaCl;
猜想2:
滤液中溶质是NaCl和____________(填化学式)的混合物;
猜想3:
滤液中溶质是NaCl和Na2CO3的混合物。
【实验探究】
(1)取少量滤液于试管中,滴加2~3滴无色酚酞试液,振荡,无明显现象。
同学们认为猜想___________不成立。
(2)另取少量滤液于另一支试管中,滴加硫酸钠溶液,若有_________(填实验现象)证明猜想2成立。
【问题讨论】
(1)甲同学认为要证明猜想2成立也可以改用碳酸钠溶液。
你认为甲同学______(填“能”或“不能”)达到实验目的。
(2)乙同学认为要证明猜想2成立也可以改用硝酸银溶液。
你认为乙同学_______(填“能”或“不能”)达到实验目的。
27、某无色溶液可能含有氢氧化钠、氢氧化钙、硫酸钠、氯化钠、碳酸钠中的一种或几种物质。
为探究其组成,某化学兴趣小组的同学进行了如下探究活动。
请根据实验填空。
探究活动一:
取适量原无色溶液放入试管中,滴加1—2滴无色酚酞溶液后,将所得溶液分成两份。
(1)向第一份溶液中加入一种物质后,观察现象,得出结论:
原溶液中一定含有碳酸钠。
由此可推出:
原溶液中一定不含____________________.(写化学式、物质名称皆可,下同)。
(2)向第二份溶液中加入足量另一种物质后,观察现象,得出结论:
原溶液中一定含有氢氧化钠。
能证明该结论的现象是______________________________。
探究活动二:
为探究其他两种物质是否存在,该小组的同学进行了如下实验,
实验过程中所得液体均为无色溶液。
(1)加入过量稀硝酸的目的是____________________;
(2
)加入的X是_________________________________
__;
(3)由探究活动二得出的结论是______________________________;
(4)溶液C中含有的溶质是_______________________________________________________
28、某化学兴趣小组探究常温下碳酸钠饱和溶液的酸碱度。
【猜想与假设】溶液的pH可能是(填入你的猜想与假设):
①pH>
7;
②pH________;
③pH________。
【设计与实验】小方、小钟、小陈三位同学进行了如下实验:
小方:
取pH试纸于玻璃片上,用玻璃棒蘸取碳酸钠溶液沾在pH试纸上,测得p
H>
7。
小钟:
取pH试纸于玻璃片上,先用蒸馏水润湿pH试纸,然后用玻璃棒蘸取碳酸钠溶液沾在pH试纸上,测得pH>
小陈:
取pH试纸直接浸入碳酸钠溶液中,测得pH>
【评价】以上三位同学中操作规范的是________同学,其余两位同学操作上的错误是_________________________________________________;
___________
【结论】从物质的类别看,碳酸钠是一种__________(填“酸”“碱”或“盐”),它的溶液显碱性,说明显碱性的溶液________(填“一定”或“不一定”)是碱溶液。
29、已知氯化镁样品中含有杂质氯化钠,某化学兴趣小组的同学通过以下实验测定其中氯化镁的质量分数:
称取该样品15g溶于水得到溶液,然后将一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡(实验数据见下表)。
第1次
第2次
第3次
第4次
加入氢氧化钠溶液的质量/g
25
生成沉淀的质量/g
2.9
x
8.7
(1)表中x=
▲
(2)样品中氯化镁的质量分数是
▲
(3)若实验室中只有80g质量分数为30%的氢氧化钠溶液,要想配成本实验所需溶质质量分数的氢氧化钠溶液,还需加入水的质量是多少?
四、计算题
30、某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反
应制取二氧化碳,在准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他们决定利用该废液,测定Na2CO3溶液中溶质的质量分数。
他们将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示
(1)在加入Na2CO3溶液的过程中,开始时没有发现沉淀生成,说明滤液中的溶质除含有CaCl2外,还含有______________________;
(2)计算Na2CO3溶液中溶质的质量分数。
(计算结果精确到0.1%)
31、实验后的废液一般需回收处理,不能直接倒入排污管。
小科实验后收集到含有碳酸钠和氧氧化钠的混合废液10.22g,他向废液中缓缓滴入溶质质量分数为19.6%的稀硫酸,生成二氧化碳质量与滴入稀硫酸质量的关系如图所示。
当废液恰好处理完毕时,溶液总质量为20g。
溶于水的气体忽略不计,则
(1)废液恰好处理完毕时,溶液的pH为
(2)图中m=
g。
(3)废液恰好处理完毕时,回收所得溶液的溶质质量分数是多少?
32、山东省汶上县白石镇山区拥有丰富的大理石矿产资源.今有坛山上的大理石样品,其中只含二氧化硅杂质(二氧化硅是一种既不溶于水也不与盐酸反应且耐高温的固体).白石镇中学的同学们想测定该样品中碳酸钙的质量分数,他们选取了一块大理石样品,将其敲打粉碎后,称出6g放入烧杯内(烧杯质量为20g).然后加入50g某一定溶质质量分数的稀盐酸,用玻璃棒搅拌至不再产生气泡为止.反应所需时间(t)和烧杯及其所盛物质总质量(m)的关系如图所示.请完成下列问题:
(1)将大理石样品敲打粉碎的主要目的是:
;
(2)实验结束时,理论上共放出二氧化碳的质量为 g.
(3)计算该石灰石样品中碳酸钙的质量分数.(保留小数点后一位小数)
33、为测定某BaCl2溶液的溶质质量分数,现取100gBaCl2溶液,不断加入稀H2SO4,反应过程中溶液质量与加入稀H2SO4的质量关系如图所示,请回答:
①P点意义_______________。
②反应生成BaSO4沉淀的质量为_________g。
③求原BaCl2溶液的溶质质量分数。
参考答案
1、选A。
胃液pH小于7,人体喝大量的水后,胃液中的胃酸会被稀释,酸性减弱,pH增大,但不可能大于7(即变成了碱性),只能越来越接近于7。
2、A3、B4、【答案】C
【解析】MgO
Mg(OH)2、CuO
Cu(OH)2,其中增加的水的质量为3.6g,增加的水中氢元素的质量与氢氧化钠中氢元素的质量相等,所以氢氧化钠的质量为:
3.6g×
2/18÷
1/40=16.0g。
5、B6、B7、C8、D
9、试题分析:
氢氧化钠部分变质是由于部分氢氧化钠和空气中的二氧化碳反应生成了碳酸钠,利用碳酸钠化学式中碳和钠的质量比,根据碳元素质量可求出钠元素的质量。
然后用钠元素的总质量减去碳酸钠中钠元素的质量,就得到氢氧化钠中钠元素的质量,然后求出氢氧化钠的质量,最后进一步求出氢氧化钠的质量分数。
解:
设Na2CO3中钠元素的质量为x
根据Na2CO3中碳元素和钠元素的质量比可得:
=
解得x=4.6g
所以氢氧化钠中钠元素的质量为16.1g﹣4.6g=11.5g
根据NaOH的化学式可得NaOH中钠元素的质量分数为:
×
100%=57.5%
所以氢氧化钠的质量为:
=20g
这是500g溶液中所含氢氧化钠的质量,那么在1000g溶液中含有的氢氧化钠应该为40g
因此原固体样品中氢氧化钠的质量分数为:
100%=65.4%
所以答案选A
10、B11、D12、A
13、选B。
酸和碱反应能生成盐和水,废水含有较多的盐酸,排放前可加入碱将废水调至中性,氢氧化钠属于碱。
14、B15、B16、D
17、Al+3O2
2Al2O3
(2)6HCl+Fe2O3
2FeCl3+3H2O
(3)CO2+C
2CO
(4)Fe+CuSO4
FeSO4+Cu
(5)NH4HCO2
NH3↑+H2O+CO2↑
18、
19、Cu(OH)2
酸
复分解反应 2NaOH+CuSO4==Cu(OH)2
↓+Na2SO4(合理即可)
【解析】第一步:
A是黑色氧化物可推出A可能是氧化铜、四氧化三铁或二氧化锰;
第二步:
C溶液呈蓝色可推出C可能是硫酸铜(或氯化铜等可溶性铜盐);
第三步:
A和B反应生成C和水,可推出A为氧化铜,B为盐酸或硫酸,C为氯化铜或硫酸铜;
第四步:
D在加热条件下生成A(氧化铜),可推出D为氢氧化铜;
第五步:
A和E在加热条件下生成水,可推出E为氢气。
故A为氧化铜,B为硫酸或盐酸,C为硫酸铜或氯化铜,D为氢氧化铜,E为氢气。
20、酸雨的pH小于5.6,防治酸雨的方案中,加高烟囱,污染物仍可向空中排放,SO2能和碱反应,故方案②和③可行,分别发生如下反应:
2NaOH+SO2====Na2SO3+H2O,
Ca(OH)2+SO2====CaSO3↓+H2O
因为硫酸不与SO2反应,故方案④不可行。
答案:
5.6 ②③ 2NaOH+SO2====Na2SO3+H2O或Ca(OH)2+SO2====CaSO3↓+H2O
21、
(2)Na2CO3,CaCO3
KMnO4
BaCl2,KCl
22、
23、
(1)向下排空气法,
固体氢氧化钠或碱石灰或生石灰等(任一种)
(2)O2
,
(3)4NH3+6NO
5N2+6H2O
三、实验,探究题
24、
(1)CuO+H2SO4
CuSO4+H2O 需制取CO;
CO有剧毒;
尾气未作处理;
装置复杂等
(2)>
(3)FeSO4
25、【答案】Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
[猜想]Ca(OH)2微溶于水
[实验]蓝色沉淀
[组成测定]50:
37
[猜想]Ca(OH)2过量(或固体A中含有Ca(OH)2)
[实验]Na2CO3[或K2CO3、(
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 中考 化学 复习 专题
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《城市规划基本知识》深刻复习要点.docx
《城市规划基本知识》深刻复习要点.docx
