 影响速率因素专题练习文档格式.docx
影响速率因素专题练习文档格式.docx
- 文档编号:22364049
- 上传时间:2023-02-03
- 格式:DOCX
- 页数:10
- 大小:51.15KB
影响速率因素专题练习文档格式.docx
《影响速率因素专题练习文档格式.docx》由会员分享,可在线阅读,更多相关《影响速率因素专题练习文档格式.docx(10页珍藏版)》请在冰豆网上搜索。
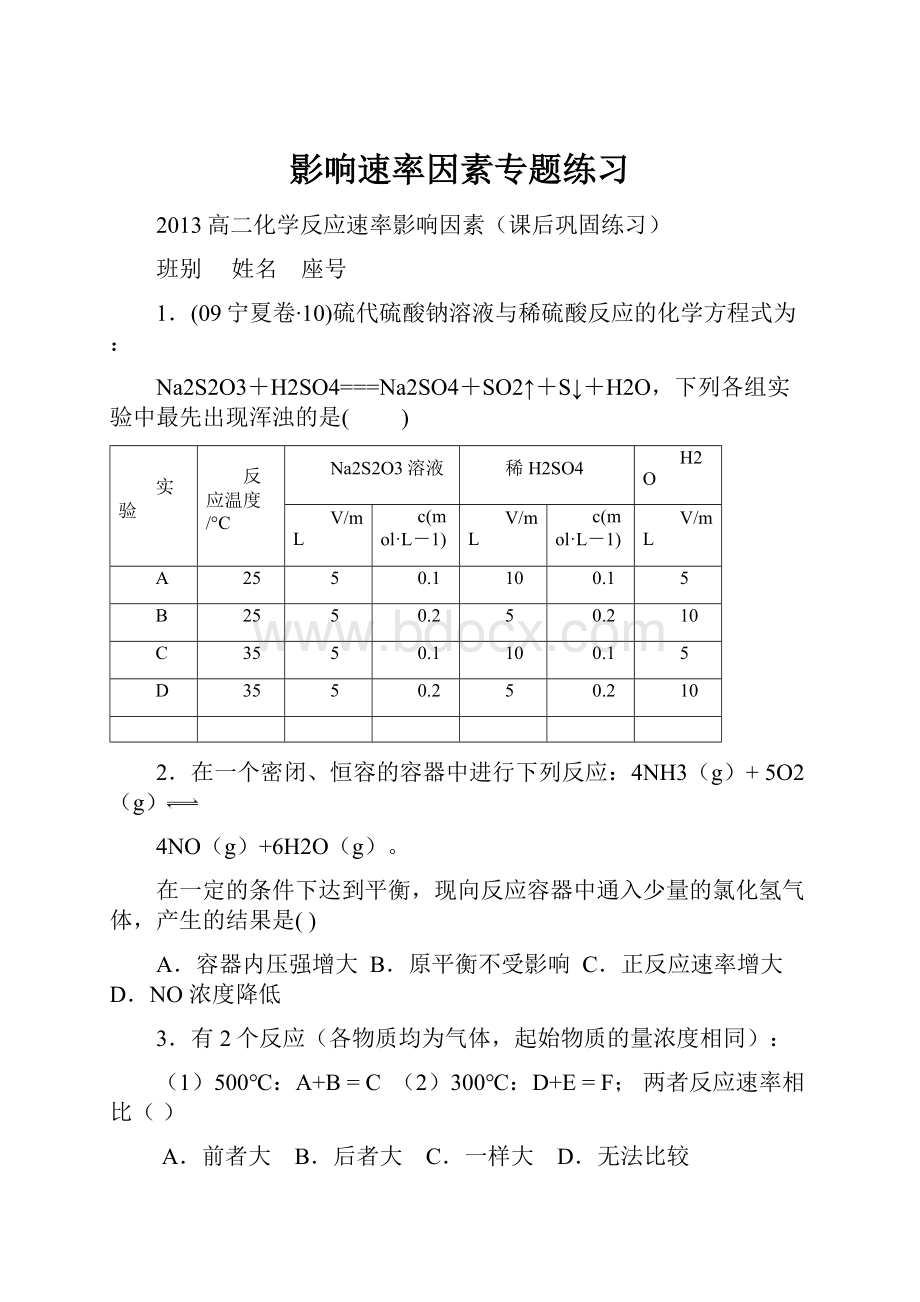
在一定的条件下达到平衡,现向反应容器中通入少量的氯化氢气体,产生的结果是()
A.容器内压强增大B.原平衡不受影响C.正反应速率增大D.NO浓度降低
3.有2个反应(各物质均为气体,起始物质的量浓度相同):
(1)500℃:
A+B=C
(2)300℃:
D+E=F;
两者反应速率相比()
A.前者大B.后者大C.一样大D.无法比较
4.把除去氧化膜的镁条投入到稀盐酸的试管中,发现氢气发生的速率变化情况如右图所示。
其中t1~t2速率变化的主要原因是
,
t2~t3速率变化的主要原因是
。
5.漂白剂亚氯酸钠(NaClO2)在常温与黑暗处可保存一年。
亚氯酸不稳定可分解,反应的离子方程式为:
5HClO2=4ClO2↑+H++Cl-+2H2O。
向NaClO2溶液中滴加H2SO4,开始反应缓慢,随后反应迅速,其原因是()
A.在酸性条件下亚氯酸的氧化性增强B.溶液中的H+起催化作用
C.ClO2逸出,使反应的生成物降低D.溶液中的Cl-起催化作用
6.将Ag块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如下图的实线所示,在相同的条件下,将Bg(A>
B)粉末状碳酸钙与同浓度足量盐酸反应,则相应的曲线(图中虚线所示)正确的是( )
7.下列说法中有明显错误的是()
A.对有气体参加的化学反应,增大压强,体系体积减小,可使单位体积内活化分子数增加,因而反应速率增大
B.升高温度,一般可使活化分子的百分数增大,因而反应速率增大
C.活化分子之间发生的碰撞一定为有效碰撞
D.加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大化学反应的速率
8.对于在一定条件下进行的化学反应:
2SO2+O2
2SO3,改变下列条件,可以提高反应物中活化分子百分数的是()
A.增大压强B.升高温度C.加入催化剂D.增加反应物浓度
9.对于在一密闭容器中进行的下列反应:
C(s)+O2(g)
CO2(g),下列说法中错误的是()
A.将木炭粉碎成粉末状可以加快化学反应速率B.升高温度可以加快化学反应速率
C.增加压强不能加快化学反应速率D.增加木炭的量可以加快化学反应速率
10.100mL6mol·
L-1H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量()
A.碳酸钠溶液B.水C.硫酸钾溶液D.硝酸钠溶液
11.等质量的铁与过量的盐酸在不同的试验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的试验组别可能是()
组别
c(HCl)(mol·
温度(℃)
状态
1
2.0
块状
2
2.5
30
3
50
4
粉末状
A.4-3-2-1B.1-2-3-4C.3-4-2-1D.1-2-4-3
12.在锌与某浓度的盐酸起反应的实验中,一个学生得到下面的结果:
序号
锌的质量/g
锌的形状
温度/℃
完全溶于水的时间/s
薄片
400
15
200
100
t1
E
F
颗粒
t2
G
粉末
t3
则下列说法正确的是()
①t1=75s②t2>
200>
t3③单位时间内消耗的锌的质量mG>
mF>
mB
A.①B.①②C.只有②D.全部正确
13.亚硫酸钠和碘酸钾在酸性溶液中发生以下反应:
Na2SO3+KIO3+H2SO4→Na2SO4+K2SO4+I2+H2O
(1)配平上面的氧化还原反应方程式,将系数填入方框中。
(2)其中氧化剂是,若反应中有5mol电子转移,则生成的碘是mol。
(3)该反应的过程和机理较复杂,一般认为发生以下①~④反应:
①IO3-+SO32-=IO2-+SO42-(反应速率慢)
②IO2-+2SO32-=I-+2SO42-(反应速率快)
③5I-+6H++IO3-=3I2+3H2O(反应速率快)
④I2+SO32-+H2O=2I-+SO42-+2H+(反应速率快)
根据上述步骤推测该反应总的反应速率由应应决定(填写上述四步反应的序号)。
(4)若预先加入淀粉溶液,由上述四步反应可以看出必须在离子消耗完全时,才会有使淀粉变蓝的现象产生。
14.(2007海南·
17)下表是稀硫酸与某金属反应的实验数据:
实验序号
金属
质量/g
金属状态
C(H2SO4)
/mol·
L-1
V(H2SO4)
/mL
溶液温度/℃
金属消失的时间/s
反应前
反应后
0.10
丝
0.5
20
34
500
0.7
36
250
0.8
6
1.0
125
7
8
1.1
9
44
40
分析上述数据,回答下列问题:
(1)实验4和5表明,
对反应速率有影响,
反应速率越快,能表明同一规律的实验还有
(填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有
(3)本实验中影响反应速率的其他因素还有
,其实验序号是
。
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:
15.氯酸钾和亚硫酸氢钠发生氧化一还原反应生成Cl(-1价)和S(+6价)的反应速率如右图所示,已知这个反应的速率随着溶液的[H+]增大而加快,则:
(1)反应开始时,速率加快的原因为
(2)后期反应速率下降的原因为
16.某中学化学小组查阅资料发现金属氧化物A也能催化氯酸钾的分解,且A和二氧化锰的最佳催化温度均在500℃左右,于是对A和二氧化锰的催化性能进行了定量对照实验。
实验时均以收满500mL氧气为准其他可能影响实验的因素均已忽略。
表一用MnO2作催化剂
KClO3质量g
MnO2质量g
反应温度℃
待测数据
8.00
2.00
表2用A作催化剂
A质量g
请回答:
上述实验中的待测数据应是:
。
完成此研容后,他们准备发表一篇研究报告,请你替他们拟一个报告的题目:
。
17.乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。
实验室制备乙酸乙酯的化学方程式如下:
CH3COOH+C2H5OH
CH3COOC2H5+H2O
为证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下四个实验,实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。
实验结束后充分振荡试管Ⅱ再测有机层的厚度,实验记录如下:
编号
试管Ⅰ中的试剂
试管Ⅱ中试剂
测得有机层的厚度/cm
2mL乙醇、2mL乙酸、1mL18mol/L浓硫酸
饱和碳酸钠
溶液
5.0
3mL乙醇、2mL乙酸
3mL乙醇、2mL乙酸、6mL3mol/L硫酸
1.2
3mL乙醇、2mL乙酸、盐酸
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。
实验D中应加入盐酸的体积和浓度分别是mL和mol/L。
②分析实验(填实验编号)的数据,可以推测出浓硫酸的吸水性提高了乙酸乙酯的产率。
浓硫酸的吸水性能够提高乙酸乙酯产率的原因是。
③加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,可能的原因是。
18.将4molA气体和2molB气体在2L的容器中混合并在一定条件下发生如下反应:
2A(g)+B(g)
2C(g)。
若经2s后测得C的浓度为0.6mol·
L-1,现有下列几种说法:
①用物质A表示的反应平均速率为0.3mol·
L-1·
s-1②用物质B表示的反应的平均速率为0.6mol·
s-1
③2
s时物质A的转化率为70%④2
s时物质B的浓度为0.7mol·
其中正确的是
A.①③B.①④C.②③D.③④
19.在298K时,实验测得溶液中的反应:
H2O2+2HI===2H2O+I2,在不同浓度时的化学反应速率见下表,由此可推知当c(HI)=0.500mol·
L-1,c(H2O2)=0.400mol·
L-1时的反应速率为( )
实验编号
c(HI)/mol·
L-1
0.100
0.200
0.300
c(H2O2)/mol·
v/mol·
L-1·
s-1
0.00760
0.0153
0.0227
0.0151
0.0228
A.0.0380mol·
s-1B.0.152mol·
s-1C.0.608mol·
s-1D.0.760mol·
答案
1.D2.D3.D
4.t1~t2速率逐渐增加的原因是镁条与盐酸反应放热,温度升高使反应速度加快;
t2~t3速率减小,是因为[H+]浓度减小,反应速率减慢。
5.D6.C7.C8.BC9.CD10.BC11.AC12.C
13.
(1)5、2、1、5、1、1、1
(2)KIO30.5(3)①(4)SO32-
14.
(1)固体反应物的表面积表面积越大1和2
(2)1、3、4、6、8(或2和5)
(3)开始反应温度6和7
(4)一定量的金属跟足量的硫酸反应放出的热量相同
15.
(1)2KClO3+6NaHSO3=3Na2SO4+2KCl+3H2SO4[H+]增速度加快
(2)反应物浓度减小,生成的H2SO4与NaHSO3反应使[H+]及[HSO4-]浓度减小,速度减慢
16.时间;
催化效果的对照研究
17.①66
②A、C(多答B不扣分;
A、C漏选一个则得0分;
答ABCD不得分)
浓H2SO4可以吸收酯化反应中生成的水,降低了生成物的浓度使平衡向生成乙酸乙酯的方向移动。
(划线部分是得分要点,下同)(“降低了生成物的浓度”写为“减少了水的量”或“从体系中移走水”也得分。
)
③大量乙酸、乙醇未经反应就脱离反应体系;
温度过高发生其他反应。
18.B19.B
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 影响 速率 因素 专题 练习
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《Java程序设计》考试大纲及样题试行.docx
《Java程序设计》考试大纲及样题试行.docx
