 备战中考化学经典题练专题十四常见的盐Word文件下载.docx
备战中考化学经典题练专题十四常见的盐Word文件下载.docx
- 文档编号:22351134
- 上传时间:2023-02-03
- 格式:DOCX
- 页数:20
- 大小:177.85KB
备战中考化学经典题练专题十四常见的盐Word文件下载.docx
《备战中考化学经典题练专题十四常见的盐Word文件下载.docx》由会员分享,可在线阅读,更多相关《备战中考化学经典题练专题十四常见的盐Word文件下载.docx(20页珍藏版)》请在冰豆网上搜索。
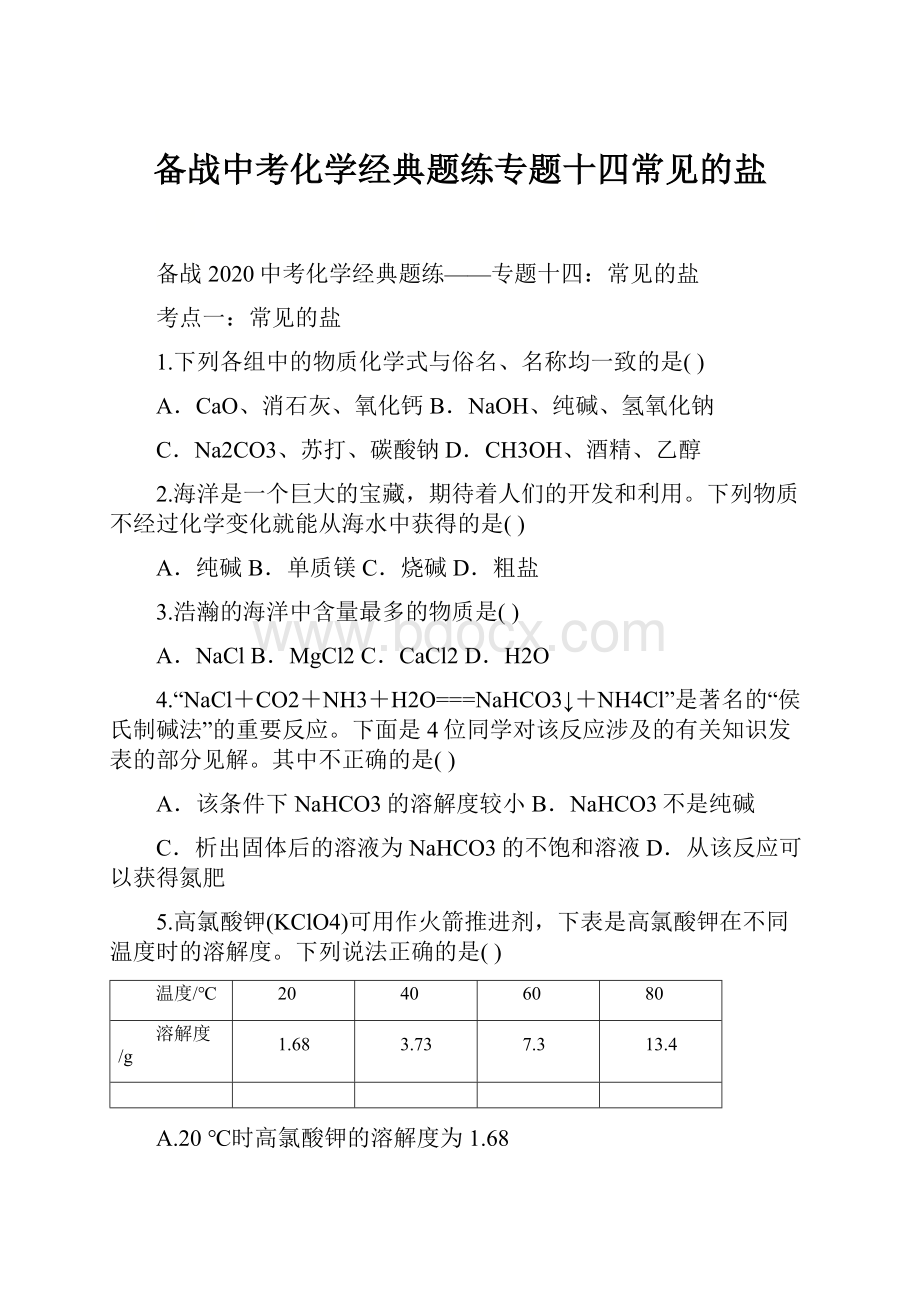
20
40
60
80
溶解度/g
1.68
3.73
7.3
13.4
A.20℃时高氯酸钾的溶解度为1.68
B.40℃时,将4g高氯酸钾溶于100g水中可得到104g溶液
C.80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象
D.高氯酸钾的溶解度随温度升高而减小
6.现有盐酸和CaCl2的混合溶液,向其中逐滴滴入Na2CO3溶液,生成沉淀质量与滴入Na2CO3溶液质量的变化关系如图所示。
下列说法错误的是()
A.滴加碳酸钠溶液质量为a~c克时,溶液中发生的反应为CaCl2+Na2CO3===2NaCl+CaCO3↓
B.滴加碳酸钠溶液质量至b克时,溶液中含三种溶质
C.滴加碳酸钠溶液质量至a克时,溶液中溶质质量比原混合溶液中溶质质量大
D.滴加碳酸钠溶液质量至c克时,溶液呈中性
7.下列物质:
①熟石灰、②碳酸钠、③氯化钠、④碳酸钙、⑤碳酸氢钠、⑥氢氧化铝、⑦稀盐酸,在生产生活中有广泛用途,请按下列要求填空(填序号)。
(1)农业中用来降低土壤酸性,改良土壤结构的是;
(2)用于造纸、玻璃生产、印染、洗涤剂生产的是;
(3)常用于面制品发酵的是;
(4)天安门前的华表,其主要成分是;
(5)用于金属除锈的是;
(6)用作厨房调味品的是。
8.如图是氯化钾和硝酸钾两种固体溶解度曲线图。
(1)20℃时,KNO3的溶解度(填“大于”“小于”或“等于”)KCl的溶解度。
(2)40℃时,KCl的溶解度是g,向100g水中加入40gKCl,所得溶液中溶质与溶液的质量比为。
(3)下列说法正确的是。
A.KNO3饱和溶液一定比不饱和溶液浓
B.饱和KCl溶液析出晶体后,溶液中溶质的质量分数可能不变
C.30℃时,分别将10gKCl和10gKNO3配制成饱和溶液,前者需要水的质量较多
D.分别将40℃时的KCl和KNO3的饱和溶液降温到20℃时,后者析出的晶体较多
9.请同学们搭乘“化学地铁”一起畅游物质世界吧!
如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站。
2~5号站各站的对应物质属于不同类别的纯净物。
(1)若列车上的物质为“碳酸钠溶液”。
①列车途经“2号站”时,若氧化物为二氧化碳,二氧化碳与碳酸钠溶液反应生成碳酸氢钠(NaHCO3)的化学方程式为。
②列车途经“3号站”时,反应的化学方程式为
(写一个)。
(2)“碳酸钠溶液”列车抵达“4号站”时,将列车上的物质更换为“稀盐酸”后出发。
①与“碳酸钠溶液”和“稀盐酸”都能反应的“4号站”的对应物质为(填一种)。
②“稀盐酸”列车途经“5号站”时,反应的化学方程式为(写一个)。
10.某化学兴趣小组对固体混合物A的组成进行实验研究,已知A中可能含有K2CO3、KCl、Fe2O3中的一种或多种,请根据如图所示实验过程回答问题(过程中所有可能发生的反应均恰好完全进行)。
(1)A中一定含有的物质是(写化学式)。
(2)溶液G中大量存在的酸根离子是(写离子符号)。
(3)写出③发生的化学反应方程式:
_,该反应属于(填一种基本反应类型)。
考点二:
物质的鉴别与提纯
1.下列表示的实验操作中,可以将食盐结晶出来的是()
2.下列是关于“粗盐提纯”实验的几种说法,其中正确的是()
A.为加快过滤速度,应用玻璃棒不断搅拌过滤器内的液体
B.如果经两次过滤滤液仍浑浊,则应检查实验装置并分析原因
C.蒸发滤液时要用玻璃棒不断搅拌,用酒精灯持续加热直到蒸干为止
D.蒸发完成后,直接用手将蒸发皿拿下来
3.实验室中有两瓶失去标签的稀盐酸和氯化钠溶液,下列四种试剂中能将其鉴别出来的是()
A.AgNO3溶液B.无色酚酞试液
C.K2CO3溶液D.Na2SO4溶液
4.下列各种溶质的溶液混合后无明显现象的一组是()
A.HCl、Na2CO3、K2SO4B.KNO3、Ba(OH)2、NaCl
C.KCl、AgNO3、HNO3D.NaOH、FeCl3、(NH4)2SO4
5.关于化学反应A+B―→C+D,下列说法中正确的是()
A.若生成物C和D分别是盐和水,则反应物一定是酸和碱
B.若该反应为复分解反应,则生成物中一定有水
C.若B是酸,则C和D一定有一种是盐
D.若A、B各取10g混合,使其充分反应,则C、D质量的总和一定等于20g
6.除去食盐溶液中的Na2SO4和CaCl2杂质的操作有:
①加入过量BaCl2溶液;
②过滤;
③加入适量盐酸;
④蒸发结晶;
⑤加入过量Na2CO3溶液。
正确的操作顺序是()
A.①⑤②③④B.③①⑤②④
C.①③⑤④②D.⑤③②①④
7.从海水中制备纯碱和金属镁的流程如下图所示:
A.流程Ⅰ依次向粗盐水中加入过量Ca(OH)2溶液、Na2CO3溶液和适量稀盐酸去除杂质
B.流程Ⅱ吸氨是使溶液呈碱性,有利于吸收二氧化碳
C.上述流程涉及三种基本反应类型
D.流程Ⅳ、Ⅴ是通过化学方法富集氯化镁
8.下列为达到实验目的所设计的实验方案中不合理的是(D)
选项
实验目的
实验方案
A
区别NaCl、Na2CO3两种溶液
滴加酚酞试剂
B
鉴别某种溶液是FeCl2溶液
观察溶液颜色,滴加AgNO3溶液
C
除去NaCl溶液中的Na2SO4
滴加适量BaCl2溶液,充分反应后,过滤
D
分离出含有少量NaCl的KNO3
高温下配制KNO3的饱和溶液,趁热过滤
9.海洋是个巨大的宝藏。
人类利用海洋化学资源大体上经历了如下图所示几个阶段。
―→
图1
(1)海水经日晒蒸发水分变为饱和溶液,再晒析出食盐,这一过程叫,这样得到的是“粗盐”,不仅含有泥沙,还含有Ca2+、SO
、Mg2+等离子。
为去除这三种杂质离子,可向粗盐水中依次加入过量的(填化学式),过滤去除沉淀后再加入适量盐酸,将溶液调至中性。
(2)制碱工业基本流程:
图2
由图示可知工艺中可循环利用的物质是NaCl。
(3)海水提镁流程:
,写出其中任意一个反应的化学方程式,提取氯化镁历经a、b两步转换的目的是。
(4)下列方法中能淡化海水的是(填字母)。
A.过滤法 B.沉淀法 C.多级闪急蒸馏法 D.分解法
10.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g5%的氯化钠溶液。
实验一:
如图是同学们做粗盐提纯实验的操作示意图。
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是。
(2)操作⑥中的错误是。
(3)粗盐提纯实验的操作顺序为(填操作序号)、称量精盐并计算产率。
(4)操作④中,当观察到时,停止加热。
实验二:
用提纯得到的精盐配制了50g5%的氯化钠溶液。
经检测,溶质质量分数偏小,其原因可能有(填序号)。
①氯化钠固体仍然不纯 ②称量时砝码端忘垫质量相同的纸片
③量取水时,仰视读数④装瓶时,有少量溶液洒出
11.小明同学欲回收中考化学实验操作考试(考题:
鉴别碳酸钠和氯化钠两瓶白色固体)用剩的药品。
他对其中的一瓶药品是否纯净产生怀疑,于是他在老师的指导下对其成分展开了如下探究:
【猜想与假设】猜想一:
白色固体为碳酸钠;
猜想二:
白色固体为氯化钠;
猜想三:
白色固体为碳酸钠和氯化钠的混合物。
【设计与实验】
实验步骤
实验现象
实验结论
取少量固体药品,装入试管,加蒸馏水溶解,然后加入过量的稀硝酸,最后滴加几滴硝酸银溶液
若只有产生
则猜想一正确
若只有白色沉淀生成
则猜想二正确,反应的化学方程式为
若先有气泡产生,后有白色沉淀生成
则猜想三正确
【实验结论】小明同学根据实验现象得出猜想三正确。
【反思评价】小明同学根据实验结论领悟到:
老师强调加入稀硝酸并且至过量的目的是。
他认为,若只将实验步骤中的过量稀硝酸换成过量稀盐酸,重复以上实验操作,虽然也会产生相同的实验现象,但不能确认猜想二是否正确,理由是。
【归纳总结】
(1)在选加试剂检验物质成分时,既要考虑除尽原有的干扰物质,又要防止新的干扰物质。
(2)在实验操作过程中,应规范操作以避免药品被。
12.镁在国产大飞机“C-919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图象如图),过滤,称量滤液质量为147g,求:
(1)图象中m=g。
(2)滤液中溶质的质量分数是多少?
常见的盐参考答案
【答案】C
【答案】D
【答案】B
【答案】①②⑤④⑦③
【答案】小于402∶7BC
【答案】Na2CO3+H2O+CO2===2NaHCO3Na2CO3+Ca(OH)2===CaCO3↓+2NaOHAgNO3Fe+2HCl===FeCl2+H2↑
【答案】K2CO3、Fe2O3Cl-FeCl3+3KOH===Fe(OH)3↓+3KCl复分解反应
【答案】A
【答案】结晶(蒸发结晶)BaCl2、NaOH、Na2CO3(BaCl2、Na2CO3、NaOH或NaOH、BaCl2、Na2CO3)MgCl2+Ca(OH)2===Mg(OH)2↓+CaCl2[或Mg(OH)2+2HCl===MgCl2+2H2O或MgCl2
Mg+Cl2↑](答案合理即可)获得比较纯净的氯化镁(富集氯化镁)C
【答案】加速溶解未用玻璃棒引流①⑤②③⑥④出现较多固体①②③
【答案】气泡AgNO3+NaCl===AgCl↓+NaNO3检验并除去CO
引入Cl-对实验造成干扰引入污染
【答案】11.6
解:
设氯化镁质量为x,反应生成氯化钠质量为y。
MgCl2+2NaOH===2NaCl+Mg(OH)2↓
9511758
xy11.6g
=
x=19g
y=23.4g
滤液中溶质的质量分数是
×
100%=20%
答:
滤液中溶质的质量分数是20%。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 备战 中考 化学 经典 专题 十四 常见
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
