 版高考化学一轮总复习限时训练第八章第28讲限Word下载.docx
版高考化学一轮总复习限时训练第八章第28讲限Word下载.docx
- 文档编号:22111047
- 上传时间:2023-02-02
- 格式:DOCX
- 页数:15
- 大小:99.27KB
版高考化学一轮总复习限时训练第八章第28讲限Word下载.docx
《版高考化学一轮总复习限时训练第八章第28讲限Word下载.docx》由会员分享,可在线阅读,更多相关《版高考化学一轮总复习限时训练第八章第28讲限Word下载.docx(15页珍藏版)》请在冰豆网上搜索。
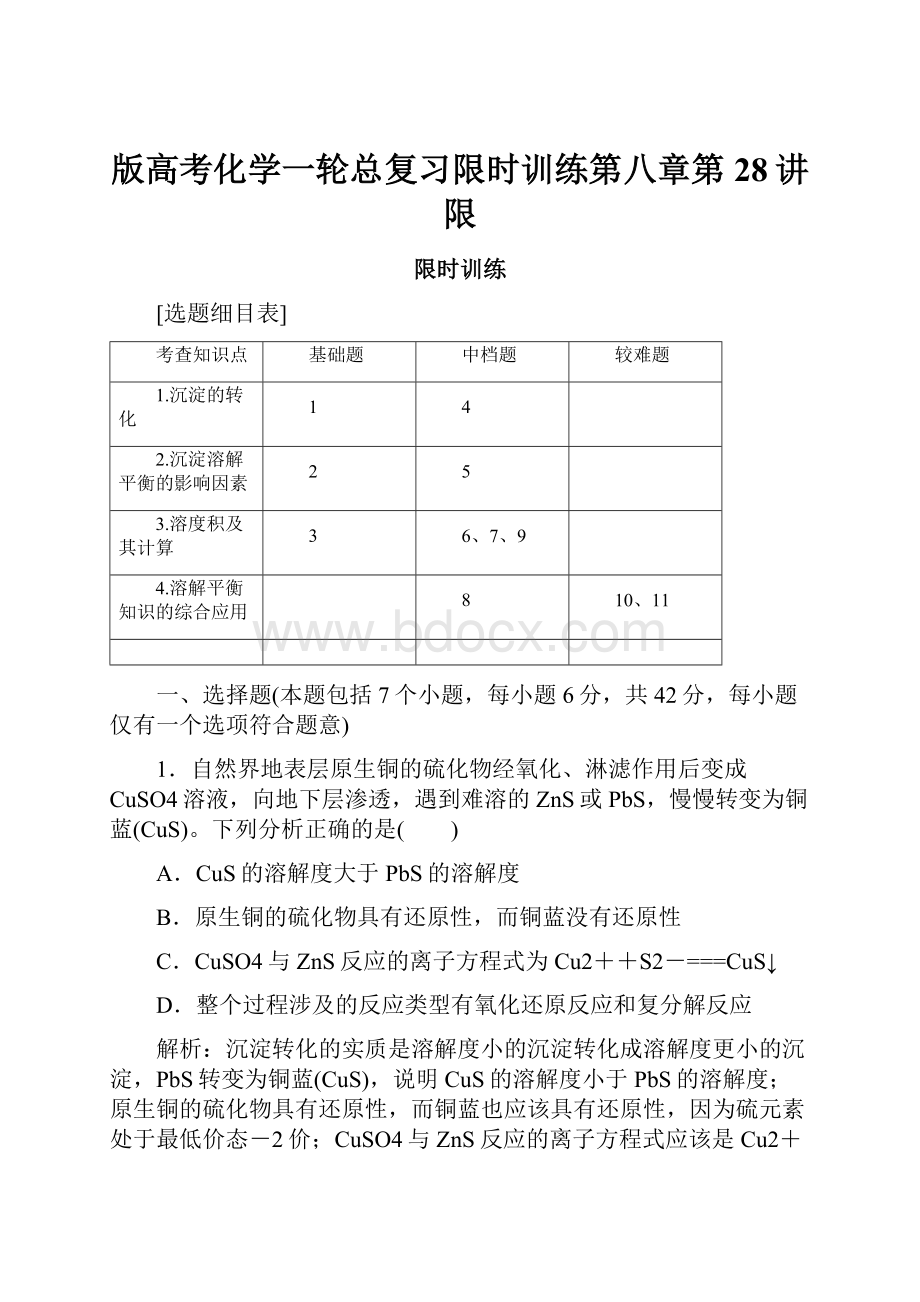
A.恒温下向溶液中加入CaO,溶液的pH升高
B.给溶液加热,溶液的pH升高
C.向溶液中加入Na2CO3溶液,其中固体质量增加
D.向溶液中加入少量NaOH固体,Ca(OH)2固体质量不变
恒温下Ksp不变,加入CaO后,溶液仍为Ca(OH)2的饱和溶液,pH不变,A错误;
加热,Ca(OH)2的溶解度减小,溶液的pH降低,B错误;
加入Na2CO3溶液,沉淀溶解平衡向右移动,Ca(OH)2固体转化为CaCO3固体,固体质量增加,C正确;
加入NaOH固体平衡向左移动,Ca(OH)2固体质量增加,D错误。
C
3.化工生产中常用MnS作为沉淀剂除去工业废水中Cu2+:
Cu2+(aq)+MnS(s)
CuS(s)+Mn2+(aq),下列说法错误的是( )
A.MnS的Ksp比CuS的Ksp大
B.该反应达平衡时c(Mn2+)=c(Cu2+)
C.往平衡体系中加入少量CuSO4固体后,c(Mn2+)变大
D.该反应的平衡常数K=
根据沉淀转化向溶度积小的方向进行,Ksp(MnS)>Ksp(CuS),A对;
该反应达平衡时c(Mn2+)、c(Cu2+)保持不变,但不一定相等,B错;
往平衡体系中加入少量CuSO4固体后,平衡向正方向移动,c(Mn2+)变大,C对;
该反应的平衡常数K=
=
,D对。
B
4.已知,同温度下的溶解度:
Zn(OH)2>
ZnS,MgCO3>
Mg(OH)2;
就溶解或电离出S2-的能力而言,FeS>
H2S>
CuS,则以下离子方程式错误的是( )
A.Mg2++2HCO
+2Ca2++4OH-===Mg(OH)2↓+2CaCO3↓+2H2O
B.Cu2++H2S===CuS↓+2H+
C.Zn2++S2-+2H2O===Zn(OH)2↓+H2S↑
D.FeS+2H+===Fe2++H2S↑
A项,因为溶解度MgCO3>
Mg(OH)2,所以生成的沉淀是Mg(OH)2而不是MgCO3,该项正确;
B项,电离出S2-的能力H2S>
CuS,所以能生成CuS沉淀,该项正确;
C项,溶解度:
ZnS,所以应该生成ZnS沉淀,该项错误;
D项,电离出S2-的能力FeS>
H2S,所以能生成H2S,该项正确。
5.某些盐能溶解沉淀,利用下表三种试剂进行实验,相关分析不正确的是( )
编号
①
②
③
分散质
Mg(OH)2
HCl
NH4Cl
备注
悬浊液
1mol·
L-1
A.向①中加入酚酞,溶液显红色说明物质的“不溶性”是相对的
B.分别向少量Mg(OH)2沉淀中加入适量等体积的②③,沉淀均能快速彻底溶解
C.①③混合后发生反应:
Mg(OH)2(s)+2NH
Mg2++2NH3·
H2O
D.向①中加入②,c(OH-)减小,Mg(OH)2溶解平衡正向移动
使酚酞显红色的溶液呈碱性,说明Mg(OH)2在水中有一定的溶解,电离使溶液呈碱性,A项正确;
Mg(OH)2与NH4Cl溶液反应速率较小,沉淀不能快速彻底溶解,B项错误;
NH
结合Mg(OH)2悬浊液中的OH-,促进Mg(OH)2的沉淀溶解平衡正向移动,促使Mg(OH)2沉淀溶解,C项正确;
盐酸能够与Mg(OH)2发生中和反应,促使Mg(OH)2的沉淀溶解平衡正向移动,D项正确。
6.(2017·
珠海模拟)一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时。
已知下表数据
物质
Fe(OH)2
Cu(OH)2
Fe(OH)3
Ksp/25℃
8.0×
10-16
2.2×
10-20
4.0×
10-38
完全沉淀时的pH
≥9.6
≥6.4
3~4
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法错误的是( )
A.向该溶液中加入少量铁粉不能观察到红色固体析出
B.该溶液中c(SO
)∶[c(Cu2+)+c(Fe2+)+c(Fe3+)]>
5∶4
C.向该溶液中加入适量氯水,并调节pH到3~4后过滤,得到纯净的CuSO4溶液
D.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
A项,因为Fe3+的氧化性强于Cu2+,所以投入少量铁粉,先发生的反应是:
2Fe3++Fe===3Fe2+,不能观察到红色固体析出,正确;
B项,因为Cu2+、Fe2+、Fe3+对应的碱全是弱碱,所以这三种离子在溶液中都会发生水解,因此它们的物质的量会减少,正确;
C项,加入氯水,可以把Fe2+全部氧化成+3价,但它的还原产物Cl-肯定还在溶液中,而且在调节pH时加入的试剂也会在溶液中有所保留,所以不可能只有CuSO4一种溶质,错误;
D项,从表格中可以看出,Fe(OH)3的Ksp是最小的,所以它最先出现沉淀,正确。
7.(2016·
洛阳模拟)①已知t℃时AgCl的Ksp=2×
10-10;
②在t℃时Ag2CrO4在水中的沉淀溶解平衡曲线如图所示。
A.在t℃时,Ag2CrO4的Ksp为1×
10-9
B.在饱和Ag2CrO4溶液中加入K2CrO4可使溶液由Y点到X点
C.在t℃时,以0.01mol·
L-1AgNO3溶液滴定20mL0.01mol·
L-1KCl和0.01mol·
L-1K2CrO4的混合溶液,CrO
先沉淀
D.在t℃时,反应Ag2CrO4(s)+2Cl-(aq)
2AgCl(s)+CrO
(aq)的平衡常数K=2.5×
107
依据图象曲线上的数据,结合溶度积常数概念计算即可得到,曲线上的点是沉淀溶解平衡,Ag2CrO4的沉淀溶解平衡为Ag2CrO4(s)
2Ag+(aq)+CrO
(aq);
Ksp=c2(Ag+)·
c(CrO
)=(10-3)2×
10-6=10-12,故A错误;
在饱和溶液中加入K2CrO4可使沉淀溶解平衡左移,溶度积常数不变,还是饱和溶液,点应在曲线上,故B错误;
依据溶度积常数计算Ksp(Ag2CrO4)=c2(Ag+)·
)=1×
10-12,Ksp(AgCl)=c(Ag+)·
c(Cl-)=2×
10-10,以0.01mol·
L-1K2CrO4的混合溶液,c(CrO
)=0.01mol·
L-1,得到c(Ag+)=
=1×
10-5(mol·
L-1),0.01mol·
L-1KCl溶液中,c(Cl-)=0.01mol·
L-1,依据溶度积计算得c(Ag+)=
=2×
10-8(mol·
L-1),所以先析出氯化银沉淀,故C错误;
在t℃时,Ag2CrO4(s)+2Cl-(aq)
(aq),离子浓度相同时,依据氯化银的溶度积和Ag2CrO4的溶度积计算,K=
=2.5×
107,故D正确。
二、非选择题(本题包括4个小题,共58分)
8.(15分)钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。
工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。
已知:
SrSO4(s)
Sr2+(aq)+SO
(aq)
Ksp=2.5×
10-7
SrCO3(s)
Sr2+(aq)+CO
(1)将SrSO4转化成SrCO3的离子方程式为_______________,该反应的平衡常数表达式为____________;
该反应能发生的原因是
_______________________________________________________
______________________________________________________。
(用沉淀溶解平衡的有关理论解释)
(2)对于上述反应,实验证明增大CO
的浓度或降低温度都有利于提高SrSO4的转化率。
判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”):
①升高温度,平衡常数K将________;
②增大CO
的浓度,平衡常数K将________。
(3)已知,SrSO4和SrCO3在酸中的溶解性与BaSO4和BaCO3类似,设计实验证明上述过程中SrSO4是否完全转化成SrCO3。
实验所用的试剂为________;
实验现象及其相应结论为____________。
(1)SrSO4转化成SrCO3的离子反应为:
SrSO4(s)+CO
(aq)
SrCO3(s)+SO
(aq),平衡常数表达式为K=
,根据沉淀转化的原理,该反应能够发生,是因为Ksp(SrCO3)<
Ksp(SrSO4)。
(2)①降低温度有利于提高SrSO4的转化率,说明降温平衡向正反应方向移动,因此升高温度,平衡向逆反应方向移动,故平衡常数K减小。
②平衡常数只与温度有关,增大CO
的浓度,平衡常数不变。
(3)根据提供的信息,可以推断SrSO4难溶于盐酸,而SrCO3可溶于盐酸,因此向溶液中加入盐酸,若沉淀全部溶解,则SrSO4完全转化成SrCO3,若沉淀没有全部溶解,则SrSO4没有完全转化成SrCO3,需要注意的是,不能选择稀硫酸,因为SrCO3与稀硫酸反应生成SrSO4。
(1)SrSO4(s)+CO
(aq) K=
Ksp(SrCO3)<
Ksp(SrSO4),加入CO
后,平衡SrSO4(s)
(aq)正向移动,生成SrCO3
(2)①减小 ②不变
(3)盐酸 若沉淀完全溶解,则证明SrSO4完全转化成SrCO3,否则,未完全转化
9.(14分)根据题目提供的溶度积数据进行计算并回答下列问题:
(1)在Ca(NO3)2溶液中加入(NH4)2CO3溶液后过滤,若测得滤液中c(CO
)=10-3mol·
L-1,则Ca2+是否沉淀完全________(填“是”或“否”)[已知c(Ca2+)≤10-5mol·
L-1时可视为沉淀完全;
Ksp(CaCO3)=4.96×
10-9]。
(2)已知:
25℃时,Ksp[Mg(OH)2]=5.6×
10-12;
酸碱指示剂百里酚蓝变色的pH范围如下:
pH
<
8.0
8.0~9.6
>
9.6
颜色
黄色
绿色
蓝色
25℃时,在Mg(OH)2饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为________。
(3)向50mL0.018mol·
L-1的AgNO3溶液中加入50mL0.020mol·
L-1的盐酸,生成沉淀。
已知该温度下AgCl的Ksp=1.0×
10-10,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中c(Ag+)=____________。
②完全沉淀后,溶液的pH=________。
③如果向完全沉淀后的溶液中继续加入50mL0.001mol·
L-1的盐酸,是否有白色沉淀生成________(填“是”或“否”)。
(1)根据Ksp(CaCO3)=c(Ca2+)·
c(CO
)=4.96×
10-9,得c(Ca2+)=
mol·
L-1=4.96×
10-6mol·
L-1<
10-5mol·
L-1,可视为沉淀完全。
(2)设Mg(OH)2饱和溶液中c(OH-)为xmol·
L-1,则0.5x3=5.6×
10-12,x>
1×
10-4,c(H+)<
10-10mol·
L-1,pH>
10,溶液为蓝色。
(3)①反应前,n(Ag+)=0.018mol·
L-1×
0.05L=0.9×
10-3mol,n(Cl-)=0.020mol·
0.05L=1×
10-3mol;
反应后剩余的Cl-为0.1×
10-3mol,则混合溶液中,c(Cl-)=1.0×
10-3mol·
L-1,c(Ag+)=
=1.0×
10-7mol·
L-1。
②H+没有参与反应,完全沉淀后,c(H+)=0.010mol·
L-1,pH=2。
③因为加入的盐酸中c(Cl-)和反应后所得溶液中的c(Cl-)相同,c(Cl-)没有改变,c(Ag+)变小,所以Qc=c(Ag+)·
c(Cl-)<
Ksp(AgCl),没有沉淀产生。
(1)是
(2)蓝色
(3)①1.0×
L-1 ②2 ③否
10.(14分)硝酸铈铵[(NH4)2Ce(NO3)6]广泛应用于电子、催化工业,其合成路线如下:
―→
Ⅰ Ⅱ Ⅲ
Ⅳ
(1)步骤Ⅰ中,将Ce(NO3)3·
6H2O配成溶液,保持pH为4~5,缓慢加入H2O2溶液搅拌混合均匀,再加入氨水调节溶液pH,得到Ce(OH)4沉淀。
该过程中参加反应的氧化剂与还原剂物质的量之比为________。
(2)298K时,Ksp[Ce(OH)4]=1×
10-29。
Ce(OH)4的溶度积表达式为Ksp=__________。
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×
L-1,需调节pH为________以上。
(3)为了研究步骤Ⅲ的工艺条件,科研小组测定了(NH4)2Ce(NO3)6在不同温度、不同浓度硝酸中的溶解度,结果如图。
从图中可得出三条主要规律:
①(NH4)2Ce(NO3)6在硝酸中的溶解度随温度升高而增大;
②___________________________________________________;
③____________________________________________________
(1)由得失电子相等得2n(Ce3+)=n(H2O2),所以氧化剂与还原剂物质的量比为1∶2。
(2)Ksp[Ce(OH)4]=c(Ce4+)·
c4(OH-),c4(OH-)===10-24,所以OH-的最小浓度为10-6mol·
L-1,则溶液的pH最小为8。
(3)由图象可知温度相同时,(NH4)2Ce(NO3)6在硝酸中的溶解度随硝酸浓度增大而减小;
硝酸浓度越小,温度对(NH4)2Ce(NO3)6的溶解度影响越大。
(1)1∶2
(2)c(Ce4+)·
c4(OH-) 8
(3)②其他条件相同时,(NH4)2Ce(NO3)6的溶解度随c(HNO3)减小而增大
③c(HNO3)越小,温度对(NH4)2Ce(NO3)6溶解度的影响越大或c(HNO3)越大,温度对(NH4)2Ce(NO3)6溶解度的影响越小
11.(2016·
天门模拟)(15分)以硫铁矿为原料生产硫酸所得的酸性废水中砷元素含量极高,为控制砷的排放,采用化学沉降法处理含砷废水,相关数据如表。
表1.几种砷酸盐的Ksp
难溶物
Ksp
Ca3(AsO4)2
6.8×
10-19
AlAsO4
1.6×
FeAsO4
5.7×
10-21
表2.工厂污染物排放浓度及允许排放标准
污染物
H2SO4
As
浓度
28.42g·
1.6g·
排放标准
pH6~9
0.5mg·
回答以下问题:
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=________mol·
(2)写出难溶物Ca3(AsO4)2的Ksp表达式:
Ksp[Ca3(AsO4)2]=____________,若混合溶液中Al3+、Fe3+的浓度均为1.0×
10-4mol·
L-1,c(AsO
)最大是________mol·
(3)工厂排放出的酸性废水中的三价砷(H3AsO3弱酸)不易沉降,可投入MnO2先将其氧化成五价砷(H3AsO4弱酸),写出该反应的离子方程式_________________________________________________
_____________________________________________________。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右使五价砷以Ca3(AsO4)2形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为________;
②Ca3(AsO4)2在pH调节到8左右才开始沉淀的原因为________
(1)H2SO4的浓度为28.42g·
L-1,转化为物质的量浓度为c=
=0.29mol·
(2)Ksp的表达式为离子浓度幂的乘积。
Ksp小的物质先生成沉淀,所以Fe3+先沉淀,c(AsO
)=
=5.7×
10-17(mol·
L-1)。
(3)弱酸在写离子方程式时写成化学式,氧化还原反应方程式依据得失电子守恒进行配平。
(4)①当Ca2+的浓度增大时,Ca2+与SO
可生成CaSO4沉淀。
②酸与碱发生中和反应,c(AsO
)增大,当Ca2+与AsO
浓度幂的乘积达到Ca3(AsO4)2的Ksp时,开始沉淀。
(1)0.29
(2)c3(Ca2+)·
c2(AsO
) 5.7×
10-17
(3)2H++MnO2+H3AsO3===H3AsO4+Mn2++H2O
(4)①CaSO4 ②H3AsO4是弱酸,当溶液中pH调节到8左右时AsO
浓度增大,Ca3(AsO4)2开始沉淀
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 高考 化学 一轮 复习 限时 训练 第八 28
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
