 临床英语术语缩写表文档格式.docx
临床英语术语缩写表文档格式.docx
- 文档编号:22037469
- 上传时间:2023-02-02
- 格式:DOCX
- 页数:10
- 大小:18.04KB
临床英语术语缩写表文档格式.docx
《临床英语术语缩写表文档格式.docx》由会员分享,可在线阅读,更多相关《临床英语术语缩写表文档格式.docx(10页珍藏版)》请在冰豆网上搜索。
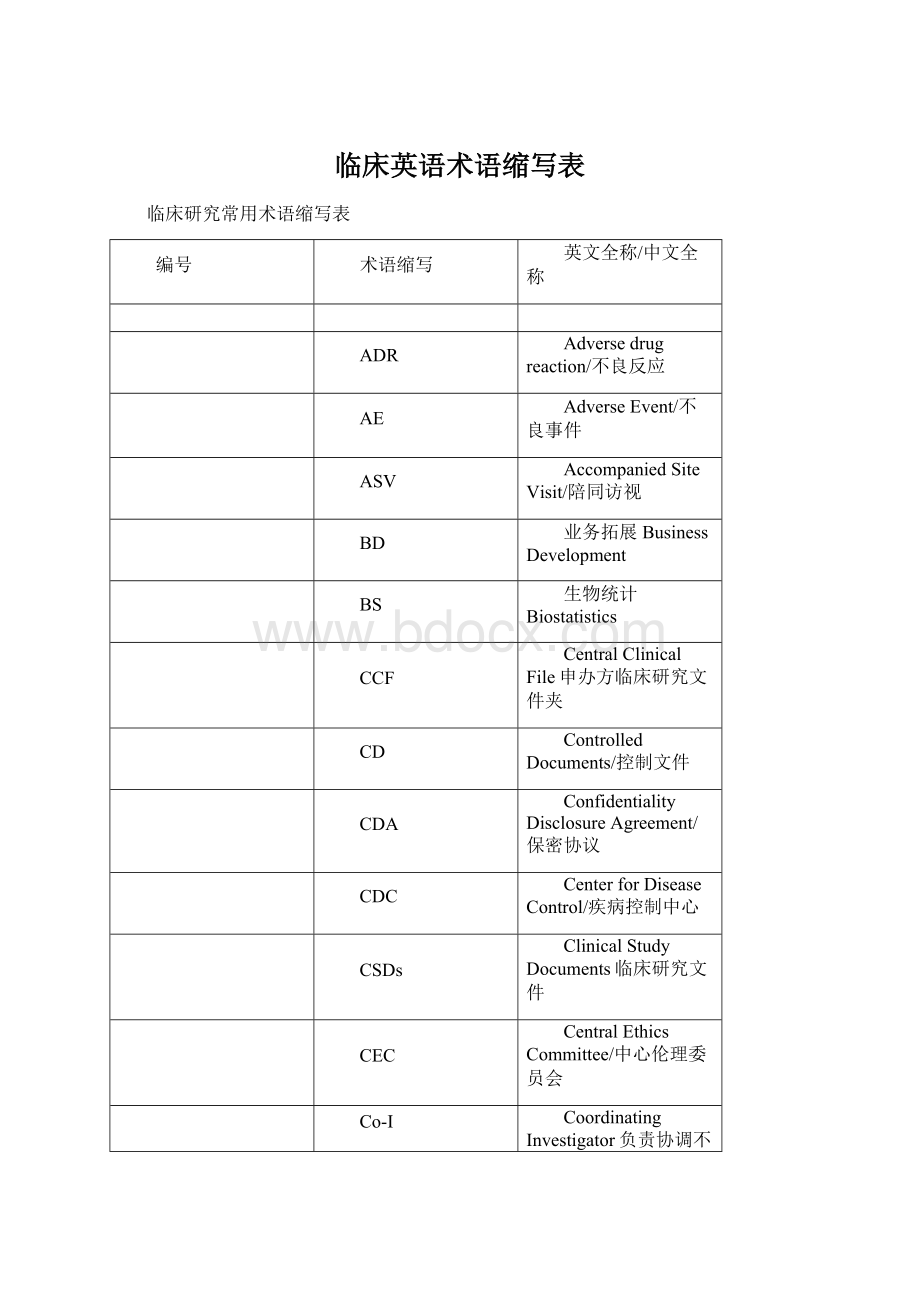
CentralEthicsCommittee/中心伦理委员会
Co-I
CoordinatingInvestigator负责协调不同中心参加多中心临床试验研究者的研究者
COF
ChangeOrderForm/工作范围变更申请表
CIF
CentralInvestigator’sFile申办者—研究者文件夹(中心研究者文件夹)
CM
ClinicalMonitoring/Operations/临床监查/运营
CMA
ClinicalMonitoringAssociate/临床研究监查助理
CR
CompleteResponse痊愈
CRA
ClinicalResearchAssociate(equivalenttoClinicalStudyMonitor)
临床监查员
CRC
ClinicalResearchCoordinator/临床研究协调员
CRF
CaseReportFormorCaseRecordForm/病例报告表
CRO
ContractResearchOrganization/合同研究组织
ClinicalStudyDocuments/临床研究文件
CSR
ClinicalStudyReport/临床研究报告
CTA
ClinicalTrialAssistant(equivalenttoClinicalResearchAssistant)
临床研究助理
ClinicalTrialAgreement/临床试验协议
ClinicalTrialApplication/临床试验申请
CTS
ClinicalTrialSupplies/临床试验用品
CTX
ClinicalTrialExemption/临床试验免责
CV
CurriculumVitae/履历
DCF
DataClarificationForm/数据澄清表
DCR
DataClarificationReport(seeDCF)/数据澄清报告
DCRF
DataClarificationandResolutionForm(seeDCF)/数据澄清和解决表
DM
DataManagement/数据管理
DMP
DataManagementPlan/数据管理计划书
DQF
DataQueryForm/数据疑问表
DS
DataSource/数据源
EC
EthicsCommittee/伦理委员会
eCRF
ElectronicCaseReportForm/电子病历报告表
EDC
ElectronicDataCapture/电子数据采集
EOS
EndofStudy/研究结束
EU
EuropeanUnion/欧盟
FAS
FullAnalysisSet/全分析集
FDA
FoodandDrugAdministration/美国食品药品管理局
FM
ApprovedStandardForm/批准的标准表格
GCP
GoodClinicalPractice/临床试验质量管理规范
GLP
GoodLaboratoryPractice/实验室质量管理规范
GMP
GoodManufacturingPractice/药品生产质量管理规范
GRP
GoodResearchPractice/科学研发质量管理规范
GSP
GoodStatisticalPractice/统计质量管理规范
HCO
HeadofClinicalOperations临床运营总监
IB
Investigator'
sBrochure/研究者手册
IC
InformedConsent/知情同意
ICF
InformedConsentForm(alsoseeIC)/知情同意书
ICH
InternationalConferenceonHarmonization/国际协调会议
ICH-GCP
InternationalConferenceonHarmonisationTripartiteGuidelineonGoodClinicalPractice
国际协调会议药品临床试验质量管理规范指南
IDB
InvestigationalDrugBrochure/试验药物手册
IEC
IndependentEthicCommittee/独立伦理委员会
IND
InvestigationalNewDrug(USFDA)/研究用新药
IP
InvestigationalProduct/研究用产品
IRAEs
ImmediatelyReportableAdverseEvents/立即上报的不良事件
IRB
InstitutionalReviewBoard./机构审查委员会
ITT
Intentiontotreat/意向性治疗
ISA
InvestigatorStudyAgreement/研究者合同
ISF
InvestigationalSiteFile研究者文件夹
LM
LineManager/直线经理
LOI
LetterofIntent/意向书
MOH
MinistryofHealth/卫生部
MSA
MasterServicesAgreement/主服务协议
MTD
MaximumToleratedDose/最大耐受剂量
MW
MedicalWriting/医学写作
NA
NotAvailable/不可用
NCE
NewChemicalEntity/新化学实体
NCS
NotClinicallySignificant/无临床意义
ND
NotDone/未做
NDA
NewDrugApplication./新药上市申请
OD
OtherDocuments/其他文件
OP
OperatingProcedure/操作规程
OOS
OutOfScope/超工作范围
OS
OverallSurvival/总体生存期
OTL
OperationalTeamLead/运营团队负责人
PD
ProtocolDeviation/方案偏离
PI
PrincipleInvestigator/主要研究者
PIN
PersonalIdentificationNumber/个人确认密码
PK
Pharmacokinetics/药物代谢动力学
PM
ProjectManager/项目经理
PMF
ProjectManagermentFile/项目管理文件夹
PMI
PeriodicMaintenanceInspection/定期维护检查
PMS
Post-MarketingSurveillance/上市后药物检测
PP
ProjectPlan/项目计划
PerProtocol/符合方案集
PR
PatientRecruitment/患者招募
QA
QualityAssurance/质量管理
QC
QualityControl/质量控制
RA
RegulatoryAuthorities/监督管理部门
RM
RemoteMonitoring/远程监查
On-SiteMonitoring/现场监查=On-TargetMonitoring/目标化监查
SAE
SeriousAdverseEvent/严重不良事件
SC
StudyCoordinator/研究协调员
SCV
SiteClose-outVisit/中心关闭访视
SSV
SiteSelectionVisit/中心筛选访视
SMV
SiteMonitoringVisit/中心监查访视
SVR
SiteVisitReport/中心访视报告
SD
SourceData/源数据
SDV
SourceDataVerification/原始数据核查
SFDA
StateFoodandDrugAdministration/国家食品药品监督管理局
SIC
SubjectIdentificationCode/受试者识别代码
SIF
SiteInformationForm/中心信息表
SIV
SiteInitiationVisit/中心启动访视
SOP
StandardOperatingProcedure/标准操作规程
SOW
ScopeofWork/工作范围
Sub-I
Subinvestigator次要研究者
SUSAR
SuspectedUnexpectedSeriousAdverseReaction
可疑的非预期的严重不良反应
TP
Template/模版
TMF
TrialMasterFile/试验主文档
UADR
UnexpectedAdverseDrugReaction/非预期药物不良反应
UADE
Unanticipatedadversedrugeffect/非预期的不良反应
UAE
Unexpectedadverseevent/非预期的不良事件
WI
WorkInstruction/工作指南
SOP类型缩写表
OP操作规程OperatingProcedures
WI工作指南WorkInstructions
TP模板Template
FM批准的标准表格ApprovedStandardForms
OD其他文件OtherDocuments
业务部门缩写表/FunctionalAreaAbbreviationTable:
BS生物统计Biostatistics
BD业务拓展BusinessDevelopment
CM临床监查/运营ClinicalMonitoring/Operation
DM数据管理DataManagement
IT信息技术InformationTechnology
MS医学科学服务MedicalScienceService
PM项目管理ProjectManagement
QA质量保证QualityAssurance
RM记录管理RecordsManagement
RA注册事务RegulatoryAffairs
SMSOP管理SOPManagement
ST研究中心管理服务SiteManagementService
TR培训Training
试验主文档:
(TMF)TrialMasterFile
PMF项目管理文件夹ProjectManagementFile
CCF申办方临床研究文件夹CentralClinicalFile
CIF申办方-研究者文件夹CentralInvestigatorFile
ISF研究者文件夹InvestigatorSiteFile
BSF生物统计学文件夹BiostatisticsStudyFile
DMSF数据管理研究文件夹DataManagementStudyFile
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 临床 英语 术语 缩写
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 《城市规划基本知识》深刻复习要点.docx
《城市规划基本知识》深刻复习要点.docx
