 最新高中化学盐类的水解学案3 精品文档格式.docx
最新高中化学盐类的水解学案3 精品文档格式.docx
- 文档编号:21944917
- 上传时间:2023-02-01
- 格式:DOCX
- 页数:10
- 大小:36.02KB
最新高中化学盐类的水解学案3 精品文档格式.docx
《最新高中化学盐类的水解学案3 精品文档格式.docx》由会员分享,可在线阅读,更多相关《最新高中化学盐类的水解学案3 精品文档格式.docx(10页珍藏版)》请在冰豆网上搜索。
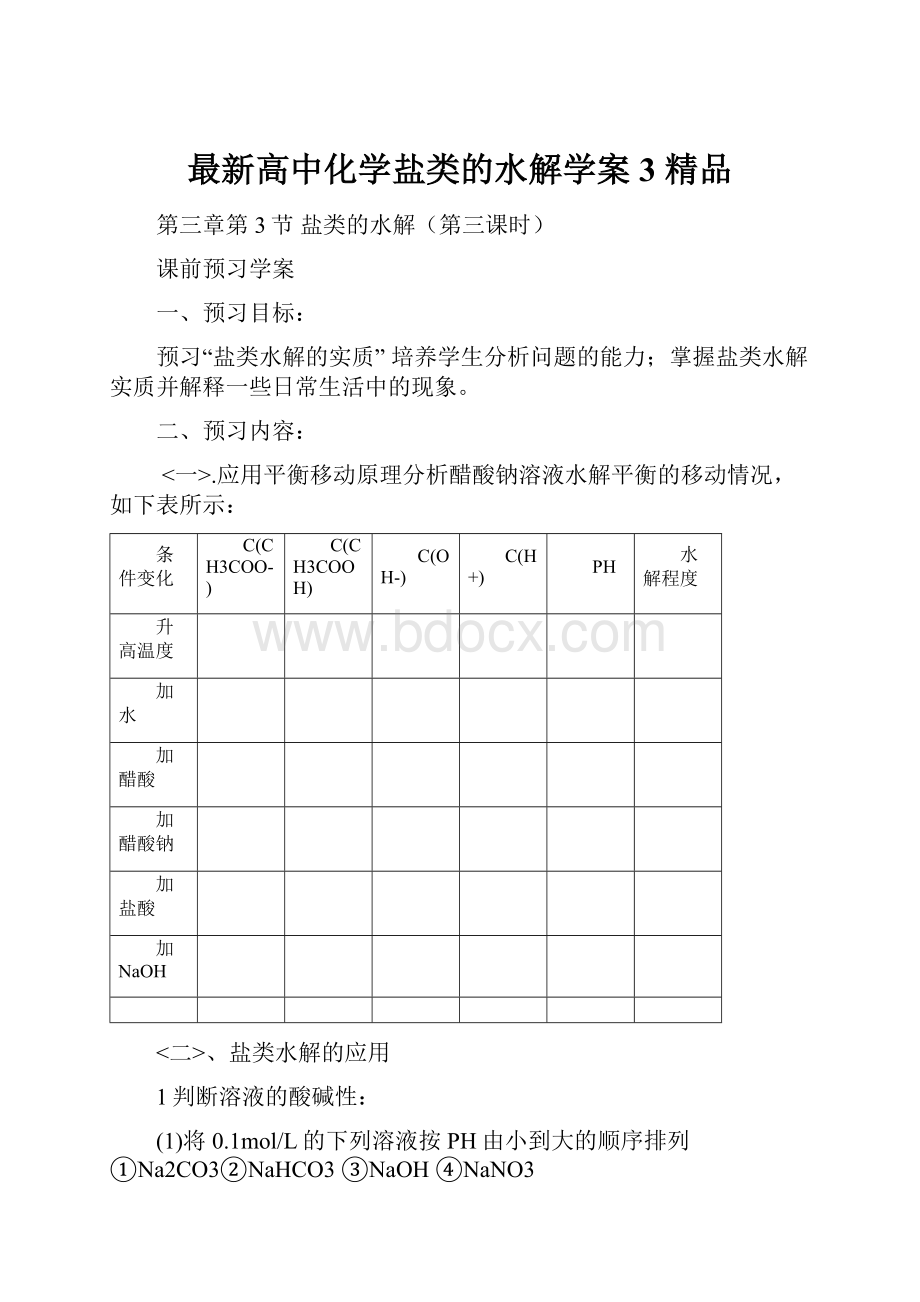
1判断溶液的酸碱性:
(1)将0.1mol/L的下列溶液按PH由小到大的顺序排列①Na2CO3②NaHCO3③NaOH④NaNO3
⑤CH3COOH⑥NaHSO4⑦NH4Cl_______________________
(2)酸式盐溶液的酸碱性:
酸性:
NaHSO3NaH2PO4碱性:
NaHCO3NaHSNa2HPO4
2判断溶液中离子浓度的大小:
(1)CH3COONa溶液中离子浓度大小顺序为________________________
(2)(NH4)2SO4溶液中离子浓度大小顺序为__________________
(3)Na2CO3溶液中离子浓度大小顺序为__________________________
3配制盐溶液时,加酸或碱抑制水解:
为了防止配制FeCl3溶液时可能浑浊,应向溶液中加入抑制水解。
4把盐溶液蒸干制取无水盐晶体:
把下列盐溶液蒸干得到何种物质:
AlCl3_______Al2(SO4)3________FeCl3________
Na2CO3_______CuSO4_____
5判断溶液中的离子能否共存:
主要掌握Al3+(Fe3+)与HCO3-、CO32-,AlO2-、S2-不共存。
三>
、电解质溶液中的守恒关系:
(1)电荷守恒:
电解质溶液中无论含多少种离子,但溶液总是呈电中性的。
即整个溶液中________所带的负电荷总数一定等于_____所带正电荷总数。
如在NH4Cl溶液中有_____________________
(2)原子守恒(物料守恒):
电解质溶液中尽管有些离子水解、电离等原因发生改变,但某原子总数是保持不变的。
如NH4Cl中存在____________________.
[思考与交流]写出下列溶液中的各种守恒关系:
10.1mol/LNa2CO3溶液中:
电荷守恒:
__________物料守恒:
_____.
②0.1mol/LH2S溶液中:
___________物料守恒:
_____
三、提出疑惑
同学们,通过你的自主学习,你还有哪些疑惑,请把它填在下面的表格中:
疑惑点
疑惑内容
课内探究学案
【学习目标】1进一步巩固对盐类水解实质的理解
2解释一些日常生活中的现象
【学习重点】盐类水解的本质和离子浓度大小比较
【学习难点】盐类水解方程式的书写和离子浓度大小比较
【学习过程】
【必备相关知识】
一、电离平衡理论和水解平衡理论
1.电离理论:
⑴弱电解质的电离是微弱的,电离消耗的电解质及产生的微粒都是少量的,同时注意考虑水的电离的存在;
例如NH3·
H2O溶液中微粒浓度大小关系。
⑵多元弱酸的电离是分步的,主要以第一步电离为主;
例如H2S溶液中微粒浓度大小关系。
2.水解理论:
⑴弱酸的阴离子和弱碱的阳离子因水解而损耗;
如NaHCO3溶液中有
c(Na+)>c(HCO3-)。
⑵弱酸的阴离子和弱碱的阳离子的水解是微量的(双水解除外),因此水解生成的弱电解质及产生H+的(或OH-)也是微量,但由于水的电离平衡和盐类水解平衡的存在,所以水解后的酸性溶液中c(H+)(或碱性溶液中的c(OH-))总是大于水解产生的弱电解质的浓度;
例如(NH4)2SO4溶液中微粒浓度关系。
⑶一般来说“谁弱谁水解,谁强显谁性”,如水解呈酸性的溶液中c(H+)>c(OH-),水解呈碱性的溶液中c(OH-)>c(H+);
⑷多元弱酸的酸根离子的水解是分步进行的,主要以第一步水解为主。
例如Na2CO3溶液中微粒浓度关系。
二、电荷守恒和物料守恒
1.电荷守恒:
如NaHCO3溶液中n(Na+)+n(H+)=n(HCO3-)+2n(CO32-)+n(OH-)
2.物料守恒:
由于电离或水解因素,有些离子会发生变化变成其它离子或分子等,但离子或分子中某种特定元素的原子的总数是不会改变的。
如NaHCO3溶液中n(Na+):
n(C)=1:
1,推出:
c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
3.导出式——质子守恒:
如碳酸钠溶液中由电荷守恒和物料守恒将Na+离子消掉可得:
c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3)。
【当堂检测】
1、(18徐州期初调研)下列叙述正确的是
A.常温下,10mLpH=12的Ba(OH)2溶液与40mLcmol·
L-1的NaHSO4溶液混合,当溶液中的Ba2+、SO42-均恰好完全沉淀,若混合后溶液的体积为50mL,则溶液pH=11
B.某二元酸(用H2A表示)在水中的电离方程式是:
H2A=H++HA-,HA-H++A2-
则NaHA溶液中:
c(Na+)=c(A2-)+c(HA-)+c(H2A)
C.10mL0.1mol·
L-1NH4Cl与5mL0.2mol·
L-1NaOH溶液混合:
c(Na+)=c(Cl-)>
c(OH-)>
c(H+)
D.浓度均为0.1mol·
L-1的小苏打溶液与烧碱溶液等体积混合:
c(Na+)+c(H+)=2c(CO32-)+c(OH-)
2、(18苏南四市调研)下列关于溶液中离子的说法正确的是
A.0.1mol·
L-1的Na2CO3溶液中离子浓度
B.0.1mol·
L-1的NH4Cl和0.1mol·
L-1的NH3·
H2O等体积混合后溶液中的离子浓度关系:
C.常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子度关系:
D.0.1mol·
L-1的NaHS溶液中离子浓度关系:
3、(18南通一模)25℃时,将稀氨水逐滴加入到稀硫酸中,当溶液的pH=7时,下列关系正确的是
A.c(NH4+)<c(SO42-)B.2c(NH4+)=c(SO42-)
C.c(NH4+)>c(SO42-)D.c(OH-)+c(SO42-)=c(NH4+)+c(H+)
4、(18苏北五市调研)25℃时,在25mLo.1mol·
L-1的NaOH溶液中,逐滴加入
0.2mol·
Lˉ1的CH3COOH溶液。
溶液pH的变化曲线如图
所示。
下列分析的结论中,正确的是·
A、B点的横坐标a=12.5
B、C点时c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C、D点时c(CH3COO-)+c(CH3COOH)=2c(Na+)
D、曲线上A、B间任一点,溶液中都有:
c(Na+)>c(CH3COOˉ)>
c(H+)
5、(18无锡期末调研)下列叙述正确的是
A.0.01mol/LCH3COOH与pH=12的NaOH溶液混合,若有c(CH3COO-)>
c(Na+),则混合液一定呈碱性
B.常温下,将等体积0.01mol/LHCl与pH=12的氨水混合,则混合液的pH=7,
C.0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2c(H2A)+2c(HA)+2c(A2-)
D.将5mL0.02mol/L的H2SO4与5mL0.02mol/LNaOH溶液充分混合,若混合后溶液的体积为10mL,则混合液的pH=2
6、(2018重庆)11.温度相同、浓度均为0.2mol/L的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、⑤
、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是
A.③①④②⑥⑤B.①③⑥④②⑤
C.③②①⑥④⑤D.⑤⑥②④①③
课后练习与提高
1.在0.1mol/L的NaHCO3溶液中,下列关系式正确的是.
A.c(Na+)>c(HCO3-)>c(H+)>c(OH-)B.c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-)
C.c(Na+)=c(HCO3-)>c(OH-)>c(H+)D.c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
2.0.1mol/LKHSO4和0.1mol/LNa2S溶液等体积混合后,溶液能使pH试纸变蓝,则离子浓度关系正确的是
Ac(SO42-)>c(HS-)>c(OH-)>c(H+)
Bc(Na+)>c(K+)>c(H+)>c(OH-)
Cc(Na+)=c(S2-)+c(H2S)+c(HS-)+c(SO42-)
Dc(Na+)+c(K+)+c(H+)=c(SO42-)+c(S2-)+c(HS-)+c(OH-)
3、300C时,在0.1mol/L的Na2S、NaHS两溶液中均存在的关系是
A.C(H+)•C(OH-)>
10-14B.C(Na+)=C(S2-)+C(HS-)+C(H2S)
C.C(OH-)=C(H+)+C(HS-)+2C(H2S)D.C(Na+)+C(H+)=C(OH-)+C(HS-)+2C(S2-)
4、物质的量浓度相同的200mLBa(OH)2溶液和150mLNaHCO3混合后,最终溶液中离子的物质的量浓度关系正确的是
A、c(OH-)>
c(Ba2+)>
c(Na+)>
c(CO32-)B、c(OH-)>
C、c(OH-)=c(Ba2+)+c(Na+)+c(H+)D、c(H+)+c(Na+)+2c(Ba2+)=c(OH-)
5、经测定某溶液中只含NH4+、C1-、H+、OH-四种离子,下列说法错误的是
A.若溶液中粒子间满足:
c(NH4+)>
c(C1-)>
c(OH-)>
c(H+)则溶液中溶质一定为:
NH4Cl和NH3·
H2O
B.溶液中四种粒子之间不可能满足:
c(C1-)>
c(H+)>
c(NH4+)>
c(OH-)
C.若溶液中粒子间满足:
c(OH-)溶液中溶质一定只有NH4Cl
D.若溶液中c(NH4+)=c(Cl-),则该溶液一定显中性
6.将100毫升0.1摩/升的BaCl2溶液加入到100毫升0.2摩/升的H2SO4溶液中,则溶液中离子浓度关系是
A.c(H+)>
c(Cl-)>
c(SO42-)B.c(H+)>
c(Cl-)>
c(SO42-)>
c(Ba2+)
C.c(H+)>
c(SO42-)>
c(Cl-)D.c(Cl-)>
c(H+)>
c(SO42-)
7.将7.8g铁粉加入200mL2mol/L的HNO3溶液中,使之充分反应放出NO气体,所得溶液中主要离子浓度的大小关系是
A.c(NO3-)>c(Fe2+)>c(Fe3+)>c(H+)B.c(NO3-)>c(Fe3+)>c(Fe2+)>c(H+)
C.c(Fe2+)>c(Fe3+)>c(NO3-)>c(H+)D.c(Fe2+)>c(NO3-)>c(Fe3+)>c(H+)
8、一元酸HA溶液中,加入一定量强碱MOH溶液后,恰好完全反应,反应后的溶液中,下列判断正确的是
A.c(A-)≥c(M+)B.c(A-)≤c(M+)
C.若MA不水解,则c(OH-)<
c(A-)D.若MA水解,则c(OH-)>
c(A-)
9、某二元弱酸的酸式盐NaHA溶液,若pH<
7,则溶液中各离子浓度的关系不正确的是
A、c(Na+)>
c(HA—)>
c(A2—)>
c(OH—)
B、c(Na+)+c(H+)==c(HA—)+2c(A2—)+c(OH—)
C、c(H+)+(A2—)==c(OH—)+c(H2A)
D、c(Na+)==c(HA—)+c(H2A)+2c(A2—)
10、(18江苏卷18题)将0.2mol·
L-1HCN溶液和0.1mol·
L-1的NaOH溶液等体积混合后,溶液显碱性,下列关系式中正确的是
Ac(HCN)<c(CN-)Bc(Na+)>c(CN-)
Cc(HCN)-c(CN-)=c(OH-)Dc(HCN)+c(CN-)=0.1mol·
L-1
11、(18江苏卷17题)草酸是二元弱酸,草酸氢钾溶液呈酸性。
在0.1mol·
L-1KHC2O4溶液中,下列关系正确的是
A.c(K+)+c(H+)=c(HC2O4—)+c(OH—)+c(C2O42-)
B.c(HC2O4-)+c(C2O42-)=0.1mol·
L-1
C.c(C2O42-)>c(H2C2O4)
D.c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42—)
12、(18年广东化学·
15)下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1mol·
L-1Na2CO3溶液:
c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
B.0.1mol·
L-1NH4Cl溶液:
c(NH4+)=c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:
c(Na+)=c(NO3-)
17)盐酸、醋酸和碳酸氢钠是生活中常见的物质。
下列表述正确的是
A.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH-
B.NaHCO3溶液中:
c(H+)+c(H2CO3)=c(OH-)
C.10mL0.10mol·
L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:
c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同
13、(18年广东化学·
9)下列浓度关系正确的是
A.氯水中:
c(Cl2)=2c(ClO-)+c(Cl-)+C(HCl)}
B.氯水中:
c(Cl-)>c(H+)>c(OH-)>c(ClO-)
C.等体积等浓度的氢氧化钠与醋酸混合:
c(Na+)=c(CH3COO-)
D.Na2CO3溶液中:
c(CO32-)>
c(HCO3-)>
c(H+)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 最新高中化学盐类的水解学案3 精品 最新 高中化学 盐类 水解
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 1212中级汽车维修工考试试题三.docx
1212中级汽车维修工考试试题三.docx
