 教学设计案例Word下载.docx
教学设计案例Word下载.docx
- 文档编号:21820735
- 上传时间:2023-02-01
- 格式:DOCX
- 页数:16
- 大小:37.16KB
教学设计案例Word下载.docx
《教学设计案例Word下载.docx》由会员分享,可在线阅读,更多相关《教学设计案例Word下载.docx(16页珍藏版)》请在冰豆网上搜索。
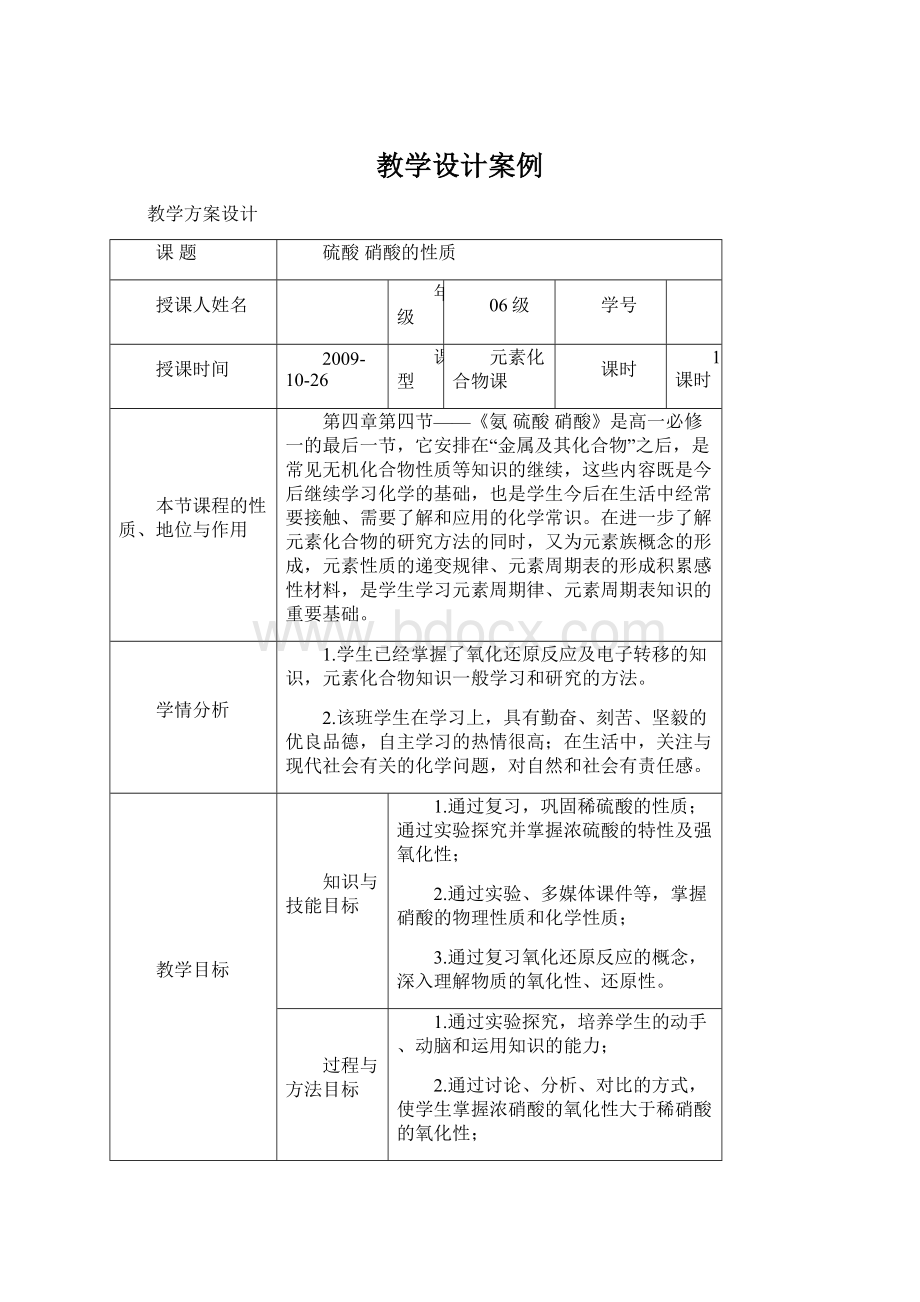
通过实验探究并掌握浓硫酸的特性及强氧化性;
2.通过实验、多媒体课件等,掌握硝酸的物理性质和化学性质;
3.通过复习氧化还原反应的概念,深入理解物质的氧化性、还原性。
过程与方法目标
1.通过实验探究,培养学生的动手、动脑和运用知识的能力;
2.通过讨论、分析、对比的方式,使学生掌握浓硝酸的氧化性大于稀硝酸的氧化性;
4.通过观察实验现象和药品实物,培养学生的实验观察、分析思维能力。
情感、态度、价值观目标
1.通过实验和科学探究,激发学生的学习兴趣,培养学生严谨求实、勇于创新的科学品质。
2.通过浓硝酸与稀硝酸的对比学习,渗透“量变质变”规律和尊重客观实际、力求实事求是的原则的教育。
教学重点、难点与关键
教学重点
浓硫酸的特性,硝酸的不稳定性和氧化性。
教学难点与关键
通过实验和表格对比的方式利于知识的吸收和记忆,突破浓硫酸和硝酸的氧化性这个难点。
教学资源与手段
仪器药品
仪器:
试管(若干),大烧杯(1个),胶塞(带导管和一个小孔),胶头滴管(2支)
药品:
浓硫酸,木屑,棉花,纸屑,蔗糖,酸性KMnO4溶液,铜丝,铜片,品红溶液,浓硝酸,稀硝酸,石蕊试液
教具
PPT课件,图片,实验用品
教与学的过程设计
教学内容
教学手段与方法
教师教授活动
学生学习活动
设计宗旨与意图
硫酸的性质
多媒体课件
讲授法
展示图片
展示实物
实验
展示表格
讨论
阅读教科书
【复习引课】上节课我们重点学习了氨的性质及氨的实验室制法,现在谁能回答一下氨有什么样的性质呢?
氨的实验室制法呢?
写下化学方程式。
【思考与交流】1.概括酸的通性。
2.实验室里用金属与酸反应制取氢气时,往往用稀硫酸或盐酸,而不用浓硫酸或硝酸,这是为什么?
【板书】一硫酸与硝酸都具有酸的通性。
【过渡】硫酸与硝酸都有酸的通性,但是还记得在初中时我们就知道,浓硫酸是有一些特殊的性质的,下面我们就来回忆一下浓硫酸的一些性质。
【提问】浓硫酸在稀释时应注意的问题?
(图片讲解)
【板书】二浓硫酸的性质
1.物理性质
【展示】一瓶浓硫酸
1.物理性质:
无色油状液体,其密度比水大,难挥发性。
吸水性
【板书】2.特性脱水性
【实验】
(1)浓硫酸与木屑、棉花、纸屑反应。
(2)浓硫酸与蔗糖反应。
【对比表格】吸水性和脱水性的比较。
【板书】与金属反应
强氧化性
【实验】浓硫酸与铜反应
【练习】书写化学方程式并分析电子转移方向和数目,指出氧化剂和还原剂。
【练习】写出浓硫酸和铁的反应方程式并并分析电子转移方向和数目,指出氧化剂和还原剂。
【思考】为什么浓硫酸可以用铁槽车或铝槽车运输?
【讲授】大家还记得我们讲到金属铝的时候提到了铝的表面有一层氧化膜,保护活泼的铝在空气中能稳定存在。
而我们这里也是相似的原因。
【提出概念】浓硫酸可使铁或铝的表面生成一层致密的氧化膜,阻止了内部金属与浓硫酸进一步反应,这种现象叫做钝化。
与非金属反应
【引导】大家还记得浓硫酸和蔗糖的反应现象吧?
这个反应产生了气体,可是我们知道浓硫酸的脱水性只是把蔗糖从白变黑了,那么气体是从哪来的呢?
这就是我们现在要讲的浓硫酸和非金属的反应。
【思考并讨论】设计实验方案,验证C和浓硫酸反应的产物。
【提问】为什么要先用无水硫酸铜验证水?
为什么需要再次验证二氧化硫是否全部被氧化?
【过渡】大家都知道,性质决定用途,那么大家能不能试着总结一下硫酸的用途呢?
【板书】3用途
现在大家可以看一下书的第96页最后一段,看看这些用途你们都想到几条呢?
【课堂练习】下列现象体现了硫酸的哪些性质?
(1)把浓硫酸滴入放在蒸发皿里的蔗糖上,蔗糖就会炭化变黑
(2)把浓硫酸露置在空气里,质量会增加。
(3)把锌粒放入稀硫酸里,会产生氢气。
(4)把铜片放入浓硫酸里并加热,会产生SO2。
(5)利用浓硫酸和食盐固体反应,制HCl气体。
【回答】回忆上节课知识,回答问题
【思考】回答问题
【观察和思考】
【观察思考并回答】仔细看图,思考问题
【观察和思考】总结物理性质
【观察实验现象】理解浓硫酸的脱水性。
(1)与木屑、棉花、纸屑反应现象:
都变黑
(2)与蔗糖反应现象:
①蔗糖由白→黑;
②生成的黑色物质呈面包状;
③闻一闻有刺激性气味。
【观察实验现象】
①固:
红→黑
②液:
无→棕黑→蓝色
③气:
无色有刺激性气味,使酸性KMnO4溶液退色;
使品红溶液退色。
【回答】同学回答并书写
【思考讨论】
【回答】
【阅读材料】
【回答】巩固知识
复习上节课的知识
旧知新析,引入新课。
提出问题,让同学带着问题去学习
巩固稀硫酸的性质,让新知识与旧知识相结合,完整学生的知识体系
情景创设
培养学生的实验观察、分析思维能力,使学生记忆深刻
激发学生的学习兴趣,加深对浓硫酸的脱水性的理解
以表格的方式展现给学生,让知识更清晰有条理
复习氧化还原反应及电子转移的知识
多次练习巩固,渗透“量变质变”规律
联系之前的实验现象进一步引出下一个问题
联系铝的氧化膜使学生更深刻的体会钝化的概念
提醒学生注意验证产物时的一些注意事项
结合简单习题巩固知识
硝酸的性质
探究法
【过渡】学完了硫酸的性质,下面我们来一起学习硝酸的性质。
大家在学习的过程中要注意硝酸和硫酸的性质都有什么相同和不同呢?
【板书】三硝酸的性质
【展示】一瓶浓硝酸,一瓶稀硝酸
【板书】酸性
2.化学性质不稳定性
【思考】常用的浓硝酸为什么会呈黄色?
【科学探究】向少量石蕊试液中逐滴加入浓硝酸,观察现象,并解释。
【过渡】我们前面学习了浓硫酸的强氧化性,而硝酸呢,也是具有强氧化性的,我们现在来看一下下面这两个实验。
【实验】浓稀硝酸与铜反应
氧化性
【练习】分析反应中电子转移的方向和数目,并指出氧化剂和还原剂。
【过渡】浓硫酸有钝化现象,那浓硝酸呢?
【资料卡片】若将浓HNO3和浓HCl按体积比1:
3混合所得混合物叫王水,可溶解不活泼金属金等。
【过渡】除了课上的这些知识以外,还有许多关于硫酸和硝酸的知识,大家要是有兴趣可以在课下自己去学习探索
【科学探究】有人认为,“比较浓硝酸和稀硝酸的还原产物的化合价,浓HN03中的氮从+5降为+4而稀HN03中的氮从+5价降为+2,从化合价变化可以判断稀硝酸的氧化性比浓硝酸强。
”这种看法是否正确?
为什么?
【提示】氧化剂氧化性的强弱要看它得电子的难易程度,反应的剧烈程度,与有变价元素的还原剂使还原剂相应元素化合价上升的高低来判断,并不是化合价变化的多少,对于还原剂还原性的强弱也是这样判断的
【讲授】我们这样来看还是比较抽象的,老师可以给出这样的比喻:
将铜升高到+2价,浓硝酸只需要花费小小的力气,自己降低一价就够了,而稀硝酸则要花大力气,降低三价才行,当然就是花力气小的氧化性就强了。
【引导】浓硫酸除了和金属反应还可以和非金属反应,那么硝酸呢?
是不是也可以和非金属反应?
【讲授】当硝酸与金属或非金属及某些有机物反应时,反应物或反应条件不同,硝酸被还原所得到的产物也不同,如:
NO2、HNO2、NO、N2O、N2、NH3
【总结】浓硫酸和硝酸氧化性的比较和方程式的书写(表格)
【课堂练习】
下列反应中,硝酸所起的作用属于:
A、强氧化性B、酸性
C、不稳定性D、上述都不是
(1)久置的浓硝酸变黄色
(2)用硝酸浸洗附有银的试管
(3)用硝酸浸洗久置石灰水的试剂上的白膜
(4)用硝酸浸洗积碳的试管
【思考】
【观察思考】观察实物
【思考并回答】浓硝酸易分解生成NO2溶于硝酸
【观察实验现象并思考】
浓硝酸+Cu
1.Cu片:
有大量气泡产生
2.溶液颜色:
无色变为绿色
3.气体颜色:
红棕色
4.反应剧烈程度:
剧烈
5.触摸容器外壁:
很热
稀硝酸+Cu
有气泡产生
无色变为蓝色
无色(打开止水夹后)无色变为红棕色
缓慢
温热
【思考回答】
【倾听并思考】
【倾听思考】
【填写表格】
【完成练习】
带着问题学习下一部分
两个实验的现象相对比,更加直观
联系之前学习的氧化还原反应及电子转移的知识
知识适当的扩展,培养自主学习的兴趣
培养学生的探究能力
从理论和比喻两方面来解释这个问题,易于理解
让同学填写表格,巩固重点,记忆更深刻
板书设计
§
4.4氮硫酸硝酸
一硫酸与硝酸都具有酸的通性
二浓硫酸的性质
1物理性质
2特性脱水性与金属反应(钝化:
Fe,Al)
强氧化性
3用途
三硝酸的性质
酸性浓硝酸(钝化)
2化学性质不稳定性与金属反应
氧化性稀硝酸
教学反思
他人评价
1图片、实物和理论相结合,记忆深刻。
2讲解钝化概念时联系了铝的氧化膜,能够使学生贯穿以前所学的知识。
在其他的知识上也常常联系旧知识和生活,使理论的东西具体化。
3在浓稀硝酸与铜反应的讲解之后提出了一个科学探究,讲解这个问题时用了比喻的解释方法,是这节课的亮点。
4在资料卡片处注重了情感、态度、价值观的体现,让同学们在课下也能够对生活上的一些和化学有关的知识进行学习。
自我反思
1注重和旧知识的联系,和生活的联系,很多问题都是在旧知识的基础上提出来的。
2实验→观察→分析是本节教学的重要手段与方法,给学生一个“实验是研究化学的基础”、“实验是最高法庭”的深刻印象。
3注意教学方式的多样性。
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 教学 设计 案例
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
