 江西省上饶市届高三下学期第三次高考模拟考试理综化学试题Word版 含答案Word格式.docx
江西省上饶市届高三下学期第三次高考模拟考试理综化学试题Word版 含答案Word格式.docx
- 文档编号:21631162
- 上传时间:2023-01-31
- 格式:DOCX
- 页数:11
- 大小:421.57KB
江西省上饶市届高三下学期第三次高考模拟考试理综化学试题Word版 含答案Word格式.docx
《江西省上饶市届高三下学期第三次高考模拟考试理综化学试题Word版 含答案Word格式.docx》由会员分享,可在线阅读,更多相关《江西省上饶市届高三下学期第三次高考模拟考试理综化学试题Word版 含答案Word格式.docx(11页珍藏版)》请在冰豆网上搜索。
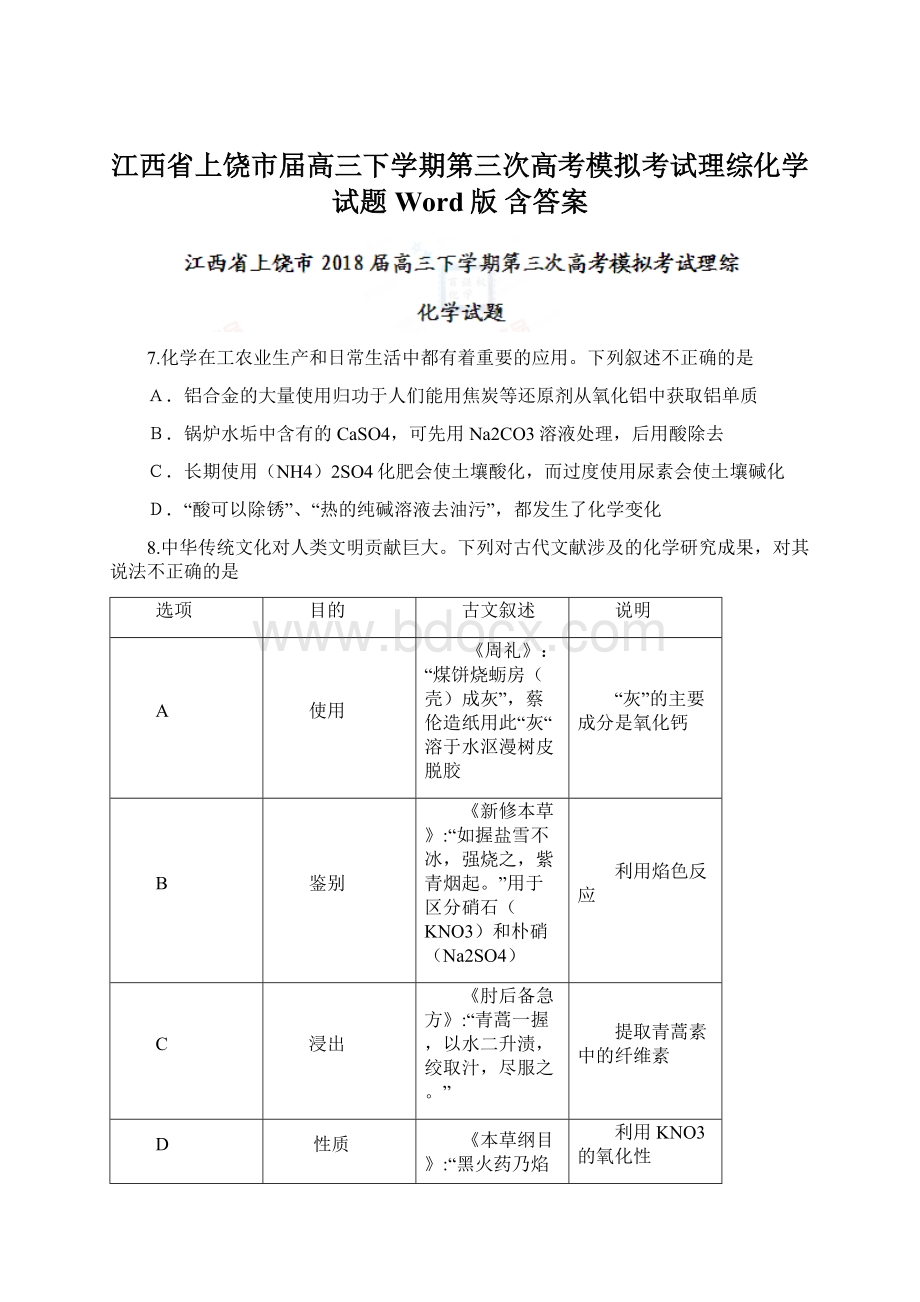
提取青蒿素中的纤维素
D
性质
《本草纲目》:
“黑火药乃焰硝.硫磺、杉木炭所合,以为烽燧铳机诸药者。
”
利用KNO3的氧化性
9.己烯雌酚是一种激素类药物,其结构简式如右图所示。
下列有关叙述中不正确的是
A.己烯雌酚的分子式为C18H20O2
B.己烯雌酚分子中一定有16个碳原子共平面
C.己烯雌阶为芳香族化合物
D.己烯雌酚可发生加成、取代、氧化、加聚、酯化、硝化反应
10.用下列实验方案及所选玻璃仪器(非玻璃任选),就能实现相应实验目的的是
序号
实验目的
实验方案
所选玻璃仪器
除去KNO3中少量NaCl
将混合物制成热的饱和溶液,冷却结晶,过滤
酒精灯、烧杯、玻璃棒
证明HClO与CH3COOH的酸性强弱
同温下用pH试纸测定浓度为0.1mol/LNaClO溶液和
0.1mol/LCH3COONa溶液
玻璃棒、玻璃片
检验蔗糖水解产物且具有还原性
向蔗糖容易中加入几滴稀硫酸,水浴加热5分钟,再向其中加入新制银氨溶液,水浴加热
试管、烧杯、酒精灯、滴管
配制1L1.6%的硫酸铜溶液(其密度为1.0g/mL)
将25gCuSO4·
5H2O溶解在97.5g水中
烧杯、量筒、玻璃棒
11.有一类电池,它虽然也可以说经历了氧化还原过程,但电池的总反应中并没有反映出这种变化,它是通过一种物质从高浓度状态向低浓度状态的转移而获得电动势,这一类电池被称为浓差电池。
现有如图所示装置,该装置工作时,下列说法不正确的是
A.电子流向:
Cu
(2)→Cu(3),Cu(4)→Cu
(1)
B.一段时间后,图II装置中CuSO4溶液浓度增大
C.电极Cu
(1)和Cu(3)的电极反应式都是Cu2++2e-=Cu
D.若0.5molSO42-从阴离子交换膜左侧迁移到右侧,理论上Cu(4)极质量减少32g。
12.短周期主族元素X、Y、Z、W的原子序数依次增大,其中Y、W处于同一主族。
Y、Z的最原子最外层电子数之和等于9,X的简单氢化物与W的单质组成的混合气体见光可生成W的氢化物和油状混合物。
下列说法正确的是
A.简单离子半径:
Y<
Z<
W
B.Y分别与X、Z形成的化合物,其所含化学键的类型相同
C.W的氧化物对应的水化物的酸性一定比X的强
D.Y的简单气态氢化物的热稳定性一定比W的强
13.25℃时,将氨水与氯化铵溶液混合得到c(NH3·
H2O)+c(NH4+)=0.1mol/L的混合溶液。
溶液中c(NH3·
H2O)、c(NH4+)与pH的关系如图所示。
下列有关离子浓度关系叙述一定正确的是
A.W点表示溶液中:
c(NH4+)+c(H+)=c(OH-)
B.pH=10.5溶液中:
c(Cl-)+c(OH-)+c(NH3·
H2O)<
0.1mol/L
C.pH=9.5溶液中:
c(NH3·
H2O)>
c(NH4+)>
c(OH-)>
c(H+)
D.向W点所表示1L溶液中加入0.05moINaOH固体(忽略溶液体积变化):
c(Cl-)>
c(Na+)>
c(OH-)>
26.氢化铝锂(LiAlH4)是有机合成中的重要还原剂。
某课题组设计实验制备氢化铝锂并测定其纯度。
已知:
氢化铝锂、氢化锂遇水都剧烈反应,并产生同一种气体。
回答下列问题:
I.制备氢化锂(LiH):
选择图I中的装置制备氢化锂(必要时可重复使用):
(1)装置D中NaOH溶液的作用是____________。
(2)装置的连接顺序(从左至右)为A→_____________。
II.制各氢化铝锂:
1947年,Schlesinger、Bond
和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按定比例在乙醚中混合,榄拌,充分反应后,经一系列操作得到LiAlH4晶体。
(3)将乙醚换为水是否可行,请简述理出:
______________。
(4)氲化锂与无水三氯化铝反应的化学方程式为______________。
III.测定氢化铝锂产品(不含氢化锂)的纯度。
(5)按图2装配仪器、检查装置气密性并装好药品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氛呋喃作稀释剂),启动反应的操作是_______。
读数之前,上下移动量气暂在右侧的容器,使量气管左、右两侧的液面在同一水平而上,其目的是_____。
(6)标准状况下,反应前量气管读数为Vml,反应完毕并冷却之后,量气管读数为V2mL。
该样品的纯度为______(用含a、V1、V2的代数式表示)。
若起始读数时俯视刻度线,测得的结果将____(填“偏高"
”偏低”或“无影响”)。
27.(15分)铅蓄电池是我国目前使用二次电池的数量最多之一。
从含铅废料中回收铅,对废旧电池进行科学处理和综合利用,意义重大。
其中一种回收铅的生产流程如下:
(1)过程I,已知20℃时PbSO4、PbCO3的溶解度如甲图所示;
Na2SO4、Na2CO3的溶解度如图乙所示。
①根据图甲,写出过程I的离子反应方程式:
________________
②生产过程中的温度应保持在40℃,若温度降低,PbSO4的转化速率下降。
機器图乙解释可能的原因:
A.温度降低,反应速率降低。
B.__________________
(2)①过程II,发生反应2PbO2+H2C2O4=2PbO+H2O2+2CO2↑。
实验中检测到有大量的氧气产生。
推洲PbO2氧化了H2O2,通过实验证实了这一推测。
实验方案是:
(已知:
PbO2为棕黑色固体,PbO为橙黄色固体)
②写出双氧水分子的电子式:
__________
③PbO2具有强氧化性,写出PbO2与Mn(NO3)2和HNO3反生成紫红色溶液的离子方程式:
_____。
(3)过程III,将PbO粗品溶解在HCl和NaCl的混合溶液中,
得到含Na2PbCl4的电解液。
电解Na2PbCl4溶液,
生成Pb,其原理如右图所示:
①阴极的电极反应式:
_______________
②电解一段时间后,PbCl42-浓度大幅下降,为了恢复容易的浓度,并且实现物质的循环利用,应采取的方法是:
_____________
(4)现用某铅蓄电池(含有0.8L硫酸浓度为4.5mol/L容易)来电解饱和食盐水制氯气。
当制得氯气26.88L(标准状况下)时,理论上电解后,蓄电池中硫酸溶液的浓度为:
______(忽略电解前后溶液体积变化)。
28.化学反应原理在科研和生产中有广泛应用。
(1)用生物质热解气(主要成分为CO、CH4、H2)将SO2在一定条件下还原为单质硫进行烟气脱硫。
己知:
①C(s)+O2(g)=CO2(g)
△H=-393.5
kJ/mol
②CO2(g)+C(s)=2CO(g)
△H=+1725kJ/mol
③S(s)+O2(g)=SO2(g)
△H=-296.0kJ/mol
写出CO将SO2
还原为单质硫的热化学方程式为______________。
(2)CO可用于合成甲醇,一定温度下,向体积为2L的密闭容器中加入CO和H2,发生反应
CO(g)+2H2(g)
CH3OH(g)
达到平衡测得各组分浓度如下:
物质
CO
H2
CH3OH
浓度(mol/L)
0.9
1.0
0.6
①反应达到平衡时,CO的转化率为_______。
②恒温恒容条件下,可以说明反应已达到平衡状态的是______(填号)。
A.v正(CO)=2v逆(H2)
B.混合气体的平均相对分子质量不变
C.混合气体的密度不变
D.CH3OH、CO、H2的浓度都不再发生变化
③若将容器体积压缩到1L,则达到新平衡时c(H2)的取值范围是________。
④若保持容器体积不变,再充入0.6molCO和0.4molCH3OH,此时v正____v逆(填“>
”“<
”或“=”)。
(3)
常留下,HNO2的电离常数Ka=7.1×
10-4mol/L,NH3·
H2O的电离常数Kb=1.7×
10-5mol/L。
0.1mol/LNH4NO2溶液中离子浓度由大到小的顺序是_______,常温下NO2-
水解反应的平衡常数K=
_______(保留两位有效数字)。
35.【化学-选修3物质结构与性质】
(15分)
N、P、As、Ga、Cr、Cu
等元素化合物种类繁多,具有重要的研究价值和应用价值。
请回答下列问题:
(1)Cr元素价电子排布式为__________。
(2)N2F2分子中,氮原子的杂化轨道类型为______,画出N2F2可能的结构式________。
PCl3和PCl5是磷元素形成的两种重要化合物,请根据价电子互斥理论推测PCl3的空间构型__________。
(4)
砷化嫁以第三代半导体著称,熔点为1230℃,具有空间网状结构,性能比硅更优良。
广泛用于雷达、电子计算机、人造卫星、宇宙飞船等尖端技术中。
砷化镓属于_____晶体。
已知氮化硼与砷化镓属于同种晶体类型。
则两种晶体熔点较高的是______(填化学式),其理由是_______。
上述两种晶体中的
四种元素电负性最小的是______(填元素符号)。
(5)
铜的化合物种类很多,右图是氯化亚铜的晶胞结构,已知晶胞的棱长为acm,则氢化亚铜密度的计算式为ρ=_____g/cm3(用NA表示阿佛加德罗常数)。
36.【化学-选修5有机化学】
(15分)
具有抗菌作用的白头翁素衍生物H的合成路线如下图示:
ⅰ.RCH2Br
R-HC=CH-R'
ⅱ.
ⅲ.
(以上R、R'
、R"
代表氢、烷基成芳基等)
(1)A属于芳香烃,其名称是_________。
(2)
B的结构简式是__________。
(3)由C生成D的化学方程式是______________。
由E与I2在一定条件下反应生成F的化学方程式是___________;
此反应同时生成另外一个有机副产物且与F互为同分异构体,此有机副产物的结构简式是___。
试剂b是______。
(6)
下列说法正确的是________(选填字母序号)。
A.G存在顺反异构体
B.由G生成H的反应是加成反应
C.1molG最多可以与1molH2发生加成反应。
D.1molF或1molH
与足量NaOH溶液反应,均消耗2molNaOH
(7)
以乙烯为起始原料,结合已知信息选用必要的无机试剂合成,写出合成
路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
________________________。
7.A
8.C
9.B
10.D
11.B
12.D
13.C
26、(14分,除标注外,每空2分(下同))
I.
(1)
除去H2中混有的H2S(1分);
(2)DBCBE;
II.(3)不可行,因为氢化铝锂、氢化锂遇水都剧烈反应;
(4)4LiH+AlCl3==LiAlH4+3LiCl
III.(5)倾斜Y形管,将蒸馏水注入ag产品中;
使量气管内气体的压强与大气压强相等(1分);
;
偏高。
27.(15分)
(1)①PuSO4(s)+CO32-(aq)===PbCO3(s)+SO42-(aq)
②温度降低,Na2CO3
浓度降低,反应速率减小;
①取少里PbO2于试管中,加入双氧水,产生使带火星的木条复燃的气体,同时棕黑色固体变为橙黄色。
证实推测正确。
②
③5PbO2+
2Mn2+
+4H+===2MnO4-+5Pb2++2H2O
(3)①PbCl42-+2e-===
Pb+4Cl-
②继续向阴极区加PbO粗品
(1分)
(4)1.5mo1/L
28.(14
分)
(1)
2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-
270kJ/mol
(2)①40%
②BD;
③1rmo1/L<
c(H2)<
2mo1/L;
④=
c(NO2-)>
c(H+)>
c(OH-)
1.4×
2021┄2022
35.(15分)
(1)3d54s1(1分);
(2)sp2(1分)
或
三角锥形
原子晶体;
BN(1分)
二者均为原子晶体,B、N
间的键长比Ga、As的键长短,键能大;
Ga
(5)
36.(15分)
(1)
1,2-二甲苯(邻二甲苯)
(2)
(3)
(4)
;
NaOH醇溶液(1分)
bd
(7)(3分)
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 江西省上饶市届高三下学期第三次高考模拟考试理综化学试题Word版 含答案 江西省 上饶市 届高三 下学 第三次 高考 模拟考试 化学试题 Word 答案
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
