 人教版化学选修四第3章 水溶液中的离子平衡 检测题6Word下载.docx
人教版化学选修四第3章 水溶液中的离子平衡 检测题6Word下载.docx
- 文档编号:21150636
- 上传时间:2023-01-28
- 格式:DOCX
- 页数:11
- 大小:140.91KB
人教版化学选修四第3章 水溶液中的离子平衡 检测题6Word下载.docx
《人教版化学选修四第3章 水溶液中的离子平衡 检测题6Word下载.docx》由会员分享,可在线阅读,更多相关《人教版化学选修四第3章 水溶液中的离子平衡 检测题6Word下载.docx(11页珍藏版)》请在冰豆网上搜索。
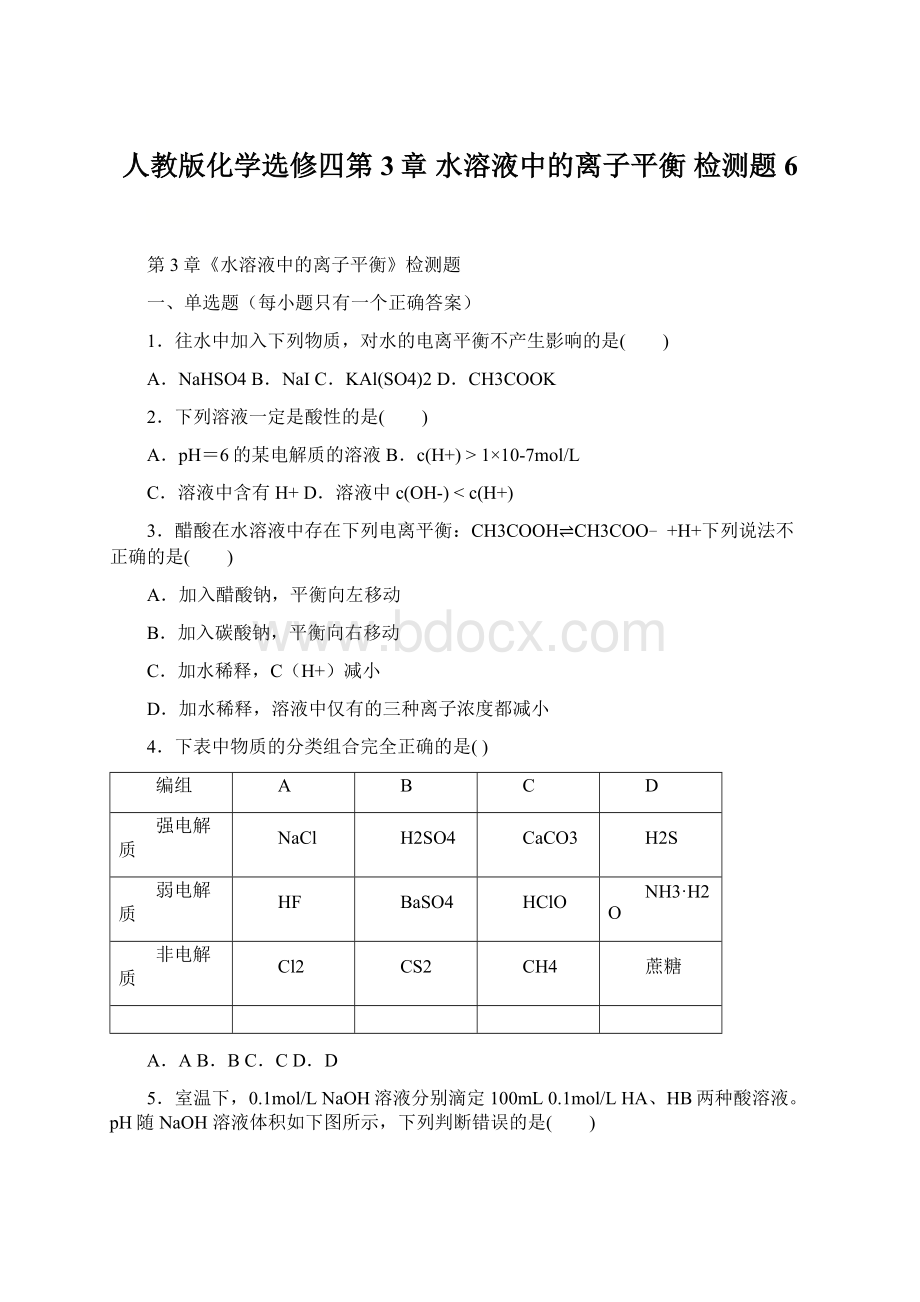
NH3·
H2O
非电解质
Cl2
CS2
CH4
蔗糖
A.AB.BC.CD.D
5.室温下,0.1mol/LNaOH溶液分别滴定100mL0.1mol/LHA、HB两种酸溶液。
pH随NaOH溶液体积如下图所示,下列判断错误的是( )
A.电离常数:
Ka(HA)>
Kb(HB)
B.由P点计算Ka(HB)≈10-4
C.pH=7时,c(A-)=c(B-)
D.中和分数达100%时,HA溶液中存在
6.25℃时,下列叙述中,正确的是()
A.CH3COONa溶液中:
c(Na+)=c(CH3COO-)
B.pH=3的醋酸溶液加水稀释过程中:
溶液中各离子浓度均变小
C.pH相同的NaOH溶液与NaHCO3溶液中:
水的电离程度相同
D.pH=9的NaHX溶液中:
c(H2X)>c(X2-)
7.对水的电离平衡不会产生影响的粒子是()
A.
B.
C.O=C=OD.
8.短周期元素R、X、Y、Z的原子序数依次增大。
R和X可形成两种液态化合物(常温常压),Y+和X2-具有相同的电子层结构,X和Z位于同一主族。
下列说法正确的是( )
A.原子半径大小顺序为:
r(Y)>r(X)>r(Z)>r(R)
B.R与X形成的两种液态化合物中均只含极性共价键
C.Y与X可形成碱性氧化物Y2X2
D.由R、X、Y、Z四种元素形成的常见化合物可抑制水的电离
9.已知Cl2、Al2S3、CaC2、C2H5Br、CH3COOCH3等物质的均能与水发生反应,反应可视为各物质和水均分别离解成两部分,然后再两两重新组合,形成新的物质。
下列化学反应符合这一特点的是:
( )
①ICl+H2O=HIO+HCl;
②CH3COCl+H2O→CH3COOH+HCl;
③CaC2+2H2O→Ca(OH)2+C2H2↑;
④Mg3N2+6H2O=3Mg(OH)2+2NH3↑;
⑤SiCl4+4H2O=H4SiO4↓+4HCl↑。
A.只有①④⑤B.只有②③⑤C.只有①②③④D.全部
10.下列叙述错误的是( )
A.BaCO3是难溶于水的强电解质,在医学上用作钡餐
B.中国古代利用明矾溶液的酸性清除铜镜表面的铜锈
C.施肥时,草木灰不能与铵态氮肥混合使用,否则会降低肥效
D.锅炉水垢中含有的CaSO4,可先用饱和碳酸钠溶液处理,而后用盐酸除去
11.向pH=1的某酸溶液和pH=13的氢氧化钠溶液中,加入足量的铝片,放出H2的物质的量之比为3:
1其原因可能是( )
A.两溶液的体积相同,酸是多元强酸
B.若酸为一元强酸,酸溶液的体积是碱溶液体积的3倍
C.两溶液的体积相同,酸是弱酸
D.酸是强酸,且酸溶液的浓度比NaOH溶液浓度大
12.将某一电解质溶于水,得浓度不相等但体积相等的两溶液A、B,其pH分别为3和5,则下列说法不正确的是( )
A.两溶液的浓度A>
B.该电解质可能为盐
C.该电解质可能为酸
D.用等浓度的氢氧化钠溶液来中和,需氢氧化钠溶液的体积VA和VB关系为VA=100VB
13.在一定体积pH=12的Ba(OH)2溶液中,逐滴加入pH=2的NaHSO4溶液,当溶液的pH恰好为7时,则参加反应的Ba(OH)2溶液与NaHSO4溶液的体积比是( )
A.1∶9B.1∶1C.1∶2D.1∶4
14.下列说法错误的是( )
A.除去MgCl2溶液中少量的FeCl3,可选用MgCO3
B.等物质的量浓度的(NH4)2SO4溶液和(NH4)2CO3溶液中NH4+的浓度前者大于后者
C.NaHS溶液中,滴入少量CuCl2溶液,产生黑色沉淀,HS-的水解程度增大,pH增大
D.用饱和氯化铵溶液可以清洗金属表面的锈迹
15.下列有关实验的说法正确的是( )
A.测定中和反应反应热实验中,为了充分反应,应将NaOH溶液缓缓倒入盐酸中
B.配制FeCl3溶液时,将FeCl3晶体溶解在较浓的盐酸中,再加蒸馏水稀释到所需浓度
C.用盐酸滴定NaOH溶液时,左手控制酸式滴定管活塞,右手振荡锥形瓶,眼睛注视滴定管内液面
D.检验Fe(NOs)2晶体是否变质时,将Fe(NO3)2样品溶于稀H2SO4后,再滴加KSCN溶液
二、填空题
16.
(1)配制AgNO3溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以______(填“促进”或“抑制”)其水解.
(2)明矾可用于净水,原因是(用离子方程式表示):
____________________
(3)泡沫灭火器灭火原理(用离子方程式表示)_____________________
(4)纯碱可代替洗涤剂洗涤餐具,原因是(用离子方程式表示)______________
17.现有25℃时0.1mol·
L-1的氨水,请回答以下问题:
(1)若向氨水中加入少量硫酸铵固体,此时溶液中
________(填“增大”、“减小”或“不变”)。
(2)若向氨水中加入稀硫酸,使其恰好中和,写出反应的离子方程式:
__________;
所得溶液的pH________7(填“>
”、“<
”或“=”),用离子方程式表示其原因:
__________;
所得溶液中各离子物质的量浓度由大到小的顺序是____________________。
(3)若向氨水中加入稀硫酸至溶液的pH=7,此时c(NH
)=amoL.L-1,则c(SO42-)为________。
18.用实验确定某酸HA是弱电解质。
两同学的方案是:
甲:
①称取一定量的HA配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH值,即可证明HA是弱电解质。
乙:
①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质。
(1)在两个方案的第①步中,都要用到的定量仪器是__________。
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH________(选填<、>、=)1。
乙方案中,说明HA是弱电解质的现象是_________(多选不给分)。
a.装盐酸溶液的试管放出H2的速率快。
b.装HA溶液的试管放出H2的速率快。
c.两个试管中产生H2的速率一样快。
(3)请你再提出一个合理而比较容易进行的方案(药品可任取),作简明扼要表述。
____________________________________________________________。
19.硝酸铵钙晶体[5Ca(NO3)2•NH4NO3•10H2O]极易溶于水,是一种绿色的复合肥料。
(1)硝酸铵钙晶体的溶液显酸性,原因是_____________(用离子方程式表示)。
(2)已知磷酸钙是一种难溶物,常温下,其Ksp=2.0×
10-33,
≈1.414。
工业上生产硝酸铵钙的方法是以硝酸浸取磷矿石得到的粗硝酸钙(含硝酸钙、磷酸钙及硝酸)为原料制备,其生产流程为:
①在粗硝酸钙浊液中,c(Ca2+)≈0.1mol/L,则其中c(PO43-)约为____________
②加入适量的碳酸钙后发生反应的离子方程式为_____________________。
③硝酸铵是一种易分解的物质,保存和利用时,需控制在较低温度.230~400℃时,它会分解成空气中含量最大的两种气体,其反应的化学方程式为_________________。
(3)生产硝酸铵钙工厂的废水中常含有硝酸铵,净化方法有反硝化净化法和电解法。
①NO3-在酸性条件下可转化为N2,该反硝化方法可用半反应(同电极反应式)表示_______________。
②目前常用电解法净化,工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过);
Ⅰ.阳极的电极反应为_________________,Ⅰ室可回收的产品为___________(填名称).
Ⅱ.Ⅲ室可回收到氨气,请结合方程式和文字解释其原因________________。
20.下表为常见几种弱酸的电离常数,
酸
电离常数(Ka)
CH3COOH
1.8×
10-5
3×
10-8
H2O2
K1=2.4×
10-12
K2=1×
10-25
H2CO3
K1=4.4×
10-7
K2=4.7×
10-11
I.结合上表回答下列问题(均为常温下的数据):
(1)在常温下,相同物质的量浓度的①CH3COONa②Na2CO3③NaClO三种溶液的pH由小到大的顺序为______________________(用序号回答)
(2)向Na2CO3溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的钠盐,同时还有另两种钠盐生成,该反应的化学方程式为_________________
II.过氧化氢(H2O2)为淡蓝色粘稠液体,是中学常见试剂.
(1)H2O2含有的共价键类型为_____________________
(2)实验室可用稀硫酸与BaO2反应来制取H2O2,该反应的化学方程式为__________________
(3)经测定H2O2为二元弱酸,酸性比碳酸还弱,不稳定易分解.已知Na2O2中通人干燥的CO2不反应,但通人潮湿的CO2却可以产生O2,试用化学方程式表示这一过程___________________
三、推断题
21.A、B、C、D、E五种可溶性化合物,分别由阳离子Fe3+、Ba2+、Al3+、Na+、Ag+和阴离子NO3—、OH-、SO42—、Cl-、CO32—中的各一组成(离子不重复)。
现做如下实验:
①A和E的溶液显碱性,0.1mol·
L-1A溶液的pH小于13;
②在B的溶液中逐滴加入氨水有白色沉淀生成,继续加氨水至过量,沉淀消失;
③在C的溶液中加入铁粉,溶液的质量增加;
④在D的溶液中加入过量的Ba(OH)2溶液,没有沉淀。
根据以上事实推断各物质的化学式:
A____________;
B____________;
C____________;
D____________;
E____________。
写出③中涉及的离子方程式
写出④中涉及的离子方程式
22.A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素。
在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。
请填空:
(1)若D是生产、生活中用量最大、用途最广的金属单质,加热蒸干棕黄色的B的溶液不能得到B,则B的化学式可能是________。
用有关离子方程式解释B溶液显酸性的原因是:
______________________________________;
(2)若A是一种碱性气体,常用作制冷剂,B和D为空气的主要成分,则反应②的化学方程式为________________________________;
(3)若D的氯碱工业的主要产品,B有两性,则反应③的离子方程式是________________;
(4)若D为酸或酸性气体,则A、C可以是___________,_______________;
(5)若C是一种温室气体,D是空气的主要成分之一,1mol黑色固体A完全燃烧放出393.5kJ热量,1molB气体完全燃烧放出283.0kJ热量,则A→B反应的热化学方程式为__________________________________。
四、实验题
23.聚合氯化铁铝(简称PAFC),其化学通式为[FexAly(OH)aClb·
zH2O]m。
某同学为测定其组成,进行如下实验:
①准确称取4.5050g样品,溶于水,加入足量的稀氨水,过滤,将滤渣灼烧至质量不再变化,得到2.3300g固体。
②另准确称取等质量样品溶于水,在溶液中加入适量Zn粉和稀硫酸,将Fe3+完全还原为Fe2+。
用0.1000mol·
L-1标准KMnO4溶液滴定Fe2+,消耗标准溶液的体积为20.00mL。
③另准确称取等质量样品,用硝酸溶解后,加入足量AgNO3溶液,得到4.3050g白色沉淀。
(1)若滴定管在使用前未用KMnO4标准溶液润洗,测得的Al3+含量将________(填“偏高”“偏低”或“不变”)。
(2)实验室检验Fe3+常用的方法是__________________。
(3)通过计算确定PAFC的化学式(写出计算过程;
m为聚合度,不必求出)。
24.某研究小组模拟工业上以黄铁矿为原料制备硫酸的第一步反应如下:
4FeS2+11O2
2Fe2O3+8SO2进行以下实验,并测定该样品中FeS2样品的纯度(假设其它杂质不参与反应)。
实验步骤:
称取研细的样品4.000g放入上图b装置中,然后在空气中进行煅烧。
为测定未反应高锰酸钾的量(假设其溶液体积保持不变),实验完成后取出d中溶液10mL置于锥形瓶里,用0.1000mol/L草酸(H2C2O4)标准溶液进行滴定。
(已知:
5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4)请回答下列问题:
(1)称量样品质量能否用托盘天平_______(填“能”或“不能”),取出d中溶液10mL需要用______准确量取(填序号)
A.容量瓶B.量筒C.碱式滴定管D.酸式滴定管
(2)上述反应结束后,仍需通一段时间的空气,其目的是__________
(3)已知草酸与高锰酸钾酸性溶液作用有CO2和Mn2+等物质生成,则滴定时发生反应的离子方程式为_______________﹔判断滴定到达终点的方法是___________。
(4)已知滴定管初读数为0.10mL,末读数如图所示,消耗草酸溶液的体积为___________mL。
下列操作会导致该样品中FeS2的纯度测定结果偏高的是_________(填序号)
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(5)该样品中FeS2的纯度为__________________
(6)若用下图装置替代上述实验装置d,同样可以达到实验目的的是_______(填编号)。
五、计算题
25.常温下,HCN的电离常数Ka=6.2×
10-10。
浓度均为0.5mol·
L-1的NaCN和HCN的混合溶液呈________(填“酸”“碱”或“中”)性,通过计算说明:
____________________________。
26.在100mL1mol/L的Ba(OH)2溶液中滴加100mLNaHSO4溶液,测得溶液的pH为1,求产生的沉淀的质量以及NaHSO4溶液的物质的量浓度。
参考答案
1.B2.D3.D4.C5.C6.D7.D8.D9.D10.A11.C12.D13.B14.C15.B16.抑制Al3++3H2O
Al(OH)3(胶体)+3H+Al3++3HCO3-═3CO2↑+Al(OH)3↓CO32-+H2O
HCO3-+OH-
17.减小NH3·
H2O+H+==NH4++H2O<
NH4++H2O
H2O+H+c(NH4+)>
c(SO42-)>
c(H+)>
c(OH-)a/2mol·
L-1
18.(4分,每空1分)
(1)100mL容量瓶
(2)>
b
(3)配制NaA溶液,测其pH>7即证明HA是弱电解质(其它答案合理均可)
19.
(1)NH4++H2O
NH3•H2O+H+;
(2)①1.414×
10-15mol/L;
②CaCO3+2H+═Ca2++CO2↑+H2O;
③2NH4NO3
2N2↑+O2↑+4H2O;
(3)①2NO3-+10e-+12H+═6H2O+N2↑;
②Ⅰ.2H2O﹣4e-═4H++O2↑;
硝酸;
Ⅱ.电解时Ⅲ室氢离子得电子发生还原反应(或2H++2e-=H2),使碱性增强,同时NH4+通过阳离子膜进入III室,发生反应:
NH4++OH-=NH3+H2O,生成氨气;
20.①<
③<
②2Na2CO3+Cl2+H2O=2NaHCO3+NaCl+NaClO非极性键、极性键H2SO4+BaO2=BaSO4↓+H2O2Na2O2+CO2+H2O=Na2CO3+H2O22H2O2=2H2O+O2↑
21.A、Na2CO3;
B、AgNO3;
C、Fe2(SO4)3;
D、AlCl3;
E、Ba(OH)2
2Fe3++Fe=3Fe2+;
Al3++4OH-=AlO2-+2H2O
22.FeCl3Fe3++3H2O
Fe(OH)3+3H+N2+O2
2NO3AlO2-+Al3++6H2O=4Al(OH)3↓NaOH、NaHCO3Fe、Fe(NO3)32C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
23.
(1)偏低(2分)
(2)取试样少许,向其中滴加少量KSCN溶液,若溶液变为(血)红色,证明溶液中含有Fe3+(2分)
(3)n(Fe3+)=n(Fe2+)=5×
n(MnO4-)=0.1mol·
L-1×
0.02L×
5=0.01mol(1分)
m(Fe2O3)=0.01mol×
1/2×
160g·
mol-1=0.8g
n(Al3+)=2n(Al2O3)=2×
=0.03mol(1分)
n(Cl-)=n(AgCl)=
根据电荷守恒:
3n(Fe3+)+3n(Al3+)=n(Cl-)+n(OH-)
n(OH-)=3×
0.01mol+3×
0.03mol-0.03mol=0.09mol(2分)
n(H2O)=
=
=0.03mol(2分)
即n(Fe3+):
n(Al3+):
n(OH-):
n(Cl-):
n(H2O)=1:
3:
9:
3
则PAFC的化学式为[FeAl3(OH)9Cl3·
3H2O]m或FeAl3(OH)9Cl3·
3H2O(1分)
24.不能D促进装置中的二氧化硫气体全部吸收2MnO4—+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O滴入最后一滴草酸溶液,溶液由紫红色变为无色,且半分钟内不恢复15.00C90%②
25.碱Kh=
≈1.6×
10-5>
6.2×
10-10,即水解平衡常数大于电离平衡常数,所以溶液呈碱性
26.(8分)m(BaSO4)=2.2mol/L
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 人教版化学选修四第3章 水溶液中的离子平衡 检测题 人教版 化学 选修 水溶液 中的 离子 平衡 检测
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
