 专题7化学反应速率和化学平衡Word下载.docx
专题7化学反应速率和化学平衡Word下载.docx
- 文档编号:21093245
- 上传时间:2023-01-27
- 格式:DOCX
- 页数:15
- 大小:119.24KB
专题7化学反应速率和化学平衡Word下载.docx
《专题7化学反应速率和化学平衡Word下载.docx》由会员分享,可在线阅读,更多相关《专题7化学反应速率和化学平衡Word下载.docx(15页珍藏版)》请在冰豆网上搜索。
500
2
粉末
35
3
0.7
36
250
4
0.8
200
5
25
6
1.0
125
7
8
1.1
100
9
44
40
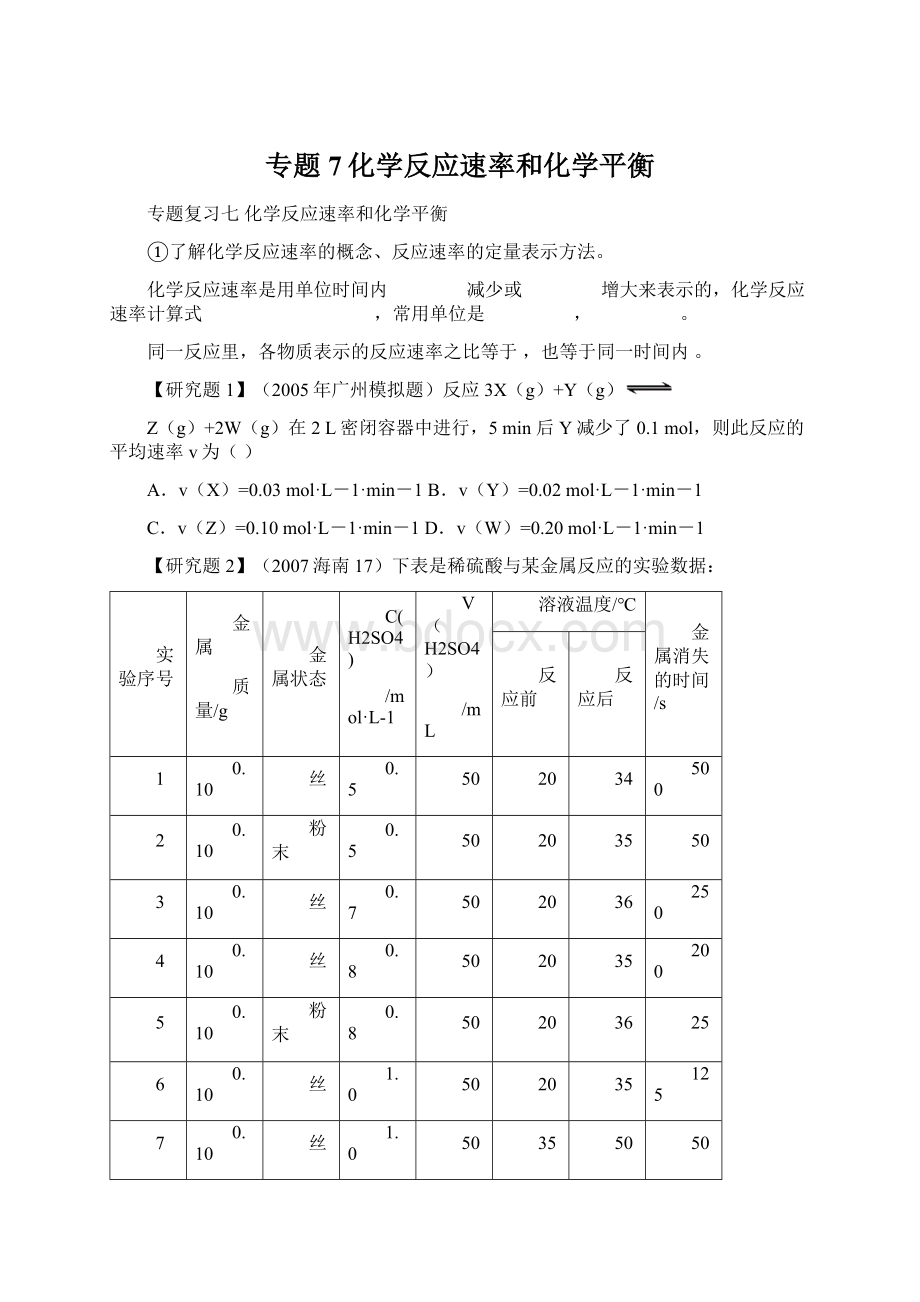
分析上述数据,回答下列问题:
(1)实验4和5表明,
对反应速率有影响,
反应速率越快,能表明同一规律的实验还有
(填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有
(3)本实验中影响反应速率的其他因素还有
,其实验序号是
(4)实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因:
②了解活化能对化学反应速率的影响,认识温度、浓度、压强和催化剂影响化学反应速率的一般规律。
影响化学反应速率主要因素是。
外界条件、、
(对于有气体参与的反应)和使用都能加快化学反应速率。
反应物浓度增大时,单位体积内分子数增多,也相应增大,单位体积内的有效碰撞次数也相应增多,化学反应速率。
增大压强,就是增加单位体积里反应物的物质的量,即,反应速率相应;
相反,减小压强,气体的体积就扩大,减小,反应速率随之。
升高温度,反应物分子的能量增加,使一部分原来能量较低的分子变成活化分子,从而增加了反应物分子中,使有效碰撞次数增多,反应速率。
催化剂能参与反应,改变反应历程,降低活化能,也就等于提高了,从而提高了有效碰撞频率,加快了。
【研究题3】
(2007广东22)“碘钟”实验中,3I-+S2O82-=I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。
某探究性学习小组在20℃进行实验,得到的数据如下表:
实验编号
①
②
③
④
⑤
c(I-)/mol·
L-
0.040
0.080
0.160
0.120
c(SO42-)/mol·
0.020
t/s
88.0
44.0
22.0
t2
回答下列问题:
(1)该实验的目的是。
(2)显色时间t2=。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为(填字母)
A<
22.0sB22.0~44.0sC>44.0sD数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是。
③认识催化剂在生产、生活和科学研究领域中的重大作用。
催化剂:
催化剂能参与反应,改变反应历程,降低活化能,也就等于提高了活化分子的百分数,从而提高了有效碰撞频率,加快了反应速率。
催化剂对化学平衡,但能缩短达到平衡所需。
【研究题4】
(2004江苏18)在容积固定的密闭容器中存在如下反应:
A(g)+3B(g)
2C(g);
△H<
0某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是
A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
④了解化学反应的可逆性。
能用焓变和熵变说明常见化学反应的方向。
*化学反应自发进行的方向的判断,根据体系存在着力图使自己的能量趋于“最低”和“有序”的自然规律,由焓变和熵变判据组合的复合判据适合于所有的过程。
反应热ΔH
混乱度ΔS
ΔG=ΔH-TΔS
自发性
>
低温>
0,高温<
<
高温>
0,低温<
*【研究题5】某化学反应其△H==—122kJ/mol,∆S==231J/(mol·
K),则此反应在下列哪种情况下可自发进行()
A.在任何温度下都能自发进行B.在任何温度下都不能自发进行
C.仅在高温下自发进行D.仅在低温下自发进行
⑤理解化学平衡和化学平衡常数的含义,能用化学平衡常数计算反应物的转化率。
化学平衡建立的条件________________________
化学平衡的特征:
定_____________动_____________等变_____________
化学平衡常数用符号表示,只与有关。
值愈大,表示反应正向进行程度愈,反应物的转化率也愈。
【研究题6】
(2007海南16部分改编)PCl5的热分解反应如下:
PCl5(g)PCl3(g)+Cl2(g)
⑴写出反应的平衡常数表达式;
⑵已知某温度下,在容积为10.0L的密闭容器中充入2.00molPCl5,达到平衡后,测得容器内PCl3的浓度为0.15mol/L。
计算该温度下的平衡常数。
⑶在⑵中达到平衡后,向容器中再通入2.00mol的PCl5,求再次达到平衡后,PCl5的转化率。
【研究题7】
(2007广东25部分)
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
⑴将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:
2SO2(g)+O2(g)2SO3(g)在一定条件下达到平衡,测得c(SO3)=0.040mol·
L-1。
计算该条
件下反应的平衡常数K和SO2的平衡转化率(写出计算过程)。
【研究题8】
(2006上海25)
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示______________,K值大小与温度的关系是:
温度升高,K值______________。
(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)
CO2(g)+H2(g)+Q(Q>0)
CO和H2O浓度变化如右图,则0~4min的平均反应速率v(CO)=______mol/(L·
min)
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。
①表中3min~4min之间反应处于_________状态;
C1数值________0.08mol/L(填大于、小于或等于)。
②反应在4min~5min问,平衡向逆方向移动,可能的原因是________(单选),
表中5min—6min之间数值发生变化,可能的原因是________(单选)。
A增加水蒸气B降低温度
C使用催化剂D增加氢气浓度
⑥理解浓度、温度、压强、催化剂等对化学平衡影响的一般规律。
影响化学平衡移动的条件:
浓度:
其他条件不变的情况下,增大反应物浓度或减小生成物浓度,平衡向方向移动,此时v(正)v(逆);
反之,如果,可使化学平衡向逆反应方向移动,此时v(正)v(逆)。
压强:
对有气体参加的可逆反应,反应前后体积发生变化时,若其他条件不变,加大压强会使平衡向的方向移动,反之向的方向移动。
气体体积在反应前后保持不变的反应,则改变压强对平衡。
温度:
其他条件不变时,升温使平衡向方向移动;
降温使平衡向方向移动。
对于一个可逆反应,如果正反应放热,则逆反应一定。
化学平衡移动原理(勒夏特列原理):
如果改变影响化学平衡的一个条件(如、、等),平衡就向能够这种改变的方向移动。
【研究题9】
(2006江苏16)某化学科研小组研究在其他条件不变时,改变某一条件对化
学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量):
根据以上规律判断,下列结论正确的是()
A.反应Ⅰ:
△H>0,P2>P1
B.反应Ⅱ:
△H<0,T1>T2
C.反应Ⅲ:
△H>0,T2>T1;
或△H<0,T2<T1
D.反应Ⅳ:
△H<0,T2>T1
【研究题10】
(2007上海25)一定条件下,在体积为3L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):
CO(g)+2H2(g)
CH3OH(g)
根据题意完成下列各题:
(1)反应达到平衡时,平衡常数表达式K=
,升高温度,K值(填“增大”、“减小”或“不变”)。
(2)在500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是
a氢气的浓度减少b正反应速率加快,逆反应速率也加快
c甲醇的物质的量增加d重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是:
(用化学方程式表示)。
⑦认识化学反应速率和化学平衡的调控在生活、生产和科学研究领域中的重要作用。
【研究题11】
(2006广东19)合成氨工业对国民经济和社会发展具有重要的意义。
对于密闭容器中的反应:
N2(g)+3H2(g)
2NH3(g),673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。
下列叙述正确的是()
A.点a的正反应速率比点b的大
B.点c处反应达到平衡
C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大
【研究题12】
(2007广东25)黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其煅烧产物为SO2和Fe3O4。
(2)已知上述反应是放热反应,当该反应处于平衡状态时,在体积不变的条件下,下列措施中有利于提高SO2平衡转化率的有(填字母)
A升高温度B降低温度C增大压强
D减小压强E加入催化剂G移出氧气
(3)SO2尾气用饱和Na2SO3溶液吸收可得到更要的化工原料,反应的化学方程式为
。
(4)将黄铁矿的煅烧产物Fe3O4溶于H2SO4后,加入铁粉,可制备FeSO4。
酸溶过程中需保持溶液足够酸性,其原因是。
【研究题13】
(2003江苏26)I.恒温、恒压下,在一个可变容积的容器中发生如下发应:
A(气)+B(气)
C(气)
(1)若开始时放入1molA和1molB,到达平衡后,生成amolC,这时A的物质的量为mol。
(2)若开始时放入3molA和3molB,到达平衡后,生成C的物质的量为mol。
(3)若开始时放入xmolA,2molB和1molC,到达平衡后,A和C的物质的量分别是ymol和3amol,则x=mol,y=mol。
平衡时,B的物质的量(选填一个编号)
(甲)大于2mol(乙)等于2mol
(丙)小于2mol(丁)可能大于、等于或小于2mol
作出此判断的理由是。
(4)若在(3)的平衡混合物中再加入3molC,待再次到达平衡后,C的物质的量分数是。
II.若维持温度不变,在一个与
(1)反应前起始体积相同、且容积固定的容器中发生上述反应。
(5)开始时放入1molA和1molB到达平衡后生成bmolC。
将b与
(1)小题中的a进行比较(选填一个编号)。
(甲)a<b(乙)a>b(丙)a=b(丁)不能比较a和b的大小
(5)溶液中的离子平衡
①了解电离、电解质、强电解质和弱电解质的概念。
电解质的概念类型
强电解质的概念类型
弱电解质的概念类型
【研究题1】有下列物质①铝②硫化氢③金刚石④氢氧化铝⑤干冰⑥液氨⑦氯水⑧氢氧化钠固体⑨碳酸氢钾溶液⑩硫酸钡粉末。
其中能导电的是;
属于非电解质的是;
属于电解质的是;
属于弱电解质的是。
写出下列物质溶于水的电离方程式:
硫化氢
碳酸氢钾
硫酸氢钠
②了解弱电解质在水溶液中的电离平衡。
弱电解质的电离平衡决定性因素由于弱电解质电离过程均要吸热,因此温度升高,电离。
溶液越,越有利于电离。
加入与弱电解质有相同离子的强电解质,电离。
(2007山东14)氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,
减小
B.通入少量SO2,溶液的漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量水,水的电离平衡向正反应方向移动
(2007上海21)已知0.1mol/L的醋酸溶液中存在电离平衡:
CH3COOH
CH3COO-+H+要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是()
A.加少量烧碱溶液B.升高温度C.加少量冰醋酸D.加水
(2003广东17)在甲烧杯中放入盐酸,乙烧杯中放入醋酸,两种溶液的体积和pH都相等,向两烧杯中同时加入质量不等的锌粒,反应结束后得到等量的氢气。
下列说法正确的是()
A.甲烧杯中放入锌的质量比乙烧杯中放入锌的质量大
B.甲烧杯中的酸过量
C.两烧杯中参加反应的锌等量
D.反应开始后乙烧杯中的c(H+)始终比甲烧杯中的c(H+)小
③了解水的电离和水的离子积常数。
水是极弱的电解质,原因能发生自偶电离
水的离子积——纯水及电解质稀溶液中有c(OH-)·
c(H+)=Kw,Kw只受影响,常温时(25℃)Kw=,温度升高,水的电离程度,Kw亦。
记牢公式c(OH-)·
c(H+)=Kw计算时看是否是常温,不是常温要看该温度下的Kw值
【研究题5】
(2007天津11)25℃时,水的电离达到平衡:
H2O
H++OH-;
ΔH>
0,下列叙述正确的是()
A.向水中加人稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加人少量固体CH3COONa,平衡逆向移动,c(H+)降低
D.将水加热,Kw增大,pH不变
(2006全国卷II7)将纯水加热至较高温度,下列叙述正确的是
A.水的离子积变大、pH变小、呈酸性B.水的离了积不变、pH不变、呈中性
C.水的离子积变小、pH变大、呈碱性D.水的离子积变大、pH变小、呈中性
④了解溶液pH的定义,能进行pH的简单计算。
溶液的pH表示方法:
pH=(适用范围:
稀溶液)
强酸(强碱)、弱酸(弱碱)加水稀释后的pH的计算
强酸pH=a,加水稀释10n倍,则pH弱酸pH=a,加水稀释10n倍,则pH
强碱pH=b,加水稀释10n倍,则pH弱碱pH=b,加水稀释10n倍,则pH
酸碱溶液无限稀释时,pH只能约等于或接近于7,酸的pH不能>
7,碱的pH不能<
(2007海南3)下列叙述正确的是()
A.95℃纯水的pH<
7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2mol/L的盐酸,与等体积水混合后pH=1
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
(2006上海20)室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是()
A.0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液
B.0.1mol/L的盐酸和0.1mol/L的氢氧化钡溶液
C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液
D.pH=4的盐酸和pH=l0的氨水
⑤了解盐类水解的原理,能说明影响盐类水解程度的主要因素,认识盐类水解在生产、
生活中的应用(弱酸弱碱盐的水解不作要求)。
盐类的水解:
在中电离出来的离子跟水所电离出来的或结合生成的反应。
任何一种盐都可以看作是和反应的产物,按生成盐的酸和碱的强弱可以把盐分为:
盐,水溶液呈碱性;
盐,水溶液呈性;
盐,水溶液呈中性。
盐类的水解实质是复分解反应:
盐+水
酸+碱(中和反应的逆反应)。
中和反应热,所以水解热。
中和反应程度,所以水解程度(填“较大”、“较小”),书写水解方程式时要用可逆符号。
由于程度较小一般不标明气体、沉淀符号。
(2007上海6)下列过程或现象与盐类水解无关的是()
A.纯碱溶液去油污B.铁在潮湿的环境下生锈
C.加热氯化铁溶液颜色变深D.浓硫化钠溶液有臭味
(2007广东15).下列各溶液中,微粒的物质的量浓度关系正确的是()
A.1.0mol/LNa2CO3溶液:
c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
B.1.0mol/LNH4Cl溶液:
c(NH4+)=c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:
c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:
c(Na+)=c(NO3-)
【研究题11】草酸是二元弱酸,草酸氢钾溶液呈酸性。
在0.1mol·
L-1KHC2O4溶液中,下列关系正确的是()
A.c(K+)+c(H+)=c(HC2O4-)+c(OH)+c(C2O42-)
B.c(HC2O4-)+c(C2O42-)=0.1mol·
L-1
C.c(C2O42-)>c(H2C2O4)
D.c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-)
(2005江苏12).常温下将稀NaOH学溶液和稀CH3COOH溶液混合,不可能出现的结果是()
A.pH>
7,且c(OH—)>
c(Na+)>
c(H+)>
c(CH3COO—)
B.pH>
7,且c(Na+)+c(H+)=c(CH3COO—)+c(OH—)
C.PH<7,且c(CH3COO—)>
c(H+)>
c(OH—)
D.pH=7,且c(CH3COO—)>
c(H+)=c(OH—)
⑥了解难溶电解质的沉淀溶解平衡。
不同电解质在中的溶解度差别很大,有的很大,有的很小。
在20℃时电解质的溶解性与溶解度的关系如下:
溶解性
易溶
可溶
微溶
难溶
溶解度
物质在水中“溶”与“不溶”是相对的,“不溶”是指“难溶”,绝对不溶的物质是没有的。
在一定条件下,难溶强电解质溶于水,当沉淀和沉淀相等时,形成溶质的
溶液,达到平衡状态,这种平衡称为沉淀溶解平衡。
(2007上海12)往含I-和Cl-的稀溶液中滴人AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如右图所示。
则原溶液中c(I-)/c(Cl-)的比值为()
A.(V2-V1)/V1B.V1/V2
C.V1/(V2-V1)D.V2/V1
【研究题14】
(06广东23)水体中重金属铅的污染问题备受关注。
水溶液中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2、Pb(OH)3-、Pb(OH)42-,各形态的浓度分数α随溶液pH变化的关系如图所示:
【1表示Pb2+,2表示Pb(OH)+,3表示Pb(OH)2,4表示Pb(OH)3-,5表示Pb(OH)42-】
⑴Pb(NO3)2溶液中,
2(填“>
”、“=”、“<
”);
往该溶液中滴入氯化铵溶液后,
增加,可能的原因是。
⑵往Pb(NO3)2溶液中滴稀NaOH溶液,pH=8时溶液中存在的阳离子(Na+除外)有,pH=9时,主要反应的离子方程式为。
⑶某课题组制备了一种新型脱铅剂,能有效去除水中的痕量铅,实验结果如下表:
离子Pb2+Ca2+Fe3+Mn2+Cl-
处理前浓度/(mg·
L-1)0.10029.80.1200.08751.9
处理后浓度/(mg·
L-1)0.00422.60.0400.05349.8
上表中除Pb2+外,该脱铅剂对其它离子的去除效果最好的是。
⑷如果该脱铅剂(用EH表示)脱铅过程中主要发生的反应为:
2EH(s)+Pb2+
E2Pb(s)+2H+
则脱铅的最合适pH范围为(填代号)。
A.4~5B.6~7C.9~10D.11~12
⑦了解离子反应的概念,掌握离子反应发生的条件。
能正确书写简单的离子方程式。
离子反应的概念。
离子反应的实质。
【研究题15】下列反应的离子方程式正确的是()
A.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:
Fe3++3H2O=Fe(OH)3↓+3H+
B.用小苏打治疗胃酸过多:
HCO3—+H+==CO2↑+H2O
C.实验室用浓盐酸与MnO2反应制Cl2:
MnO2+2H++2Cl—=Cl2↑+Mn2++H2O
D.用FeCl3溶液腐蚀印刷电路板:
Fe3++Cu==Fe2++Cu2+
【研究题16】某溶液既能溶解Al(OH)3,又能溶解H2SiO3,在该溶液中可以大量共存的离子组是()
A.K+、Na+、HCO3-、NO3-B.Na+、SO42、Cl-、ClO-
C.H+、Mg
- 配套讲稿:
如PPT文件的首页显示word图标,表示该PPT已包含配套word讲稿。双击word图标可打开word文档。
- 特殊限制:
部分文档作品中含有的国旗、国徽等图片,仅作为作品整体效果示例展示,禁止商用。设计者仅对作品中独创性部分享有著作权。
- 关 键 词:
- 专题 化学反应 速率 化学平衡
 冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。
冰豆网所有资源均是用户自行上传分享,仅供网友学习交流,未经上传用户书面授权,请勿作他用。


 对中国城市家庭的教育投资行为的理论和实证研究.docx
对中国城市家庭的教育投资行为的理论和实证研究.docx
